VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN
|
|
|
- Gustav Ivarsson
- för 5 år sedan
- Visningar:
Transkript
1 [Contact Name] [Department/Title] [Hospital Name] [Address Line 1] [Town/City] [Postal Code] [Country] [Date] Referens: FA VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN MEDDELANDE OM UPPDATERING AV LIFESTREAM DOKUMENTATION Bästa kund! Med detta brev vill vi informera dig om en korrigerande säkerhetsåtgärd för marknaden initierad av ClearStream Technologies (BD) och som involverar LifeStream ballongexpanderbar vaskulär täckt stent. Orsak till säkerhetsmeddelandet Ett antal klagomål har rapporterats gällande restenos efter implantation av LifeStream ballongexpanderbar vaskulär täckt stent. Dessa klagomål rapporterades efter normal klinisk användning av, och även vid uppföljning efter klinisk prövning av, BARD LIFESTREAM ballongexpanderbar vaskulär täckt stent vid behandling av ocklusion av höftartären (BOLSTER). Inga patientskador rapporterades. Mängden klagomål för restenos (0,04 %) överskrider den mängd som listas i feleffektsanalysen (0,01 %). ClearStream Technologies utfärdar ett säkerhetsmeddelande till marknaden för att avisera användarna om mängden restenosfall och om en uppdatering av bruksanvisningen till LifeStream ballongexpanderbar vaskulär täckt stent, i form av bifogad bilaga (bilaga 1). Denna information kommer att finnas med i dokumentationen för alla kommande enheter som distribueras av ClearStream (BD). Sida 1 av 13
2 Etikettuppdateringen ger information om aktuella resultat från kliniska studier av BARD LIFESTREAM ballongexpanderbar vaskulär täckt stent i behandling av ocklusion av höftartären (BOLSTER). Det här är inte en produktåterkallelse och ClearStream begär inte att någon enhet ska returneras från marknaden med anledning av detta meddelande. Våra register visar att din vårdinrättning har köpt en eller flera enheter av produkten som detta säkerhetsmeddelande gäller, i enlighet med tabell 1 nedan. Artikelnummer Ballongens diameter Ballongens längd Axelns längd LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM Sida 2 av 13
3 Artikelnummer Ballongens diameter Ballongens längd Axelns längd LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM Tabell 1: Berörda produktkoder Observera att behöriga myndigheter har informerats om den här korrigerande säkerhetsåtgärden. Sida 3 av 13
4 Som del av denna åtgärd kräver vi att du följer anvisningarna nedan och meddelar International Business Centre (IBC) i [insert country] om din efterlevnad av denna korrigerande säkerhetsåtgärd för marknaden. Åtgärder som krävs av dig och vårdinrättningen med anledning av detta säkerhetsmeddelande 1. Vidarebefordra detta säkerhetsmeddelande till all personal som är involverad i användningen av LifeStream system med ballongexpanderbar vaskulär täckt stent. 2. Se till att all berörd personal förstår innehållet i detta säkerhetsmeddelande till marknaden. 3. Bifogad dokumentationsuppdatering (bilaga 1) ska användas tillsammans med bruksanvisningen till LifeStream ballongexpanderbar vaskulär täckt stent för alla LifeStream-enheter som för närvarande har distribuerats. 4. Om du har distribuerat produkten vidare ska du identifiera till vilken organisation och omedelbart meddela denna om detta meddelande. Du kan inkludera en kopia av detta brev i meddelandet. 5. Fyll i det bifogade formuläret för kontroll av svarseffektivitet och skicka det till [insert country IBC] antingen via [FAX#] eller via e-post till [IBC address] Obs! Även om du inte behöver returnera produkten med anledning av detta säkerhetsmeddelande är det av högsta vikt att du skickar in det ifyllda formuläret för kontroll av svarseffektivitet så snart som möjligt. Vi uppskattar din hjälp med att hantera det här ärendet och ber om ursäkt för eventuella besvär som kan uppstå på grund av den här åtgärden. Om du har frågor eller behöver hjälp kontaktar du den lokala specialiserade försäljaren eller BD:s lokala kundtjänstrepresentant. Med vänlig hälsning, Olof Bachman Tender, Customer Care & RA/QA Manager 1. Bilaga 1: Text som ska läggas till i bruksanvisningen till LifeStream Sida 4 av 13
5 REFERENS: FA FORMULÄR FÖR KONTROLL AV SVARSEFFEKTIVITET LifeStream system med ballongexpanderbar vaskulär täckt stent Genom att fylla i informationen nedan bekräftar du att korrigerande säkerhetsåtgärd för marknaden med referensnummer har mottagits av din vårdinrättning eller organisation, att den lästs och förståtts och att begärda åtgärder vidtagits. SKRIV UT kontaktinformationen och fyll i hela formuläret. Namn Titel Kontots/sjukhusets namn [förifyllt fält] Telefonnummer Undertecknat Datum Returnera det ifyllda formuläret till: support.nordic@crbard.com Richard Krantz RA/QA Coordinator Bard Norden AB Tel: , Fax: , richard.krantz@crbard.com Sida 5 av 13
6 Bilaga 1 Förslag till ytterligare text som ska läggas till i dokumentationen för LifeStream Sida 6 av 13
7 Sammanfattning av klinisk studie Totat 155 patienter behandlades på 17 undersökningsplatser i USA, Europa och Nya Zeeland i den prospektiva, icke-randomiserade, enkelarmade multicenterstudien av Bard LifeStream ballongexpanderbar vaskulär täckt stent vid behandling av ocklusionssjukdom i arteria iliaca (BOLSTER). 228 försökspersoner deltog i studien, varav 155 behandlades med den produkt som var studiens föremål och dessa ingick i As Treated-populationen. Målet med denna studie var att bedöma säkerheten och effekten hos Bard LifeStream ballong-expanderbar vaskulär täckt stent för behandling av aterosklerotiska lesioner i arteria iliaca communis och externa. Ett sammansatt säkerhets- och effektmått för försökspersoner som fick Bard LifeStream ballong-expanderbar vaskulär täckt stent jämfördes med ett resultatmål (PG) framtaget från publicerad litteratur om stentning av arteria iliaca. Vid tidpunkten för denna analys hade 155 försökspersoner passerat sitt 9-månadersbesök och utvärderats enligt de primära och sekundära ändpunkterna. Patienterna kommer att följas i 36 månader. Studiens ändpunkter Den primära ändpunkten för studien är ett sammansatt mått på säkerhet och effekt, definierat som dödsfall eller hjärtinfarkt relaterad till produkten och/eller ingreppet fram till och med 30 dagar, eventuell revaskularisering av mållesionen (TLR), amputation av det aktuella benet (benen), eller restenos till och med 9 månader efter indexingreppet. Dödsfall, hjärtinfarkt och amputation av det aktuella benet (benen) relaterat till produkten och/eller ingreppet fastställs av en kommitté för kliniska händelser (CEC). TLR definieras som det första revaskulariseringsingreppet (t.ex. PTA, aterektomi, osv.) på mållesionen(-erna) efter indexingreppet, och fastställs av ett oberoende angiografiskt laboratorium (eller en CEC enligt behov). Restenos bedöms genom duplexultraljud (DUS), där mållesionerna bedöms ha ett maximalt systoliskt flödeshastighetsförhållande (PSVR) > 2,4 med poststenotisk turbulens, enligt bedömning på ett oberoende DUS-laboratorium. I denna studie antyder ett PSVR på > 2,4 > 50 % restenos. De sekundära ändpunkterna inkluderar följande, vilka utvärderas vid olika tidpunkter under studien: (1) Antalet allvarliga komplikationer (MAE), (2) Omedelbar framgång, lesion, (3) Omedelbar framgång, ingrepp, (4) Omedelbar teknisk framgång, (5) revaskularisering av mållesionen (TLR), (6) revaskularisering av målkärlet (TVR), (7) långvarig klinisk framgång, (8) primär öppenhet, (9) primär assisterad öppenhet, (10) sekundär öppenhet och (11) livskvalitet. Studerade patienter De patienter som var kvalificerade för studien hade claudicatio intermittens eller ischemisk smärta vid vila och ny(a) eller restenosisk(a) (icke-stentade) lesion(-er) 50 % (inklusive totalocklusioner) i arteria iliaca communis och/eller externa, bekräftade med angiografi. Kravet för att inkluderas i studien var att referenskärlet skulle vara mellan 4,5 och 12,0 mm i diameter och mållesionerna 100 mm i kombinerad längd (per sida). Patienterna skulle ha angiografiskt bevis på patent profunda och/eller ytlig arteria femoralis. Patienter som tidigare fått ett vaskulärt graft i det nativa iliac-kärlet eller drabbats av hemorragisk stroke eller TIA (transient ischemic attack) inom 3 månader före indexingreppet uteslöts. Metoder Kvalificerade försökspersoner ansågs som deltagare i studien när de hade gett medgivande till att delta. När de hade behandlats med LifeStream ballong-expanderbar vaskulär täckt stent Sida 7 av 13
8 genomfördes kliniska uppföljningar vid utskrivning, efter 30 dagar samt 9, 12, 24 och 36 månader efter indexingreppet. Uppföljningsbesöken omfattade en fullständig fysisk undersökning, duplexultraljud, Rutherford-klassificering, ABI-mätning och livskvalitetsbedömning bland annat. En telefon-screening för alla behandlade försökspersoner genomfördes vid 6 månader efter ingreppet. En oberoende kommitté för kliniska händelser (CEC) granskade alla komplikationer och fastställde alla allvarliga, oväntade och produktrelaterade komplikationer. Dessutom granskades säkerhetsinformation av en oberoende datasäkerhetsövervakningsgrupp (DSMB) inklusive händelser som rapporterats på plats och sammanfattningar av CEC:s bedömningsaktiviteter. DSMB fastställde och utfärdade rekommendationer om huruvida studien skulle fortsätta enligt beskrivningen eller om ändringar skulle genomföras. Resultat Patientdemografi I tabellerna 1 4 sammanfattas patientdemografi, anamnes, basegenskaper och behandlade mållesioner. Tabell 1: Patientdemografi Bolster (N=155) Ålder (år) N 155 Medel (SD) 64,3 (9,75) Min Max 42,0 86,0 Kön Man 107 (69,0 %) Kvinna 48 (31,0 %) Vikt (kg) N 151 Medel (SD) 79,6 (16,60) Längd (cm) N 154 Medel (SD) 170,7 (8,80) BMI (kg/m2) N 151 Medel (SD) 27,2 (4,81) Sida 8 av 13
9 Tabell 2: Patientens anamnes Kategori Benämning Bolster (N=155) Hjärt-kärlsjukdom Totalt 142 (91,6 %) Aortabråck, buk (AAA) 7 (4,5 %) Kärlkramp (Angina pectoris) 11 (7,1 %) Aortasjukdom 7 (4,5 %) Förmaksflimmer (A-FIB) 12 (7,7 %) Hjärtsvikt (CHF) 9 (5,8 %) Kransartärsjukdom (CAD) 49 (31,6 %) Dyslipidemi 101 (65,2 %) Högt blodtryck 117 (75,5 %) Hjärtinfarkt (MI) 21 (13,5 %) Stroke 8 (5,2 %) Övrigt 54 (34,8 %) Njursjukdom Totalt 27 (17,4 %) Hemodialys 1 (0,6 %) Njursvikt 3 (1,9 %) Övrigt 27 (17,4 %) Andra sjukdomar Totalt 152 (98,1 %) Cancer 13 (8,4 %) Rökning (cigaretter) 132 (85,2 %) Diabetes 50 (32,3 %) Mag-tarmsjukdom 17 (11,0 %) Luftvägssjukdom 23 (14,8 %) Övrigt 78 (50,3 %) Anmärkning: En försöksperson kan ta flera läkemedel Tabell 3: Sammanfattning av baseline-egenskaper per försöksperson Behandlad extremitet Bolster (N=155) Bilateralt 34 (21,9 %) Vänster ben 72 (46,5 %) Höger ben 49 (31,6 %) Antal mållesioner (75,5 %) 2 34 (21,9 %) 3 4 (2,6 %) Mållesionens placering Arteria iliaca communis 103 (66,5 %) Arteria iliaca externa 36 (23,2 %) Både arteria iliaca communis och externa 16 (10,3 %) Antal behandlade lesionsplatser (71,6 %) 2 40 (25,8 %) 3 4 (2,6 %) Behandlad lesionsplats Vänster Arteria iliaca communis 83 (53,5 %) Höger Arteria iliaca communis 65 (41,9 %) Vänster Arteria iliaca externa 30 (19,4 %) Höger Arteria iliaca externa 25 (16,1 %) Baseline/stenos före ingreppet 1 Ocklusion 21 (13,5 %) Stenos 134 (86,5 %) Baseline TASC-poäng 2 A 96 (61,9 %) B 42 (27,1 %) C 15 (9,7 %) D 2 (1,3 %) 1,2 Om en försöksperson har fler än en lesion används den allvarligaste typen som kategori för baseline/stenos före ingreppet och för baseline TASC-poängen. Sida 9 av 13
10 När analysen genomfördes hade 197 lesioner behandlats med LifeStream ballongexpanderbar vaskulär täckt stent. I tabell 4 visas egenskaperna för de lesioner som behandlades. Tabell 4: Sammanfattning av mållesioner Förkalkningsgrad Bolster (N=155) Ingen 19 / 197 (9,6 %) Mild 51 / 197 (25,9 %) Måttlig 89 / 197 (45,2 %) Allvarlig 38 / 197 (19,3 %) Mållesionens längd (mm) N 197 Medel (SD) 30,7 (17,35) Min Max 3,0-100,0 Referenskärlets diameter (mm) N 197 Medel (SD) 8,0 (1,27) Min Max 5,0-12,0 Stenos i mållesionen (före ingreppet) % N 197 Medel (SD) 80,3 (13,60) Min Max 30,0-100,0 Enligt rapport från undersökningsplatsen. Patientansvar Försökspersonalen behandlade 155 patienter på 17 olika platser. I en förspecificerad analys var 130 försökspersoner utvärderbara vid 9 månader. En post hoc-analys genomfördes baserat på 138 försökspersoner. Primära effektresultat Den primära ändpunkten för studien är ett sammansatt mått på säkerhet och effekt, definierat som dödsfall eller hjärtinfarkt relaterad till produkten och/eller ingreppet fram till och med 30 dagar, eventuell revaskularisering av mållesionen (TLR), amputation av det aktuella benet (benen), eller restenos till och med 9 månader efter indexingreppet. Den primära sammansatta ändpunkten analyserades per försöksperson. Andelen försökspersoner med dessa effekthändelser jämfördes med resultatmålet på 19,5 %. Restenos fastställdes av DUS-laboratoriet baserat på objektiva mått för DUS-bilddiagnostik och baserades inte på andra typer av bilddiagnostik, behov av ny intervention eller andra kliniska faktorer för att avgöra lesionernas öppenhet efter behandling med LifeStream -produkten. I en förhandsspecificerad analys av de 155 försökspersonerna som behandlades i studien uteslöts totalt 25 försökspersoner från 9-månadersanalysen. 17 av dessa försökspersoner uteslöts av orsaker som icke-bedömningsbar bilddiagnostik, förlorat kontakt för uppföljning före 9-månadersbedömningen eller tidigt avbrott. 8 försökspersoner missade sitt 9-månadersbesök, eller hade ingen utvärderingsbar bilddiagnostik och hade vid tidpunkten för denna analys genomfört sitt 12-månadersbesök. Sida 10 av 13
11 Tabell 5: Resultat för primär sammansatt ändpunkt (förhandsspecificerad analys) Bolster (N=155) 93,3 % konfidensintervall Försökspersoner med komplikationer enl. primär ändpunkt 21/130 (16,2 %) (10,6 %, 23,2 %) Försökspersoner som underkänts pga. Dödsfall relaterat till produkt och/eller ingrepp (<=30 dagar) 0 / 130 (0,0 %) Hjärtinfarkt relaterad till produkt och/eller ingrepp (<=30 dagar) 0 / 130 (0,0 %) Amputation av ben till och med 9 månader* 1/ 130 (0,8 %) TLR till och med 9 månader 6 / 130 (4,6 %) Restenos t.o.m. 9 månader 15 / 130 (11,5 %) * inte relaterat till produkt och/eller ingrepp Enligt analys baserad på förhandsspecifikationer var resultatet för den primära sammansatta ändpunkten 16,2 % (p-värde 0,1987) och uppfyllde inte det fördefinierade statistiska resultatmålet. En post hoc-analys utfördes. Denna analys omfattade de 8 försökspersoner som missade eller inte hade bedömningsbara bilder vid sitt 9-månadersbesök, men kunde utvärderas vid 12-månadersbesöket. Mållesionerna hos alla 8 fastställdes av DUS-laboratoriet som öppna. Dessutom bedömdes mållesionerna hos 5 försökspersoner som öppna vid 9-månadersanalysen av CEC-ordföranden, baserat på en granskning av DUS-bilddiagnostiken inklusive bedömning av ytterligare tillgänglig bilddiagnostik, status för ny intervention, förbättringar i Rutherford-kategori samt andra kliniska faktorer. I tabell 6 visas resultaten av denna post hocanalys, där mållesionerna hos alla dessa 13 försökspersoner bedömdes som öppna. Tabell 6: Resultat för primär sammansatt ändpunkt (post hoc-analys) Bolster (N=155) 93,3 % konfidensintervall 1 Försökspersoner med komplikationer enl. primär ändpunkt 16 / 138 (11,6 %) (7,0 %, 17,8 %) Försökspersoner som underkänts pga. Hjärtinfarkt relaterad till produkt och/eller ingrepp (<=30 dagar) 0 / 138 (0,0 %) Hjärtinfarkt relaterad till produkt och/eller ingrepp (<=30 dagar) 0 / 138 (0,0 %) Amputation av ben t.o.m. 9 månader 2 1/ 138 (0,7 %) TLR till och med 9 månader 6 / 138 (4,3 %) Restenos t.o.m. 9 månader 10 / 138 (7,2 %) 1 Konfidensintervallen har inte justerats enligt multiplicitet och tillhandahålls för att illustrera variabiliteten hos motsvarande sammanfattningsstatistik. De ska inte användas för att dra statistiska slutsatser. 2 Inte relaterat till produkt och/eller ingrepp Den primära sammansatta ändpunkten baserat på post hoc-analysen med hjälp av 12-månadersbedömning och ytterligare kliniska faktorer var 11,6 %. Analys per extremitet Baserat på förhandsspecifikationerna bedöms den primära sammansatta ändpunkten per extremitet vara 21/157 = 13,4 %. Baserat på post hoc-analysen bedöms den primära sammansatta ändpunkten per extremitet vara 16/168 = 9,5 %. Sekundära effektresultat I tabell 7 och 8 nedan ges en sammanfattning av de sekundära ändpunkterna för effekt vid tidpunkten för denna analys. Sida 11 av 13
12 Sannolikhet för överlevnad Tabell 7: Sekundära effektresultat (förhandsspecificerad analys) Resultat N 95 % konfidensintervall 1 Andel allvarliga komplikationer (MAE) 4,7 % (1,9 %, 9,4 %) Omedelbar framgång, lesion 98,4 % (95,5 %, 99,7 %) Omedelbar framgång, ingrepp 97,4 % (93,4 %, 99,3 %) Omedelbar framgång, teknisk 98,3 % (95,6 %, 99,5 %) Revaskularisering av mållesion (TLR) 4,0 % (1,5 %, 8,5 %) Revaskularisering av målkärlet (TVR) 4,0 % (1,5 %, 8,5 %) Långvarig klinisk framgång 90,5 % (84,3 %, 94,9 %) Primär öppenhet 84,5 % (77,1 %, 90,3 %) Primär assisterad öppenhet 85,3 % (78,0 %, 90,9 %) Sekundär öppenhet 87,5 % (80,5 %, 92,7 %) Tabell 8: Sekundära ändpunkter för effekt (post hoc-analys) Resultat N 95 % konfidensintervall 1 Primär öppenhet 89,1 % (82,6 %, 93,7 %) Primär assisterad öppenhet 89,8 % (83,4 %, 94,3 %) Sekundär öppenhet 91,9 % (86,0 %, 95,9 %) 1 Konfidensintervallen har inte justerats enligt multiplicitet och tillhandahålls för att illustrera variabiliteten hos motsvarande sammanfattningsstatistik. De ska inte användas för att dra statistiska slutsatser. 2 Alla försökspersoner följdes till och med dag Alla behandlade lesioner/försökspersoner/stentar med bedömningsbar angiografisk bilddiagnostik vid implantering 4 Alla försökspersoner som genomförde 9-månadersbesöket där Rutherford-kategori bedömdes av försöksledaren 5 Alla försökspersoner som genomförde 9-månadersbesöket med bedömningsbart duplexultraljud 6 Alla försökspersoner som genomförde 9-månadersbesöket och/eller 12-månadersbesöket med bedömningsbart duplexultraljud Kaplan-Meier-analysen av TLR per försöksperson utfördes och resultaten tillhandahålls i figur 3. Kaplan-Meierberäkningen av TLR vid 9 månader (dag 300) var 3,9 % (95 % CI 1,8 %, 8,6 %). Figur 3: Kaplan-Meier-analys av TLR per försöksperson (As Treated-population) Tid till händelsen (dagar) Livskvalitet bedömdes med hjälp av WIQ-enkäten (Walking Impairment Questionnair). Genomsnittlig baseline för totalpoäng var 32,0. Vid 9 månader var den genomsnittliga totalpoängen 64,7 vilket representerar en ökning över baseline för totalpoäng på 32,7. Överlag sågs förbättringar i alla delar av WIQ-enkäten. Sida 12 av 13
13 Sammanfattning av säkerhet Av de 155 försökspersonerna rapporterade 110 personer (71,0 %) 299 komplikationer (AE). Sextio (60) försökspersoner rapporterade allvarliga komplikationer (60/110 = 54,5 %). Majoriteten av försökspersonerna hade komplikationer som inte var relaterade till produkten (86/110; 78,2 %) och/eller relaterade till ingreppet (81/110; 73,6 %). Inga oväntade komplikationer relaterade till produkten rapporterades (UADE). Tabell 9: Sammanfattning av säkerhet Totalt antal händelser 299 Bolster (N=155) Rapporterade på plats Totalt antal försökspersoner med minst en AE 110 (71,0 %) Grad av relation till produkten 1,2 Definitivt relaterad 8 (7,3 %) Möjligen relaterad 16 (14,5 %) Inte relaterad 86 (78,2 %) Grad av relation till ingreppet 1,2 Definitivt relaterad 20 (18,2 %) Möjligen relaterad 9 (8,2 %) Inte relaterad 81 (73,6 %) Allvarlig AE (SAE) 1 60 (54,5 %) SAE, definitivt eller möjligen relaterad till produkten 9 (15,0 %) Inte produktrelaterad SAE 51 (85,0 %) 1 Försökspersonerna räknas endast en gång med den högsta graden av relation. 2 Procentandelarna baseras på nämnaren 110, det totala antalet försökspersoner med minst 1 AE. De typer av säkerhetsrelaterade händelser som upplevdes i studien är väntade för denna patientpopulation. Alla produkt- och ingreppsrelaterade komplikationer som rapporterades var av de typer som identifierades i avsnitt F Potentiella komplikationer. Överlag förefaller komplikationsprofilerna jämförbara med omvårdnadsstandard för PTA och stentning av arteria iliaca. Sammanfattning av mortalitet Fem försökspersoner har avlidit fram till denna rapports datum. Inget av dödsfallen ansågs relaterade till den studerade produkten eller ingreppet, enligt CEC:s bedömning. Slutsatser av studien Den prospektiva, icke-randomiserade, enkelarmade multicenterstudien av Bard LifeStream ballongexpanderbar vaskulär täckt stent vid behandling av ocklusionssjukdom i arteria iliaca (BOLSTER) jämförde ett sammanställt mått på säkerhet och effekt med ett resultatmål (PG) framtaget från publicerad litteratur om stentning av arteria iliaca. Vid tidpunkten för denna analys hade 155 försökspersoner passerat sitt 9-månadersbesök och utvärderats enligt de primära och sekundära ändpunkterna. De typer av säkerhetsrelaterade händelser som upplevdes i studien är väntade för denna patientpopulation. Överlag förefaller komplikationsprofilerna jämförbara med omvårdnadsstandard för PTA och stentning av arteria iliaca. Resultaten av den kliniska studien visar på säkerheten och effektiviteten hos LifeStream ballong-expanderbar vaskulär täckt stent för behandling av arterosklerotiska lesioner i arteria iliaca communis eller externa. Sida 13 av 13
VIKTIGT SÄKERHETSMEDDELANDE Ref /10/ R LÄS IGENOM NOGGRANT. Greatbatch Medical Offset Reamer Handle
 VIKTIGT SÄKERHETSMEDDELANDE Ref-3004976965-10/10/16-003-R LÄS IGENOM NOGGRANT Greatbatch Medical Offset Reamer Handle Offset Reamer Handle Offset Reamer Handle Katalognummer Modell 00-7804-080-00 T5766
VIKTIGT SÄKERHETSMEDDELANDE Ref-3004976965-10/10/16-003-R LÄS IGENOM NOGGRANT Greatbatch Medical Offset Reamer Handle Offset Reamer Handle Offset Reamer Handle Katalognummer Modell 00-7804-080-00 T5766
BRÅDSKANDE: Säkerhetsmeddelande för marknaden
 5 juli 2011 BRÅDSKANDE: Säkerhetsmeddelande för marknaden Berörd produkt: HMRS-Distal femur resektionskomponent samt distal femur komponent. FSCA-identifiering: Åtgärd för produkter på marknaden RA 2009-436
5 juli 2011 BRÅDSKANDE: Säkerhetsmeddelande för marknaden Berörd produkt: HMRS-Distal femur resektionskomponent samt distal femur komponent. FSCA-identifiering: Åtgärd för produkter på marknaden RA 2009-436
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Mon-a-Therm Foley-kateter med temperatursensor
 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Mon-a-Therm Foley-kateter med temperatursensor Augusti 2018 Medtronic-referens: FA835 Till: Chefen för riskhantering och chefen för materialhantering Bästa kund:
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Mon-a-Therm Foley-kateter med temperatursensor Augusti 2018 Medtronic-referens: FA835 Till: Chefen för riskhantering och chefen för materialhantering Bästa kund:
VIKTIGT MEDDELANDE TILL MARKNADEN: RA2011-161
 VIKTIGT MEDDELANDE TILL MARKNADEN: RA2011-161 «ShipTo_Customer_Name» «Contact _Name» «ShipTo_Address_1» «ShipTo_Address_2_» «ShipTo_Address_3_» «SHIPTOCITY», «SHIPTOST» «SHIPTOZIP» Bäste kund, Beskrivning:
VIKTIGT MEDDELANDE TILL MARKNADEN: RA2011-161 «ShipTo_Customer_Name» «Contact _Name» «ShipTo_Address_1» «ShipTo_Address_2_» «ShipTo_Address_3_» «SHIPTOCITY», «SHIPTOST» «SHIPTOZIP» Bäste kund, Beskrivning:
Viktigt säkerhetsmeddelande till marknaden (återkallelse)
 Viktigt säkerhetsmeddelande till marknaden (återkallelse) beträffande CORAIL COXA VARA HIGH OFFSET STEM med krage, storlek 9 (artikelnummer: 3L93709, tillverkningssats: 5291990) och CORAIL HIGH OFFSET
Viktigt säkerhetsmeddelande till marknaden (återkallelse) beträffande CORAIL COXA VARA HIGH OFFSET STEM med krage, storlek 9 (artikelnummer: 3L93709, tillverkningssats: 5291990) och CORAIL HIGH OFFSET
Brådskande fältsäkerhetsmeddelande Viktig information om medicinteknisk produkt
 VASCUTEK Ltd Newmains Avenue, Inchinnan, Renfrewshire, PA4 9RR, Skottland, Storbritannien Tel: +44 (0) 141 812 5555 www.vascutek.com 30 oktober 2017 Till: Kärlkirurger, radiologer, riskansvariga, upphandling,
VASCUTEK Ltd Newmains Avenue, Inchinnan, Renfrewshire, PA4 9RR, Skottland, Storbritannien Tel: +44 (0) 141 812 5555 www.vascutek.com 30 oktober 2017 Till: Kärlkirurger, radiologer, riskansvariga, upphandling,
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN
 Teleflex Medical IDA Business & Technology Park Dublin Road, Athlone Westmeath, Irland VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN 21 september 2018 Typ av åtgärd Återkallning Teleflex-referens: EIF-000291
Teleflex Medical IDA Business & Technology Park Dublin Road, Athlone Westmeath, Irland VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN 21 september 2018 Typ av åtgärd Återkallning Teleflex-referens: EIF-000291
Om du har frågor, kontakta din lokala representant för Biosense Webster, Inc.
 VIKTIGT SÄKERHETSMEDDELANDE ÅTERKALLANDE AV MEDICINSK ENHET MOBICATH Bi-Directional Guiding Sheath Arikelnummer: D140010 och D140011 Lotnummer: Se bilaga 15 februari, 2017 Bästa kund, Greatbatch Medical,
VIKTIGT SÄKERHETSMEDDELANDE ÅTERKALLANDE AV MEDICINSK ENHET MOBICATH Bi-Directional Guiding Sheath Arikelnummer: D140010 och D140011 Lotnummer: Se bilaga 15 februari, 2017 Bästa kund, Greatbatch Medical,
VIKTIGT SÄKERHETSMEDDELANDE: RA
 2013-08-30 VIKTIGT SÄKERHETSMEDDELANDE: RA2013-104 FSCA-identifiering: Produktåtgärd på marknaden RA 2013-104 Typ av åtgärd: Beskrivning: Korrigerande säkerhetsåtgärd på marknaden Katalognr.: Se den bifogade
2013-08-30 VIKTIGT SÄKERHETSMEDDELANDE: RA2013-104 FSCA-identifiering: Produktåtgärd på marknaden RA 2013-104 Typ av åtgärd: Beskrivning: Korrigerande säkerhetsåtgärd på marknaden Katalognr.: Se den bifogade
Viktigt säkerhetsmeddelande till marknaden
 Viktigt säkerhetsmeddelande till marknaden Produktnamn: ADEPT Hip Resurfacing System (Finsbury Orthopaedics Ltd) FSCA-ID: DVA-108558-HHE Typ av åtgärd: Säkerhetsmeddelande till marknaden Datum: januari
Viktigt säkerhetsmeddelande till marknaden Produktnamn: ADEPT Hip Resurfacing System (Finsbury Orthopaedics Ltd) FSCA-ID: DVA-108558-HHE Typ av åtgärd: Säkerhetsmeddelande till marknaden Datum: januari
Viktigt säkerhetsmeddelande till marknaden Viktig information om medicinsk enhet Imager II Angiographic Catheter
 Boston Scientific International S.A. ZAC Paris Nord II/Bât Emerson - 33 rue des Vanesses 93420 Villepinte Siège social : Parc du Val Saint Quentin 2 rue René Caudron 78960 Voisins le Bretonneux France
Boston Scientific International S.A. ZAC Paris Nord II/Bât Emerson - 33 rue des Vanesses 93420 Villepinte Siège social : Parc du Val Saint Quentin 2 rue René Caudron 78960 Voisins le Bretonneux France
VIKTIGT SÄKERHETSMEDDELANDE: RA
 20 januari 2014 VIKTIGT SÄKERHETSMEDDELANDE: RA 2014-126 FSCA-identifiering: Åtgärd för produkter på marknaden RA 2014-126 Juridisk tillverkare: Stryker Leibinger GmbH & Co. KG, Boetzingerstraße 41, 79111
20 januari 2014 VIKTIGT SÄKERHETSMEDDELANDE: RA 2014-126 FSCA-identifiering: Åtgärd för produkter på marknaden RA 2014-126 Juridisk tillverkare: Stryker Leibinger GmbH & Co. KG, Boetzingerstraße 41, 79111
Diane huvudversion av patientkort och checklista för förskrivare 17/12/2014. Patientinformationskort:
 Patientinformationskort: Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de
Patientinformationskort: Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de
Bilaga III Ändringar av produktresumé och märkning
 Bilaga III Ändringar av produktresumé och märkning Anm.: Dessa ändringar av produktresumén och bipacksedeln gäller vid tidpunkten för kommissionens beslut. Efter kommissionens beslut kommer behöriga myndigheter
Bilaga III Ändringar av produktresumé och märkning Anm.: Dessa ändringar av produktresumén och bipacksedeln gäller vid tidpunkten för kommissionens beslut. Efter kommissionens beslut kommer behöriga myndigheter
VIKTIGT SÄKERHETSMEDDELANDE: RA
 Datum 28/12/12 «ShipTo_Customer_Name» «Contact _Name» «ShipTo_Address_1» «ShipTo_Address_2_» «ShipTo_Address_3_» «SHIPTOCITY», «SHIPTOST» «SHIPTOZIP» VIKTIGT SÄKERHETSMEDDELANDE: RA2012-138 Beskrivning:
Datum 28/12/12 «ShipTo_Customer_Name» «Contact _Name» «ShipTo_Address_1» «ShipTo_Address_2_» «ShipTo_Address_3_» «SHIPTOCITY», «SHIPTOST» «SHIPTOZIP» VIKTIGT SÄKERHETSMEDDELANDE: RA2012-138 Beskrivning:
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN KORRIGERING
 13 november 2017 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Till: Ämne: Kirurger/sjukhus VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN KORRIGERING Referens: ZFA 2017-425 Berörda produkter: Bone Cement och
13 november 2017 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Till: Ämne: Kirurger/sjukhus VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN KORRIGERING Referens: ZFA 2017-425 Berörda produkter: Bone Cement och
10 januari, 2018 BRÅDSKANDE: VIKTIGT SÄKERHETSMEDDELANDE GÄLLANDE PRODUKTERNA TISSU-TRANS
 10 januari, 2018 BRÅDSKANDE: VIKTIGT SÄKERHETSMEDDELANDE GÄLLANDE PRODUKTERNA TISSU-TRANS Bästa kund/distributör av enheten, Syftet med detta brev är att göra dig uppmärksam på att Shippert Medical Technologies
10 januari, 2018 BRÅDSKANDE: VIKTIGT SÄKERHETSMEDDELANDE GÄLLANDE PRODUKTERNA TISSU-TRANS Bästa kund/distributör av enheten, Syftet med detta brev är att göra dig uppmärksam på att Shippert Medical Technologies
VIKTIGT SÄKERHETSMEDDELANDE Korrigering av medicinteknisk produkt Säkerhetsmeddelande till marknaden
 Therapeutic Care -1/6- FSN86600042A 30-aug-2019 VIKTIGT SÄKERHETSMEDDELANDE Korrigering av medicinteknisk produkt Säkerhetsmeddelande till marknaden Philips V60-ventilatorer kan ha en icke-responsiv pekskärm
Therapeutic Care -1/6- FSN86600042A 30-aug-2019 VIKTIGT SÄKERHETSMEDDELANDE Korrigering av medicinteknisk produkt Säkerhetsmeddelande till marknaden Philips V60-ventilatorer kan ha en icke-responsiv pekskärm
Produktnamn Referensnummer GPN Partinummer IP-7110 G20254 IP-S7010 IP-S7110 IP-S9010 G26438 IP-S9110
 COOK Cook Medical Europe O Halloran Road, National Technological park, Limerick, Irland. Tel: + 353 61 334440 Viktigt säkerhetsmeddelande till marknaden Fax: + 353 61 334441 Handelsnamn för den berörda
COOK Cook Medical Europe O Halloran Road, National Technological park, Limerick, Irland. Tel: + 353 61 334440 Viktigt säkerhetsmeddelande till marknaden Fax: + 353 61 334441 Handelsnamn för den berörda
Viktigt säkerhetsmeddelande
 IMMULITE 2500 Viktigt säkerhetsmeddelande FSCA IMC 13-06B/3510 Mars 2013 IMMULITE 2500 IGF-I förskjutning i patientmedianer Enligt våra noteringar har du mottagit följande produkt: Tabell 1. Produkt Katalognummer
IMMULITE 2500 Viktigt säkerhetsmeddelande FSCA IMC 13-06B/3510 Mars 2013 IMMULITE 2500 IGF-I förskjutning i patientmedianer Enligt våra noteringar har du mottagit följande produkt: Tabell 1. Produkt Katalognummer
Viktigt säkerhetsmeddelande
 ADVIA Centaur -systemen Dimension Vista -systemen IMMULITE -systemen CC 16-03.A.OUS Januari 2016 Korsreaktivitet för fulvestrant i Siemens Healthcares östradiolanalyser Enligt våra noteringar kan ditt
ADVIA Centaur -systemen Dimension Vista -systemen IMMULITE -systemen CC 16-03.A.OUS Januari 2016 Korsreaktivitet för fulvestrant i Siemens Healthcares östradiolanalyser Enligt våra noteringar kan ditt
Viktigt säkerhetsmeddelande
 Kära kund, Som en del av Samsung Electronics kontinuerliga fokus på prestanda och säkerhet, har vi identifierat ett potentiellt problem som kan påverka Samsungs digitala röntgensystem GC80, GC85 och GC70.
Kära kund, Som en del av Samsung Electronics kontinuerliga fokus på prestanda och säkerhet, har vi identifierat ett potentiellt problem som kan påverka Samsungs digitala röntgensystem GC80, GC85 och GC70.
12 juni, 2017 VIKTIGT! SÄKERHETSMEDDELANDE TILL MARKNADEN TISSU-TRANS-PRODUKTER
 12 juni, 2017 VIKTIGT! SÄKERHETSMEDDELANDE TILL MARKNADEN TISSU-TRANS-PRODUKTER Bästa kund/distributör! Syftet med detta brev är att informera om att Shippert Medical Technologies utfärdar ett säkerhetsmeddelande
12 juni, 2017 VIKTIGT! SÄKERHETSMEDDELANDE TILL MARKNADEN TISSU-TRANS-PRODUKTER Bästa kund/distributör! Syftet med detta brev är att informera om att Shippert Medical Technologies utfärdar ett säkerhetsmeddelande
Viktigt säkerhetsmeddelande till marknaden
 Viktigt säkerhetsmeddelande till marknaden Den berörda produktens marknadsnamn: Aptio Automation FSCA-identifierare: FSCA AP2 201808 03 FSN-identifierare: FSN AP2 201808 Datum: augusti 2018 Information
Viktigt säkerhetsmeddelande till marknaden Den berörda produktens marknadsnamn: Aptio Automation FSCA-identifierare: FSCA AP2 201808 03 FSN-identifierare: FSN AP2 201808 Datum: augusti 2018 Information
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN
 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN PLATINIUM: periodisk kontaktförlust på DF-4 kontakten FSCA ID: Affected Devices: CRM-SAL-2017-001 Date: 16. Mars, 2018 Attention: Platinium implanterbara hjärtdefibrillatorer
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN PLATINIUM: periodisk kontaktförlust på DF-4 kontakten FSCA ID: Affected Devices: CRM-SAL-2017-001 Date: 16. Mars, 2018 Attention: Platinium implanterbara hjärtdefibrillatorer
BRÅDSKANDE: SÄKERHETSMEDDELANDE
 14 september 2015 BRÅDSKANDE: SÄKERHETSMEDDELANDE Berörda enheter: Alla serienummer av systemstyrenheten HeartMate II, modell nr. 105109 (Pocket Controller TM ), som levereras inom följande förpackningskonfigurationer:
14 september 2015 BRÅDSKANDE: SÄKERHETSMEDDELANDE Berörda enheter: Alla serienummer av systemstyrenheten HeartMate II, modell nr. 105109 (Pocket Controller TM ), som levereras inom följande förpackningskonfigurationer:
Återkallande av medicintekniska produkter
 VIKTIGT säkerhetsmeddelande till marknaden pro med instruments GmbH, Boetzinger Str. 38, 79111 Freiburg, Tyskland Företag Kontaktperson Gatuadress Postnummer, ort, land Telefon, e-postadress Återkallande
VIKTIGT säkerhetsmeddelande till marknaden pro med instruments GmbH, Boetzinger Str. 38, 79111 Freiburg, Tyskland Företag Kontaktperson Gatuadress Postnummer, ort, land Telefon, e-postadress Återkallande
14 november 2016 BRÅDSKANDE Viktigt säkerhetsmeddelande Bridge ocklusionsballong
 «Attention» «Hospital» «AddressBlock» Bäste kund! 14 november 2016 BRÅDSKANDE Viktigt säkerhetsmeddelande Bridge ocklusionsballong Syftet med detta brev är att informera dig om att Spectranetics återkallar
«Attention» «Hospital» «AddressBlock» Bäste kund! 14 november 2016 BRÅDSKANDE Viktigt säkerhetsmeddelande Bridge ocklusionsballong Syftet med detta brev är att informera dig om att Spectranetics återkallar
VIKTIGT SÄKERHETSMEDDELANDE
 Teleflex Medical IDA Business & Technology Park Dublin Road, Athlone Co. Westmeath, Irland 07 Jan 2010 VIKTIGT SÄKERHETSMEDDELANDE Den berörda produktens kommersiella namn: Typ av åtgärd: Produktnummer:
Teleflex Medical IDA Business & Technology Park Dublin Road, Athlone Co. Westmeath, Irland 07 Jan 2010 VIKTIGT SÄKERHETSMEDDELANDE Den berörda produktens kommersiella namn: Typ av åtgärd: Produktnummer:
Att: Laboratoriechefen. Viktigt säkerhetsmeddelande. Beskrivning av problemet: Uppdatering av användarhandboken:
 Agilent Technologies Denmark ApS Produktionsvej 42 2600 Glostrup Danmark +45 44 85 95 00, telefon www.agilent.com CVR: 21852902 Att: Laboratoriechefen «Account_Name» «Shipped-to account no.» «Address1»
Agilent Technologies Denmark ApS Produktionsvej 42 2600 Glostrup Danmark +45 44 85 95 00, telefon www.agilent.com CVR: 21852902 Att: Laboratoriechefen «Account_Name» «Shipped-to account no.» «Address1»
Säkerhetsmeddelande (Återkallande) Alla partier av DePuy Synthes Reach System Handle-instrument. Delnummer:
 Säkerhetsmeddelande (Återkallande) Alla partier av DePuy Synthes Reach System Handle-instrument Delnummer 950505154 Produktnamn: Reach System Handle-instrument FSCA-identifiering: 103189242 (HHE) Typ av
Säkerhetsmeddelande (Återkallande) Alla partier av DePuy Synthes Reach System Handle-instrument Delnummer 950505154 Produktnamn: Reach System Handle-instrument FSCA-identifiering: 103189242 (HHE) Typ av
BRÅDSKANDE SÄKERHETSMEDDELANDE
 CareFusion Switzerland 317 Sàrl A-One Business Centre Z.A. Vers-La-Pièce n 10 1180 Rolle / Switzerland Tel: +41 21 556 30 00 Fax: +41 21 556 30 99 Namn Adress carefusion.com Produktnamn: Produktreferens:
CareFusion Switzerland 317 Sàrl A-One Business Centre Z.A. Vers-La-Pièce n 10 1180 Rolle / Switzerland Tel: +41 21 556 30 00 Fax: +41 21 556 30 99 Namn Adress carefusion.com Produktnamn: Produktreferens:
Viktigt säkerhetsmeddelande
 Viktigt säkerhetsmeddelande 4009/FSCA IMC 14-05 December 2013 IMMULITE IMMULITE 1000 IMMULITE 2000 IMMULITE 2000 XPi Positiv avvikelse av total IgE i förhållande till WHO 2 nd IRP 75/502 Enligt våra noteringar
Viktigt säkerhetsmeddelande 4009/FSCA IMC 14-05 December 2013 IMMULITE IMMULITE 1000 IMMULITE 2000 IMMULITE 2000 XPi Positiv avvikelse av total IgE i förhållande till WHO 2 nd IRP 75/502 Enligt våra noteringar
Viktigt säkerhetsmeddelande till marknaden
 Viktigt säkerhetsmeddelande till marknaden Den berörda produktens marknadsnamn: FlexLab FSCA-identifierare: FSCA FLX 201808 01 FSN-identifierare: FSN FLX 201808 Datum: augusti 2018 Information om berörda
Viktigt säkerhetsmeddelande till marknaden Den berörda produktens marknadsnamn: FlexLab FSCA-identifierare: FSCA FLX 201808 01 FSN-identifierare: FSN FLX 201808 Datum: augusti 2018 Information om berörda
Viktigt säkerhetsmeddelande till marknaden. Senographe Pristina med Serena Biopsipositioneraren kan glida när gantryt roteras under en biopsi.
 Viktigt säkerhetsmeddelande till marknaden 3000 N. Grandview Blvd. - W440 Waukesha, WI 53188 USA 29 maj 2019 internref.: FMI 12283 Till: Betr: Chefen för bröstavbildning Radiologichef Medicinskteknisk
Viktigt säkerhetsmeddelande till marknaden 3000 N. Grandview Blvd. - W440 Waukesha, WI 53188 USA 29 maj 2019 internref.: FMI 12283 Till: Betr: Chefen för bröstavbildning Radiologichef Medicinskteknisk
ANSELL SANDEL SÄKERHETSSKALPELL MED VIKT FSCA-2013/11/80
 Brevhuvud Ansell EU --------------------------------------------------------------------------------------------------------------------------- Viktigt säkerhetsmeddelande ANSELL SANDEL SÄKERHETSSKALPELL
Brevhuvud Ansell EU --------------------------------------------------------------------------------------------------------------------------- Viktigt säkerhetsmeddelande ANSELL SANDEL SÄKERHETSSKALPELL
BRÅDSKANDE: FÄLTSÄKERHETSMEDDELANDE
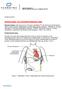 23 februari 2012 BRÅDSKANDE: FÄLTSÄKERHETSMEDDELANDE Berörda enheter: Alla lotnummer av Thoratec HeartMate II Left Ventricular Assist System (HM II LVAS) Förslutet utflödesgraft med böjningsavlastare (katalognr.
23 februari 2012 BRÅDSKANDE: FÄLTSÄKERHETSMEDDELANDE Berörda enheter: Alla lotnummer av Thoratec HeartMate II Left Ventricular Assist System (HM II LVAS) Förslutet utflödesgraft med böjningsavlastare (katalognr.
VIKTIGT: SÄKERHETSMEDDELANDE. Externa nätaggregat för RENASYS GO. SÄKERHETSMEDDELANDE: 19 februari 2016
 Smith & Nephew, Inc. 970 Lake Carillon Dr, Suite 300 St. Petersburg, FL 33716 USA Kundtjänst: +1 800 876-1261 www.smith-nephew.com 19 februari 2016 Berörd produkt: FSCA-referens: 19 februari 2016 FSCA-åtgärd:
Smith & Nephew, Inc. 970 Lake Carillon Dr, Suite 300 St. Petersburg, FL 33716 USA Kundtjänst: +1 800 876-1261 www.smith-nephew.com 19 februari 2016 Berörd produkt: FSCA-referens: 19 februari 2016 FSCA-åtgärd:
VIKTIGT säkerhetsmeddelande Korrigering av medicinsk utrustning IntelliVue MX40 saknade varningar i bruksanvisning
 Bästa kund, Vi har upptäckt ett problem med bruksanvisningen till Philips IntelliVue MX40 för programvaruversionerna B.05, B.06 och B.06.5X. Din IntelliVue MX40 är fortfarande säker att använda. De här
Bästa kund, Vi har upptäckt ett problem med bruksanvisningen till Philips IntelliVue MX40 för programvaruversionerna B.05, B.06 och B.06.5X. Din IntelliVue MX40 är fortfarande säker att använda. De här
Viktigt säkerhetsmeddelande
 Siemens Healthcare AB. ADVIA Centaur ADVIA Centaur XP ADVIA Centaur XPT ADVIA Centaur CP CC 18-17.A-1.OUS juli 2018 ADVIA Centaur CKMB Kalibratoravvikelse och resultat utanför intervallet vid användning
Siemens Healthcare AB. ADVIA Centaur ADVIA Centaur XP ADVIA Centaur XPT ADVIA Centaur CP CC 18-17.A-1.OUS juli 2018 ADVIA Centaur CKMB Kalibratoravvikelse och resultat utanför intervallet vid användning
Ämne: VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN KORRIGERING Referens: ZFA
 11 maj, 2017 Till: Kirurger Ämne: VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN KORRIGERING Referens: Berörd produkt: T.E.S.S. omvänd krona, T.E.S.S. omvänd Monobloc-humerusstam och tillhörande T.E.S.S. humerusinlägg
11 maj, 2017 Till: Kirurger Ämne: VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN KORRIGERING Referens: Berörd produkt: T.E.S.S. omvänd krona, T.E.S.S. omvänd Monobloc-humerusstam och tillhörande T.E.S.S. humerusinlägg
VIKTIGT SÄKERHETSMEDDELANDE Återkallelse av produkt
 Årstaängsvägen 25 Box 472 04 SE-100 74 Stockholm, Sweden Tel: +46 (0) 8 775 5100 Fax: +46 (0) 8 645 0808 www.bd.com VIKTIGT SÄKERHETSMEDDELANDE Återkallelse av produkt BD referensnummer: FA_11_049_102
Årstaängsvägen 25 Box 472 04 SE-100 74 Stockholm, Sweden Tel: +46 (0) 8 775 5100 Fax: +46 (0) 8 645 0808 www.bd.com VIKTIGT SÄKERHETSMEDDELANDE Återkallelse av produkt BD referensnummer: FA_11_049_102
Viktigt säkerhetsmeddelande till marknaden Viktig information om medicinsk enhet ilab Polaris Systems
 Reference: 92417423-FA 18 september 2019 Viktigt säkerhetsmeddelande till marknaden Viktig information om medicinsk enhet ilab Polaris Systems Bäste «Users_Name», Boston Scientific (BSC) inleder en frivillig
Reference: 92417423-FA 18 september 2019 Viktigt säkerhetsmeddelande till marknaden Viktig information om medicinsk enhet ilab Polaris Systems Bäste «Users_Name», Boston Scientific (BSC) inleder en frivillig
Ekvivalenta doser av betablockerare (peroral administrering)
 Ekvivalenta doser av betablockerare (peroral administrering) Sammanfattning Nedanstående tabell illustrerar genomsnittlig dosekvivalens baserat på gruppnivå. Sotalol utgör referens. Observera att det inte
Ekvivalenta doser av betablockerare (peroral administrering) Sammanfattning Nedanstående tabell illustrerar genomsnittlig dosekvivalens baserat på gruppnivå. Sotalol utgör referens. Observera att det inte
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Litiumjonbatteripaket som används i BIS Vista och BIS View övervakningssystem.
 Augusti 2018 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Litiumjonbatteripaket som används i BIS Vista och BIS View övervakningssystem. Medtronic-referens: FA832 Till: Materialansvarig för operationsavdelningen,
Augusti 2018 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Litiumjonbatteripaket som används i BIS Vista och BIS View övervakningssystem. Medtronic-referens: FA832 Till: Materialansvarig för operationsavdelningen,
Viktigt säkerhetsmeddelande till marknaden ÅTERKALLANDE AV MEDICINTEKNISK PRODUKT GLIDESCOPE VIDEOLARYNGOSKOP TITANIUM-BLAD FÖR ENGÅNGSBRUK
 1 26 februari 2016 www.verathon.com Viktigt säkerhetsmeddelande till marknaden ÅTERKALLANDE AV MEDICINTEKNISK PRODUKT GLIDESCOPE VIDEOLARYNGOSKOP TITANIUM-BLAD FÖR ENGÅNGSBRUK Kära GlideScope-kund, syftet
1 26 februari 2016 www.verathon.com Viktigt säkerhetsmeddelande till marknaden ÅTERKALLANDE AV MEDICINTEKNISK PRODUKT GLIDESCOPE VIDEOLARYNGOSKOP TITANIUM-BLAD FÖR ENGÅNGSBRUK Kära GlideScope-kund, syftet
Viktig frivillig korrigering av märkning på medicinteknisk produkt
 DePuy Synthes Luzernstrasse 21 4528 Zuchwil Schweiz Tel. +41 32 720 40 60 Fax +41 32 720 40 61 http://www.depuysynthes.com/ tt uppmärksammas av: Operationsavdelningschef 28 juli 2014 Viktig frivillig korrigering
DePuy Synthes Luzernstrasse 21 4528 Zuchwil Schweiz Tel. +41 32 720 40 60 Fax +41 32 720 40 61 http://www.depuysynthes.com/ tt uppmärksammas av: Operationsavdelningschef 28 juli 2014 Viktig frivillig korrigering
Delprov 3 Vetenskaplig artikel
 Delprov 3 Vetenskaplig artikel of Questions: 10 Total Exam Points: 10.00 Question #: 1 I denna uppgift ska du besvara ett antal frågor kring en vetenskaplig artikel: Different systolic blood pressure targets
Delprov 3 Vetenskaplig artikel of Questions: 10 Total Exam Points: 10.00 Question #: 1 I denna uppgift ska du besvara ett antal frågor kring en vetenskaplig artikel: Different systolic blood pressure targets
UPPFÖLJNING BRÅDSKANDE SÄKERHETSMEDDELANDE TILL MARKNADEN
 19 december 2013 UPPFÖLJNING BRÅDSKANDE SÄKERHETSMEDDELANDE TILL MARKNADEN Användardefinierade analysspädningsfaktorer, resultatvalidering och hantering av intermediära resultat* med engen Laboratory Automation
19 december 2013 UPPFÖLJNING BRÅDSKANDE SÄKERHETSMEDDELANDE TILL MARKNADEN Användardefinierade analysspädningsfaktorer, resultatvalidering och hantering av intermediära resultat* med engen Laboratory Automation
Berörd produkt: Olika trauma- och extremitetsinstrument (borrar och skruvtappar)
 7 juni, 2017 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Till: Kirurger Ämne: VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN ANGÅENDE MEDICINTEKNISKA PRODUKTER BORTTAGNING, LOTSPECIFIK Berörd produkt: Olika
7 juni, 2017 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Till: Kirurger Ämne: VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN ANGÅENDE MEDICINTEKNISKA PRODUKTER BORTTAGNING, LOTSPECIFIK Berörd produkt: Olika
RA : VIKTIGT SÄKERHETSMEDDELANDE
 RA2009-379: VIKTIGT SÄKERHETSMEDDELANDE Bästa kund Beskrivning: Triathlon Tibial Alignment Handle och Nav Tibial Alignment Handle Produktref: 6541-2-807, 6541-2-808 Lotnr: Se bifogad lista för specifika
RA2009-379: VIKTIGT SÄKERHETSMEDDELANDE Bästa kund Beskrivning: Triathlon Tibial Alignment Handle och Nav Tibial Alignment Handle Produktref: 6541-2-807, 6541-2-808 Lotnr: Se bifogad lista för specifika
VIKTIG FÄLTKORRIGERING AV MEDICINSK ENHET TCAutomation /engen Laboratory Automation Systems
 Bästa kund, VIKTIG FÄLTKORRIGERING AV MEDICINSK ENHET TCAutomation /engen Laboratory Automation Systems 9 april, 2015 Syftet med detta brev är att informera dig om att Thermo Fisher Scientific Oy, en del
Bästa kund, VIKTIG FÄLTKORRIGERING AV MEDICINSK ENHET TCAutomation /engen Laboratory Automation Systems 9 april, 2015 Syftet med detta brev är att informera dig om att Thermo Fisher Scientific Oy, en del
Viktigt säkerhetsmeddelande till marknaden HALYARD CLOSED SUCTION KITS WITH FLEX CONNECTOR
 TILL: AVDELNINGEN FÖR ANDNINGSTERAPI 7 februari 2018 Bästa Halyard Health-kund: Vad är skälet till detta frivilliga produktrådgivande meddelande? Vi har nyligen tagit emot rapporter som visar att vissa
TILL: AVDELNINGEN FÖR ANDNINGSTERAPI 7 februari 2018 Bästa Halyard Health-kund: Vad är skälet till detta frivilliga produktrådgivande meddelande? Vi har nyligen tagit emot rapporter som visar att vissa
VIKTIGT: SÄKERHETSMEDDELANDE TILL MARKNADEN MSS FA. Säkerhetsmeddelande om medicinteknisk produkt BD Plastipak sprutor / BD oralsprutor
 Becton Dickinson GmbH Tullastr. 8-12 69126 Heidelberg Postfach 10 16 29 69006 Heidelberg Tfn: 06221 3050 Fax: 06221 305216 www.bd.com/de Becton Dickinson GmbH Postfach 10 16 29 69006 Heidelberg VIKTIGT:
Becton Dickinson GmbH Tullastr. 8-12 69126 Heidelberg Postfach 10 16 29 69006 Heidelberg Tfn: 06221 3050 Fax: 06221 305216 www.bd.com/de Becton Dickinson GmbH Postfach 10 16 29 69006 Heidelberg VIKTIGT:
1.1 Vilken sjukdom misstänker Du i första hand, ange namnet på svenska (1p) och på latin (1p).
 Du vikarierar i väntan på AT-tjänst på vårdcentralen i Korpilombolo. Din första patient på måndag morgon visar sig vara en manlig renskötare, 66 år, som klagar över att han sedan två veckor tillbaka får
Du vikarierar i väntan på AT-tjänst på vårdcentralen i Korpilombolo. Din första patient på måndag morgon visar sig vara en manlig renskötare, 66 år, som klagar över att han sedan två veckor tillbaka får
VIKTIGT säkerhetsmeddelande till marknaden: RA
 07 februari 2019 VIKTIGT säkerhetsmeddelande till marknaden: RA2018-1976124 FSCA-identifiering: Produktåterkallelse RA2018-1976124 Åtgärdstyp: Korrigerande säkerhetsåtgärd på marknaden Berörda produkter:
07 februari 2019 VIKTIGT säkerhetsmeddelande till marknaden: RA2018-1976124 FSCA-identifiering: Produktåterkallelse RA2018-1976124 Åtgärdstyp: Korrigerande säkerhetsåtgärd på marknaden Berörda produkter:
Viktigt säkerhetsmeddelande
 Viktigt säkerhetsmeddelande Juli 2016 Xprecia Stride koagulationsinstrument CD med datahanteringsprogramvara V1.0 som medföljer vissa instrument Enligt våra noteringar kan ditt laboratorium ha mottagit
Viktigt säkerhetsmeddelande Juli 2016 Xprecia Stride koagulationsinstrument CD med datahanteringsprogramvara V1.0 som medföljer vissa instrument Enligt våra noteringar kan ditt laboratorium ha mottagit
Viktigt säkerhetsmeddelande till marknaden
 Viktigt säkerhetsmeddelande till marknaden MAHURKAR * och Argyle * katetrar för akut hemodialys Maj 2019 Medtronic-referens: FA866 Till läkare och vårdpersonal Med detta brev vill vi meddela dig att Medtronic
Viktigt säkerhetsmeddelande till marknaden MAHURKAR * och Argyle * katetrar för akut hemodialys Maj 2019 Medtronic-referens: FA866 Till läkare och vårdpersonal Med detta brev vill vi meddela dig att Medtronic
VIKTIGT SÄKERHETSMEDDELANDE
 06.01.2015 Produkt: Typ av åtgärd: Produktkoder: Serieintervall #s: Återkallande av Kära HeartWare-läkare, 2013 rekommenderade HeartWare er om åtgärder i samband med patientsäkerhetsrisker förknippade
06.01.2015 Produkt: Typ av åtgärd: Produktkoder: Serieintervall #s: Återkallande av Kära HeartWare-läkare, 2013 rekommenderade HeartWare er om åtgärder i samband med patientsäkerhetsrisker förknippade
VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE
 VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE Handelsnamn: LOT-nr: FSCA-ID: Typ av åtgärd: HandyVac TM lågvakuumsystem för dränering av kirurgiska sår CH (Fr.) 14 HandyVac TM ATS lågvakuumsystem för dränering
VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE Handelsnamn: LOT-nr: FSCA-ID: Typ av åtgärd: HandyVac TM lågvakuumsystem för dränering av kirurgiska sår CH (Fr.) 14 HandyVac TM ATS lågvakuumsystem för dränering
Tillbehörsrem till SAM Junctional Tourniquet (SJT) blodtrycksmanschett 2014/11/06 Modifiering/utbyte/destruktion av enheten
 BRÅDSKANDE SÄKERHETSMEDDELANDE TILL MARKNADEN Tillbehörsrem till SAM Junctional Tourniquet (SJT) blodtrycksmanschett 2014/11/06 Modifiering/utbyte/destruktion av enheten Till SAM Medicals kunder/distributörer
BRÅDSKANDE SÄKERHETSMEDDELANDE TILL MARKNADEN Tillbehörsrem till SAM Junctional Tourniquet (SJT) blodtrycksmanschett 2014/11/06 Modifiering/utbyte/destruktion av enheten Till SAM Medicals kunder/distributörer
Tel Fax
 Datum: 2016-12-30 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN: SÄKERHETSMEDDELANDE OM MEDICINTEKNISK PRODUKT Produktåterkallelse 555531 Radiushuvudprotessystem VÄNLIGEN, SPRID DENNA INFORMATION TILL DEN
Datum: 2016-12-30 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN: SÄKERHETSMEDDELANDE OM MEDICINTEKNISK PRODUKT Produktåterkallelse 555531 Radiushuvudprotessystem VÄNLIGEN, SPRID DENNA INFORMATION TILL DEN
Viktigt säkerhetsmeddelande till marknaden
 Audionomens namn Gatuadress Postnummer, ort WIDEX A/S Nymoellevej 6 3540 Lynge Danmark Tel.: (+45) 44 35 56 00 Fax: (+45) 44 35 56 01 widex@widex.com www.widex.com 28 augusti 2018 Viktigt säkerhetsmeddelande
Audionomens namn Gatuadress Postnummer, ort WIDEX A/S Nymoellevej 6 3540 Lynge Danmark Tel.: (+45) 44 35 56 00 Fax: (+45) 44 35 56 01 widex@widex.com www.widex.com 28 augusti 2018 Viktigt säkerhetsmeddelande
14 maj 2018 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Risk för imprecision vid användning av VITROS Chemistry Products PHYT slides
 URGENT 14 maj 2018 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Risk för imprecision vid användning av VITROS Chemistry Products PHYT slides Bäste kund Som en del av en Viktig korrigerande säkerhetsåtgärd
URGENT 14 maj 2018 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Risk för imprecision vid användning av VITROS Chemistry Products PHYT slides Bäste kund Som en del av en Viktig korrigerande säkerhetsåtgärd
Bilaga 6 till rapport 1 (5)
 till rapport 1 (5) Bilddiagnostik vid misstänkt prostatacancer, rapport UTV2012/49 (2014). Värdet av att undvika en prostatabiopsitagning beskrivning av studien SBU har i samarbete med Centrum för utvärdering
till rapport 1 (5) Bilddiagnostik vid misstänkt prostatacancer, rapport UTV2012/49 (2014). Värdet av att undvika en prostatabiopsitagning beskrivning av studien SBU har i samarbete med Centrum för utvärdering
Viktigt säkerhetsmeddelande
 Viktigt säkerhetsmeddelande FSCA DC 13-10/13-33 Maj 2013 Dimension Chemistry Wash (RD701) CTNI, LTNI, FT4, TSH, PBNP förskjutning i QC- och patientresultat för flera lotter Bästa kund, Enligt våra noteringar
Viktigt säkerhetsmeddelande FSCA DC 13-10/13-33 Maj 2013 Dimension Chemistry Wash (RD701) CTNI, LTNI, FT4, TSH, PBNP förskjutning i QC- och patientresultat för flera lotter Bästa kund, Enligt våra noteringar
VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE
 VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE Handelsnamn: AbViserTM AutoValveTM IAP-mätinstrument (se bilaga 1 för fullständig information) Utgivningsdatum: 25 april, 2018 REF.nr: Se bilaga 1 LOT-nr: Alla
VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE Handelsnamn: AbViserTM AutoValveTM IAP-mätinstrument (se bilaga 1 för fullständig information) Utgivningsdatum: 25 april, 2018 REF.nr: Se bilaga 1 LOT-nr: Alla
VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE
 VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE Handelsnamn: Female-kateter Nelatonkateter Rektal kateter Mülly-sugkateter LOT-nr: Se tabell på sida 13 FSCA-ID: 2011/09/CTH3 Typ av åtgärd: Återkallande retur
VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE Handelsnamn: Female-kateter Nelatonkateter Rektal kateter Mülly-sugkateter LOT-nr: Se tabell på sida 13 FSCA-ID: 2011/09/CTH3 Typ av åtgärd: Återkallande retur
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN PAS
 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN PAS-18-1162 Katalognummer: 368879, : 6319963 25-01-2018 Till: Distributören Det här brevet innehåller viktig information som kräver din omedelbara uppmärksamhet.
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN PAS-18-1162 Katalognummer: 368879, : 6319963 25-01-2018 Till: Distributören Det här brevet innehåller viktig information som kräver din omedelbara uppmärksamhet.
BRÅDSKANDE KORRIGERING FÖR MEDICINSK UTRUSTNING PÅ MARKNADEN
 BRÅDSKANDE KORRIGERING FÖR MEDICINSK UTRUSTNING PÅ MARKNADEN Thermo Scientific Indiko- och Indiko Plus-analysatorer Katalognummer: 98630000, 98631000, 98640000, 98641000 28 februari 2014 Bästa kund: Syftet
BRÅDSKANDE KORRIGERING FÖR MEDICINSK UTRUSTNING PÅ MARKNADEN Thermo Scientific Indiko- och Indiko Plus-analysatorer Katalognummer: 98630000, 98631000, 98640000, 98641000 28 februari 2014 Bästa kund: Syftet
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN ETHICON PHYSIOMESH flexibelt kompositnät (alla produktkoder)
 Bästa Operationsrumsansvariga, materielpersonal och operationschef VÄNLIGEN, SPRID DENNA INFORMATION TILL ALL PERSONAL PÅ ER ENHET SOM ANVÄNDER FLEXIBELT KOMPOSITNÄT På Ethicon är vår första prioritet
Bästa Operationsrumsansvariga, materielpersonal och operationschef VÄNLIGEN, SPRID DENNA INFORMATION TILL ALL PERSONAL PÅ ER ENHET SOM ANVÄNDER FLEXIBELT KOMPOSITNÄT På Ethicon är vår första prioritet
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN INFORMATION PERIFIX KATETERKOPPLING
 Danderyd 2018-10-02 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN INFORMATION PERIFIX KATETERKOPPLING Bäste vårdgivare, Vi, B. Braun Medical, har beslutat att proaktivt informera våra kunder via ett frivilligt
Danderyd 2018-10-02 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN INFORMATION PERIFIX KATETERKOPPLING Bäste vårdgivare, Vi, B. Braun Medical, har beslutat att proaktivt informera våra kunder via ett frivilligt
1.2 Vid vilken diameter anser man att en operation är motiverad pga rupturrisk? (1p)
 6 sidor - 22 poäng En 65-årig man har för två dagar sedan i samband med screening för aortaaneurysm visat sig ha ett infrarenalt aortaaneurysm med diameter 65 mm. Han är tidigare frisk. Han slutade att
6 sidor - 22 poäng En 65-årig man har för två dagar sedan i samband med screening för aortaaneurysm visat sig ha ett infrarenalt aortaaneurysm med diameter 65 mm. Han är tidigare frisk. Han slutade att
Viktigt säkerhetsmeddelande till marknaden Brådskande medicinteknisk korrigeringsåtgärd /08/ C
 Viktigt säkerhetsmeddelande till marknaden Brådskande medicinteknisk korrigeringsåtgärd - 2955842-08/08/15-008-C da Vinci Si Single-Site Grip Release Bästa da Vinci-kund, Syftet med det här säkerhetsmeddelandet
Viktigt säkerhetsmeddelande till marknaden Brådskande medicinteknisk korrigeringsåtgärd - 2955842-08/08/15-008-C da Vinci Si Single-Site Grip Release Bästa da Vinci-kund, Syftet med det här säkerhetsmeddelandet
PREOPERATIV BEDÖMNING DUPLEX
 Patient: Randomiserad extremitet Inklusion efter skriftlig och muntlig information Kirurgens signatur PREOPERATIV BEDÖMNING Markera sida i bilden DUPLEX Symtomgivande varicer i randomiserad extremitet
Patient: Randomiserad extremitet Inklusion efter skriftlig och muntlig information Kirurgens signatur PREOPERATIV BEDÖMNING Markera sida i bilden DUPLEX Symtomgivande varicer i randomiserad extremitet
DISTRIBUERA DENNA INFORMATION TILL ALL PERSONAL INOM SJUKHUSET SOM ANVÄNDER PROXIMATE cirkulär stapler för hemorrojder
 PROXIMATE cirkulär stapler för hemorrojder (specifika loter av produktkoderna PPH01 och December 2018 Bästa kunder, DISTRIBUERA DENNA INFORMATION TILL ALL PERSONAL INOM SJUKHUSET SOM ANVÄNDER PROXIMATE
PROXIMATE cirkulär stapler för hemorrojder (specifika loter av produktkoderna PPH01 och December 2018 Bästa kunder, DISTRIBUERA DENNA INFORMATION TILL ALL PERSONAL INOM SJUKHUSET SOM ANVÄNDER PROXIMATE
Viktigt säkerhetsmeddelande till marknaden
 Viktigt säkerhetsmeddelande till marknaden IMC18-02.A.OUS December 2017 IMMULITE /IMMULITE 1000 IMMULITE 2000/IMMULITE -analyser Enligt våra noteringar kan ditt laboratorium ha mottagit de produkter som
Viktigt säkerhetsmeddelande till marknaden IMC18-02.A.OUS December 2017 IMMULITE /IMMULITE 1000 IMMULITE 2000/IMMULITE -analyser Enligt våra noteringar kan ditt laboratorium ha mottagit de produkter som
Viktigt säkerhetsmeddelande till marknaden: Brådskande produktåterkallelse. Engångsartiklar inom bildtagnings tillbehör Slangar och sprutor
 Viktigt säkerhetsmeddelande till marknaden: Brådskande produktåterkallelse Engångsartiklar inom bildtagnings tillbehör Slangar och sprutor DATUM: Februari, 2012 ANGÅENDE: Engångsartiklar inom bildtagningstillbehör,
Viktigt säkerhetsmeddelande till marknaden: Brådskande produktåterkallelse Engångsartiklar inom bildtagnings tillbehör Slangar och sprutor DATUM: Februari, 2012 ANGÅENDE: Engångsartiklar inom bildtagningstillbehör,
Läkarguide för bedömning och övervakning av kardiovaskulär risk vid förskrivning av Strattera
 Läkarguide för bedömning och övervakning av kardiovaskulär risk vid förskrivning av Strattera Strattera är indicerat för behandling av ADHD (Attention-Deficit/Hyperactivity Disorder) hos barn (från 6 års
Läkarguide för bedömning och övervakning av kardiovaskulär risk vid förskrivning av Strattera Strattera är indicerat för behandling av ADHD (Attention-Deficit/Hyperactivity Disorder) hos barn (från 6 års
Viktigt säkerhetsmeddelande till marknaden (FSN)
 Bild 1: S-ROM Noiles Rotating Hinge Femur with Pin Viktigt säkerhetsmeddelande till marknaden (FSN) Produktnamn: DePuy S-ROM Noiles Rotating Hinge Femur with Pin Typ av åtgärd: Säkerhetsmeddelande till
Bild 1: S-ROM Noiles Rotating Hinge Femur with Pin Viktigt säkerhetsmeddelande till marknaden (FSN) Produktnamn: DePuy S-ROM Noiles Rotating Hinge Femur with Pin Typ av åtgärd: Säkerhetsmeddelande till
Rekommendationer angående Zimmer Biomet Pulsavac Plus-enheter
 27 september 2017 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Till: Kirurger/sjukhus Ämne:VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN ANGÅENDE MEDICINTEKNISK PRODUKT (KORRIGERING) Referens: ZFA2017-266 Berörd
27 september 2017 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Till: Kirurger/sjukhus Ämne:VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN ANGÅENDE MEDICINTEKNISK PRODUKT (KORRIGERING) Referens: ZFA2017-266 Berörd
ÅTERKALLANDE AV MEDICINSK PRODUKT Mucolexx/Mucolytic Agent
 19 maj, 2015 Ditt svar behövs OMEDELBART (vänligen fyll i sidorna 4-6). ÅTERKALLANDE AV MEDICINSK PRODUKT Mucolexx/Mucolytic Agent BRÅDSKANDE ÅTERKALLANDE AV MEDICINSK PRODUKT [Skriv in distributörens
19 maj, 2015 Ditt svar behövs OMEDELBART (vänligen fyll i sidorna 4-6). ÅTERKALLANDE AV MEDICINSK PRODUKT Mucolexx/Mucolytic Agent BRÅDSKANDE ÅTERKALLANDE AV MEDICINSK PRODUKT [Skriv in distributörens
VIKTIGT SÄKERHETSMEDDELANDE Viktig korrigerande säkerhetsåtgärd
 VIKTIGT SÄKERHETSMEDDELANDE Viktig korrigerande säkerhetsåtgärd Maquet CARDIOSAVE Hybrid Intra-Aortic Balloon Pump (IABP) Maquet CARDIOSAVE Rescue Intra-Aortic Balloon Pump (IABP) BERÖRDA PRODUKTER KOMPONENTNUMMER
VIKTIGT SÄKERHETSMEDDELANDE Viktig korrigerande säkerhetsåtgärd Maquet CARDIOSAVE Hybrid Intra-Aortic Balloon Pump (IABP) Maquet CARDIOSAVE Rescue Intra-Aortic Balloon Pump (IABP) BERÖRDA PRODUKTER KOMPONENTNUMMER
Säkerhetsmeddelande till marknaden
 Säkerhetsmeddelande till marknaden 2018 12 14 MSA-2018-002-IU Vänligen vidarebefodra denna information till alla användare hos er [inkl. biomedicinsk personal för kapitalutrustning, materialhantering och/eller
Säkerhetsmeddelande till marknaden 2018 12 14 MSA-2018-002-IU Vänligen vidarebefodra denna information till alla användare hos er [inkl. biomedicinsk personal för kapitalutrustning, materialhantering och/eller
Komplikationer vid PCI. Dr. Berglind Libungan
 Komplikationer vid PCI Dr. Berglind Libungan Översikt Risk stratifiering Komplikationer vid coronar angiografi/pci Hur kan man förebygga komplikationer? Vid komplikation, Hur ska man agera? Komplikationer
Komplikationer vid PCI Dr. Berglind Libungan Översikt Risk stratifiering Komplikationer vid coronar angiografi/pci Hur kan man förebygga komplikationer? Vid komplikation, Hur ska man agera? Komplikationer
Viktigt säkerhetsmeddelande
 IMMULITE IMMULITE 1000 IMMULITE 2000 IMMULITE 2000 XPi Viktigt säkerhetsmeddelande 4009B/FSCA IMC 14-05 Rev B Januari 2014 Positiv avvikelse med analysen Totalt IgE i förhållande till WHO:s andra IRP 75/502
IMMULITE IMMULITE 1000 IMMULITE 2000 IMMULITE 2000 XPi Viktigt säkerhetsmeddelande 4009B/FSCA IMC 14-05 Rev B Januari 2014 Positiv avvikelse med analysen Totalt IgE i förhållande till WHO:s andra IRP 75/502
Viktigt säkerhetsmeddelande till marknaden
 Viktigt säkerhetsmeddelande till marknaden Kommersiellt namn på den Alcon or Endure LuxOR E71 Ophthalmic Microscope; berörda produkten: Alcon or Endure LuxOR E71 Q-Vue Ophthalmic Microscope Referens (er):
Viktigt säkerhetsmeddelande till marknaden Kommersiellt namn på den Alcon or Endure LuxOR E71 Ophthalmic Microscope; berörda produkten: Alcon or Endure LuxOR E71 Q-Vue Ophthalmic Microscope Referens (er):
Viktigt säkerhetsmeddelande till marknaden
 Helsingborg, 10 januari 2017 Till: Distributörer och sjukvårdspersonal Viktigt säkerhetsmeddelande till marknaden Bästa kund, Vigmed AB har frivilligt initierat en korrigerande säkerhetsåtgärd på marknaden
Helsingborg, 10 januari 2017 Till: Distributörer och sjukvårdspersonal Viktigt säkerhetsmeddelande till marknaden Bästa kund, Vigmed AB har frivilligt initierat en korrigerande säkerhetsåtgärd på marknaden
Viktigt säkerhetsmeddelande!
 Fresenius Medical Care Sverige AB Box 548 192 05 Sollentuna Medicinskt ansvarig Fresenius Medical Care Sverige AB Box 548, 192 05 Sollentuna Besöksadress: Djupdalsvägen 1 Sverige www.freseniusmedicalcare.se
Fresenius Medical Care Sverige AB Box 548 192 05 Sollentuna Medicinskt ansvarig Fresenius Medical Care Sverige AB Box 548, 192 05 Sollentuna Besöksadress: Djupdalsvägen 1 Sverige www.freseniusmedicalcare.se
Viktigt säkerhetsmeddelande
 ADVIA Centaur ADVIA Centaur XP ADVIA Centaur XPT ADVIA Centaur CP CC 19-4.A-1.OUS December 218 Enligt våra uppgifter kan ditt laboratorium ha mottagit följande produkt: Table 1. ADVIA Centaur berörd produkt
ADVIA Centaur ADVIA Centaur XP ADVIA Centaur XPT ADVIA Centaur CP CC 19-4.A-1.OUS December 218 Enligt våra uppgifter kan ditt laboratorium ha mottagit följande produkt: Table 1. ADVIA Centaur berörd produkt
Seminarium läkemedelsvärdering. Klinisk farmakologi
 Seminarium läkemedelsvärdering Klinisk farmakologi 2017-05-02 1) Bifogad reklam för Maxistark (1) illustrerar skillnaden mellan relativ riskreduktion (RRR) och absolut riskreduktion (ARR). a) Hur stor
Seminarium läkemedelsvärdering Klinisk farmakologi 2017-05-02 1) Bifogad reklam för Maxistark (1) illustrerar skillnaden mellan relativ riskreduktion (RRR) och absolut riskreduktion (ARR). a) Hur stor
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN. Beskrivning av problemet och hälsoriskerna:
 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Datum: 15-01-2018 Produktnamn Produktkatalognummer Lotnummer Utgångsdatum (ÅÅÅÅMMDD) BD Phoenix Gram Negative Panels med kolistin Se bifogad lista Se bifogad
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Datum: 15-01-2018 Produktnamn Produktkatalognummer Lotnummer Utgångsdatum (ÅÅÅÅMMDD) BD Phoenix Gram Negative Panels med kolistin Se bifogad lista Se bifogad
Kliniska studier av och klinisk utvärdering av medicintekniska produkter idag och i framtiden
 TOPRA 2014 Kliniska studier av och klinisk utvärdering av medicintekniska produkter idag och i framtiden Margareth Jorvid, Methra Uppsala AB, LSM group Malmö, 23 september 2014 ENABLING AND PROMOTING EXCELLENCE
TOPRA 2014 Kliniska studier av och klinisk utvärdering av medicintekniska produkter idag och i framtiden Margareth Jorvid, Methra Uppsala AB, LSM group Malmö, 23 september 2014 ENABLING AND PROMOTING EXCELLENCE
2. Hur många procent av patienterna får postoperativt förmaksflimmer efter öppen hjärtkirurgi? (1p)
 Kortsvars frågor Kardiologi 1.Ung man där pappa dog plötsligt 35 år gammal. Vad visar EKG? Vilken sjukdom vill du utesluta? (2p) (Notera amerikansk koppling samt 25 mm/s) 2. Hur många procent av patienterna
Kortsvars frågor Kardiologi 1.Ung man där pappa dog plötsligt 35 år gammal. Vad visar EKG? Vilken sjukdom vill du utesluta? (2p) (Notera amerikansk koppling samt 25 mm/s) 2. Hur många procent av patienterna
Vi delger er korrigerande säkerhetsåtgärder eftersom våra register visar att ni har levererats berörda produkter som anges i bilaga 1.
 Till kvalitetssäkringsavdelningen, avdelningen för tillsyns- och regelfrågor eller ledningen Saint Priest, 2019-09-12 Ämne: VIKTIGT - SÄKERHETSMEDDELANDE Integra Mall För regenerering av hud ett lager
Till kvalitetssäkringsavdelningen, avdelningen för tillsyns- och regelfrågor eller ledningen Saint Priest, 2019-09-12 Ämne: VIKTIGT - SÄKERHETSMEDDELANDE Integra Mall För regenerering av hud ett lager
Brådskande SÄKERHETSMEDDELANDE TILL MARKNADEN
 Enhet: Brådskande SÄKERHETSMEDDELANDE TILL MARKNADEN Terumo CDI Blood Parameter Monitoring System 500, givarhuvud Referens: FSN 1509 2016 04 Åtgärd: Avlägsnande Till: Perfusionsansvarig, avdelningen för
Enhet: Brådskande SÄKERHETSMEDDELANDE TILL MARKNADEN Terumo CDI Blood Parameter Monitoring System 500, givarhuvud Referens: FSN 1509 2016 04 Åtgärd: Avlägsnande Till: Perfusionsansvarig, avdelningen för
Läkarens guide för att bedöma och kontrollera kardiovaskulär risk vid förskrivning av Atomoxetin Mylan
 Läkarens guide för att bedöma och kontrollera kardiovaskulär risk vid förskrivning av Atomoxetin Mylan Atomoxetin Mylan är avsett för behandling av ADHD (Attention Deficit Hyperactivity Disorder) hos barn
Läkarens guide för att bedöma och kontrollera kardiovaskulär risk vid förskrivning av Atomoxetin Mylan Atomoxetin Mylan är avsett för behandling av ADHD (Attention Deficit Hyperactivity Disorder) hos barn
Ett fel kan uppstå så defibrilleringsknappen inte aktiveras och defibrilleringen fördröjs eller förhindras
 Cardiac Care Emergency Care Solutions -1/5- FSN86100088A 2010 JANUARI BRÅDSKANDE återkallande av medicinsk utrustning Philips återanvändbara interna defibrilleringsspatlar med defibrilleringsknapp (Produktnummer
Cardiac Care Emergency Care Solutions -1/5- FSN86100088A 2010 JANUARI BRÅDSKANDE återkallande av medicinsk utrustning Philips återanvändbara interna defibrilleringsspatlar med defibrilleringsknapp (Produktnummer
BRÅDSKANDE VIKTIGT FÄLTSÄKERHETSMEDDELANDE
 BRÅDSKANDE VIKTIGT Det här är viktig information om en säkerhetsrisk som kan förekomma med din utrustning och om vilka åtgärder som måste vidtas för att upprätthålla säkerheten för personal och patienter.
BRÅDSKANDE VIKTIGT Det här är viktig information om en säkerhetsrisk som kan förekomma med din utrustning och om vilka åtgärder som måste vidtas för att upprätthålla säkerheten för personal och patienter.
CTO-PCI. Evidens, indikation, teknik. Regionmöte Kalmar, Georgios Panayi, Kardiologiska Kliniken, US Linköping
 CTO-PCI Evidens, indikation, teknik Regionmöte Kalmar, 2017-03-22 Georgios Panayi, Kardiologiska Kliniken, US Linköping CTO-PCI Evidens Indikationer Teknik 2 CTO-definition och prevalens ockluderat koronart
CTO-PCI Evidens, indikation, teknik Regionmöte Kalmar, 2017-03-22 Georgios Panayi, Kardiologiska Kliniken, US Linköping CTO-PCI Evidens Indikationer Teknik 2 CTO-definition och prevalens ockluderat koronart
