HeartWare -batteri FSCA APR Återkallande av HeartWare -batteri 1650, 1650-DE BAT till BAT039999; BAT till BAT099999
|
|
|
- Viktor Gustafsson
- för 9 år sedan
- Visningar:
Transkript
1 VIKTIGT SÄKERHETSMEDDELANDE Produkt: Identifierare: Typ av åtgärd: Produktkod: Serieintervall #s: HeartWare -batteri FSCA APR Återkallande av HeartWare -batteri 1650, 1650-DE BAT till BAT039999; BAT till BAT Hej HeartWare-läkare, Information angående berörda produkter HeartWare utökar sina frivilliga förbättrande säkerhetsåtgärder, FSCA APR2014, så att dessa inkluderar återkallande av särskilda batterier inom HeartWare ventrikulära hjälpsystem, produktkoder 1650 och 1650-DE. Beskrivning av problemet I maj 2014, delade HeartWare ut säkerhetsmeddelandet FSCA APR2014 efter ett ökat antal rapporterade klagomål om energihantering relaterat till att batteriet förbrukas tidigare än väntat. Information om tidig batteriförbrukning, identifiering av möjligt felaktiga batterier och rekommenderad praxis för energihantering gavs i säkerhetsmeddelandet. En kopia på säkerhetsmeddelandet är bifogat till detta brev som referens. HeartWare utökar de förbättrande säkerhetsåtgärderna för att inkludera återkallandet av batterier som producerades inom serienummerintervallen: BAT till BAT och BAT till BAT Batterier som tillverkades inom dessa intervall löper större risk för, för tidig eller oigenkännlig försämring av batterikapacitet, vilket utgör en risk för patienten eftersom det kan leda till pumpstopp. Åtgärder att vidta för läkaren Batterier i serienummerintervallet BAT till BAT och BAT till BAT bör identifieras och avlägsnas från drift. Gör följande: 1. Underteckna omgående Bekräftelseformulär och skicka in det till HeartWare via fax: eller e-post: FSCA@heartware.com. 2. Identifiera och lägg undan batterier med serienummerintervall BAT till BAT och BAT till BAT Gå igenom inventariet på ditt sjukhus. Ta bort och lägg undan berörda batterier. Inspektera batterier och byt ut berörda batterier vid varje patients nästa regelbundna schemalagda besök, mot batterier som har serienummer BAT till BAT eller BAT och högre. Om en patient inte har något regelbundet besök schemalagt inom de närmsta 90 dagarna, så kontakta patienten per telefon för att kontrollera serienumret på patientens batteri. Schemalägg ett besök så snart som möjligt för patienter med berörda batterier. Informera dessa patienter om att i första hand använda batterier med serienummer BAT till BAT eller BAT och högre, i största möjliga mån, framtill deras schemalagda besök. Serienumret finns på den vita etiketten på batteriets baksida (se bild 1 nedan) NW 60 th Avenue, Miami Lakes, FL USA T F Fil: FSCA APR SV Sida 1 av 3
2 Bild 1. Exempel på HeartWare -batteri 3. Lämna tillbaka alla berörda batterier till HeartWare. Sätt på ett HeartWare FSCA APR märke på varje påverkat batteri (se bild 1 ovan). Skaffa ett unikt nummer för tillstånd för återlämning av varor (RGA: Return Goods Authorization) för återlämning av batterier genom att kontakta: HeartWares kundtjänst per telefon: eller e-post: cseurope@heartware.com. Din lokala HeartWare-representant. Ersättningsbatterier för patienter som för närvarande stöds kommer att skickas efter utförande av RGA. Vid behov kommer din HeartWare-representant att samarbeta med dig för att upprätta ett lämpligt lager av ersättningsbatterier. 4. Fyll i, underteckna och skicka Fullbordandeformulär inom 4 månader från att detta brev mottogs till HeartWare via fax: eller e-post: FSCA@heartware.com. Ange: Alla batterier i inventariet har kontrollerats och batterier inom serienummerintervallet BAT till BAT och BAT till BAT har tagits bort och skickats till HeartWare. Alla batterier för patienter som stöds har kontrollerats och batterier inom serienummerintervallet BAT till BAT och BAT till BAT har tagits bort och skickats till HeartWare. Om du inte har påverkade batterier i inventariet och ingen av patienterna har påverkade batterier. 5. För serienummer BAT till BAT eller BAT och högre, fortsätt att övervaka batteriprestandaden och rapportera all ovanlig batterifunktion enligt beskrivning i säkerhetsmeddelande FSCA APR Denna utökade handling ersätter inte de erforderliga handlingarna för FSCA APR2014, påbörjade i maj Fortsätt att följa alla krav för FSCA APR2014 och skicka erforderliga formulär till HeartWare före slutdatum. OBS! HeartWare -batterier är en förbrukningsvara och förväntas ha en användbar driftstid på 500 laddnings och urladdningscykler vilket ska räcka för en patient under ett år. Batterier som når slutet av sin användbara livslängd ska tas ur drift NW 60 th Avenue, Miami Lakes, FL USA T F Fil: FSCA APR SV Sida 2 av 3
3 Överföring av detta säkerhetsmeddelande Vidarebefordra detta meddelande till alla som bör ha kännedom inom din organisation, likaså till någon organisation där de potentiellt berörda batterierna har överförts. Om du har frågor eller om du vill ha ytterligare förklaring, kontakta din lokala HeartWare -representant eller skicka e-post till oss på Undertecknad bekräftar att detta meddelande kommer att tillhandahållas för lämpliga tillsynsmyndigheter i enlighet med gällande föreskrifter. Tack för ditt samarbete. Vänliga hälsningar, Robert Yocher Vice ordförande tillsyn Företagsadress Klinisk support dygnet runt HeartWare, Inc. Telefon: (Tyskland) NW 60th Avenue Telefon: (Storbritannien) Miami Lakes, Florida USA Fax: E-post: FSCA@heartware.com Europa: HeartWare kan också nås via den europeiska tillståndsrepresentanten, MedPass International Ltd., på +44 (0) (telefon och fax) och MedPass.AR@medpass.org (e-post). Bilagor: Bilaga 1: Bekräftelseformulär (Krävs) Bilaga 2: Fullbordandeformulär (Krävs) Bilaga 3: Referenskopia på säkerhetsmeddelande FSCA APR2014 HeartWare FSCA APR blått märke NW 60 th Avenue, Miami Lakes, FL USA T F Fil: FSCA APR SV Sida 3 av 3
4 BILAGA 1 Bekräftelseformulär Svar krävs Identifierare: Typ av åtgärd: Produktnamn: Katalog #: Serie #: FSCA APR Återkallande av HeartWare -batteri HeartWare -batteri 1650, 1650-DE BAT till BAT039999; BAT till BAT Klinik/Sjukhusets namn Undertecknad bekräftar härmed mottagande och förståelse av de åtgärder som krävs för att följa HeartWares brådskande säkerhetsmeddelande FSCA APR Svar krävs för båda nedanstående frågor. 1. Har du batterier inom serienummer BAT till BAT eller BAT till BAT i sjukhusets inventarier? Nej Ja 2. Har du överfört några batterier med serienummer BAT till BAT eller BAT till BAT till andra institutioner? Nej Ja. Lämna information om påverkade batterier som har överförts. Klinik/Sjukhusets namn Antalet påverkade batterier som överförts Befattning/Titel Fullständigt namn Underskrift/datum Skanna och returnera snarast det underskrivna formuläret via fax eller e-post nedan. Kvalitetschef Fax: e-post: FSCA@heartware.com NW 60 th Avenue, Miami Lakes, FL USA T F Fil: FSCA APR SV Sida 1 av 1
5 BILAGA 2 Fullbordandeformulär Svar krävs Identifierare: Typ av åtgärd: Produktnamn: Katalog #: Serie #: FSCA APR Återkallande av HeartWare -batteri HeartWare -batteri 1650, 1650-DE BAT till BAT039999; BAT till BAT Klinik/Sjukhusets namn Undertecknad bekräftar härmed nedanstående information i samband med HeartWares brådskande säkerhetsmeddelande FSCA APR Fyll i antingen AVSNITT 1 eller AVSNITT 2 nedan. AVSNITT 1 (Alla rutor i detta avsnitt måste kyssas i) Alla batterier i inventariet har kontrollerats och batterier inom serienummerintervall BAT till BAT och BAT till BAT har tagits bort och skickats till HeartWare. Alla batterier från patienter har kontrollerats och batterier inom serienummerintervall BAT till BAT och BAT till BAT har tagits bort och skickats till HeartWare ELLER AVSNITT 2 Det finns inga påverkade batterier i inventariet och ingen av patienterna har påverkade batterier. Befattning/Titel Fullständigt namn Underskrift/datum Skicka in det undertecknade formuläret via fax eller e-post nedan, inom 4 månader från att du tog emot detta meddelande. Kvalitetschef Fax: e-post: FSCA@heartware.com NW 60 th Avenue, Miami Lakes, FL USA T F Fil: FSCA APR SV Sida 1 av 1
6 VIKTIGT SÄKERHETSMEDDELANDE Produkt: Identifierare: Typ av åtgärd: Produktkod: Serieintervall #s: HeartWare -batteri FSCA APR2014 Säkerhetsmeddelande 1650, 1650-DE Alla HeartWare serienummer för batterier Bästa HeartWare kliniker, Detaljer angående påverkade enheter: HeartWare distribuerar frivilligt ett säkerhetsmeddelande som gäller alla batterier för HeartWare ventrikulära hjälpsystem med produktkod 1650 och 1650-DE. Beskrivning av problemet: Vi har sett en ökning av antalet inrapporterade klagomål för HeartWare -systemets strömhantering som är relaterade till både tidigt batterifel och rutinmässig batterihantering. För tidig eller okänd försämring av batterikapacitet eller misstag i rekommenderad strömhantering utgör en risk för patienten och kan i sällsynta fall leda till allvarlig skada eller döden. Denna rättelse är avsedd att ge patienter och vårdgivare information så att de kan känna igen batterier med mindre än två timmars driftstid, åter granska instruktioner för åtgärder som ska vidtas när batterilarm inträffar och understryka lämplig strömhantering. Råd för åtgärder som ska vidtas av klinikern (1) : Tidig identifiering av batteriurladdning i förtid, patientträning och noggrant uppmärksammande av rekommenderade strömhanteringsrutiner är viktiga för att minska risken för patienten. HeartWare tillhandahåller information för att hjälpa patienter och kliniker att övervaka batteriprestanda och känna igen onormalt beteende. Vänligen utför följande steg för att se till att alla patienter med HeartWare -batterier hanterar sina strömkällor på ett säkert sätt och att batterier hanteras i enlighet med bruksanvisningen. 1. Granska medföljande brev och bekanta dig med dess innehåll. Skriv omgående under "Bekräftelseformulär" och skicka in det till HeartWare via fax: (364) E-post: FSCA@heartware.com. 2. Understryk rekommenderade rutiner (nedan) för tidig upptäckt av onormalt batteribeteende och effektiv strömhantering för dina patienter. Tillhandahåll i synnerhet de medföljande breven till var och en av dina nuvarande HeartWare -systempatienter vid nästa rutinbesök. 3. Fyll i och skicka in "Formulär för slutförande av nödvändiga åtgärder" till HeartWare via fax inom 7 månader efter att du mottagit detta brev: (364) E-post: FSCA@heartware.com NW 60 th Avenue, Miami Lakes, FL USAT F Fil: FSCA APR2014.SV Sida 1 av 4
7 Rekommenderade rutiner för effektiv strömhantering (1) Övervakningssystem för onormalt batteribeteende. o HeartWare -systemets förväntade beteende är följande: En styrenhet varnar och byter till den andra strömkällan endast när batteriet har mindre än (<) 25 % kapacitet (1 indikatorlampa) ännu lysande. HeartWare -systemets onormala beteenden är följande: En styrenhet byter till det andra batteriet när det första batteriet har mer än (>) 25 % kapacitet (2 eller fler indikatorlampor) ännu lysande. Ersätt det första batteriet och ta det ur bruk. Det inträffar en plötslig förändring i batterikapacitet i ett batteri (t.ex. en plötslig minskning från 4 lampor till 1 lampa). Ersätt det onormalt uppträdande batteriet och ta det ur bruk. Du hör "pipande" och styrenheten skiftar snabbt fram och tillbaka mellan batterierna. Ersätt först batteriet med flera indikatorlampor lysande, ersätt sedan batteriet med färre lampor lysande. Ta batteriet med fler lampor lysande ur bruk, eftersom det kan vara ett ej fungerande batteri. Något av dessa beteenden skulle kunna indikera ett batteri som behöver ersättas och som potentiellt skulle kunna leda till en kritiskt låg batterinivå eller möjlig strömförlust. Dessa batterier måste tas ur bruk och returneras. o Identifiera batterier som har tagits ur bruk på grund av onormalt beteende genom att fästa en av de medföljande orange etiketterna (märkta "HeartWare FSCA APR2014") innan enheten returneras till HeartWare. Uppdatera dig och förstärk befintlig träning med dina patienter. o Koppla ALDRIG ur båda strömkällorna (batterier och växelströms- eller likströmsadapter) samtidigt då detta kommer att leda till att pumpen stannar. Minst en strömkälla måste alltid vara ansluten. o Bortsett från de korta stunder då du byter ut en av strömkällorna måste styrenheten alltid vara ansluten till två strömkällor. Dessa kan vara antingen två batterier eller ett batteri och en växelströmsadapter eller likströmsadapter (t.ex. biladapter). För att spara på batteriet ska du använda växelströmsadaptern när du vilar eller sover.när du kopplar bort växelströmmen, anslut alltid HeartWare -systemet till två batterier. o Undersök och åtgärda om möjligt alltid orsaken till något larm enligt HeartWare bruksanvisningen eller patientmanualen. Ett larmtillstånd blir inte åtgärdat genom att man stänger av larmsignalen. o Ladda alltid om helt urladdade batterier inom ett dygn för att undvika permanent skada på dem. o Se till att det alltid finns ett fulladdat batteri till hands så att du kan byta det använda eller urladdade batteriet. o Se alltid till att ha en extra styrenhet tillgänglig, och om möjligt, en vårdare i närheten vid byte av strömkällor eller styrenheter. Var uppmärksam på kraftförändringar eller flödeslarm en period efter förändringar av utrustningen, o Bekräfta ALLTID att strömkablarna sitter ordentligt fast på styrenheten genom att försiktigt dra i kabeln intill styrenhetens strömanslutning, annars kan strömkablarna lossna och leda till ett larm eller att pumpen stannar NW 60 th Avenue, Miami Lakes, FL USAT F Fil: FSCA APR2014.SV Sida 2 av 4
8 o o o Inspektera batterierna efter fysisk skada minst en gång i veckan, inklusive batterikablar och anslutningar. Använd INTE batterier som ser ut att vara skadade. Skadade batterier måste tas ur bruk och utbytta. Roterande användning av batterier tillåter alla batterier att åldras i en gemensam takt så att inget batteri har betydande färre laddningscykler är andra. En patient som alternerar användandet av hans/hennes batterier bör de kunna uppnå ungefär 1 års livslängd. Påminn patienter att ta med alla batterier till klinikbesök. Batteribyte HeartWare -batterier innehåller litiumjon-celler för att driva HVAD -systemet i cirka 4 till 6 timmar när de är helt laddade. Ungefär som för batterier för konsumentelektronik förlorar HeartWare -batterier laddningskapacitet över tid. Om ett batteri ger mindre än 2 timmars driftska det tas ur bruk och bytas ut. OBS! HeartWare -batterier förväntas fungera under minst 500 laddnings- och urladdningscykler; detta ska ge patientsupport under minst ett år. Om du vill ha en beräkning av antalet battericykler, vänligen skicka loggfiler till HeartWare (hvadlogs@heartware.com) och be om en granskning av antalet battericykler (tillgänglig för styrenheter REF 1407XX/1408). Åtgärd från HeartWare Märkningsspråk klargörs i bruksanvisningen och patientmanualen för att vara i linje med den information som tillhandahålls i denna rättelse efter en granskning utförd av tillsynsmyndigheterna. Klagomål kommer att fortsätta att övervakas noggrant för att se till att HeartWare -systemet fungerar som avsett och för att utvärdera effektiviteten av denna rättelse. HeartWare kommer att fortsätta att undersöka batterier som laddar ur i förtid och kommer att vidta ytterligare lämpliga åtgärder. Överföring av detta säkerhetsmeddelande Detta meddelande måste vidarebefordras till alla som bör ha kännedom inom din organisation eller till en organisation där de potentiellt berörda produkterna har överförts. Om du har några frågor eller om du behöver ytterligare förtydliganden, kontakta din Heartwarerepresentant eller Heartwares kundtjänst. Tack för ditt samarbete. Undertecknad bekräftar att detta meddelande kommer att tillhandahållas för lämpliga tillsynsmyndigheter i enlighet med gällande föreskrifter. Vänliga hälsningar Ramon Augusto Paz Vice ordförande, Kvalitetskontroll Företagsadress HeartWare, Inc. Klinisk support dygnet runt (Tyskland) (England) NW 60 th Avenue, Miami Lakes, FL USAT F Fil: FSCA APR2014.SV Sida 3 av 4
9 14400 NW 60th Avenue Fax: + +1 (305) Miami Lakes, FL USA E-post: FSCA@heartware.com Europa:HeartWare kan nås genom den auktoriserade representanten i Europa, MedPass International Ltd., on +44 (0) (telefon och fax). Bilagor: Bekräftelseformulär Patientbrev Orange etiketter, HeartWare FSCA APR2014 Formulär för slutförande av nödvändiga åtgärder NW 60 th Avenue, Miami Lakes, FL USAT F Fil: FSCA APR2014.SV Sida 4 av 4
10 Bekräftelseformulär Svar krävs Identifierare: Typ av åtgärd: Produktnamn: Katalognr: Serienr: FSCA APR2014 Säkerhetsmeddelande HeartWare -batteri 1650, 1650-DE Alla HeartWare serienummer för batterier Klinik/Sjukhusets namn Undertecknad bekräftar härmed mottagande och förståelse av de åtgärder som krävs för att följa HeartWare:s säkerhetsmeddelande FSCA APR2014. Befattning/Titel Namn Underskrivet/Datum Scanna och returnera omgående det underskrivna formuläret via fax eller e-post till: Kvalitetschef Fax: + +1 (305) E-post: FSCA@heartware.com NW 60 th Avenue, Miami Lakes, FL USAT F Fil: FSCA APR2014.SV
11 Slutförande av nödvändiga åtgärder Svar krävs Identifierare: Typ av åtgärd: Produktnamn: Katalognr: Serienr: FSCA APR2014 Säkerhetsmeddelande HeartWare -batteri 1650, 1650-DE Alla HeartWare serienummer för batterier Klinik/Sjukhusets namn Undertecknad bekräftar härmed mottagande och förståelse av de åtgärder som krävs för att följa HeartWare:s säkerhetsmeddelande FSCA APR2014. Befattning/Titel Namn Underskrivet/Datum Returnera det underskrivna formuläret inom 7 månader efter mottagande via fax eller e-post till: Kvalitetschef Fax: + +1 (305) E-post: FSCA@heartware.com NW 60 th Avenue, Miami Lakes, FL USAT F Fil: FSCA APR2014.SV
12 VIKTIG INFORMATION FÖR HEARTWARE-PATIENTER Produktnamn: HeartWare -batteri Orsak till detta brev Tillverkaren av HeartWare -systemet informerade oss nyligen om att de har sett en ökning av klagomål på batterier gällande tidigare än förväntad urladdning av batteriet. Vi vill kommunicera och understryka lämpliga strömhanteringsinstruktioner, inklusive hur man känner igen batterier som beter sig onormalt och när dina batterier behöver ersättas. HeartWare vill hjälpa dig att identifiera ett batteri som beter sig onormalt och vi vill understryka vikten av den utbildning som ditt sjukhus tillhandahöll för att hjälpa dig att hantera din strömförsörjning. Detta brev omfattar vikten av att övervaka strömkällorna som är anslutna till din HeartWare -kontroll och åtgärder som du kan vidta när ett batterilarm inträffar eller när ett batteri behöver ersättas. Hälsorisker Ström är nödvändigt för att hålla din pump i drift. Om din pump stannar på grund av strömförlust, återanslut till en annan strömkälla omgående. Om inte det görs så kan du uppleva yrsel, svimningsanfall och andra symptom. I sällsynta fall kan dödsfall förekomma. Vad ska du göra? Bekanta dig med detta brev och granska din patientmanual angående lämplig strömhantering. Diskutera med din hjälpmedelsrådgivare om du har frågor angående HeartWare-system eller detta brev. Ha alltid två (2) strömkällor anslutna till din kontroll; låt aldrig din styrenhet vara ansluten till endast en (1) strömkälla utom just när du snabbt byter till en annan strömkälla. Granska rekommenderade rutiner för strömhantering som tillhandahålls senare i detta brev. Om ett batteri visar något av de onormala beteendena beskrivna ovan, sluta använda det batteriet och kontakta din doktor eller hjälpmedelsrådgivare omgående för att byta ut det. Mer information om dina strömkällor kan du hitta i din patientmanual i sektionen "Strömkällor för HeartWare -styrenheten". Sida 1 av 4 / APR2014.SV
13 Indikatorer för batteriprestanda Lampor på styrenheten och på varje batteri ger information om batteriets laddningskapacitet. Larm talar om för dig när det är dags att ladda ett batteri. Indikator för batterikapacitet Aktiv strömkällsindikator Svagt batteri 1 Byt batteri 1 Larmmeddelan de Exempel på HeartWare styrenhetsdisplay När ett batteri laddas och är klart att användas lyser alla 4 gröna lampor. När batteriet laddas ur lyser färre lampor. Batteriladdning Batteriindikatorn på BATTERIET Batteriindikatorn på STYRENHETEN % 4 GRÖNA lampor 4 GRÖNA lampor % 3 GRÖNA lampor 3 GRÖNA lampor % 2 GRÖNA lampor 2 GULA lampor Mindre än 24 % 1 GRÖN lampa 1 RÖD lampa REKOMMENDERADE RUTINER FÖR STRÖMHANTERING (1) Behåll alltid 2 strömkällor anslutna till din styrenhet: o Två laddade batterier eller o Ett laddat batteri och en växelströmsadapter eller o Ett laddat batteri och en likströms (billaddare)-adapter Kontrollera dina batterier under dagen. Var uppmärksam på onormalt beteende. o HeartWare -systemets förväntade beteende är följande: En styrenhet varnar och byter till den andra strömkällan endast när batteriet har mindre än (<) 25 % kapacitet (1 indikatorlampa) ännu lysande. o HeartWare -systemets onormala beteenden är följande: Sida 2 av 4 / APR2014.SV
14 En styrenhet byter till det andra batteriet när det första batteriet har mer än (>) 25 % kapacitet (2 eller fler indikatorlampor) ännu lysande. ÅTGÄRD SOM SKA UTFÖRAS AV PATIENTEN: Ersätt det första batteriet och ta det ur bruk. Det inträffar en plötslig förändring i batterikapacitet i ett batteri (t.ex. en plötslig minskning från 4 lampor till 1 lampa). ÅTGÄRD SOM SKA UTFÖRAS AV PATIENTEN: Ersätt det onormalt uppträdande batteriet och ta det ur bruk. Du hör "pipande" och styrenheten skiftar snabbt fram och tillbaka mellan batterierna. ÅTGÄRD SOM SKA UTFÖRAS AV PATIENTEN: Ersätt först batteriet med flera indikatorlampor lysande, ersätt sedan batteriet med färre lampor lysande. Ta batteriet med fler lampor lysande ur bruk, eftersom det kan vara ett ej fungerande batteri. Något av dessa beteenden indikerar ett batteri som behöver ersättas och som potentiellt skulle kunna leda till en kritiskt låg batterinivå eller möjlig strömförlust. Dessa batterier måste tas ur bruk och returneras. o Ungefär som batteriet i en mobiltelefon så laddas HeartWare -batterier med tiden ur. Om ett fulladdat batteri varar mindre än 2 timmar, ta det ur bruk och ersätt det med ett nytt. Hur återlämnar man ett batteri? Vänligen separera batterier tagna ur bruk på grund av ovanlig aktivitet och återlämna det till din doktor eller hjälpmedelsrådgivare för ersättning. Rutinmässig batterihantering (1 Rotera användandet av dina batterier. Om du alternerar användandet av dina batterier bör de kunna uppnå ungefär 1 års livslängd. Inspektera batterier, batterikablar och anslutningar och sök efter fysiska skador åtminstone en gång i veckan. Använd INTE batterier som ser ut att vara skadade. Skadade batterier måste tas ur bruk och ersättas med nya. När du byter batterier, ha det nya batteriet inom räckhåll innan det urladdade batteriet kopplas ur. När det är möjligt, se till att ha en vårdgivare i närheten om ett larm skulle inträffa. Se till att du har med fulladdade reservbatterier när du reser. Kom ihåg att ta med alla batterier när du besöker kliniken. Sida 3 av 4 / APR2014.SV
15 Viktig information om patientmanual: VARNING! Koppla ALDRIG ur båda strömförsörjningskällorna (batterier, växelströmsadapter, likströmsadapter) samtidigt. Detta får pumpen att stanna och aktiverar larmet No Power (ingen ström). Minst en strömkälla måste alltid vara ansluten. VARNING! Se till att ALLTID ha en reservstyrenhet och fulladdade reservbatterier tillgängliga i händelse av nödsituation. VARNING! Undersök ALLTID orsaken till alla larm och försök om möjligt att åtgärda dem. Ett larmtillstånd blir inte åtgärdat genom att man stänger av larmsignalen. FÖRSIKTIGT! Kontrollera ALLTID att nätsladdarna är ordentligt låsta på plats i styrenheten genom att fatta tag i sladden i närheten av kontakten och försiktigt dra i den. FÖRSIKTIGT! Ladda ALLTID om helt urladdade batterier inom ett dygn för att undvika permanent skada på dem. Kontakta din doktor eller hjälpmedelsrådgivare om du har frågor angående ditt HeartWare - system eller tror att dina batterier behöver bytas ut. Tack för ditt samarbete. Sida 4 av 4 / APR2014.SV
Råd för åtgärder som ska vidtas av klinikern (1) :
 20.05.14 VIKTIGT SÄKERHETSMEDDELANDE Prdukt: Identifierare: Typ av åtgärd: Prduktkd: Serieintervall #s: HeartWare -batteri FSCA APR2014 Säkerhetsmeddelande 1650, 1650-DE Alla HeartWare serienummer för
20.05.14 VIKTIGT SÄKERHETSMEDDELANDE Prdukt: Identifierare: Typ av åtgärd: Prduktkd: Serieintervall #s: HeartWare -batteri FSCA APR2014 Säkerhetsmeddelande 1650, 1650-DE Alla HeartWare serienummer för
BRÅDSKANDE RÄTTELSE AV MEDICINTEKNISK PRODUKT
 23 december 2013 BRÅDSKANDE RÄTTELSE AV MEDICINTEKNISK PRODUKT Identifierare: FSCA DEC2013 Typ av åtgärd: Produktinspektion Produktnamn: HeartWare ventrikulära hjälpsystem Katalog #: 1100, 1101, 1102,
23 december 2013 BRÅDSKANDE RÄTTELSE AV MEDICINTEKNISK PRODUKT Identifierare: FSCA DEC2013 Typ av åtgärd: Produktinspektion Produktnamn: HeartWare ventrikulära hjälpsystem Katalog #: 1100, 1101, 1102,
VIKTIGT SÄKERHETSMEDDELANDE
 06.01.2015 Produkt: Typ av åtgärd: Produktkoder: Serieintervall #s: Återkallande av Kära HeartWare-läkare, 2013 rekommenderade HeartWare er om åtgärder i samband med patientsäkerhetsrisker förknippade
06.01.2015 Produkt: Typ av åtgärd: Produktkoder: Serieintervall #s: Återkallande av Kära HeartWare-läkare, 2013 rekommenderade HeartWare er om åtgärder i samband med patientsäkerhetsrisker förknippade
XX maj 2015 BRÅDSKANDE FÄLTSÄKERHETSMEDDELANDE. HeartWare HVAD System
 XX maj 2015 BRÅDSKANDE FÄLTSÄKERHETSMEDDELANDE HeartWare HVAD System Identifierare: FSCA APR2015A Typ av åtgärd: Säkerhetsmeddelande Produktkoder: 1100, 1101, 1102, 1103, 1104, 1104JP, 1205 Serienummerintervall:
XX maj 2015 BRÅDSKANDE FÄLTSÄKERHETSMEDDELANDE HeartWare HVAD System Identifierare: FSCA APR2015A Typ av åtgärd: Säkerhetsmeddelande Produktkoder: 1100, 1101, 1102, 1103, 1104, 1104JP, 1205 Serienummerintervall:
BRÅDSKANDE: SÄKERHETSMEDDELANDE
 14 september 2015 BRÅDSKANDE: SÄKERHETSMEDDELANDE Berörda enheter: Alla serienummer av systemstyrenheten HeartMate II, modell nr. 105109 (Pocket Controller TM ), som levereras inom följande förpackningskonfigurationer:
14 september 2015 BRÅDSKANDE: SÄKERHETSMEDDELANDE Berörda enheter: Alla serienummer av systemstyrenheten HeartMate II, modell nr. 105109 (Pocket Controller TM ), som levereras inom följande förpackningskonfigurationer:
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Litiumjonbatteripaket som används i BIS Vista och BIS View övervakningssystem.
 Augusti 2018 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Litiumjonbatteripaket som används i BIS Vista och BIS View övervakningssystem. Medtronic-referens: FA832 Till: Materialansvarig för operationsavdelningen,
Augusti 2018 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Litiumjonbatteripaket som används i BIS Vista och BIS View övervakningssystem. Medtronic-referens: FA832 Till: Materialansvarig för operationsavdelningen,
Det här dokumentet innehåller viktig information om fortsatt säker och korrekt användning av din utrustning
 Philips Healthcare - 1/6 - FSN86100179A Bästa kund, Philips har upptäckt att HeartStart MRx-monitorn/defibrillatorn kan fungera onormalt. I mycket sällsynta fall kan en fungera felaktigt på följande sätt.
Philips Healthcare - 1/6 - FSN86100179A Bästa kund, Philips har upptäckt att HeartStart MRx-monitorn/defibrillatorn kan fungera onormalt. I mycket sällsynta fall kan en fungera felaktigt på följande sätt.
Viktigt säkerhetsmeddelande till marknaden
 Helsingborg, 10 januari 2017 Till: Distributörer och sjukvårdspersonal Viktigt säkerhetsmeddelande till marknaden Bästa kund, Vigmed AB har frivilligt initierat en korrigerande säkerhetsåtgärd på marknaden
Helsingborg, 10 januari 2017 Till: Distributörer och sjukvårdspersonal Viktigt säkerhetsmeddelande till marknaden Bästa kund, Vigmed AB har frivilligt initierat en korrigerande säkerhetsåtgärd på marknaden
Philips Healthcare - 1/8 - FSN A Maj 2019
 Philips Healthcare - 1/8 - FSN86100188A Bästa kund, Philips har fastställt att växelströmsmodulen M3539A för monitorn/defibrillatorn kan uppvisa fel oftare än förväntat. Felen berodde på en felaktig intern
Philips Healthcare - 1/8 - FSN86100188A Bästa kund, Philips har fastställt att växelströmsmodulen M3539A för monitorn/defibrillatorn kan uppvisa fel oftare än förväntat. Felen berodde på en felaktig intern
Viktigt säkerhetsmeddelande December 11, 2015
 Viktigt säkerhetsmeddelande December 11, 2015 Ambu AuraGain ------------------------------------------------------------------------------------------------------------------------------- Detaljer på berörda
Viktigt säkerhetsmeddelande December 11, 2015 Ambu AuraGain ------------------------------------------------------------------------------------------------------------------------------- Detaljer på berörda
Viktigt säkerhetsmeddelande till marknaden
 Viktigt säkerhetsmeddelande till marknaden Ämne: Mobila uppresningslyftar Liko Viking L, Viking M, Viking XL och Viking 300 Potentiell skada på domkraft FSCA-referens: Mod 1228 Typ av åtgärd: Meddelande
Viktigt säkerhetsmeddelande till marknaden Ämne: Mobila uppresningslyftar Liko Viking L, Viking M, Viking XL och Viking 300 Potentiell skada på domkraft FSCA-referens: Mod 1228 Typ av åtgärd: Meddelande
VIKTIGT: SÄKERHETSMEDDELANDE. Externa nätaggregat för RENASYS GO. SÄKERHETSMEDDELANDE: 19 februari 2016
 Smith & Nephew, Inc. 970 Lake Carillon Dr, Suite 300 St. Petersburg, FL 33716 USA Kundtjänst: +1 800 876-1261 www.smith-nephew.com 19 februari 2016 Berörd produkt: FSCA-referens: 19 februari 2016 FSCA-åtgärd:
Smith & Nephew, Inc. 970 Lake Carillon Dr, Suite 300 St. Petersburg, FL 33716 USA Kundtjänst: +1 800 876-1261 www.smith-nephew.com 19 februari 2016 Berörd produkt: FSCA-referens: 19 februari 2016 FSCA-åtgärd:
Brådskande säkerhetsmeddelande
 Brådskande säkerhetsmeddelande Kommersiellt namn/modell: Infusionspump BeneFusion VP1 och BeneFusion VP3 FSCA-identifierare: XS-20170717 Typ av åtgärd: Säkerhetsmeddelande och ändring av enhet - Juli 2017
Brådskande säkerhetsmeddelande Kommersiellt namn/modell: Infusionspump BeneFusion VP1 och BeneFusion VP3 FSCA-identifierare: XS-20170717 Typ av åtgärd: Säkerhetsmeddelande och ändring av enhet - Juli 2017
90520US; 90520EU; 90520UK; 90520AU Integra Battery Kits US; 90530EU; 90530UK; 90530AU Integra LED Battery Charger, Single Bay 90523
 Till avdelningen för kvalitetssäkring och/eller juridiska frågor eller företagsledningen Ärende: BRÅDSKANDE MEDDELANDE OM FRIVILLIG ÅTERKALLELSE Medicinteknisk produkt: Integra LED Battery Charger, Single
Till avdelningen för kvalitetssäkring och/eller juridiska frågor eller företagsledningen Ärende: BRÅDSKANDE MEDDELANDE OM FRIVILLIG ÅTERKALLELSE Medicinteknisk produkt: Integra LED Battery Charger, Single
10 januari, 2018 BRÅDSKANDE: VIKTIGT SÄKERHETSMEDDELANDE GÄLLANDE PRODUKTERNA TISSU-TRANS
 10 januari, 2018 BRÅDSKANDE: VIKTIGT SÄKERHETSMEDDELANDE GÄLLANDE PRODUKTERNA TISSU-TRANS Bästa kund/distributör av enheten, Syftet med detta brev är att göra dig uppmärksam på att Shippert Medical Technologies
10 januari, 2018 BRÅDSKANDE: VIKTIGT SÄKERHETSMEDDELANDE GÄLLANDE PRODUKTERNA TISSU-TRANS Bästa kund/distributör av enheten, Syftet med detta brev är att göra dig uppmärksam på att Shippert Medical Technologies
12 juni, 2017 VIKTIGT! SÄKERHETSMEDDELANDE TILL MARKNADEN TISSU-TRANS-PRODUKTER
 12 juni, 2017 VIKTIGT! SÄKERHETSMEDDELANDE TILL MARKNADEN TISSU-TRANS-PRODUKTER Bästa kund/distributör! Syftet med detta brev är att informera om att Shippert Medical Technologies utfärdar ett säkerhetsmeddelande
12 juni, 2017 VIKTIGT! SÄKERHETSMEDDELANDE TILL MARKNADEN TISSU-TRANS-PRODUKTER Bästa kund/distributör! Syftet med detta brev är att informera om att Shippert Medical Technologies utfärdar ett säkerhetsmeddelande
VIKTIGT SÄKERHETSMEDDELANDE
 VIKTIGT SÄKERHETSMEDDELANDE Kommersiellt namn på berörd produkt: Medrad Continuum infusionssystem för MR FSCA-ID: SA-13-RAD-13 Typ av åtgärd: Inspektion av systemhållaren/-stiftet på icke-trådlösa system
VIKTIGT SÄKERHETSMEDDELANDE Kommersiellt namn på berörd produkt: Medrad Continuum infusionssystem för MR FSCA-ID: SA-13-RAD-13 Typ av åtgärd: Inspektion av systemhållaren/-stiftet på icke-trådlösa system
BRÅDSKANDE SÄKERHETSMEDDELANDE
 CareFusion Switzerland 317 Sàrl A-One Business Centre Z.A. Vers-La-Pièce n 10 1180 Rolle / Switzerland Tel: +41 21 556 30 00 Fax: +41 21 556 30 99 Namn Adress carefusion.com Produktnamn: Produktreferens:
CareFusion Switzerland 317 Sàrl A-One Business Centre Z.A. Vers-La-Pièce n 10 1180 Rolle / Switzerland Tel: +41 21 556 30 00 Fax: +41 21 556 30 99 Namn Adress carefusion.com Produktnamn: Produktreferens:
Powerware 3105 UPS Användarhandbok
 Powerware 3105 UPS 2005 Eaton Corporation Innehållet i denna handbok är skyddat enligt upphovsrättslagen och får varken helt eller delvis kopieras utan uttrycklig tillåtelse av utgivaren. Stor noggrannhet
Powerware 3105 UPS 2005 Eaton Corporation Innehållet i denna handbok är skyddat enligt upphovsrättslagen och får varken helt eller delvis kopieras utan uttrycklig tillåtelse av utgivaren. Stor noggrannhet
Powerware 3105 UPS Användarhandbok
 Powerware 3105 UPS 2005 Eaton Corporation Innehållet i denna handbok är skyddat enligt upphovsrättslagen och får varken helt eller delvis kopieras utan uttrycklig tillåtelse av utgivaren. Stor noggrannhet
Powerware 3105 UPS 2005 Eaton Corporation Innehållet i denna handbok är skyddat enligt upphovsrättslagen och får varken helt eller delvis kopieras utan uttrycklig tillåtelse av utgivaren. Stor noggrannhet
Handbok Automatisk batteriladdare modell BATIUM 7-24 och BATIUM 15-24
 Handbok Automatisk batteriladdare modell BATIUM 7-24 och BATIUM 15-24 Lämplig för blyackumulatorer med elektrolyt i form av vätska eller gel Vi gratulerar till att du valt den här produkten, som har konstruerats
Handbok Automatisk batteriladdare modell BATIUM 7-24 och BATIUM 15-24 Lämplig för blyackumulatorer med elektrolyt i form av vätska eller gel Vi gratulerar till att du valt den här produkten, som har konstruerats
BRÅDSKANDE: FÄLTSÄKERHETSMEDDELANDE
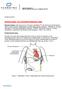 23 februari 2012 BRÅDSKANDE: FÄLTSÄKERHETSMEDDELANDE Berörda enheter: Alla lotnummer av Thoratec HeartMate II Left Ventricular Assist System (HM II LVAS) Förslutet utflödesgraft med böjningsavlastare (katalognr.
23 februari 2012 BRÅDSKANDE: FÄLTSÄKERHETSMEDDELANDE Berörda enheter: Alla lotnummer av Thoratec HeartMate II Left Ventricular Assist System (HM II LVAS) Förslutet utflödesgraft med böjningsavlastare (katalognr.
Power Pods. Garanti & Support. Teknisk Support
 Garanti & Support Denna produkt är försedd med ett års garanti för fel som uppstår vid normal användning. Vid missbruk av det Power Pods eller vid öppning av enheten upphör garantin. Allt utöver garantireparationer
Garanti & Support Denna produkt är försedd med ett års garanti för fel som uppstår vid normal användning. Vid missbruk av det Power Pods eller vid öppning av enheten upphör garantin. Allt utöver garantireparationer
Viktiga säkerhetsmeddelanden. Paradigm insulinpumpssystem
 Viktiga säkerhetsmeddelanden Paradigm insulinpumpssystem 5 juli 2013 Till dig som arbetar inom hälso- och sjukvården Bifogat finns viktig säkerhetsinformation och rekommendationer för patienthantering
Viktiga säkerhetsmeddelanden Paradigm insulinpumpssystem 5 juli 2013 Till dig som arbetar inom hälso- och sjukvården Bifogat finns viktig säkerhetsinformation och rekommendationer för patienthantering
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN
 Teleflex Medical IDA Business & Technology Park Dublin Road, Athlone Westmeath, Irland VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN 21 september 2018 Typ av åtgärd Återkallning Teleflex-referens: EIF-000291
Teleflex Medical IDA Business & Technology Park Dublin Road, Athlone Westmeath, Irland VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN 21 september 2018 Typ av åtgärd Återkallning Teleflex-referens: EIF-000291
VIKTIGT MEDDELANDE TILL MARKNADEN: RA2011-161
 VIKTIGT MEDDELANDE TILL MARKNADEN: RA2011-161 «ShipTo_Customer_Name» «Contact _Name» «ShipTo_Address_1» «ShipTo_Address_2_» «ShipTo_Address_3_» «SHIPTOCITY», «SHIPTOST» «SHIPTOZIP» Bäste kund, Beskrivning:
VIKTIGT MEDDELANDE TILL MARKNADEN: RA2011-161 «ShipTo_Customer_Name» «Contact _Name» «ShipTo_Address_1» «ShipTo_Address_2_» «ShipTo_Address_3_» «SHIPTOCITY», «SHIPTOST» «SHIPTOZIP» Bäste kund, Beskrivning:
ALERTpager, Repeaterstation
 Bruksanvisning ALERTpager, Repeaterstation Artikelnr: 464 303 ALERTpager, Repeaterstation är en kombinerad sändare och mottagare som sänder vidare signalerna från ALERTpager personsökare. Innehållsförteckning
Bruksanvisning ALERTpager, Repeaterstation Artikelnr: 464 303 ALERTpager, Repeaterstation är en kombinerad sändare och mottagare som sänder vidare signalerna från ALERTpager personsökare. Innehållsförteckning
ANSELL SANDEL SÄKERHETSSKALPELL MED VIKT FSCA-2013/11/80
 Brevhuvud Ansell EU --------------------------------------------------------------------------------------------------------------------------- Viktigt säkerhetsmeddelande ANSELL SANDEL SÄKERHETSSKALPELL
Brevhuvud Ansell EU --------------------------------------------------------------------------------------------------------------------------- Viktigt säkerhetsmeddelande ANSELL SANDEL SÄKERHETSSKALPELL
VIKTIGT säkerhetsmeddelande till marknaden: RA
 07 februari 2019 VIKTIGT säkerhetsmeddelande till marknaden: RA2018-1976124 FSCA-identifiering: Produktåterkallelse RA2018-1976124 Åtgärdstyp: Korrigerande säkerhetsåtgärd på marknaden Berörda produkter:
07 februari 2019 VIKTIGT säkerhetsmeddelande till marknaden: RA2018-1976124 FSCA-identifiering: Produktåterkallelse RA2018-1976124 Åtgärdstyp: Korrigerande säkerhetsåtgärd på marknaden Berörda produkter:
VIKTIGT SÄKERHETSMEDDELANDE: RA
 2013-08-30 VIKTIGT SÄKERHETSMEDDELANDE: RA2013-104 FSCA-identifiering: Produktåtgärd på marknaden RA 2013-104 Typ av åtgärd: Beskrivning: Korrigerande säkerhetsåtgärd på marknaden Katalognr.: Se den bifogade
2013-08-30 VIKTIGT SÄKERHETSMEDDELANDE: RA2013-104 FSCA-identifiering: Produktåtgärd på marknaden RA 2013-104 Typ av åtgärd: Beskrivning: Korrigerande säkerhetsåtgärd på marknaden Katalognr.: Se den bifogade
VIKTIGT SÄKERHETSMEDDELANDE
 Teleflex Medical IDA Business & Technology Park Dublin Road, Athlone Co. Westmeath, Irland 07 Jan 2010 VIKTIGT SÄKERHETSMEDDELANDE Den berörda produktens kommersiella namn: Typ av åtgärd: Produktnummer:
Teleflex Medical IDA Business & Technology Park Dublin Road, Athlone Co. Westmeath, Irland 07 Jan 2010 VIKTIGT SÄKERHETSMEDDELANDE Den berörda produktens kommersiella namn: Typ av åtgärd: Produktnummer:
Viktigt säkerhetsmeddelande
 Viktigt säkerhetsmeddelande SONY LMD-1951MD BILDSKÄRMAR Det föreligger risk för att bildskärmen stängs av eller inte visar någon bild Återkallande av medicinsk enhet Datum: 14 januari 2015 För kännedom:
Viktigt säkerhetsmeddelande SONY LMD-1951MD BILDSKÄRMAR Det föreligger risk för att bildskärmen stängs av eller inte visar någon bild Återkallande av medicinsk enhet Datum: 14 januari 2015 För kännedom:
VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE
 VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE Handelsnamn: Olika syrgasmasker med hög koncentration från Unomedical (se bilaga 1 för fullständig information) Utfärdandedatum: 16 maj 2017 REF-nr: Se bilaga
VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE Handelsnamn: Olika syrgasmasker med hög koncentration från Unomedical (se bilaga 1 för fullständig information) Utfärdandedatum: 16 maj 2017 REF-nr: Se bilaga
Viktigt säkerhetsmeddelande
 Retur av en medicinteknisk produkt till leverantören Förfylld silikonoljespruta av glas kan gå sönder när den används i kombination med VFI-pack för silikonoljesprutor Artikelnummer 1363.DD Beskrivning
Retur av en medicinteknisk produkt till leverantören Förfylld silikonoljespruta av glas kan gå sönder när den används i kombination med VFI-pack för silikonoljesprutor Artikelnummer 1363.DD Beskrivning
Bruksanvisning Svensk. Larmenhet & Sensorplåster
 Bruksanvisning Svensk Larmenhet & Sensorplåster Bruksanvisning Larmenhet & Sensorplåster Svensk version 2009 Redsense Medical AB Box 287 301 07 Halmstad www.redsensemedical.com RM-1-RM014 Innehåll Varningar
Bruksanvisning Svensk Larmenhet & Sensorplåster Bruksanvisning Larmenhet & Sensorplåster Svensk version 2009 Redsense Medical AB Box 287 301 07 Halmstad www.redsensemedical.com RM-1-RM014 Innehåll Varningar
Viktigt säkerhetsmeddelande till marknaden: Brådskande produktåterkallelse. Engångsartiklar inom bildtagnings tillbehör Slangar och sprutor
 Viktigt säkerhetsmeddelande till marknaden: Brådskande produktåterkallelse Engångsartiklar inom bildtagnings tillbehör Slangar och sprutor DATUM: Februari, 2012 ANGÅENDE: Engångsartiklar inom bildtagningstillbehör,
Viktigt säkerhetsmeddelande till marknaden: Brådskande produktåterkallelse Engångsartiklar inom bildtagnings tillbehör Slangar och sprutor DATUM: Februari, 2012 ANGÅENDE: Engångsartiklar inom bildtagningstillbehör,
Viktigt säkerhetsmeddelande till marknaden
 Audionomens namn Gatuadress Postnummer, ort WIDEX A/S Nymoellevej 6 3540 Lynge Danmark Tel.: (+45) 44 35 56 00 Fax: (+45) 44 35 56 01 widex@widex.com www.widex.com 28 augusti 2018 Viktigt säkerhetsmeddelande
Audionomens namn Gatuadress Postnummer, ort WIDEX A/S Nymoellevej 6 3540 Lynge Danmark Tel.: (+45) 44 35 56 00 Fax: (+45) 44 35 56 01 widex@widex.com www.widex.com 28 augusti 2018 Viktigt säkerhetsmeddelande
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Mon-a-Therm Foley-kateter med temperatursensor
 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Mon-a-Therm Foley-kateter med temperatursensor Augusti 2018 Medtronic-referens: FA835 Till: Chefen för riskhantering och chefen för materialhantering Bästa kund:
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Mon-a-Therm Foley-kateter med temperatursensor Augusti 2018 Medtronic-referens: FA835 Till: Chefen för riskhantering och chefen för materialhantering Bästa kund:
VIKTIGT SÄKERHETSMEDDELANDE
 VIKTIGT SÄKERHETSMEDDELANDE PAS-14-408-FA 12 juli 2014 BD Vacutainer CPT TM (Cell Preparation Tube) Till berörda personer inom: Riskhantering, Laboratorie, Logistik, Blodprovstagare, kliniska studier och
VIKTIGT SÄKERHETSMEDDELANDE PAS-14-408-FA 12 juli 2014 BD Vacutainer CPT TM (Cell Preparation Tube) Till berörda personer inom: Riskhantering, Laboratorie, Logistik, Blodprovstagare, kliniska studier och
Viktigt säkerhetsmeddelande
 IMMULITE 2000 IMMULITE 2000 XPi Viktigt säkerhetsmeddelande 3022/ 044 FSCA IMI 14-02 Mars 2015 Problem med flaskor för vatten och flytande avfall Enligt våra noteringar kan ditt laboratorium ha mottagit
IMMULITE 2000 IMMULITE 2000 XPi Viktigt säkerhetsmeddelande 3022/ 044 FSCA IMI 14-02 Mars 2015 Problem med flaskor för vatten och flytande avfall Enligt våra noteringar kan ditt laboratorium ha mottagit
Viktigt säkerhetsmeddelande
 Kära kund, Som en del av Samsung Electronics kontinuerliga fokus på prestanda och säkerhet, har vi identifierat ett potentiellt problem som kan påverka Samsungs digitala röntgensystem GC80, GC85 och GC70.
Kära kund, Som en del av Samsung Electronics kontinuerliga fokus på prestanda och säkerhet, har vi identifierat ett potentiellt problem som kan påverka Samsungs digitala röntgensystem GC80, GC85 och GC70.
Produktkod Beskrivning Produktkod Beskrivning
 Till avdelningen för kvalitetssäkring eller registrerings- och regelfrågor eller företagsledningen 8 juli 2013 Angående: BRÅDSKANDE MEDDELANDE ANGÅENDE FÄLTSÄKERHET - ÅTERKALLNINGSBREV Medicinsk anordning:
Till avdelningen för kvalitetssäkring eller registrerings- och regelfrågor eller företagsledningen 8 juli 2013 Angående: BRÅDSKANDE MEDDELANDE ANGÅENDE FÄLTSÄKERHET - ÅTERKALLNINGSBREV Medicinsk anordning:
Eurocharger Bruksanvisning
 Batteriladdare till mobiltelefonen Eurocharger Bruksanvisning 4 12 13 LZTA 804 3258, 96-03 Översikt Grön: laddaren är på Telefon med batteri Röd: batteriet laddas Ljusgrön: batteriet är laddat Rödgul blink:
Batteriladdare till mobiltelefonen Eurocharger Bruksanvisning 4 12 13 LZTA 804 3258, 96-03 Översikt Grön: laddaren är på Telefon med batteri Röd: batteriet laddas Ljusgrön: batteriet är laddat Rödgul blink:
VIKTIGT SÄKERHETSMEDDELANDE Viktig korrigerande säkerhetsåtgärd
 VIKTIGT SÄKERHETSMEDDELANDE Viktig korrigerande säkerhetsåtgärd Maquet CARDIOSAVE Hybrid Intra-Aortic Balloon Pump (IABP) Maquet CARDIOSAVE Rescue Intra-Aortic Balloon Pump (IABP) BERÖRDA PRODUKTER KOMPONENTNUMMER
VIKTIGT SÄKERHETSMEDDELANDE Viktig korrigerande säkerhetsåtgärd Maquet CARDIOSAVE Hybrid Intra-Aortic Balloon Pump (IABP) Maquet CARDIOSAVE Rescue Intra-Aortic Balloon Pump (IABP) BERÖRDA PRODUKTER KOMPONENTNUMMER
Viktigt säkerhetsmeddelande till marknaden
 Viktigt säkerhetsmeddelande till marknaden Varumärke/modell: Beneview T1 Patient Monitor FSCA-identifiering: CP17-JH0008 Åtgärdstyp: Enhetsbyte OBS! [Namn på sjukhus/distributör] Hej! April 2017 Efter
Viktigt säkerhetsmeddelande till marknaden Varumärke/modell: Beneview T1 Patient Monitor FSCA-identifiering: CP17-JH0008 Åtgärdstyp: Enhetsbyte OBS! [Namn på sjukhus/distributör] Hej! April 2017 Efter
Brådskande fältsäkerhetsmeddelande Viktig information om medicinteknisk produkt
 VASCUTEK Ltd Newmains Avenue, Inchinnan, Renfrewshire, PA4 9RR, Skottland, Storbritannien Tel: +44 (0) 141 812 5555 www.vascutek.com 30 oktober 2017 Till: Kärlkirurger, radiologer, riskansvariga, upphandling,
VASCUTEK Ltd Newmains Avenue, Inchinnan, Renfrewshire, PA4 9RR, Skottland, Storbritannien Tel: +44 (0) 141 812 5555 www.vascutek.com 30 oktober 2017 Till: Kärlkirurger, radiologer, riskansvariga, upphandling,
VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE
 VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE Handelsnamn: LOT-nr: FSCA-ID: Typ av åtgärd: HandyVac TM lågvakuumsystem för dränering av kirurgiska sår CH (Fr.) 14 HandyVac TM ATS lågvakuumsystem för dränering
VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE Handelsnamn: LOT-nr: FSCA-ID: Typ av åtgärd: HandyVac TM lågvakuumsystem för dränering av kirurgiska sår CH (Fr.) 14 HandyVac TM ATS lågvakuumsystem för dränering
BRÅDSKANDE: Säkerhetsmeddelande för marknaden
 5 juli 2011 BRÅDSKANDE: Säkerhetsmeddelande för marknaden Berörd produkt: HMRS-Distal femur resektionskomponent samt distal femur komponent. FSCA-identifiering: Åtgärd för produkter på marknaden RA 2009-436
5 juli 2011 BRÅDSKANDE: Säkerhetsmeddelande för marknaden Berörd produkt: HMRS-Distal femur resektionskomponent samt distal femur komponent. FSCA-identifiering: Åtgärd för produkter på marknaden RA 2009-436
BRÅDSKANDE SÄKERHETSVARNING och ÅTERKALLELSE av MEDICINTEKNISK UTRUSTNING
 17 maj 2013 BRÅDSKANDE SÄKERHETSVARNING och ÅTERKALLELSE av MEDICINTEKNISK UTRUSTNING www.verathon.com Kära GlideScope -kund! Verathon, tillverkare av GlideScope videolaryngoskop, genomför en säkerhetsvarning
17 maj 2013 BRÅDSKANDE SÄKERHETSVARNING och ÅTERKALLELSE av MEDICINTEKNISK UTRUSTNING www.verathon.com Kära GlideScope -kund! Verathon, tillverkare av GlideScope videolaryngoskop, genomför en säkerhetsvarning
Rekonditionering. EPIsafe och EPIsafe 2. Art.nr och Programversion x.x.x eller senare. Rev PB SE
 Instruktion Rekonditionering EPIsafe och EPIsafe 2 Art.nr 464220 och 464230 Programversion x.x.x eller senare Rev PB SE Innehållsförteckning 1. Inledning... 3 1.1 Viktig information... 3 2. Rekonditioneringsförfarande...
Instruktion Rekonditionering EPIsafe och EPIsafe 2 Art.nr 464220 och 464230 Programversion x.x.x eller senare Rev PB SE Innehållsförteckning 1. Inledning... 3 1.1 Viktig information... 3 2. Rekonditioneringsförfarande...
Användarmanual. Bluetooth Headset
 Voicecom BT-60 Användarmanual Bluetooth Headset Första gången du laddar Tack för att du köpt BT-60 blåtandsheadset. Innan du använder ditt headset för första gången är det viktigt att du laddar det minst
Voicecom BT-60 Användarmanual Bluetooth Headset Första gången du laddar Tack för att du köpt BT-60 blåtandsheadset. Innan du använder ditt headset för första gången är det viktigt att du laddar det minst
VIKTIGT SÄKERHETSMEDDELANDE Ref /10/ R LÄS IGENOM NOGGRANT. Greatbatch Medical Offset Reamer Handle
 VIKTIGT SÄKERHETSMEDDELANDE Ref-3004976965-10/10/16-003-R LÄS IGENOM NOGGRANT Greatbatch Medical Offset Reamer Handle Offset Reamer Handle Offset Reamer Handle Katalognummer Modell 00-7804-080-00 T5766
VIKTIGT SÄKERHETSMEDDELANDE Ref-3004976965-10/10/16-003-R LÄS IGENOM NOGGRANT Greatbatch Medical Offset Reamer Handle Offset Reamer Handle Offset Reamer Handle Katalognummer Modell 00-7804-080-00 T5766
Viktig uppdatering av säkerhetsinformation
 Thoratec Corporation HEARTMATE II LEFT VENTRICULAR ASSIST SYSTEM Viktig uppdatering av säkerhetsinformation Tillägg till bruksanvisning för HeartMate II LVAS (dokumentnummer 106020 och 106021) USA och
Thoratec Corporation HEARTMATE II LEFT VENTRICULAR ASSIST SYSTEM Viktig uppdatering av säkerhetsinformation Tillägg till bruksanvisning för HeartMate II LVAS (dokumentnummer 106020 och 106021) USA och
Rekommendationer angående Zimmer Biomet Pulsavac Plus-enheter
 27 september 2017 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Till: Kirurger/sjukhus Ämne:VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN ANGÅENDE MEDICINTEKNISK PRODUKT (KORRIGERING) Referens: ZFA2017-266 Berörd
27 september 2017 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN Till: Kirurger/sjukhus Ämne:VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN ANGÅENDE MEDICINTEKNISK PRODUKT (KORRIGERING) Referens: ZFA2017-266 Berörd
Teknisk support
 Teknisk support För teknisk support eller support i nödfall ber vi dig kontakta den lokala leverantör av medicintekniska produkter som levererade eller sålde LifeChoice Activox POC-enheten till dig. www.inovalabs.com
Teknisk support För teknisk support eller support i nödfall ber vi dig kontakta den lokala leverantör av medicintekniska produkter som levererade eller sålde LifeChoice Activox POC-enheten till dig. www.inovalabs.com
BRÅDSKANDE ÅTERKALLANDE AV MEDICINSK UTRUSTNING Indiko och Indiko Plus, analysatorer för klinisk kemi
 Bilaga 2. BRÅDSKANDE ÅTERKALLANDE AV MEDICINSK UTRUSTNING Indiko och Indiko Plus, analysatorer för klinisk kemi 26 september 2013 [Infoga namn på kund eller distributör Att: Laboratorieansvarig Adress
Bilaga 2. BRÅDSKANDE ÅTERKALLANDE AV MEDICINSK UTRUSTNING Indiko och Indiko Plus, analysatorer för klinisk kemi 26 september 2013 [Infoga namn på kund eller distributör Att: Laboratorieansvarig Adress
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN
 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN PLATINIUM: periodisk kontaktförlust på DF-4 kontakten FSCA ID: Affected Devices: CRM-SAL-2017-001 Date: 16. Mars, 2018 Attention: Platinium implanterbara hjärtdefibrillatorer
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN PLATINIUM: periodisk kontaktförlust på DF-4 kontakten FSCA ID: Affected Devices: CRM-SAL-2017-001 Date: 16. Mars, 2018 Attention: Platinium implanterbara hjärtdefibrillatorer
/14/ R
 Viktigt säkerhetsmeddelande till marknaden Återkallande av medicinteknisk produkt - 2955842-07/14/16-010-R Viktig uppföljning av brådskande meddelande om att stoppa användning av rullagerprodukt För specifika
Viktigt säkerhetsmeddelande till marknaden Återkallande av medicinteknisk produkt - 2955842-07/14/16-010-R Viktig uppföljning av brådskande meddelande om att stoppa användning av rullagerprodukt För specifika
BRÅDSKANDE - Korrigering av medicinsk utrustning Philips HeartStart MRx-monitor/defibrillator
 Philips Healthcare - 1/5 - FSN86100123A Bästa kund, Det här är en information från Philips Healthcare angående en produktkorrigering gällande ett problem som uppstår när används för synkroniserad elkonvertering.
Philips Healthcare - 1/5 - FSN86100123A Bästa kund, Det här är en information från Philips Healthcare angående en produktkorrigering gällande ett problem som uppstår när används för synkroniserad elkonvertering.
C
 Säkerhetsmeddelande till marknaden Brådskande: Korrigering av medicinteknisk utrustning 2955842-11-11-2013-013-C Vissa instrumentarmar på systemen da Vinci S, Si och Si-e som anges i bifogat dokument Introduktion
Säkerhetsmeddelande till marknaden Brådskande: Korrigering av medicinteknisk utrustning 2955842-11-11-2013-013-C Vissa instrumentarmar på systemen da Vinci S, Si och Si-e som anges i bifogat dokument Introduktion
Teknisk manual NASA BM-1C Kompakt Batterimonitor
 1 1 Teknisk manual NASA BM-1C Kompakt Batterimonitor 2 2 Innehållsförteckning Läs detta först... 3 Sammanfattning... 3 Teknisk data... 3 Installation... 4 Varning-viktigt... 4 Display-enhet... 4 Shunt-och
1 1 Teknisk manual NASA BM-1C Kompakt Batterimonitor 2 2 Innehållsförteckning Läs detta först... 3 Sammanfattning... 3 Teknisk data... 3 Installation... 4 Varning-viktigt... 4 Display-enhet... 4 Shunt-och
Viktigt säkerhetsmeddelande till marknaden (återkallelse)
 Viktigt säkerhetsmeddelande till marknaden (återkallelse) beträffande CORAIL COXA VARA HIGH OFFSET STEM med krage, storlek 9 (artikelnummer: 3L93709, tillverkningssats: 5291990) och CORAIL HIGH OFFSET
Viktigt säkerhetsmeddelande till marknaden (återkallelse) beträffande CORAIL COXA VARA HIGH OFFSET STEM med krage, storlek 9 (artikelnummer: 3L93709, tillverkningssats: 5291990) och CORAIL HIGH OFFSET
VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE
 VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE Handelsnamn: AbViserTM AutoValveTM IAP-mätinstrument (se bilaga 1 för fullständig information) Utgivningsdatum: 25 april, 2018 REF.nr: Se bilaga 1 LOT-nr: Alla
VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE Handelsnamn: AbViserTM AutoValveTM IAP-mätinstrument (se bilaga 1 för fullständig information) Utgivningsdatum: 25 april, 2018 REF.nr: Se bilaga 1 LOT-nr: Alla
Rekonditionering. EPIsafe 2 GSM. Art.nr 464238. Programversion x.x.x eller senare. Rev PA1 SE
 Instruktion Rekonditionering EPIsafe 2 GSM Art.nr 464238 Programversion x.x.x eller senare Rev PA1 SE Innehållsförteckning 1. Inledning... 2 1.1 Viktig information... 2 2. Rekonditioneringsförfarande...
Instruktion Rekonditionering EPIsafe 2 GSM Art.nr 464238 Programversion x.x.x eller senare Rev PA1 SE Innehållsförteckning 1. Inledning... 2 1.1 Viktig information... 2 2. Rekonditioneringsförfarande...
Återkallande av medicintekniska produkter
 VIKTIGT säkerhetsmeddelande till marknaden pro med instruments GmbH, Boetzinger Str. 38, 79111 Freiburg, Tyskland Företag Kontaktperson Gatuadress Postnummer, ort, land Telefon, e-postadress Återkallande
VIKTIGT säkerhetsmeddelande till marknaden pro med instruments GmbH, Boetzinger Str. 38, 79111 Freiburg, Tyskland Företag Kontaktperson Gatuadress Postnummer, ort, land Telefon, e-postadress Återkallande
Säkerhetsmeddelande (Återkallande) Alla partier av DePuy Synthes Reach System Handle-instrument. Delnummer:
 Säkerhetsmeddelande (Återkallande) Alla partier av DePuy Synthes Reach System Handle-instrument Delnummer 950505154 Produktnamn: Reach System Handle-instrument FSCA-identifiering: 103189242 (HHE) Typ av
Säkerhetsmeddelande (Återkallande) Alla partier av DePuy Synthes Reach System Handle-instrument Delnummer 950505154 Produktnamn: Reach System Handle-instrument FSCA-identifiering: 103189242 (HHE) Typ av
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN FSCA - ETEST ETP32 - Ertapenem - blister packaging - Ref False Susceptible results
 biomérieux NORDICS Customer Service Department Direct no.: +46 31 68 58 58 Fax no.: +46 31 68 48 68 e-mail: customersupport.nordic@biomerieux.com Our Ref.: 3329 - FSCA - ETEST ETP32 - Ertapenem - blister
biomérieux NORDICS Customer Service Department Direct no.: +46 31 68 58 58 Fax no.: +46 31 68 48 68 e-mail: customersupport.nordic@biomerieux.com Our Ref.: 3329 - FSCA - ETEST ETP32 - Ertapenem - blister
Tilläggsinformation. 31 mars 2015. Till vårdgivaren:
 Tilläggsinformation Den berörda produktens kommersiella namn: Bead Block (emboliseringssfärer) FSCA-identifierare: PR #16295 Typ av åtgärd: Råd från tillverkaren angående användningen av produkten 31 mars
Tilläggsinformation Den berörda produktens kommersiella namn: Bead Block (emboliseringssfärer) FSCA-identifierare: PR #16295 Typ av åtgärd: Råd från tillverkaren angående användningen av produkten 31 mars
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN FSCA 3061 Etest COLISTIN CO256 WW (Ref ) - False Susceptible
 Customer Service Department Direct no.: +46 31 68 58 58 Fax no.: +46 31 68 48 48 e-mail: customersupport.nordic@biomerieux.com Our Ref.: FA_3061_ Etest COLISTIN CO256 WW (Ref. 537300-537308) - False Susceptible
Customer Service Department Direct no.: +46 31 68 58 58 Fax no.: +46 31 68 48 48 e-mail: customersupport.nordic@biomerieux.com Our Ref.: FA_3061_ Etest COLISTIN CO256 WW (Ref. 537300-537308) - False Susceptible
Healthcare Viktigt säkerhetsmeddelande
 Healthcare Viktigt säkerhetsmeddelande FSCA CC 12-01/10813950 utgåva A November 2012 ADVIA Centaur ADVIA Centaur XP ADVIA Centaur CP Effekter av omgivande temperatur på ADVIA Centaur-analyser Bästa kund,
Healthcare Viktigt säkerhetsmeddelande FSCA CC 12-01/10813950 utgåva A November 2012 ADVIA Centaur ADVIA Centaur XP ADVIA Centaur CP Effekter av omgivande temperatur på ADVIA Centaur-analyser Bästa kund,
VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE
 VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE Handelsnamn: Female-kateter Nelatonkateter Rektal kateter Mülly-sugkateter LOT-nr: Se tabell på sida 13 FSCA-ID: 2011/09/CTH3 Typ av åtgärd: Återkallande retur
VIKTIGT SÄKERHETSMEDDELANDE ÅTERFÖRSÄLJARE Handelsnamn: Female-kateter Nelatonkateter Rektal kateter Mülly-sugkateter LOT-nr: Se tabell på sida 13 FSCA-ID: 2011/09/CTH3 Typ av åtgärd: Återkallande retur
Comfort Focus Bruksanvisning. Comfort Focus. För ökad koncentration och inlärning. Svenska
 Comfort Focus Bruksanvisning Comfort Focus För ökad koncentration och inlärning Svenska 1 Laddning Produkterna drivs av uppladdningsbara batterier, och har en driftstid på 6-10 timmar. Ett tomt batteri
Comfort Focus Bruksanvisning Comfort Focus För ökad koncentration och inlärning Svenska 1 Laddning Produkterna drivs av uppladdningsbara batterier, och har en driftstid på 6-10 timmar. Ett tomt batteri
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN NM implanterbar pulsgenerator Felaktig indikering av elektivt utbyte (ERI)
 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN NM implanterbar pulsgenerator Felaktig indikering av elektivt utbyte (ERI) 12 sep 2017 Bästa läkare I syfte att hålla dig kontinuerligt informerad och att säkerställa
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN NM implanterbar pulsgenerator Felaktig indikering av elektivt utbyte (ERI) 12 sep 2017 Bästa läkare I syfte att hålla dig kontinuerligt informerad och att säkerställa
MICRO-START XP-5 BRUKSANVISNING
 MICRO-START XP-5 BRUKSANVISNING Teknisk specifikation Dimension: 135x77x16 mm. Vikt:230 gram. :Startström:150 A/peak 300 A Laddtid:3 tim. Kapacitet: 6000 milliamp. Arbetstemp: -20C - 60C. Dom vanligaste
MICRO-START XP-5 BRUKSANVISNING Teknisk specifikation Dimension: 135x77x16 mm. Vikt:230 gram. :Startström:150 A/peak 300 A Laddtid:3 tim. Kapacitet: 6000 milliamp. Arbetstemp: -20C - 60C. Dom vanligaste
Viktigt säkerhetsmeddelande till marknaden
 Viktigt säkerhetsmeddelande till marknaden Produktnamn: ADEPT Hip Resurfacing System (Finsbury Orthopaedics Ltd) FSCA-ID: DVA-108558-HHE Typ av åtgärd: Säkerhetsmeddelande till marknaden Datum: januari
Viktigt säkerhetsmeddelande till marknaden Produktnamn: ADEPT Hip Resurfacing System (Finsbury Orthopaedics Ltd) FSCA-ID: DVA-108558-HHE Typ av åtgärd: Säkerhetsmeddelande till marknaden Datum: januari
Brådskande korrigering av medicinsk utrustning /21/ C
 Brådskande korrigering av medicinsk utrustning 2955842-10/21/2013-010-C Utbyte av lampmoduler i metall på da Vinci Si (IS3000)-systemets belysningsanordning Åtgärder som bör vidtas Intuitive Surgical genomför
Brådskande korrigering av medicinsk utrustning 2955842-10/21/2013-010-C Utbyte av lampmoduler i metall på da Vinci Si (IS3000)-systemets belysningsanordning Åtgärder som bör vidtas Intuitive Surgical genomför
Din manual HP PAVILION SLIMLINE S7700 http://sv.yourpdfguides.com/dref/850818
 Du kan läsa rekommendationerna i instruktionsboken, den tekniska specifikationen eller installationsanvisningarna för HP PAVILION SLIMLINE S7700. Du hittar svar på alla dina frågor i HP PAVILION SLIMLINE
Du kan läsa rekommendationerna i instruktionsboken, den tekniska specifikationen eller installationsanvisningarna för HP PAVILION SLIMLINE S7700. Du hittar svar på alla dina frågor i HP PAVILION SLIMLINE
**** Meddelande om återkallning ****
 **** Meddelande om återkallning **** Bästa användare av cochleaimplantat, 24 november 2010 Vårt uppdrag på Advanced Bionics är att förbättra livskvaliteten för personer med hörselnedsättning och vår främsta
**** Meddelande om återkallning **** Bästa användare av cochleaimplantat, 24 november 2010 Vårt uppdrag på Advanced Bionics är att förbättra livskvaliteten för personer med hörselnedsättning och vår främsta
Viktigt säkerhetsmeddelande
 Viktigt säkerhetsmeddelande FSCA CC 12-03/10813387 Juli 2012 ADVIA Centaur, ADVIA Centaur XP Stabilitet på instrumentet för Multi-Diluent 1 vid användning med analyserna BNP och TSH3 Ultra Enligt våra
Viktigt säkerhetsmeddelande FSCA CC 12-03/10813387 Juli 2012 ADVIA Centaur, ADVIA Centaur XP Stabilitet på instrumentet för Multi-Diluent 1 vid användning med analyserna BNP och TSH3 Ultra Enligt våra
MICRO-START XP-10 BRUKSANVISNING
 MICRO-START XP-10 BRUKSANVISNING Teknisk specifikation Dimension: 225x88x28 mm. Vikt:510 gram. :Startström:400 A/peak 600 A Laddtid:3-4 tim. Kapacitet: 18000 milliamp. Arbetstemp: -20C - 60C. Dom vanligaste
MICRO-START XP-10 BRUKSANVISNING Teknisk specifikation Dimension: 225x88x28 mm. Vikt:510 gram. :Startström:400 A/peak 600 A Laddtid:3-4 tim. Kapacitet: 18000 milliamp. Arbetstemp: -20C - 60C. Dom vanligaste
VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE
 VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE Handelsnamn: Female-kateter Nelatonkateter Rektal kateter Mülly-sugkateter LOT-nr: Se tabell på sida 13 FSCA-ID: 2011/09/CTH3 Typ av åtgärd: Återkallande retur
VIKTIGT SÄKERHETSMEDDELANDE SLUTANVÄNDARE Handelsnamn: Female-kateter Nelatonkateter Rektal kateter Mülly-sugkateter LOT-nr: Se tabell på sida 13 FSCA-ID: 2011/09/CTH3 Typ av åtgärd: Återkallande retur
Tillbehörsrem till SAM Junctional Tourniquet (SJT) blodtrycksmanschett 2014/11/06 Modifiering/utbyte/destruktion av enheten
 BRÅDSKANDE SÄKERHETSMEDDELANDE TILL MARKNADEN Tillbehörsrem till SAM Junctional Tourniquet (SJT) blodtrycksmanschett 2014/11/06 Modifiering/utbyte/destruktion av enheten Till SAM Medicals kunder/distributörer
BRÅDSKANDE SÄKERHETSMEDDELANDE TILL MARKNADEN Tillbehörsrem till SAM Junctional Tourniquet (SJT) blodtrycksmanschett 2014/11/06 Modifiering/utbyte/destruktion av enheten Till SAM Medicals kunder/distributörer
Nokia Bluetooth Headset BH-112 Användarhandbok
 Nokia Bluetooth Headset BH-112 Användarhandbok Utgåva 1.1 2 Inledning Om ditt headset Med Nokias Bluetooth-headset BH-112 kan du ringa och besvara samtal och hålla händerna fria, även när du använder två
Nokia Bluetooth Headset BH-112 Användarhandbok Utgåva 1.1 2 Inledning Om ditt headset Med Nokias Bluetooth-headset BH-112 kan du ringa och besvara samtal och hålla händerna fria, även när du använder två
Viktig uppdatering av säkerhetsinformation
 Thoratec Corporation HEARTMATE II LEFT VENTRICULAR ASSIST SYSTEM Viktig uppdatering av säkerhetsinformation Tillägg till patienthandboken för HeartMate II LVAS (dokumentnummer 106022) USA och Kanada Thoratec
Thoratec Corporation HEARTMATE II LEFT VENTRICULAR ASSIST SYSTEM Viktig uppdatering av säkerhetsinformation Tillägg till patienthandboken för HeartMate II LVAS (dokumentnummer 106022) USA och Kanada Thoratec
BRÅDSKANDE VIKTIGT FÄLTSÄKERHETSMEDDELANDE
 BRÅDSKANDE VIKTIGT Det här är viktig information om en säkerhetsrisk som kan förekomma med din utrustning och om vilka åtgärder som måste vidtas för att upprätthålla säkerheten för personal och patienter.
BRÅDSKANDE VIKTIGT Det här är viktig information om en säkerhetsrisk som kan förekomma med din utrustning och om vilka åtgärder som måste vidtas för att upprätthålla säkerheten för personal och patienter.
Viktigt säkerhetsmeddelande (återkallelse) 12 specifika loter av GLOBAL UNITE plattform för axelsystem
 Viktigt säkerhetsmeddelande (återkallelse) 12 specifika loter av GLOBAL UNITE plattform för axelsystem Produktnamn: GLOBAL UNITE plattform för axelsystem FSCA-identifierare: PIE 1013757 Typ av åtgärd:
Viktigt säkerhetsmeddelande (återkallelse) 12 specifika loter av GLOBAL UNITE plattform för axelsystem Produktnamn: GLOBAL UNITE plattform för axelsystem FSCA-identifierare: PIE 1013757 Typ av åtgärd:
LITIUMDUBBELLADDARE 1941-P-1368 LITIUMMINILADDARE 1941-P-1341
 LITIUMDUBBELLADDARE 1941-P-1368 LITIUMMINILADDARE 1941-P-1341 LÄS OCH FÖLJ DESSA INSTRUKTIONER NOGA Keelers litiumladdare och handtag Läs detta instruktionsavsnitt noga innan du använder din Keelerprodukt.
LITIUMDUBBELLADDARE 1941-P-1368 LITIUMMINILADDARE 1941-P-1341 LÄS OCH FÖLJ DESSA INSTRUKTIONER NOGA Keelers litiumladdare och handtag Läs detta instruktionsavsnitt noga innan du använder din Keelerprodukt.
ANVÄNDARMANUAL 12 V Blybatterier 1-85 Ah
 ANVÄNDARMANUAL 12 V Blybatterier 1-85 Ah SE 1 Tack för att du valt en laddare från Exide Technologies Din nya batteriladdare hjälper dig att hålla batteriet vid full kapacitet och förlänger livslängden.
ANVÄNDARMANUAL 12 V Blybatterier 1-85 Ah SE 1 Tack för att du valt en laddare från Exide Technologies Din nya batteriladdare hjälper dig att hålla batteriet vid full kapacitet och förlänger livslängden.
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN NM implanterbar pulsgenerator Felaktig indikering av elektivt utbyte (ERI)
 VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN NM implanterbar pulsgenerator Felaktig indikering av elektivt utbyte (ERI) 12 sep 2017 Bästa läkare I syfte att hålla dig kontinuerligt informerad och att säkerställa
VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN NM implanterbar pulsgenerator Felaktig indikering av elektivt utbyte (ERI) 12 sep 2017 Bästa läkare I syfte att hålla dig kontinuerligt informerad och att säkerställa
BRÅDSKANDE SÄKERHETSMEDDELANDE/MAGEC -SYSTEM
 BRÅDSKANDE SÄKERHETSMEDDELANDE/MAGEC -SYSTEM DATUM: 25 juni, 2019 KOMMERSIELLT NAMN: MAGEC -system TYP AV ÅTGÄRD: Rådgivande meddelande MAGEC -system tillverkat före 26 mars, 2015 Beskrivning av problemet:
BRÅDSKANDE SÄKERHETSMEDDELANDE/MAGEC -SYSTEM DATUM: 25 juni, 2019 KOMMERSIELLT NAMN: MAGEC -system TYP AV ÅTGÄRD: Rådgivande meddelande MAGEC -system tillverkat före 26 mars, 2015 Beskrivning av problemet:
Viktigt säkerhetsmeddelande till marknaden
 Viktigt säkerhetsmeddelande till marknaden Kommersiellt namn på den Alcon or Endure LuxOR E71 Ophthalmic Microscope; berörda produkten: Alcon or Endure LuxOR E71 Q-Vue Ophthalmic Microscope Referens (er):
Viktigt säkerhetsmeddelande till marknaden Kommersiellt namn på den Alcon or Endure LuxOR E71 Ophthalmic Microscope; berörda produkten: Alcon or Endure LuxOR E71 Q-Vue Ophthalmic Microscope Referens (er):
Bruksanvisning Repeater RP-900
 Bruksanvisning Repeater RP-900 KNOP REHATEK AB GIAB huset Ankdammsgatan 35 SE-171 67 Solna Tel: 020 12 12 34 KNOP REHATEK AB Version 2.0 2012-03-21 Innehåll 1 INNEHÅLL... 2 2 INTRODUKTION... 2 3 MONTERING...
Bruksanvisning Repeater RP-900 KNOP REHATEK AB GIAB huset Ankdammsgatan 35 SE-171 67 Solna Tel: 020 12 12 34 KNOP REHATEK AB Version 2.0 2012-03-21 Innehåll 1 INNEHÅLL... 2 2 INTRODUKTION... 2 3 MONTERING...
ATA Lotssignal ALS-1. For the love of lives
 ATA Lotssignal 123 45678 901 Viktig information Se till att du noga läst igenom och förstått det som står i instruktionsboken innan du tar produkten i bruk! Säkerhetsåtgärder och varningar återfinns i
ATA Lotssignal 123 45678 901 Viktig information Se till att du noga läst igenom och förstått det som står i instruktionsboken innan du tar produkten i bruk! Säkerhetsåtgärder och varningar återfinns i
MyDiagnostick 1001R - Manual till enheten UI0003-004 FINAL Revision 1. MyDiagnostick 1001R. Manual till enheten. Sid. 1 av 10
 MyDiagnostick 1001R Manual till enheten Sid. 1 av 10 Innehållsförteckning 1 INLEDNING... 3 1.1 Avsedd användning... 3 1.2 Programvara... 3 1.3 Kontaktuppgifter... 3 1.4 Varningar... 3 2 FÖRPACKNING...
MyDiagnostick 1001R Manual till enheten Sid. 1 av 10 Innehållsförteckning 1 INLEDNING... 3 1.1 Avsedd användning... 3 1.2 Programvara... 3 1.3 Kontaktuppgifter... 3 1.4 Varningar... 3 2 FÖRPACKNING...
Brådskande säkerhetsmeddelande (FSN BCT5) CaridianBCT Trima slangset för engångsbruk
 ~dianbct Brådskande säkerhetsmeddelande (FSN BCT5) CaridianBCT Trima Accel@ slangset för engångsbruk (Böjd returslang i grenröret) Till berörda parter Jleferensnunmroer CaridianBCT katalognummer Partinummer
~dianbct Brådskande säkerhetsmeddelande (FSN BCT5) CaridianBCT Trima Accel@ slangset för engångsbruk (Böjd returslang i grenröret) Till berörda parter Jleferensnunmroer CaridianBCT katalognummer Partinummer
VIKTIGT säkerhetsmeddelande Korrigering av medicinsk utrustning IntelliVue MX40 saknade varningar i bruksanvisning
 Bästa kund, Vi har upptäckt ett problem med bruksanvisningen till Philips IntelliVue MX40 för programvaruversionerna B.05, B.06 och B.06.5X. Din IntelliVue MX40 är fortfarande säker att använda. De här
Bästa kund, Vi har upptäckt ett problem med bruksanvisningen till Philips IntelliVue MX40 för programvaruversionerna B.05, B.06 och B.06.5X. Din IntelliVue MX40 är fortfarande säker att använda. De här
14 november 2016 BRÅDSKANDE Viktigt säkerhetsmeddelande Bridge ocklusionsballong
 «Attention» «Hospital» «AddressBlock» Bäste kund! 14 november 2016 BRÅDSKANDE Viktigt säkerhetsmeddelande Bridge ocklusionsballong Syftet med detta brev är att informera dig om att Spectranetics återkallar
«Attention» «Hospital» «AddressBlock» Bäste kund! 14 november 2016 BRÅDSKANDE Viktigt säkerhetsmeddelande Bridge ocklusionsballong Syftet med detta brev är att informera dig om att Spectranetics återkallar
BRÅDSKANDE Korrigering av medicinsk utrustning Philips Avalon CTG-apparater, modellerna FM20, FM30, FM40, FM50
 Patient Monitoring -1/5- FSN86201075 20 november 2009 Viktig information om fortsatt säker användning av din utrustning. Gå igenom följande information tillsammans med alla anställda som behöver känna
Patient Monitoring -1/5- FSN86201075 20 november 2009 Viktig information om fortsatt säker användning av din utrustning. Gå igenom följande information tillsammans med alla anställda som behöver känna
Personsökare RX-300 Bruksanvisning
 Personsökare RX-300 Bruksanvisning Personsökare RX-300 är en trådlös mottagare med 99 kanaler Sändarna/larmen som används tillsammans med RX-300 kan programmeras valfritt på de 99 kanalerna Man kan använda
Personsökare RX-300 Bruksanvisning Personsökare RX-300 är en trådlös mottagare med 99 kanaler Sändarna/larmen som används tillsammans med RX-300 kan programmeras valfritt på de 99 kanalerna Man kan använda
Del nummer Parti nummer PO# Cases Shipped to
 --------------------------------------------------------------------------------------------------------------------------- VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN EtCO 2 OxyMask CS201800149 Medicinteknisk
--------------------------------------------------------------------------------------------------------------------------- VIKTIGT SÄKERHETSMEDDELANDE TILL MARKNADEN EtCO 2 OxyMask CS201800149 Medicinteknisk
