Litiumatomens spektrum
|
|
|
- Karolina Sandberg
- för 6 år sedan
- Visningar:
Transkript
1 Litiumatomens spektrum Datorlaboration i Atom- och kärnfysik FAFF10 version 2010b av Sara Bargi och Jonas Cremon, omarbetning av tidigare version Före laborationens utförande ska du ha läst igenom avsnitt 1 till och med 3, samt gjort de förberedelseuppgifter som finns i dessa avsnitt. 1 Syfte Färdighetsmål - Studenten ska utveckla sin förmåga att beskriva verkligheten med hjälp av matematiska modeller. Studenten får öva sig i att testa olika modeller och se deras styrkor och svagheter. Laborationen exemplifierar hur en bra modell inte bara kan reproducera experimentella data, utan även bredda förståelsen av dem, och göra förutsägelser om verkligheten. Kunskapsmål - Studenten förväntas öka sin kunskap kring atomens uppbyggnad, vilket inkluderar Pauliprincipens följder och växelverkan mellan elektroner i ett flerelektronsystem. Laborationen syftar även till att öka förståelsen för begrepp som radiell vågfunktion och rörelsemängdsmoment i kvantmekaniken och atomfysiken. 2 Introduktion Som student får man ofta lära sig en teori som sedan exemplifieras med laborationer, men i verkligheten är det oftast så att experimentella data kommer före teoretiska förklaringar. Så var det under atomfysikens uppkomst i slutet av 1800-talet. Tidiga mätningar på atomers energispektra gav upphov till enkla fenomenologiska modeller, varav exempelvis Rydbergs formel används fortfarande. Men sådana modeller har begränsningen att de bara återupprepar ett experimentellt resultat; de lär oss ingenting om de mekanismer som ligger bakom. En kvantmekanisk behandling av ett atomfysikproblem har ofta den fördelen att den lär oss mer om naturen än att bara ge rätt siffror. Men även om kvantmekanikens principer är kända så kan beräkningarna bli mycket besvärliga. Därför är det naturligt att även här börja med en enkel modell, och sedan förbättra den efter hand. 1
2 I denna laboration studerar vi litium, som har tre elektroner och tre protoner, och de kvantmekaniska beräkningarna är inte triviala. Därför är en del av laborationen förberedelseuppgifter, som sedan används vid laborationstillfället. Dessa ges i avsnitt 3. Observera att avsnitt i övrigt väsentligen är repetition av vad som gåtts igenom på föreläsningar och i litteraturen. Avsnitt 4 innehåller själva laborationsuppgifterna, i avsnitt 5 anges vad laborationsredogörelsen ska innehålla och i appendix A finns en beskrivning av den numeriska metod datorprogrammet använder sig av. 3 Förberedelser Vi ska försöka förklara litiumatomens spektrum. Litium har tre protoner och följaktligen tre elektroner som kretsar kring kärnan. Detta kvantmekaniska mångkroppssystem har ingen analytisk lösning, och för att förstå det bättre börjar vi med att sammanfatta de enklare systemen väte och helium. 3.1 Schrödingerekvationen vid sfärisk symmetri En kvantmekanisk behandling utgår från Schrödingerekvationen HΨ = EΨ. (1) Den har formen av en egenvärdesekvation för Hamiltonoperatorn H, med egenfunktioner (vågfunktioner) Ψ, och egenenergier E. Om vi känner spektret av egenenergier så kan vi använda dessa för att till exempel räkna ut vilka våglängder av ljus en viss atom absorberar. Vågfunktionerna Ψ kan ge oss förklaringar till vissa egenskaper hos atomen. Egenfunktionerna till en Hermitesk operator, som till exempel H, har dessutom egenskapen att de utgör en fullständig bas i Hilbertrummet. I tre dimensioner karakteriseras varje sådan basfunktion av tre kvanttal som vi kallar n, l, m. Vi ska nu studera Schrödingerekvationen för sfäriskt symmetriska system och förenkla denna till en ekvation som beror av bara en variabel, radien r, istället för tre, r, θ, ϕ. Motsvarande resonemang finns i Ohlén, kapitel 7, och Foot, kapitel 2. Att systemet är sfäriskt symmetriskt betyder att potentialen är vinkeloberoende dvs. V (r) = V (r). Hamiltonoperatorn ges av H = 2 2M 2 + V (r), (2) där den första termen är bidraget från kinetisk energi, och den andra är bidraget från potentiell energi. För att undvika ihopblandning med kvanttalet m så använder vi M för att beteckna massa. För att kunna utnyttja symmetrin skriver vi om 2 i sfäriska koordinater: 2 = 1 2 r r 2 r + 1 ( 2 r 2 θ tanθ θ ) sin 2 θ ϕ 2. (3) 2
3 Om man har gott om tid kan man visa att vinkeldelen av denna operator, alltså uttrycket inom parentes, överensstämmer med operatorn för rörelsemängdsmomentets storlek, L 2, så när som på en konstant. Förberedelseuppgift: Vad innebär storheten rörelsemängdsmoment? Hur är det definierat i klassisk mekanik? Vi kan alltså skriva om vår Hamiltonoperator som H = 2 1 2M r r 2 r + 1 2Mr 2 L2 + V (r). (4) Vad har vi vunnit med detta? Poängen är att vi känner egenfunktionerna till operatorn L 2 ; de är de så kallade klotytfunktionerna Yl m och sambandet är L 2 Y m l 2 = 2 l(l + 1)Y m l. (5) Förberedelseuppgift: Hur ser motsvarande relation ut för rörelsemängdens projektion på z-axeln, L z, ut? Varför använder vi i kvantmekaniken storheterna L 2 och L z istället för det fullständiga L = (L x, L y, L z )? De första klotytfunktionerna finns explicit angivna på formelbladet, i Ohlén på insidan av pärmen, samt i Foot kapitel 2.1. Hamiltonoperatorn Ekv. (4) kommuterar med både L 2 och L z. Att de kommuterar betyder att vi kan hitta gemensamma egenfunktioner till dessa tre operatorer och vi kan skriva lösningen Ψ till Schrödingerekvationen som en produkt: Ψ(r, θ, ϕ) = R(r)Yl m (θ, ϕ). (6) Vi ansätter nu denna lösning i Ekv. (1) och utnyttjar sambandet Ekv. (5). Vi finner 2 1 2M r r 2 rr(r)y l m (θ, ϕ) + 2 l(l + 1) 2Mr 2 2 R(r)Yl m (θ, ϕ) + V (r)r(r)yl m (θ, ϕ) (7) = ER(r)Yl m (θ, ϕ). Vi ser att Yl m, som vi ju redan känner, försvinner ur ekvationen. Vi noterar även att det står 1/r framför den första termen i ekvationen. Om vi förlänger med r ser vi att funktionen R(r) alltid förekommer som en produkt med variabeln r; vi gör därför substitutionen rr(r) = u(r) (8) och löser för denna funktion u(r) istället. Vi har nu kommit fram till ekvationen 2 d 2 ( u 2 ) 2M dr 2 + l(l + 1) 2Mr 2 + V (r) u = Eu. (9) Detta är alltså en ekvation för funktionen u(r) som bestämmer hur den radiella delen av vågfunktionen ser ut. Vi ser att den är misstänkt lik Schrödingerekvationen i en dimension om vi ser hela uttrycket inom parentes som en effektiv potential, V eff (r) = 2 l(l + 1) 2Mr 2 + V (r), (10) 3
4 där kvanttalet för rörelsemängdsmomentets storlek, l, ingår explicit. Vi kan se det som att för tillstånd med rörelsemängdsmoment större än noll så tillkommer en centrifugalterm till potentialen. För en given sfäriskt symmetrisk potential V (r) får vi alltså de fullständiga lösningarna till Schrödingerekvationen Ψ nlm genom att lösa Ekv. (9) för alla värden på l och sedan koppla på de redan kända lösningarna till vinkeldelen så att Ψ nlm (r, θ, ϕ) = R nl (r)yl m (θ, ϕ) = u nl(r) Yl m (θ, ϕ). (11) r 3.2 Helium Atomkärnan är som bekant mycket tyngre än elektronerna som kretsar kring den. Vi kan därför med god approximation anta att den är stilla i förhållande till elektronerna, och därmed kan vi stryka termen för atomkärnans rörelseenergi i Hamiltonoperatorn. Detta gör att vi kan lösa Schrödingerekvationen för väteatomen analytiskt. (Om du inte kommer ihåg hur egenfunktioner och egenenergier ser ut för väteatomen så rekommenderas du repetera detta exempelvis i Ohlén kapitel 8). Vågfunktionen beror bara av en lägesvektor, nämligen lägesvektorn för elektronens position i förhållande till den stillaliggande vätekärnan. Men väteatomen är ett undantag - så fort vi har flera elektroner blir det mer komplicerat. Vill vi studera elektronbanorna i helium måste vi ta hänsyn till båda elektronerna och deras lägeskoordinater r 1 och r 2. Hamiltonoperatorn har följande utseende H = 2 ( 2 2M e 2) 2 0 2e2 0 + r 1 r 2 e 2 0 r 1 r 2. (12) Det är den sista termen, växelverkan mellan elektronerna, som gör att vi inte kan lösa Schrödingerekvationen analytiskt (utan den hade vi kunnat använda variabelseparation). För att hitta en bra approximation till grundtillståndets energi och vågfunktion kan vi istället använda variationsmetoden. Då får vi resonera oss fram till en rimlig testvågfunktion. Om vi bara hade haft en elektron så hade vi haft ett väteliknande system, till vilket vi känner egenfunktionerna. Se exempelvis formelsamlingen. Grundtillståndet ges då av ( ) 3/2 Z 1 Ψ 100 (r) = 2e Zr/a0. (13) 4π a 0 Hur förändras detta om vi lägger till en elektron till? Elektroner är ju identiska partiklar och Pauliprincipen gäller, det vill säga de två elektronerna kan inte ha samma uppsättning kvanttal. Men eftersom det förutom kvanttalen n, l, m finns ett fjärde kvanttal, spinn, så kan elektronerna fortfarande ha samma rumsvågfunktion (det vill säga samma kvanttal n, l, m) om de har olika spinn. Därför utgår vi från Ekv. (13) och som variabel parameter använder vi Z, som då blir 4
5 effektiv laddning Z eff. Vår testvågfunktion blir Ψ test (r 1, r 2 ) = Ψ 100 (r 1 ) Ψ 100 (r 2 ) = ( Zeff a 0 ) 3 4e Z eff (r 1+r 2)/a0 1 4π. (14) Notera att testvågfunktionen beror av både r 1 och r 2, alltså av vardera elektrons avstånd till kärnan. 1 Om vi minimerar väntevärdet av energin i denna vågfunktion så får vi ett värde på Z eff Vi får då att bindningsenergin är 77.5 ev, att jämföra med det experimentellt uppmätta 79.0 ev. Ekvation (14) tycks alltså vara en god approximation av elektronernas vågfunktion i grundtillståndet i helium. Förberedelseuppgift: Varför är Z eff < 2? 3.3 Litium Litium har tre elektroner. Hamiltonoperatorn är H = 2 ( 2 2M e 3) 2 0 3e2 0 3e2 0 (15) r 1 r 2 r 3 + e2 0 r 1 r 2 + e 2 0 r 2 r 3 + e 2 0 r 3 r 1, om vi som vanligt struntar i kärnans rörelseenergi. Detta är ett komplicerat trepartikelproblem som vi inte kan lösa analytiskt, så vi får göra vissa antaganden. Om vi utgår från att de två inre elektronerna är bundna i 1s-orbitaler precis som i helium, så kan vi istället lösa en ekvation för enbart valenselektronen. Vi tänker oss då att valenselektronen enbart växelverkar med den potential V (r) som de inre elektronerna ger upphov till, samt med kärnan. Detta illustreras i Fig. 1. Denna approximation ger en förenklad Hamiltonoperator för valenselektronen: H = 2 2M 2 3e2 0 + V (r). (16) r För att bestämma V (r) noterar vi att de inre elektronerna tillsammans med kärnan bildar Li +, som vi kan behandla på samma sätt som helium. Det enda som skiljer är kärnladdningen, och vi kommer alltså få samma typ av vågfunktion, Ekv. (14), men en annan effektiv laddning, nämligen Z eff = Vidare tänker vi oss att de två inre elektronerna har en utsmetad laddningsfördelning ρ(r) i enlighet med deras sannolikhetstäthet Ψ 100 (r) 2, och den sammanlagda laddningstätheten för de två elektronerna blir ρ(r) = 2e Ψ 100 (r) 2. (17) 1 Vi har inte skrivit upp spinnvågfunktionen eftersom Hamiltonoperatorn är oberoende av spinnet. Ψ test är symmetrisk i variablerna r 1 och r 2, vilket den ska vara - totala vågfunktionen måste vara antisymmetrisk för fermioner, men man kan visa att för grundtillståndet är spinnvågfunktionen antisymmetrisk och rumsvågfunktionen alltså symmetrisk. 5
6 Figure 1: Illustration av en litiumatom enligt vår förenklade modell. För att utifrån en laddningsfördelning ρ räkna ut den elektrostatiska potentialen U kan vi använda Poissons ekvation : 2 U(r) = ρ(r)/ɛ 0. (18) För att från den elektrostatiska potentialen få reda på bidraget till elektronens potentiella energi så måste vi sedan multiplicera med elektronladdningen, V (r) = eu(r), när vi sätter in i Schrödingerekvationen. Förberedelseuppgift: Beräkna den elektrostatiska potentialen U(r) som valenselektronen i litium känner av från de två inre elektronerna. Detta innebär en hel del analytiskt räknande. Den radiella delen av Laplaceoperatorn i sfäriska koordinater kan skrivas på olika ekvivalenta sätt, förslagsvis blir den slutliga ekvationen som ska lösas 1 r 2 2e Zeff 3 (ru(r)) = exp( 2Z r2 eff r/a 0 ) ɛ 0 πa 3 0 Varför kan vi här strunta i de vinkel-beroende delarna av Laplace-operatorn? Ekvationen ovan kan, efter någon liten omskrivning, lösas genom direkt integrering. Kom ihåg att få med integrationskonstanterna, dessa måste bestämmas med hjälp av randvillkor. Vilka randvillkor borde gälla för potentialen? Rita upp den slutliga energi-potentialen V (r) = eu(r) exempelvis i Matlab och ta med en utskrift eller handritad skiss till laborationen. Ställ upp Schrödingerekvationen för valenselektronen i litium. 4 Laboration Fråga 1 Studera det experimentellt uppmätta spektrum med övergångsenergier för väte som delas ut vid laborationen (många fler övergångar är möjliga men vi nöjer oss med att undersöka de som märkts ut i diagrammet). Sätt ut kvanttalen n, l, m vid aktuell energinivå och ange degenerationsgraden. Stämmer spektrum överens med vad du förväntar dig utifrån dina tidigare kunskaper försök räkna fram övergångsenergierna med hjälp av Rydbergs formel och se om de stämmer överens. 6
7 Fråga 2 Fortsätt med det experimentellt uppmätta spektret för litium, som utdelas vid laborationen. Sätt ut kvanttalen n, l, m och bestäm degenerationsgraden som du gjorde för väte. Kommentera skillnader och likheter mellan vätes och litiums spektra. För de energier som presenteras i spektrat är det bara valens-elektronen som exciteras. Det är lätt att göra fel på kvanttalen här tänk efter hur många elektroner det finns i litium, och var de får lov att finnas enligt Pauli-principen. Vi ska nu försöka förklara varför litiums spektrum ser ut som det gör, och vi börjar med det allra enklaste vi kan göra. Fråga 3 Som första approximation struntar vi helt i växelverkan mellan elektronerna och använder Rydbergs formel med Z = 3, eftersom litium har tre protoner i kärnan. Rydbergs formel ges av E bin n = RhcZ 2 1 n 2, där R är Rydbergskonstanten som efter masskorrektion är R = m 1 för litium. (hc = Jm, 1 ev= J) Vilka övergångsenergier ger detta för valenselektronen? Jämför med det experimentella spektrat och se om det stämmer bra eller dåligt. Fråga 4 Som en försöksmodell, sätt nu istället Z = 1, och gör om uppgift 3. Stämmer det nu bättre eller sämre överens med det experimentella spektrat nu? För vilka nivåer stämmer det bättre/sämre? Vad är förklaringen till detta? Redovisa din jämförelse i tabellform. Fråga 5: En kort fråga om vågfunktioner och kvanttal: Vilket samband finns mellan det radiella kvanttalet N, och kvanttalen n och l? Vilken egenskap hos vågfunktionen beskrivs av N? Se kapitel 8 (Väteatomen) i Kvantvärldens fenomen, sida 167. Den här kunskapen är viktig för att kunna tolka resultaten från datorprogrammet som ni ska använda. Nu försöker vi oss på den mer sofistikerade modellen, baserad på förberedelseuppgiften, och ser om vi kan få bättre överensstämmelse med det experimentella spektrat. Hämta hem all programvara från kurshemsidan. Huvudprogram är menu.m som körs i MatLab. Programmet löser Ekv. (9) numeriskt med en iterativ metod där funktionens värde i punkten i räknas ut med hjälp av de två föregående punkterna i 1 och i 2 enligt [ u i = 2 2m ] 2 (E V eff i 1 )( r) 2 u i 1 u i 2. Metoden är närmare beskriven i Appendix A. Som du ser ingår explicit energin E, samt potentialen V eff i detta uttryck. Därför måste du i programmet menu.m ange potential, en energi och l-kvanttal, och så räknar programmet ut vilken funktion u(r) detta ger upphov till. I fönstret plottas sedan den radiella 7
8 vågfunktionen R(r) enligt Ekv. (8). Alla energier ger inte normerbara vågfunktioner, det är bara när man lyckas ställa in exakt rätt energi som man får en rimlig vågfunktion. P g a numerisk osäkerhet är det dock nästan omöjligt att ställa in exakt rätt, och man får ibland acceptera att vågfunktionen inte ser perfekt ut. När du hittat en energi som verkar ligga nära ett bundet tillstånd, kan du använda funktionen auto i programmet. Den räknar då ut en energinivå med högre noggrannhet. Fråga 6 Använd nu Matlab-scriptet menu.m. För att bekanta er med programmet, välj väte-potential. Med instruktionerna i stycket ovan, hitta energierna och vågfunktionerna för väte. Räkna fram alla energinivåer med n 4, och kontrollera att de stämmer överens med de energier som Rydbergs formel ger. Eftersom energierna i väte inte beror på l-kvanttalet, räcker det att hitta energier för l = 0. Fråga 7 Ange nu litium-potential så att programmet istället löser Schrödingerekvationen för valens-elektronen i litium, där potentialen som ni räknade fram som förberedelseuppgift ingår. Kontrollera att potential som datorn använder stämmer med det analytiska uttrycket, i filen userdefinedpotentialenergy.m och ändra i den. Ta fram ett spektrum för litium som visar alla energinivåer med n 4, för de olika l som är möjliga. Med de framräknade energinivåerna, räkna ut övergångsenergierna och se efter hur de stämmer med de experimentellt uppmätta. Blev det bättre/sämre jämfört med resultaten från fråga 4? För vilka övergångar blev det bättre/sämre? Vi ska nu titta närmare på vågfunktionerna för valens-elektronen hos litium. Fråga 8 På vilket viktigt sätt skiljer sig s-vågfunktionerna (de med l = 0) från de övriga (de med l > 0)? Fråga 9 Studera särskilt vågfunktionerna för tillstånden 2p, 4p och 4f. Var befinner sig elektronen i de olika tillstånden? Hur hänger detta samman med rörelsemängdsmomentet? Ta med bilder eller skisser i rapporten av dessa vågfunktioner. Fråga 10 Baserat på hur vågfunktionerna ser ut för de aktuella nivåerna, kan du förklara varför beräkningen i Fråga 4 stämde så pass bra för vissa övergångsenergier? Fråga 11 Studera återigen din jämförelse från Fråga 7 mellan experimentellt uppmätt och beräknat övergångsspektrum. Med den utförliga datorberäkningen, så stämmer ändå vissa övergångsenergier fortfarande inte särskilt bra med experimentet. Vilka nivåer gäller detta? Varför blir det sämre för just dessa? Vad i vår modell för litium-atomen är det som saknas? Avslutningsvis ska vi använda våra nyvunna kunskaper om hur litiums spektrum ser ut, för att försöka göra förutsägelser om vilka atomer som är ädelgaser. 8
9 Fråga 12 Vad är karakteristiskt för en ädelgas jämfört med andra atomslag? Fråga 13 Som du vet är neon med Z = 10 den näst lättaste ädelgasen. Utgå från ditt beräknade spektrum för litium och bestäm vilka tillstånd som är besatta i grundtillståndet för neon, och hur många elektroner det finns i varje tillstånd. Fråga 14 Utgående från litiumatomens spektrum drar man lätt slutsatsen att nästa ädelgas efter neon bildas då 3s-, 3p- och 3d-tillstånden fyllts. Hur många elektroner skulle man då totalt få? Experimentellt visar det sig emellertid att istället argon med Z = 18 är en ädelgas. Vilka elektrontillstånd är fyllda i grundtillståndet för argon? Varför är argon ändå en ädelgas? Innan ni går är det bra om ni pratat igenom era resultat och svar med en handledare. 5 Till laborationsrapporten Laborationsredogörelsen ska innehålla: Introduktion och översikt över laborationen. Fullständig beräkning av potentialen valenselektronen känner av i litium, alltså din lösning av Ekv. (18). Var noggrann med motiveringar och förklaringar! Handskriven lösning godtas. Svar på de numrerade frågorna i avsnitt 4 med motiveringar, inklusive tabeller och diagram. Resultaten från relevanta uträkningar ska redovisas, t ex energier och övergångar ska redovisas tydligt i tabellform. Formulera dina svar så att de går att förstå utan att man först har läst frågan i handledningen. Diagram och figurer ska (som alltid) numreras, och hänvisas till och förklaras i texten. A Numerisk lösning av Schrödingerekvationen För fullständighet ger vi här en kortfattad beskrivning av den numeriska metod som används av programmet menu.m. Vi vill lösa den radiella Schrödingerekvationen i ett system med sfärisk symmetri, Ekv. (9). Omskrivet med effektiv potential får vi 2 d 2 u 2m dr 2 + V eff(r)u = Eu. (19) För att lösa denna ekvation numeriskt approximerar vi derivatan av funktionen u(r) med kvoten: u (r) = lim r 0 u(r) u(r r). (20) r 9
10 Derivatan är ett gränsvärde, vilket innebär att om vi väljer r tillräckligt litet ger kvoten i högerledet en bra approximation till derivatan i punkten r. Vad som är tillräckligt litet beror på hur u(r) ser ut. En funktion som har snabba förändringar kräver att man väljer kortare intervall än en långsamt varierande funktion. Se gärna kapitel 3.1, Introduktion till begreppet derivata i A. Persson och L. Böiers, Analys i en variabel. Vi kan nu diskretisera vår funktion genom att skriva u i u(i r). Vi kan därmed direkt använda Ekv. (20) för att få ett diskretiserat uttryck för derivatan i punkt i: u i(r) = u i u i 1. (21) r På motsvarande sätt kan vi diskretisera andraderivatan. Andraderivatan kring punkten i 1 kan skrivas som: u i 1 = u i 2u i 1 + u i 2 ( r) 2. (22) Nu kan vi skriva Schrödingerekvationen på diskretiserad form: u i 2u i 1 + u i 2 ( r) 2 2m 2 V eff i 1 u i 1 = 2m Eu i 1. (23) Kom ihåg att vi med denna approximation tar andraderivatan för u i 1. Därför måste vi även ta alla andra funktioner som beror av r, nämligen V eff (r) och u(r), i punkten i 1. Vi kan nu lösa ekvationen med avseende på u i : [ u i = 2 2m ] 2 (E V eff i 1 )( r) 2 u i 1 u i 2. (24) Genom att välja två funktionsvärden u i 1 och u i 2 att starta med kan man beräkna funktionsvärdet i nästa punkt, u i, och sedan iterera sig fram till en funktion, representerad av ett antal funktionsvärden u i, som är en möjlig lösning. I vårt fall är det lämpligt att börja med två värden för mycket små r, u 0 och u 1, där vi vet från lösningen av väteatomen hur u(r) beter sig asymptotiskt. Om vi ansätter ett l-kvanttal och en energi kan vi alltså alltid hitta en motsvarande lösning till den radiella Schrödingerekvationen, men vi måste fortfarande ta reda på om denna lösning faktiskt representerar ett tillåtet kvanttillstånd med energin E. En fysikaliskt rimlig lösning för ett bundet tillstånd måste vara normerbar och därför gå mot noll långt bort från kärnan, u(r) 0, r. Om vågfunktionen inte går mot noll finns inget bundet tillstånd med energin E. Uppgiften är alltså att hitta de energier där vågfunktionen går mot noll i oändligheten; en uppgift som enklast löses genom systematisk sökning. Om lösningen går mot positiva oändligheten för en energi E 1 och negativa oändligheten för en energi E 2, då vet vi att det finns (minst) en energi E, mellan E 1 och E 2 som svarar mot ett bundet tillstånd. Genom att systematiskt göra energiintervallet snävare kan vi alltså med större och större noggrannhet bestämma denna energi E. 10
Atom- och kärnfysik med tillämpningar -
 Atom- och kärnfysik med tillämpningar - Föreläsning 8 Gillis Carlsson gillis.carlsson@matfys.lth.se 19 Oktober, 2012 Föreläsningarna i kvantmekanik LP1 V1: Repetition av kvant-nano kursen. Sid 5-84 V2:
Atom- och kärnfysik med tillämpningar - Föreläsning 8 Gillis Carlsson gillis.carlsson@matfys.lth.se 19 Oktober, 2012 Föreläsningarna i kvantmekanik LP1 V1: Repetition av kvant-nano kursen. Sid 5-84 V2:
Atom- och kärnfysik med tillämpningar -
 Atom- och kärnfysik med tillämpningar - Föreläsning 6 Gillis Carlsson gillis.carlsson@matfys.lth.se 10 Oktober, 2013 Föreläsningarna i kvantmekanik LP1 V1 : Repetition av kvant-nano kursen. Sid 5-84 V2
Atom- och kärnfysik med tillämpningar - Föreläsning 6 Gillis Carlsson gillis.carlsson@matfys.lth.se 10 Oktober, 2013 Föreläsningarna i kvantmekanik LP1 V1 : Repetition av kvant-nano kursen. Sid 5-84 V2
Hjälpmedel: Det för kursen ociella formelbladet samt TeFyMa. 0 x < 0
 LÖSNINGAR TILL Deltentamen i kvantformalism, atom och kärnfysik med tillämpningar för F3 9-1-15 Tid: kl 8.-1. (MA9A. Hjälpmedel: Det för kursen ociella formelbladet samt TeFyMa. Poäng: Vid varje uppgift
LÖSNINGAR TILL Deltentamen i kvantformalism, atom och kärnfysik med tillämpningar för F3 9-1-15 Tid: kl 8.-1. (MA9A. Hjälpmedel: Det för kursen ociella formelbladet samt TeFyMa. Poäng: Vid varje uppgift
Instuderingsfrågor, Griffiths kapitel 4 7
 Joakim Edsjö 15 oktober 2007 Fysikum, Stockholms Universitet Tel.: 08-55 37 87 26 E-post: edsjo@physto.se Instuderingsfrågor, Griffiths kapitel 4 7 Teoretisk Kvantmekanik II HT 2007 Tanken med dessa frågor
Joakim Edsjö 15 oktober 2007 Fysikum, Stockholms Universitet Tel.: 08-55 37 87 26 E-post: edsjo@physto.se Instuderingsfrågor, Griffiths kapitel 4 7 Teoretisk Kvantmekanik II HT 2007 Tanken med dessa frågor
4-1 Hur lyder Schrödingerekvationen för en partikel som rör sig i det tredimensionella
 KVANTMEKANIKFRÅGOR Griffiths, Kapitel 4-6 Tanken med dessa frågor är att de ska belysa de centrala delarna av kursen och tjäna som kunskapskontroll och repetition. Kapitelreferenserna är till Griffiths.
KVANTMEKANIKFRÅGOR Griffiths, Kapitel 4-6 Tanken med dessa frågor är att de ska belysa de centrala delarna av kursen och tjäna som kunskapskontroll och repetition. Kapitelreferenserna är till Griffiths.
Andra föreläsningen kapitel 7. Patrik Lundström
 Andra föreläsningen kapitel 7 Patrik Lundström Kvantisering i klassisk fysik: Uppkomst av heltalskvanttal För att en stående våg i en ring inte ska släcka ut sig själv krävs att den är tillbaka som den
Andra föreläsningen kapitel 7 Patrik Lundström Kvantisering i klassisk fysik: Uppkomst av heltalskvanttal För att en stående våg i en ring inte ska släcka ut sig själv krävs att den är tillbaka som den
KEMA00. Magnus Ullner. Föreläsningsanteckningar och säkerhetskompendium kan laddas ner från
 KEMA00 Magnus Ullner Föreläsningsanteckningar och säkerhetskompendium kan laddas ner från http://www.kemi.lu.se/utbildning/grund/kema00/dold Användarnamn: Kema00 Lösenord: DeltaH0 F2 Periodiska systemet
KEMA00 Magnus Ullner Föreläsningsanteckningar och säkerhetskompendium kan laddas ner från http://www.kemi.lu.se/utbildning/grund/kema00/dold Användarnamn: Kema00 Lösenord: DeltaH0 F2 Periodiska systemet
2.4. Bohrs modell för väteatomen
 2.4. Bohrs modell för väteatomen [Understanding Physics: 19.4-19.7] Som vi sett, är den totala energin för elektronen i väteatomen E = 1 2 mv2 = e2 8πɛ 0 r. Eftersom L = mvr för cirkulära banor, så kan
2.4. Bohrs modell för väteatomen [Understanding Physics: 19.4-19.7] Som vi sett, är den totala energin för elektronen i väteatomen E = 1 2 mv2 = e2 8πɛ 0 r. Eftersom L = mvr för cirkulära banor, så kan
2.4. Bohrs modell för väteatomen
 2.4. Bohrs modell för väteatomen [Understanding Physics: 19.4-19.7] Som vi sett, är den totala energin för elektronen i väteatomen E = 1 2 mv2 = e2 8πɛ 0 r. Eftersom L = mvr för cirkulära banor, så kan
2.4. Bohrs modell för väteatomen [Understanding Physics: 19.4-19.7] Som vi sett, är den totala energin för elektronen i väteatomen E = 1 2 mv2 = e2 8πɛ 0 r. Eftersom L = mvr för cirkulära banor, så kan
Rydbergs formel. Bohrs teori för väteliknande system
 Chalmers Tekniska Högskola och Göteborgs Universitet Sektionen för Fysik och Teknisk Fysik Arne Rosén, Halina Roth Uppdaterad av Erik Reimhult, januari A4 Enelektronspektrum Namn... Utförd den... Godkänd
Chalmers Tekniska Högskola och Göteborgs Universitet Sektionen för Fysik och Teknisk Fysik Arne Rosén, Halina Roth Uppdaterad av Erik Reimhult, januari A4 Enelektronspektrum Namn... Utförd den... Godkänd
1-1 Hur lyder den tidsberoende Schrödingerekvationen för en partikel som rör sig längs x-axeln? Definiera ingående storheter!
 KVANTMEKANIKFRÅGOR, GRIFFITHS Tanken med dessa frågor är att de ska belysa de centrala delarna av kursen och tjäna som kunskapskontroll och repetition. Kapitelreferenserna är till Griffiths. 1 Kapitel
KVANTMEKANIKFRÅGOR, GRIFFITHS Tanken med dessa frågor är att de ska belysa de centrala delarna av kursen och tjäna som kunskapskontroll och repetition. Kapitelreferenserna är till Griffiths. 1 Kapitel
Kvantmekanik II (FK5012), 7,5 hp
 Joakim Edsjö Fysikum, Stockholms Universitet Tel.: 8-5537876 E-post: edsjo@physto.se Lösningar till Kvantmekanik II (FK51, 7,5 hp 3 januari 9 Lösningar finns även tillgängliga på http://www.physto.se/~edsjo/teaching/kvant/index.html.
Joakim Edsjö Fysikum, Stockholms Universitet Tel.: 8-5537876 E-post: edsjo@physto.se Lösningar till Kvantmekanik II (FK51, 7,5 hp 3 januari 9 Lösningar finns även tillgängliga på http://www.physto.se/~edsjo/teaching/kvant/index.html.
Kvantbrunnar -Kvantiserade energier och tillstånd
 Kvantbrunnar -Kvantiserade energier och tillstånd Inledning Syftet med denna laboration är att undersöka kvantiseringen av energitillstånd i kvantbrunnar. Till detta används en java-applet som hittas på
Kvantbrunnar -Kvantiserade energier och tillstånd Inledning Syftet med denna laboration är att undersöka kvantiseringen av energitillstånd i kvantbrunnar. Till detta används en java-applet som hittas på
Dugga i FUF040 Kvantfysik för F3/Kf3
 Dugga i FUF040 Kvantfysik för F3/Kf3 fredagen den 23 oktober 2015 kl 14.00-16.00 i V Examinator: Måns Henningson, ankn 3245. Inga hjälpmedel. Ringa in bokstaven svarande mot det unika rätta svaret på svarsblanketten!
Dugga i FUF040 Kvantfysik för F3/Kf3 fredagen den 23 oktober 2015 kl 14.00-16.00 i V Examinator: Måns Henningson, ankn 3245. Inga hjälpmedel. Ringa in bokstaven svarande mot det unika rätta svaret på svarsblanketten!
Kvantmekanik II - Föreläsning 7
 Kvantmekanik II - Föreläsning 7 Identiska partiklar Joakim Edsjö edsjo@fysik.su.se HT 2013 Kvantmekanik II Föreläsning 7 Joakim Edsjö 1/44 Innehåll 1 Generalisering av Schrödingerekvationen till fler partiklar
Kvantmekanik II - Föreläsning 7 Identiska partiklar Joakim Edsjö edsjo@fysik.su.se HT 2013 Kvantmekanik II Föreläsning 7 Joakim Edsjö 1/44 Innehåll 1 Generalisering av Schrödingerekvationen till fler partiklar
Kvantmekanik - Gillis Carlsson
 Kvantmekanik - Föreläsning 1 Gillis Carlsson gillis.carlsson@matfys.lth.se LP2 Föreläsningarna i kvantmekanik LP1 V1): Repetition av kvant-nano kursen. Sid 5-84 V2 : V3 : Formalism (I). Sid 109-124, 128-131,
Kvantmekanik - Föreläsning 1 Gillis Carlsson gillis.carlsson@matfys.lth.se LP2 Föreläsningarna i kvantmekanik LP1 V1): Repetition av kvant-nano kursen. Sid 5-84 V2 : V3 : Formalism (I). Sid 109-124, 128-131,
TENTAMEN I KVANTFYSIK del 1 (5A1324 och 5A1450) samt KVANTMEKANIK (5A1320) med SVAR och LÖSNINGSANVISNINGAR Tisdagen den 5 juni 2007
 TENTAMEN I KVANTFYSIK del (5A4 och 5A45) samt KVANTMEKANIK (5A) med SVAR och LÖSNINGSANVISNINGAR Tisdagen den 5 juni 7 HJÄLPMEDEL: Formelsamling i Fysik (teoretisk fysik KTH), matematiska tabeller, dock
TENTAMEN I KVANTFYSIK del (5A4 och 5A45) samt KVANTMEKANIK (5A) med SVAR och LÖSNINGSANVISNINGAR Tisdagen den 5 juni 7 HJÄLPMEDEL: Formelsamling i Fysik (teoretisk fysik KTH), matematiska tabeller, dock
Kvantmekanik II - Föreläsning 10
 Kvantmekanik II - Föreläsning 10 Degenererad störningsteori (tidsoberoende) Joakim Edsjö edsjo@fysik.su.se Kvantmekanik II Föreläsning 10 Joakim Edsjö 1/26 Degenererad störningsteori Innehåll 1 Allmänt
Kvantmekanik II - Föreläsning 10 Degenererad störningsteori (tidsoberoende) Joakim Edsjö edsjo@fysik.su.se Kvantmekanik II Föreläsning 10 Joakim Edsjö 1/26 Degenererad störningsteori Innehåll 1 Allmänt
Numerisk lösning till den tidsberoende Schrödingerekvationen.
 Numerisk lösning till den tidsberoende Schrödingerekvationen. Det är enbart i de enklaste fallen t ex när potentialen är sträckvis konstant som vi kan lösa Schrödingerekvationen analytiskt. I andra fall
Numerisk lösning till den tidsberoende Schrödingerekvationen. Det är enbart i de enklaste fallen t ex när potentialen är sträckvis konstant som vi kan lösa Schrödingerekvationen analytiskt. I andra fall
3.5. Schrödingerekvationen för atomer med en elektron
 3.5. Schrödingerekvationen för atomer med en elektron [Understanding Physics: 19.5-19.8] Bohrs teori lyckas väl förklara energinivåerna för en atom med en elektron, och således också spektrallinjerna,
3.5. Schrödingerekvationen för atomer med en elektron [Understanding Physics: 19.5-19.8] Bohrs teori lyckas väl förklara energinivåerna för en atom med en elektron, och således också spektrallinjerna,
Väteatomen. Matti Hotokka
 Väteatomen Matti Hotokka Väteatomen Atom nummer 1 i det periodiska systemet Därför har den En proton En elektron Isotoper är möjliga Protium har en proton i atomkärnan Deuterium har en proton och en neutron
Väteatomen Matti Hotokka Väteatomen Atom nummer 1 i det periodiska systemet Därför har den En proton En elektron Isotoper är möjliga Protium har en proton i atomkärnan Deuterium har en proton och en neutron
LABORATION ENELEKTRONSPEKTRA
 LABORATION ENELEKTRONSPEKTRA Syfte och mål Uppgiften i denna laboration är att studera atomspektra från väte och natrium i det synliga våglängdsområdet och att med hjälp av uppmätta våglängder från spektrallinjerna
LABORATION ENELEKTRONSPEKTRA Syfte och mål Uppgiften i denna laboration är att studera atomspektra från väte och natrium i det synliga våglängdsområdet och att med hjälp av uppmätta våglängder från spektrallinjerna
Kvantfysik SI1151 för F3 Tisdag kl
 TEORETISK FYSIK KTH Kvantfysik SI5 för F3 Tisdag 3008 kl. 8.00-3.00 Skriv på varje sida Namn och problemnummer Motivera noga Otillräckliga motiveringar leder till poängavdrag Hjälpmedel Teoretisk fysiks
TEORETISK FYSIK KTH Kvantfysik SI5 för F3 Tisdag 3008 kl. 8.00-3.00 Skriv på varje sida Namn och problemnummer Motivera noga Otillräckliga motiveringar leder till poängavdrag Hjälpmedel Teoretisk fysiks
Utveckling mot vågbeskrivning av elektroner. En orientering
 Utveckling mot vågbeskrivning av elektroner En orientering Nikodemus Karlsson Februari 00 . Bohrs Postulat Niels Bohr (885-96) ställde utifrån iakttagelser upp fyra postulat gällande väteatomen ¹:. Elektronen
Utveckling mot vågbeskrivning av elektroner En orientering Nikodemus Karlsson Februari 00 . Bohrs Postulat Niels Bohr (885-96) ställde utifrån iakttagelser upp fyra postulat gällande väteatomen ¹:. Elektronen
TENTAMEN I FYSIKALISK KEMI KURS: KEM040 Institutionen för kemi Göteborgs Universitet Datum: LÄS DETTA FÖRST!
 TENTAMEN I FYSIKALISK KEMI KURS: KEM040 Institutionen för kemi Del: QSM Göteborgs Universitet Datum: 111206 Tid: 8.30 14.30 Ansvariga: Gunnar Nyman tel: 786 9035 Jens Poulsen tel: 786 9089 Magnus Gustafsson
TENTAMEN I FYSIKALISK KEMI KURS: KEM040 Institutionen för kemi Del: QSM Göteborgs Universitet Datum: 111206 Tid: 8.30 14.30 Ansvariga: Gunnar Nyman tel: 786 9035 Jens Poulsen tel: 786 9089 Magnus Gustafsson
Tentamen i Modern fysik, TFYA11/TENA
 IFM - Institutionen för Fysik, Kemi och Biologi Linköpings universitet Tentamen i Modern fysik, TFYA11/TENA Torsdagen den 29/8 2013 kl. 14.00-18.00 i TER2 Tentamen består av 2 A4-blad (inklusive detta)
IFM - Institutionen för Fysik, Kemi och Biologi Linköpings universitet Tentamen i Modern fysik, TFYA11/TENA Torsdagen den 29/8 2013 kl. 14.00-18.00 i TER2 Tentamen består av 2 A4-blad (inklusive detta)
Kvantmekanik och kemisk bindning I 1KB501
 Kvantmekanik och kemisk bindning I 1KB501 TENTAMEN, 013-06-05, 8.00-13.00 Tillåtna hjälpmedel: Miniräknare, bifogade formelsamlingar. Börja på nytt blad för varje nytt problem, och skriv din kod på varje
Kvantmekanik och kemisk bindning I 1KB501 TENTAMEN, 013-06-05, 8.00-13.00 Tillåtna hjälpmedel: Miniräknare, bifogade formelsamlingar. Börja på nytt blad för varje nytt problem, och skriv din kod på varje
2.14. Spinn-bankopplingen
 2.14. Spinn-bankopplingen [Understanding Physics: 19.12-19.16] I avsnitt 2.12 konstaterade vi, att elektronen, som enligt Bohrs modell rör sig i en cirkelbana, kommer att ge upphov till en strömslinga,
2.14. Spinn-bankopplingen [Understanding Physics: 19.12-19.16] I avsnitt 2.12 konstaterade vi, att elektronen, som enligt Bohrs modell rör sig i en cirkelbana, kommer att ge upphov till en strömslinga,
2.7. Egenfunktionernas tolkning - fortsättning
 2.7. Egenfunktionernas tolkning - fortsättning [Understanding Physics: 19.7-19.10] Förra gången såg vi, att sannolikhetstätheten består av tre delar, en radiell del och två vinkelberoende delar. Vi skall
2.7. Egenfunktionernas tolkning - fortsättning [Understanding Physics: 19.7-19.10] Förra gången såg vi, att sannolikhetstätheten består av tre delar, en radiell del och två vinkelberoende delar. Vi skall
8. Atomfysik - flerelektronatomer
 Flerelektronatomer På motsvarande sätt som för väteatomen kommer elektronerna i atomerna hos grundämnen som har två eller fler elektroner också att vara instängda inom ett litet område runt kärnan. Det
Flerelektronatomer På motsvarande sätt som för väteatomen kommer elektronerna i atomerna hos grundämnen som har två eller fler elektroner också att vara instängda inom ett litet område runt kärnan. Det
c = λ ν Vågrörelse Kap. 1. Kvantmekanik och den mikroskopiska världen Kvantmekanik 1.1 Elektromagnetisk strålning
 Kap. 1. Kvantmekanik och den mikroskopiska världen Modern teori för atomer/molekyler kan förklara atomers/molekylers egenskaper: Kvantmekanik I detta och nästa kapitel: atomers egenskaper och periodiska
Kap. 1. Kvantmekanik och den mikroskopiska världen Modern teori för atomer/molekyler kan förklara atomers/molekylers egenskaper: Kvantmekanik I detta och nästa kapitel: atomers egenskaper och periodiska
Lösningar Heureka 2 Kapitel 14 Atomen
 Lösningar Heureka Kapitel 14 Atomen Andreas Josefsson Tullängsskolan Örebro Lo sningar Fysik Heureka Kapitel 14 14.1) a) Kulorna från A kan ramla på B, C, D, eller G (4 möjligheter). Från B kan de ramla
Lösningar Heureka Kapitel 14 Atomen Andreas Josefsson Tullängsskolan Örebro Lo sningar Fysik Heureka Kapitel 14 14.1) a) Kulorna från A kan ramla på B, C, D, eller G (4 möjligheter). Från B kan de ramla
Tentamen i Modern fysik, TFYA11/TENA
 IFM - Institutionen för Fysik, Kemi och Biologi Linköpings universitet Tentamen i Modern fysik, TFYA11/TENA Onsdagen den 27/3 2013 kl. 08.00-12.00 i T1 och T2 Tentamen består av 2 A4-blad (inklusive detta)
IFM - Institutionen för Fysik, Kemi och Biologi Linköpings universitet Tentamen i Modern fysik, TFYA11/TENA Onsdagen den 27/3 2013 kl. 08.00-12.00 i T1 och T2 Tentamen består av 2 A4-blad (inklusive detta)
BFL122/BFL111 Fysik för Tekniskt/ Naturvetenskapligt Basår/ Bastermin Föreläsning 7 Kvantfysik, Atom-, Molekyl- och Fasta Tillståndets Fysik
 Föreläsning 7 Kvantfysik 2 Partiklars vågegenskaper Som kunnat konstateras uppträder elektromagnetisk strålning ljus som en dubbelnatur, ibland behöver man beskriva ljus som vågrörelser och ibland är det
Föreläsning 7 Kvantfysik 2 Partiklars vågegenskaper Som kunnat konstateras uppträder elektromagnetisk strålning ljus som en dubbelnatur, ibland behöver man beskriva ljus som vågrörelser och ibland är det
Tentamen i Modern fysik, TFYA11/TENA
 IFM - Institutionen för Fysik, Kemi och Biologi Linköpings universitet Tentamen i Modern fysik, TFYA11/TENA Torsdagen den 28/8 2014 kl. 14.00-18.00 i T1 och S25 Tentamen består av 2 A4-blad (inklusive
IFM - Institutionen för Fysik, Kemi och Biologi Linköpings universitet Tentamen i Modern fysik, TFYA11/TENA Torsdagen den 28/8 2014 kl. 14.00-18.00 i T1 och S25 Tentamen består av 2 A4-blad (inklusive
Fysik TFYA86. Föreläsning 11/11
 Fysik TFYA86 Föreläsning 11/11 1 Kvantmekanik och Materialuppbyggnad University Physics: Kapitel 40-42* (*) 40.1-4 (översikt) 41.6 (uteslutningsprincipen) 42.1, 3, 4, 6, 7 koncept enklare uppgifter Översikt
Fysik TFYA86 Föreläsning 11/11 1 Kvantmekanik och Materialuppbyggnad University Physics: Kapitel 40-42* (*) 40.1-4 (översikt) 41.6 (uteslutningsprincipen) 42.1, 3, 4, 6, 7 koncept enklare uppgifter Översikt
19.4 Bohrs modell för väteatomen.
 Den moerna fysikens gruner - Föreläsning 7 42 9.4 Bohrs moell för väteatomen. Som vi sett är en totala energin för elektronen i väteatomen E = 2 mv2 = e2 8πɛ 0 r. Eftersom L = mvr för cirkulära banor så
Den moerna fysikens gruner - Föreläsning 7 42 9.4 Bohrs moell för väteatomen. Som vi sett är en totala energin för elektronen i väteatomen E = 2 mv2 = e2 8πɛ 0 r. Eftersom L = mvr för cirkulära banor så
s 1 och s 2 är icke kvantmekaniska partiklar? e. (1p) Vad blir sannolikheterna i uppgifterna b, c och d om vinkeln = /2?
 FK003 - Kvantfysikens principer, Fysikum, Stockholms universitet Tentamensskrivning, onsdag 7e mars 018, kl 17:00 - :00 Läs noggrant genom hela tentan först. Börja med uppgifterna som du tror du klarar
FK003 - Kvantfysikens principer, Fysikum, Stockholms universitet Tentamensskrivning, onsdag 7e mars 018, kl 17:00 - :00 Läs noggrant genom hela tentan först. Börja med uppgifterna som du tror du klarar
Föreläsning 6. Amplituder Kvanttillstånd Fermioner och bosoner Mer om spinn Frågor Tentan. Fk3002 Kvantfysikens grunder 1
 Föreläsning 6 Amplituder Kvanttillstånd Fermioner och bosoner Mer om spinn Frågor Tentan Fk3002 Kvantfysikens grunder 1 Betrakta ett experiment med opolariserade elektroner dvs 50% är spinn-upp och 50%
Föreläsning 6 Amplituder Kvanttillstånd Fermioner och bosoner Mer om spinn Frågor Tentan Fk3002 Kvantfysikens grunder 1 Betrakta ett experiment med opolariserade elektroner dvs 50% är spinn-upp och 50%
Kvantbrunnar Kvantiserade energier och tillstånd
 Kvantbrunnar Kvantiserade energier och tillstånd Inledning Syftet med denna laboration är att undersöka kvantiseringen av energitillstånd i kvantbrunnar. Till detta används en java-applet som hittas på
Kvantbrunnar Kvantiserade energier och tillstånd Inledning Syftet med denna laboration är att undersöka kvantiseringen av energitillstånd i kvantbrunnar. Till detta används en java-applet som hittas på
Kapitel 7. Atomstruktur och periodicitet
 Kapitel 7 Atomstruktur och periodicitet Avsnitt 7.1 Elektromagnetisk strålning Fyrverkeri i olika färger Copyright Cengage Learning. All rights reserved 2 Avsnitt 7.2 Materians karaktär Illuminerad saltgurka
Kapitel 7 Atomstruktur och periodicitet Avsnitt 7.1 Elektromagnetisk strålning Fyrverkeri i olika färger Copyright Cengage Learning. All rights reserved 2 Avsnitt 7.2 Materians karaktär Illuminerad saltgurka
Kapitel 7. Atomstruktur och periodicitet. Kvantmekanik Aufbau Periodiska systemet
 Avsnitt 7.1 Elektromagnetisk strålning Kapitel 7 Fyrverkeri i olika färger Atomstruktur och periodicitet Copyright Cengage Learning. All rights reserved 2 Illuminerad saltgurka Kapitel 7 Innehåll Kvantmekanik
Avsnitt 7.1 Elektromagnetisk strålning Kapitel 7 Fyrverkeri i olika färger Atomstruktur och periodicitet Copyright Cengage Learning. All rights reserved 2 Illuminerad saltgurka Kapitel 7 Innehåll Kvantmekanik
FK Kvantfysikens principer, Fysikum, Stockholms universitet Tentamensskrivning, onsdag 16 december 2015, kl 17:00-22:00
 FK003 - Kvantfysikens principer, Fysikum, Stockholms universitet Tentamensskrivning, onsdag 16 december 015, kl 17:00 - :00 Läs noggrant genom hela tentan först. Börja med uppgifterna som du tror du klarar
FK003 - Kvantfysikens principer, Fysikum, Stockholms universitet Tentamensskrivning, onsdag 16 december 015, kl 17:00 - :00 Läs noggrant genom hela tentan först. Börja med uppgifterna som du tror du klarar
Tentamen. TFYA35 Molekylfysik, TEN1 24 oktober 2016 kl Skrivsal: G34, G36, G37
 Thomas Ederth IFM / Molekylär Fysik ted@ifm.liu.se Tentamen TFYA35 Molekylfysik, TEN1 24 oktober 216 kl. 8.-13. Skrivsal: G34, G36, G37 Tentamen omfattar 6 problem som vardera kan ge 4 poäng. För godkänt
Thomas Ederth IFM / Molekylär Fysik ted@ifm.liu.se Tentamen TFYA35 Molekylfysik, TEN1 24 oktober 216 kl. 8.-13. Skrivsal: G34, G36, G37 Tentamen omfattar 6 problem som vardera kan ge 4 poäng. För godkänt
Mendelevs periodiska system
 Mendelevs periodiska system Notera luckorna som betecknar element som var okända vid den tiden. Med hjälp av systement lyckades Mendelev förutsäga dessa grundämnens egenskaper. Vårt nuvarande periodiska
Mendelevs periodiska system Notera luckorna som betecknar element som var okända vid den tiden. Med hjälp av systement lyckades Mendelev förutsäga dessa grundämnens egenskaper. Vårt nuvarande periodiska
Frielektron fermigas i en kristall. L z. L y L x. h 2 2m FRIELEKTRONMODELLEN
 FRIELEKTRONMODELLEN I frielektronmodellen (FEM) behandlas valenselektronerna som en gas. Elektronerna rör sig obehindrat i kristallen och växelverkar varken med jonerna eller med varandra. Figuren nedan
FRIELEKTRONMODELLEN I frielektronmodellen (FEM) behandlas valenselektronerna som en gas. Elektronerna rör sig obehindrat i kristallen och växelverkar varken med jonerna eller med varandra. Figuren nedan
F3: Schrödingers ekvationer
 F3: Schrödingers ekvationer Backgrund Vi behöver en ny matematik för att beskriva elektroner, atomer och molekyler! Den nya fysiken skall klara av att beskriva: Experiment visar att för bundna system så
F3: Schrödingers ekvationer Backgrund Vi behöver en ny matematik för att beskriva elektroner, atomer och molekyler! Den nya fysiken skall klara av att beskriva: Experiment visar att för bundna system så
Materiens Struktur. Lösningar
 Materiens Struktur Räkneövning 3 Lösningar 1. Studera och begrunda den teoretiska förklaringen till supralednigen så, att du kan föra en diskussion om denna på övningen. Skriv även ner huvudpunkterna som
Materiens Struktur Räkneövning 3 Lösningar 1. Studera och begrunda den teoretiska förklaringen till supralednigen så, att du kan föra en diskussion om denna på övningen. Skriv även ner huvudpunkterna som
Kap 1. Tidig Atomfysik
 Kap 1. Tidig Atomfysik Rydbergs formel för väte 1 λ = R ( 1 n 1 n ) Vågtal ges som ν = 1 λ. För n=1 Lymanserien, n= fås Balmersserien, n=3 Paschenserien. Balmerserien ligger i det synliga spektrat. Elektronernas
Kap 1. Tidig Atomfysik Rydbergs formel för väte 1 λ = R ( 1 n 1 n ) Vågtal ges som ν = 1 λ. För n=1 Lymanserien, n= fås Balmersserien, n=3 Paschenserien. Balmerserien ligger i det synliga spektrat. Elektronernas
Tentamen, Kvantfysikens principer FK2003, 7,5 hp
 Tentamen, Kvantfysikens principer FK2003, 7,5 hp Tid: 17:00-22:00, tisdag 3/3 2015 Hjälpmedel: utdelad formelsamling, utdelad miniräknare Var noga med att förklara införda beteckningar och att motivera
Tentamen, Kvantfysikens principer FK2003, 7,5 hp Tid: 17:00-22:00, tisdag 3/3 2015 Hjälpmedel: utdelad formelsamling, utdelad miniräknare Var noga med att förklara införda beteckningar och att motivera
1. Låt kommutatorn verka på en vågfunktion och inför att ˆp x = i h d. d2 (xψ(x)) ) = h 2 (x d2 Ψ(x) = i2 hˆp x Ψ(x) [ev] E n = 13, 6 Z2 n 2
![1. Låt kommutatorn verka på en vågfunktion och inför att ˆp x = i h d. d2 (xψ(x)) ) = h 2 (x d2 Ψ(x) = i2 hˆp x Ψ(x) [ev] E n = 13, 6 Z2 n 2 1. Låt kommutatorn verka på en vågfunktion och inför att ˆp x = i h d. d2 (xψ(x)) ) = h 2 (x d2 Ψ(x) = i2 hˆp x Ψ(x) [ev] E n = 13, 6 Z2 n 2](/thumbs/88/115915361.jpg) SVAR OCH LÖSNINGSANVISNINGAR TLLL TENTAMEN I KVANTFYSIK del för F5A450 och B5A och 5A4och KVANTMEKANIK 5A0 Måndagen den december 004 kl. 8.00 -.00 HJÄLPMEDEL: Formelsamling till kurserna i Fysikens matematiska
SVAR OCH LÖSNINGSANVISNINGAR TLLL TENTAMEN I KVANTFYSIK del för F5A450 och B5A och 5A4och KVANTMEKANIK 5A0 Måndagen den december 004 kl. 8.00 -.00 HJÄLPMEDEL: Formelsamling till kurserna i Fysikens matematiska
Poissons ekvation och potentialteori Mats Persson
 1 ärmeledning Föreläsning 21/9 Poissons ekvation och potentialteori Mats Persson i vet att värme strömmar från varmare till kallare. Det innebär att vi har ett flöde av värmeenergi i en riktning som är
1 ärmeledning Föreläsning 21/9 Poissons ekvation och potentialteori Mats Persson i vet att värme strömmar från varmare till kallare. Det innebär att vi har ett flöde av värmeenergi i en riktning som är
Föreläsning 1. Elektronen som partikel (kap 2)
 Föreläsning 1 Elektronen som partikel (kap 2) valenselektroner i metaller som ideal gas ström från elektriskt fält mikroskopisk syn på resistans, Ohms lag diffusionsström Vår första modell valenselektroner
Föreläsning 1 Elektronen som partikel (kap 2) valenselektroner i metaller som ideal gas ström från elektriskt fält mikroskopisk syn på resistans, Ohms lag diffusionsström Vår första modell valenselektroner
Extrauppgifter som kompletterar uppgifterna i Foot:
 Extrauppgifter som kompletterar uppgifterna i Foot: K1.1 a) Beräkna vågtal och våglängd för Balmer-α (H α ), Balmer-β (H β ) och Paschen-α i väte. b) Jämför skillnaden mellan vågtalen för H α och H β med
Extrauppgifter som kompletterar uppgifterna i Foot: K1.1 a) Beräkna vågtal och våglängd för Balmer-α (H α ), Balmer-β (H β ) och Paschen-α i väte. b) Jämför skillnaden mellan vågtalen för H α och H β med
Kursplanen är fastställd av Naturvetenskapliga fakultetens utbildningsnämnd att gälla från och med , vårterminen 2016.
 Humanistiska och teologiska fakulteterna ÄFYB23, Fysik: Grundläggande kvantmekanik, statistisk mekanik och kvantstatistik för lärare, 15 högskolepoäng Physics: Basic Quantum Mechanics, statistical mechanics
Humanistiska och teologiska fakulteterna ÄFYB23, Fysik: Grundläggande kvantmekanik, statistisk mekanik och kvantstatistik för lärare, 15 högskolepoäng Physics: Basic Quantum Mechanics, statistical mechanics
1. INLEDNING 2. TEORI. Arbete A4 Ab initio
 Arbete A4 Ab initio 1. INLEDNING Med Ab inition-metoder kan man, utgående från kvantmekanikens grundlagar, beräkna egenskaper som t.ex. elektronisk energi, jämviktskonformation eller dipolmoment för atomära
Arbete A4 Ab initio 1. INLEDNING Med Ab inition-metoder kan man, utgående från kvantmekanikens grundlagar, beräkna egenskaper som t.ex. elektronisk energi, jämviktskonformation eller dipolmoment för atomära
Number 14, 15, 16, and 17 also in English. Sammanställning av tentamensuppgifter Kvant EEIGM (MTF057).
 LULEÅ TEKNISKA UNIVERSITET Hans Weber, Avdelningen för Fysik, 2004 Number 14, 15, 16, and 17 also in English. Sammanställning av tentamensuppgifter Kvant EEIGM (MTF057). 1. Partikel i en en dimensionell
LULEÅ TEKNISKA UNIVERSITET Hans Weber, Avdelningen för Fysik, 2004 Number 14, 15, 16, and 17 also in English. Sammanställning av tentamensuppgifter Kvant EEIGM (MTF057). 1. Partikel i en en dimensionell
Kvantmekanik. Kapitel Natalie Segercrantz
 Kvantmekanik Kapitel 38-39 Natalie Segercrantz Centrala begrepp Schrödinger ekvationen i en dimension Fotoelektriska effekten De Broglie: partikel-våg dualismen W 0 beror av materialet i katoden minimifrekvens!
Kvantmekanik Kapitel 38-39 Natalie Segercrantz Centrala begrepp Schrödinger ekvationen i en dimension Fotoelektriska effekten De Broglie: partikel-våg dualismen W 0 beror av materialet i katoden minimifrekvens!
Egenvärdesproblem för matriser och differentialekvationer
 CTH/GU STUDIO 7 TMV36b - 14/15 Matematiska vetenskaper 1 Inledning Egenvärdesproblem för matriser och differentialekvationer Vi skall se lite på egenvärdesproblem för matriser och differentialekvationer.
CTH/GU STUDIO 7 TMV36b - 14/15 Matematiska vetenskaper 1 Inledning Egenvärdesproblem för matriser och differentialekvationer Vi skall se lite på egenvärdesproblem för matriser och differentialekvationer.
Atomer, ledare och halvledare. Kapitel 40-41
 Atomer, ledare och halvledare Kapitel 40-41 Centrala begrepp Kvantiserade energinivåer i atomer Elektronspinn och finstruktur Elektronen i en atom både banimpulsmoment, som karakteriseras av kvanttalet
Atomer, ledare och halvledare Kapitel 40-41 Centrala begrepp Kvantiserade energinivåer i atomer Elektronspinn och finstruktur Elektronen i en atom både banimpulsmoment, som karakteriseras av kvanttalet
Kvantmekanik. Kvantmekaniken: De naturlagar som styr förlopp i den mikroskopiska världen (och i den makroskopiska!) Kvantmekanik.
 Kap. 7. Kvantmekanik: introduktion 7A.1- I begynnelsen Kvantmekanik Kvantmekaniken: De naturlagar som styr förlopp i den mikroskopiska världen och i den makroskopiska! Kvantmekanik Klassisk fysik Specialfall!
Kap. 7. Kvantmekanik: introduktion 7A.1- I begynnelsen Kvantmekanik Kvantmekaniken: De naturlagar som styr förlopp i den mikroskopiska världen och i den makroskopiska! Kvantmekanik Klassisk fysik Specialfall!
FFM234, Klassisk fysik och vektorfält - Föreläsningsanteckningar
 FFM234, Klassisk fysik och vektorfält - Föreläsningsanteckningar Christian Forssén, Institutionen för fysik, Chalmers, Göteborg, Sverige Oct 16, 2018 9. Lösningar av Poissons ekvation Vi vet att Poissons
FFM234, Klassisk fysik och vektorfält - Föreläsningsanteckningar Christian Forssén, Institutionen för fysik, Chalmers, Göteborg, Sverige Oct 16, 2018 9. Lösningar av Poissons ekvation Vi vet att Poissons
FK Kvantfysikens principer, Fysikum, Stockholms universitet Tentamensskrivning, onsdag 21 december 2016, kl 17:00-22:00
 FK2003 - Kvantfysikens principer, Fysikum, Stockholms universitet Tentamensskrivning, onsdag 21 december 2016, kl 17:00-22:00 Läs noggrant genom hela tentan först. Börja med uppgifterna som du tror du
FK2003 - Kvantfysikens principer, Fysikum, Stockholms universitet Tentamensskrivning, onsdag 21 december 2016, kl 17:00-22:00 Läs noggrant genom hela tentan först. Börja med uppgifterna som du tror du
Bose-Einsteinkondensation. Lars Gislén, Malin Sjödahl, Patrik Sahlin
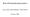 Bose-Einsteinkondensation Lars Gislén, Malin Sjödahl, Patrik Sahlin 3 mars, 009 Inledning Denna laboration går ut på att studera Bose-Einsteinkondensation för bosoner i en tredimensionell harmonisk-oscillatorpotential.
Bose-Einsteinkondensation Lars Gislén, Malin Sjödahl, Patrik Sahlin 3 mars, 009 Inledning Denna laboration går ut på att studera Bose-Einsteinkondensation för bosoner i en tredimensionell harmonisk-oscillatorpotential.
Kursplanen är fastställd av Naturvetenskapliga fakultetens utbildningsnämnd att gälla från och med , vårterminen 2018.
 Humanistiska och teologiska fakulteterna ÄFYD03, Fysik 3: Grundläggande kvantmekanik, statistisk mekanik och kvantstatistik för lärare, 15 högskolepoäng Physics 3: Basic Quantum Mechanics, Statistical
Humanistiska och teologiska fakulteterna ÄFYD03, Fysik 3: Grundläggande kvantmekanik, statistisk mekanik och kvantstatistik för lärare, 15 högskolepoäng Physics 3: Basic Quantum Mechanics, Statistical
KEMISK TERMODYNAMIK. Lab 1, Datorlaboration APRIL 10, 2016
 KEMISK TERMODYNAMIK Lab 1, Datorlaboration APRIL 10, 2016 ALEXANDER TIVED 9405108813 Q2 ALEXANDER.TIVED@GMAIL.COM WILLIAM SJÖSTRÖM Q2 DKW.SJOSTROM@GMAIL.COM Innehållsförteckning Inledning... 2 Teori, bakgrund
KEMISK TERMODYNAMIK Lab 1, Datorlaboration APRIL 10, 2016 ALEXANDER TIVED 9405108813 Q2 ALEXANDER.TIVED@GMAIL.COM WILLIAM SJÖSTRÖM Q2 DKW.SJOSTROM@GMAIL.COM Innehållsförteckning Inledning... 2 Teori, bakgrund
Kapitel 7. Atomstruktur och periodicitet. Kvantmekanik Aufbau Periodiska systemet
 Kapitel 7 Innehåll Kapitel 7 Atomstruktur och periodicitet Kvantmekanik Aufbau Periodiska systemet Copyright Cengage Learning. All rights reserved 2 Kapitel 7 Innehåll 7.1 Elektromagnetisk strålning 7.2
Kapitel 7 Innehåll Kapitel 7 Atomstruktur och periodicitet Kvantmekanik Aufbau Periodiska systemet Copyright Cengage Learning. All rights reserved 2 Kapitel 7 Innehåll 7.1 Elektromagnetisk strålning 7.2
Experimentella metoder, FK3001. Datorövning: Finn ett samband
 Experimentella metoder, FK3001 Datorövning: Finn ett samband 1 Inledning Den här övningen går ut på att belysa hur man kan utnyttja dimensionsanalys tillsammans med mätningar för att bestämma fysikaliska
Experimentella metoder, FK3001 Datorövning: Finn ett samband 1 Inledning Den här övningen går ut på att belysa hur man kan utnyttja dimensionsanalys tillsammans med mätningar för att bestämma fysikaliska
Andra EP-laborationen
 Andra EP-laborationen Christian von Schultz Magnus Goffeng 005 11 0 Sammanfattning I denna rapport undersöker vi perioden för en roterande skiva. Vi kommer fram till, både genom en kraftanalys och med
Andra EP-laborationen Christian von Schultz Magnus Goffeng 005 11 0 Sammanfattning I denna rapport undersöker vi perioden för en roterande skiva. Vi kommer fram till, både genom en kraftanalys och med
1 Hur förklarar du att det blev ett interferensmönster i interferensexperimentet med elektroner?
 Session: okt28 Class Points Avg: 65.38 out of 100.00 (65.38%) 1 Hur förklarar du att det blev ett interferensmönster i interferensexperimentet med elektroner? A 0% Vi måste ha haft "koincidens", dvs. flera
Session: okt28 Class Points Avg: 65.38 out of 100.00 (65.38%) 1 Hur förklarar du att det blev ett interferensmönster i interferensexperimentet med elektroner? A 0% Vi måste ha haft "koincidens", dvs. flera
Halogenlampa Spektrometer Optisk fiber Laserdiod och UV- lysdiod (ficklampa)
 Elektroner och ljus I den här laborationen ska vi studera växelverkan mellan ljus och elektroner. Kunskap om detta är viktigt för många tillämpningar men även för att förklara fenomen som t ex färgen hos
Elektroner och ljus I den här laborationen ska vi studera växelverkan mellan ljus och elektroner. Kunskap om detta är viktigt för många tillämpningar men även för att förklara fenomen som t ex färgen hos
Föreläsning 2 Modeller av atomkärnan
 Föreläsning 2 Modeller av atomkärnan Atomkärnan MP 11-1 Protonens och neutronens egenskaper Atomkärnors storlek och form MP 11-2, 4-2 Kärnmodeller 11-6 Vad gör denna ovanlig? Se även http://www.lbl.gov/abc
Föreläsning 2 Modeller av atomkärnan Atomkärnan MP 11-1 Protonens och neutronens egenskaper Atomkärnors storlek och form MP 11-2, 4-2 Kärnmodeller 11-6 Vad gör denna ovanlig? Se även http://www.lbl.gov/abc
Varje laborant ska vid laborationens början lämna renskrivna lösningar till handledaren för kontroll.
 Vätespektrum Förberedelser Läs i Tillämpad atomfysik om atomspektroskopi (sid 147-149), empiriska samband (sid 151-154), och Bohrs atommodell (sid 154-165). Läs genom hela laborationsinstruktionen. Gör
Vätespektrum Förberedelser Läs i Tillämpad atomfysik om atomspektroskopi (sid 147-149), empiriska samband (sid 151-154), och Bohrs atommodell (sid 154-165). Läs genom hela laborationsinstruktionen. Gör
7. Atomfysik väteatomen
 Partiklars vågegenskaper Som kunnat konstateras uppträder elektromagnetisk strålning ljus som en dubbelnatur, ibland behöver man beskriva ljus som vågrörelser och ibland är det nödvändigt att betrakta
Partiklars vågegenskaper Som kunnat konstateras uppträder elektromagnetisk strålning ljus som en dubbelnatur, ibland behöver man beskriva ljus som vågrörelser och ibland är det nödvändigt att betrakta
Checklista för funktionsundersökning
 Linköpings universitet Matematiska institutionen TATA41 Envariabelanalys 1 Hans Lundmark 2015-02-10 Checklista för funktionsundersökning 1. Vad är definitionsmängden D f? 2. Har funktionen några uppenbara
Linköpings universitet Matematiska institutionen TATA41 Envariabelanalys 1 Hans Lundmark 2015-02-10 Checklista för funktionsundersökning 1. Vad är definitionsmängden D f? 2. Har funktionen några uppenbara
Mekanik SG1108 Mekanikprojekt Dubbelpendel
 Mekanik SG1108 Mekanikprojekt Dubbelpendel Studenter: Peyman Ahmadzade Alexander Edström Robert Hurra Sammy Mannaa Handledare: Göran Karlsson karlsson@mech.kth.se Innehåll Sammanfattning... 3 Inledning...
Mekanik SG1108 Mekanikprojekt Dubbelpendel Studenter: Peyman Ahmadzade Alexander Edström Robert Hurra Sammy Mannaa Handledare: Göran Karlsson karlsson@mech.kth.se Innehåll Sammanfattning... 3 Inledning...
Laboration i Tunneltransport. Fredrik Olsen
 Laboration i Tunneltransport Fredrik Olsen 9 maj 28 Syfte och Teori I den här laborationen fick vi möjlighet att studera elektrontunnling över enkla och dubbla barriärer. Teorin bakom är den som vi har
Laboration i Tunneltransport Fredrik Olsen 9 maj 28 Syfte och Teori I den här laborationen fick vi möjlighet att studera elektrontunnling över enkla och dubbla barriärer. Teorin bakom är den som vi har
Tentamen i FTF140 Termodynamik och statistisk fysik för F3
 Chalmers Institutionen för Teknisk Fysik Göran Wahnström Tentamen i FTF4 Termodynamik och statistisk fysik för F3 Tid och plats: Tisdag aug, kl 8.3-.3 i Väg och vatten -salar. Hjälpmedel: Physics Handbook,
Chalmers Institutionen för Teknisk Fysik Göran Wahnström Tentamen i FTF4 Termodynamik och statistisk fysik för F3 Tid och plats: Tisdag aug, kl 8.3-.3 i Väg och vatten -salar. Hjälpmedel: Physics Handbook,
9. Magnetisk energi Magnetisk energi för en isolerad krets
 9. Magnetisk energi [RM] Elektrodynamik, vt 013, Kai Nordlund 9.1 9.1. Magnetisk energi för en isolerad krets Arbetet som ett batteri utför då det för en laddning dq runt en krets, från batteriets anod
9. Magnetisk energi [RM] Elektrodynamik, vt 013, Kai Nordlund 9.1 9.1. Magnetisk energi för en isolerad krets Arbetet som ett batteri utför då det för en laddning dq runt en krets, från batteriets anod
Milstolpar i tidig kvantmekanik
 Den klassiska mekanikens begränsningar Speciell relativitetsteori Höga hastigheter Klassisk mekanik Kvantmekanik Små massor Små energier Stark gravitation Allmän relativitetsteori Milstolpar i tidig kvantmekanik
Den klassiska mekanikens begränsningar Speciell relativitetsteori Höga hastigheter Klassisk mekanik Kvantmekanik Små massor Små energier Stark gravitation Allmän relativitetsteori Milstolpar i tidig kvantmekanik
Varje uppgift ger maximalt 3 poäng. För godkänt krävs minst 8,5 poäng och
 Institutionen för Fysik Göteborgs Universitet LÖSNINGAR TILL TENTAMEN I FYSIK A: MODERN FYSIK MED ASTROFYSIK Tid: Lördag 3 augusti 008, kl 8 30 13 30 Plats: V Examinator: Ulf Torkelsson, tel. 031-77 3136
Institutionen för Fysik Göteborgs Universitet LÖSNINGAR TILL TENTAMEN I FYSIK A: MODERN FYSIK MED ASTROFYSIK Tid: Lördag 3 augusti 008, kl 8 30 13 30 Plats: V Examinator: Ulf Torkelsson, tel. 031-77 3136
9. Magnetisk energi [RMC 12] Elektrodynamik, vt 2013, Kai Nordlund 9.1
![9. Magnetisk energi [RMC 12] Elektrodynamik, vt 2013, Kai Nordlund 9.1 9. Magnetisk energi [RMC 12] Elektrodynamik, vt 2013, Kai Nordlund 9.1](/thumbs/61/46243221.jpg) 9. Magnetisk energi [RMC 12] Elektrodynamik, vt 2013, Kai Nordlund 9.1 9.1. Magnetisk energi för en isolerad krets Arbetet som ett batteri utför då det för en laddning dq runt en krets, från batteriets
9. Magnetisk energi [RMC 12] Elektrodynamik, vt 2013, Kai Nordlund 9.1 9.1. Magnetisk energi för en isolerad krets Arbetet som ett batteri utför då det för en laddning dq runt en krets, från batteriets
Kommer sig osäkerheten av att vår beskrivning av naturen är ofullständig, eller av att den fysiska verkligheten är genuint obestämd?
 Inte mycket verkar säkert här...? Våg-partikeldualitet Ett system kan ha både vågoch partikelegenskaper i samma experiment. Vågfunktionen har en sannolikhetstolkning. Heisenbergs osäkerhetsrelation begränsar
Inte mycket verkar säkert här...? Våg-partikeldualitet Ett system kan ha både vågoch partikelegenskaper i samma experiment. Vågfunktionen har en sannolikhetstolkning. Heisenbergs osäkerhetsrelation begränsar
Atom-, Molekyl- och Fasta Tillståndets Fysik
 Föreläsning 8/9 Atom-, Molekyl- och Fasta Tillståndets Fysik Flerelektronatomer På motsvarande sätt som för väteatomen kommer elektronerna i atomerna hos grundämnen som har två eller fler elektroner också
Föreläsning 8/9 Atom-, Molekyl- och Fasta Tillståndets Fysik Flerelektronatomer På motsvarande sätt som för väteatomen kommer elektronerna i atomerna hos grundämnen som har två eller fler elektroner också
Tentamen i Materia, 7,5 hp, CBGAM0
 Fakulteten för teknik- och naturvetenskap Tentamen i Materia, 7,5 hp, CBGAM0 Tid Måndag den 9 januari 2012 08 15 13 15 Lärare Gunilla Carlsson tele: 1194, rum: 9D406 0709541566 Krister Svensson tele: 1226,
Fakulteten för teknik- och naturvetenskap Tentamen i Materia, 7,5 hp, CBGAM0 Tid Måndag den 9 januari 2012 08 15 13 15 Lärare Gunilla Carlsson tele: 1194, rum: 9D406 0709541566 Krister Svensson tele: 1226,
TENTAPLUGG.NU AV STUDENTER FÖR STUDENTER. Kursnamn Fysik 1. Datum LP Laboration Balkböjning. Kursexaminator. Betygsgränser.
 TENTAPLUGG.NU AV STUDENTER FÖR STUDENTER Kurskod F0004T Kursnamn Fysik 1 Datum LP2 10-11 Material Laboration Balkböjning Kursexaminator Betygsgränser Tentamenspoäng Övrig kommentar Sammanfattning Denna
TENTAPLUGG.NU AV STUDENTER FÖR STUDENTER Kurskod F0004T Kursnamn Fysik 1 Datum LP2 10-11 Material Laboration Balkböjning Kursexaminator Betygsgränser Tentamenspoäng Övrig kommentar Sammanfattning Denna
Lösningsskiss för tentamen Vektorfält och klassisk fysik (FFM234 och FFM232)
 Lösningsskiss för tentamen Vektorfält och klassisk fysik (FFM23 och FFM232) Tid och plats: Måndagen den 29 oktober 208 klockan 00-800, Maskinsalar Lösningsskiss: Christian Forssén Detta är enbart en skiss
Lösningsskiss för tentamen Vektorfält och klassisk fysik (FFM23 och FFM232) Tid och plats: Måndagen den 29 oktober 208 klockan 00-800, Maskinsalar Lösningsskiss: Christian Forssén Detta är enbart en skiss
Elektrodynamik. Elektrostatik. 4πε. eller. F q. ekv
 1 Elektrodynamik I det allmänna fallet finns det tidsberoende källor för fälten, dvs. laddningar i rörelse och tidsberoende strömmar. Fälten blir då i allmänhet tidsberoende. Vi ser då att de elektriska
1 Elektrodynamik I det allmänna fallet finns det tidsberoende källor för fälten, dvs. laddningar i rörelse och tidsberoende strömmar. Fälten blir då i allmänhet tidsberoende. Vi ser då att de elektriska
2.16. Den enkla harmoniska oscillatorn
 2.16. Den enkla harmoniska oscillatorn [Understanding Physics: 13.16-13.17] Den klassiska hamiltonfunktionen för en enkel harmonisk oscillator med den reducerade massan m och fjäderkonstanten (kraftkonstanten)
2.16. Den enkla harmoniska oscillatorn [Understanding Physics: 13.16-13.17] Den klassiska hamiltonfunktionen för en enkel harmonisk oscillator med den reducerade massan m och fjäderkonstanten (kraftkonstanten)
9. Magnetisk energi Magnetisk energi för en isolerad krets
 9. Magnetisk energi [RMC] Elektrodynamik, ht 005, Krister Henriksson 9.1 9.1. Magnetisk energi för en isolerad krets Arbetet som ett batteri utför då det för en laddning dq runt en krets, från batteriets
9. Magnetisk energi [RMC] Elektrodynamik, ht 005, Krister Henriksson 9.1 9.1. Magnetisk energi för en isolerad krets Arbetet som ett batteri utför då det för en laddning dq runt en krets, från batteriets
Tillämpad vågrörelselära FAF260, 6 hp
 Tillämpad vågrörelselära FAF260, 6 hp Inför laborationerna Förberedelser Läs (i god tid före laborationstillfället) igenom laborationsinstruktionen och de teoriavsnitt som laborationen behandlar. Till
Tillämpad vågrörelselära FAF260, 6 hp Inför laborationerna Förberedelser Läs (i god tid före laborationstillfället) igenom laborationsinstruktionen och de teoriavsnitt som laborationen behandlar. Till
Tentamen i matematisk statistik (9MA241/9MA341, STN2) kl 14 18
 LINKÖPINGS UNIVERSITET MAI Johan Thim Tentamen i matematisk statistik (9MA241/9MA341, STN2) 213-1-11 kl 14 18 Hjälpmedel är: miniräknare med tömda minnen och formelbladet bifogat. Varje uppgift är värd
LINKÖPINGS UNIVERSITET MAI Johan Thim Tentamen i matematisk statistik (9MA241/9MA341, STN2) 213-1-11 kl 14 18 Hjälpmedel är: miniräknare med tömda minnen och formelbladet bifogat. Varje uppgift är värd
LAB 3. INTERPOLATION. 1 Inledning. 2 Interpolation med polynom. 3 Splineinterpolation. 1.1 Innehåll. 3.1 Problembeskrivning
 TANA18/20 mars 2015 LAB 3. INTERPOLATION 1 Inledning Vi ska studera problemet att interpolera givna data med ett polynom och att interpolera med kubiska splinefunktioner, s(x), som är styckvisa polynom.
TANA18/20 mars 2015 LAB 3. INTERPOLATION 1 Inledning Vi ska studera problemet att interpolera givna data med ett polynom och att interpolera med kubiska splinefunktioner, s(x), som är styckvisa polynom.
Vibrationspektrometri. Matti Hotokka Fysikalisk kemi
 Vibrationspektrometri Matti Hotokka Fysikalisk kemi Teoretisk modell Translationer, rotationer och vibrationer z r y x Beaktas inte Translationer Rotationer Rotationspektrometri senare Vibrationer Basmodell
Vibrationspektrometri Matti Hotokka Fysikalisk kemi Teoretisk modell Translationer, rotationer och vibrationer z r y x Beaktas inte Translationer Rotationer Rotationspektrometri senare Vibrationer Basmodell
Konvergens för iterativa metoder
 Konvergens för iterativa metoder 1 Terminologi Iterativa metoder används för att lösa olinjära (och ibland linjära) ekvationssystem numeriskt. De utgår från en startgissning x 0 och ger sedan en följd
Konvergens för iterativa metoder 1 Terminologi Iterativa metoder används för att lösa olinjära (och ibland linjära) ekvationssystem numeriskt. De utgår från en startgissning x 0 och ger sedan en följd
Preliminärt lösningsförslag till Tentamen i Modern Fysik,
 Preliminärt lösningsförslag till Tentamen i Modern Fysik, SH1009, 008 05 19, kl 14:00 19:00 Tentamen har 8 problem som vardera ger 5 poäng. Poäng från inlämningsuppgifter tillkommer. För godkänt krävs
Preliminärt lösningsförslag till Tentamen i Modern Fysik, SH1009, 008 05 19, kl 14:00 19:00 Tentamen har 8 problem som vardera ger 5 poäng. Poäng från inlämningsuppgifter tillkommer. För godkänt krävs
Fysikaliska krumsprång i spexet eller Kemister och matematik!
 Fysikaliska krumsprång i spexet eller Kemister och matematik! Mats Linder 10 maj 2009 Ingen sammanfattning. Sammanfattning För den hugade har vi knåpat ihop en liten snabbguide till den fysik och kvantmekanik
Fysikaliska krumsprång i spexet eller Kemister och matematik! Mats Linder 10 maj 2009 Ingen sammanfattning. Sammanfattning För den hugade har vi knåpat ihop en liten snabbguide till den fysik och kvantmekanik
Räkneuppgifter 1, kvantmekanik
 Erik Sjöqvist Avdelningen för kvantkemi Uppsala Universitet Roland Lindh Avdelningen för kemi - Ångström Uppsala Universitet 3 mars 03 uppdaterade oktober 05 Räkneuppgifter, kvantmekanik Kvantmekanik och
Erik Sjöqvist Avdelningen för kvantkemi Uppsala Universitet Roland Lindh Avdelningen för kemi - Ångström Uppsala Universitet 3 mars 03 uppdaterade oktober 05 Räkneuppgifter, kvantmekanik Kvantmekanik och
2.8. Sannolikhetstäthetens vinkelberoende
 2.8. Sannolikhetstäthetens vinkelberoende [Understanding Physics: 19.7 (s. 590)-19.11] Härnäst skall vi studera vinkelberoendet av egenfunktionerna för n = 1 och n = 2. Den allmänna lösningen till den
2.8. Sannolikhetstäthetens vinkelberoende [Understanding Physics: 19.7 (s. 590)-19.11] Härnäst skall vi studera vinkelberoendet av egenfunktionerna för n = 1 och n = 2. Den allmänna lösningen till den
Kemi Grundläggande begrepp. Kap. 1. (Se även repetitionskompendiet på hemsidan.)
 Föreläsning 1. Kemins indelning Enheter Atomer, isotoper och joner Grundämnen och periodiska systemet Atomernas elektronstruktur och atomorbitaler Periodiska egenskaper Kemi Grundläggande begrepp. Kap.
Föreläsning 1. Kemins indelning Enheter Atomer, isotoper och joner Grundämnen och periodiska systemet Atomernas elektronstruktur och atomorbitaler Periodiska egenskaper Kemi Grundläggande begrepp. Kap.
