Regionalt vårdprogram för uterussarkom. Giltigt fr o m 1 mars 2017
|
|
|
- Agneta Bengtsson
- för 7 år sedan
- Visningar:
Transkript
1 Regionalt vårdprogram för uterussarkom Giltigt fr o m 1 mars 2017
2 I februari 2017 publicerades ett nationellt vårdprogram för endometriecancer som ersätter det tidigare regionala vårdprogrammet för endometriecancer från Delen för uterussarkom kvarstår som regionalt vårdprogram då nationellt vårdprogram för uterussarkom saknas. Texten rörande uterussarkom från 2012 har endast reviderats i form av förtydliganden i patologiavsnittet av Anna Måsbäck i den aktuella versionen. Jessica Wihl Regional Patientprocessledare Gynekologisk Cancervård Bitr överläkare gynonkologi/onkologi Regionalt cancercentrum syd Det regionala vårdprogrammet för uterussarkom har utarbetats av nedanstående personer. Vårdprogrammet skall vara ett arbetsredskap för gynekologerna på respektive kvinnoklinik, i synnerhet de onkologiansvariga läkarna. Vårdprogrammet är också ett arbetsredskap för gyn-onkologer, patologer och radiologer. Det är arbetsgruppens målsättning att vårdprogrammet regelbundet skall revideras och uppdateras. ARBETSGRUPPEN Maria Bjurberg, gynekologisk onkologi, Skånes onkologiska klinik, SUS, Lund Peter Hinsell, Kvinnokliniken, Helsingborg Annelie J:son-Söderström, Kvinnokliniken, Karlskrona Anjila Koul, gynekologisk onkologi, Skånes onkologiska klinik, SUS, Lund Göran Larsson, Kvinnokliniken, Karlskrona Anna Måsbäck, Klinisk Patologi Lund, Labmedicin Skåne Jan Persson, Kvinnokliniken, SUS, Lund ANDRA VÅRDPROGRAM Det nationella vårdprogrammet för endometriecancer samt vårdprogram för övriga tumörsjukdomar samt cancerrehabilitering finns tillgängliga via
3 Innehållsförteckning ARBETSGRUPPEN... 2 ANDRA VÅRDPROGRAM STADIEINDELNING... 4 FIGO stadieindelning för sarcoma uteri (uterussarkom) INCIDENS OCH KLASSIFIKATION ETIOLOGI PATOLOGI Leiomyosarkom... 6 Myxoida leiomyosarkom Endometriestromasarkom Adenosarkom Odifferentierat sarkom (inklusive höggradigt endometriestromasarkom) Heterologa sarkom PECom (Perivaskulär Epiteloidcellstumör) PROGNOSTISKA FAKTORER KLINISKA SYMTOM OCH DIAGNOSTIK KIRURGISK BEHANDLING Leiomyosarkom Endometriestromasarkom Odifferentierat sarkom ADJUVANT TERAPI TERAPI VID METASTASERAD/RECIDIVERANDE SJUKDOM UPPFÖLJNING REFERENSER... 13
4 Regionalt vårdprogram för uterussarkom, version 1 mars STADIEINDELNING Uterussarkomen har tidigare stadieindelats som endometriecancer men sedan 2009 finns en särskild FIGO-stadieindelning för de olika histologiska typerna av uterussarkom. FIGO stadieindelning för sarcoma uteri (uterussarkom) 2009 Leiomyosarkom, endometriestromasarkom och adenosarkom* Stadium I Tumören begränsad till uterus IA Tumörstorlek <5 cm IB Tumörstorlek >5 cm Stadium II Tumörutbredning i bäckenet IIA Tumörutbredning till adnexa IIB Tumörutbredning till andra extrauterina pelvina vävnader Stadium III Tumörutbredning till abdominala vävnader (att tumören pga. sin storlek sticker upp i buken utan överväxt på bukorgan berättigar inte att en tumör klassificeras som stadium III) IIIA En tumörförändring IIIB Mer än en tumörförändring IIIC Metastaser till pelvina och/eller paraaortala lymfkörtlar Stadium IV IVA IVB Tumören invaderar blåsa och/eller rektum Spridning av tumörväxt till avlägsna organ (fjärrmetastaser) Carcinosarkom CS i corporis uteri stadieindelas som carcinom i corporis uteri. * Anmärkning: Samtidiga tumörer i corporis uteri och ovarium/pelvis associerade med ovariell/pelvin endometrios skall klassificeras som multipla primära tumörer.
5 Regionalt vårdprogram för uterussarkom, version XXX 2. INCIDENS OCH KLASSIFIKATION Uterussarkom är ovanligt och visar allmänt en aggressiv och dålig prognos. De utgör < 1 % av de gynekologiska maligniteterna och endast 2 5 % av maligniteter i uterus. Drygt 100 nya fall diagnostiseras årligen i Sverige. Uterussarkomen indelas i fem grupper som skiljer sig åt beträffande histopatologi, klinisk bild och prognos: Carcinosarkom (CS), tidigare kallad Mixed Mesodermal Malignant Tumor eller Müllersk Blandtumör, uppstår från odifferentierade celler från Müllerska adenocarcinom och innehåller såväl maligna epiteliala celler och de-differentierade maligna celler med stromalt växtsätt. (McCluggage 2002) Carcinosarkomen betraktas därför som en högmalign epitelial tumör och behandlas i vårdprogrammet för endometriecancer. Leiomyosarkom (LMS) utgår från glatta muskelceller. Endometriestromasarkom (ESS, tidigare låggradig ESS), utgår från stroma celler i endometriet. Adenosarkom ovanlig blandtumör med benign epitelial komponent och malign sarkomkomponent. Odifferentierat sarkom (tidigare höggradig ESS), saknar differentiering. Carcinosarkomen är vanligast och utgör cirka 50 % av uterussarkomen, leiomyosarkomen utgör 40 % och endometriestromasarkomen 8 %. Det finns olika klassifikationssystem för uterussarkom utarbetade av bl. a International Society of Gynecologic Pathologists/WHO och Gynecologic Oncology Group. I dessa system beskrivs tumörerna som endera icke-epiteliala eller blandade epiteliala/icke-epiteliala. Skillnaden mellan systemen är att man inkluderar samtliga tumörer från vävnader normalt förekommande i uterus i den första och alla primära uterusmaligniteter i den sistnämnda. I Sverige används företrädesvis WHO-klassifikationen. 3. ETIOLOGI Etiologin är till största delen okänd. 5
6 Regionalt vårdprogram för uterussarkom, version 1 mars PATOLOGI Förslag till mall för PAD-svar Typ (leiomyosarkom, stromacellssarkom m m) Storlek Mitosförekomst/10 HPF (High Power Field) Cellatypi (lätt, måttlig, grav/fokal, generell) Nekroser Kärlinvasion Radikalitet med marginaler Infiltrerande randzon ( pushing border ) Extrauterin förekomst Nomenklatur och beskrivning nedan i huvudsak enl. WHO, Leiomyosarkom Makroskopi % solitära utan leiomyom. Oftare grå-gul/rosa snittyta, större och mjukare med nekros, blödning. Mer oregelbunden avgränsning mot omgivande myometrium än leiomyom. Vid ovanlig myombild tag 1 bit/cm Mikroskopi Mitoser: vanligen > 15/10 HPF, 5 9/10 HPF kan ses vid leiomyom, 10 20/10 HPF kan ses men är ovanligt vid leiomyom. Celltäthet åtminstone måttlig. Tumörcellsnekroser ses i 80 %. Abrupt övergång från viabla celler till nekrotiska celler utan mellanliggande granulationsvävnad eller fibros. Kvarvarande atypiska celler kan ibland ses i nekrosen, oftast perivaskulärt. Differentiera från infarkt- eller hyalina nekroser. Blödningar är vanligt. Oftast utan akut inflammation. Gradering kontroversiellt: Prognos bygger på spridning, alternativt storlek och mitotiskt index. Färgningar, differentialdiagnoser: Positiv för muskelmarkörer (Actin, Desmin) mest specifik, men inte helt sensitiv är Caldesmon. Ffa epiteloida varianter kan innehålla CAM5.2 + EMA + celler. Kan även likna stromasarkom vid förlust av fibrillär eosinofil cytoplasma och rundare kärnor, trikromfärgningar kan locka fram den fibrillära tegelröda cytoplasman. Både stromaceller och glattmuskelceller kan vara actin- och desminpositiva. Leiomyosarkom kan, liksom låggradigt endometriestromasarkom, vara ER-, PGR- eller AR-positiva (30-40%).
7 Regionalt vårdprogram för uterussarkom, version XXX Myxoida leiomyosarkom Makroskopi Gelatinös, kan te sig välavgränsad. Histologi: Oftast hypocellulär. Infiltrativt växande i oregelbundna tungor, ibland i vener. Ofta låg kärnatypi och lågt antal mitoser, p.g.a. glest liggande celler. Minst 2-4 mitoser/50 Hpf och fokalt uttalad atypi. Rikligt matrix, svagt basofilt eller eosinofilt. Myxoida områden färgas blå i Alcian-Blue (alt. färgning kolloidalt järn) Ref. Histopathol 2011;59:1144 Burch DM, Tavassoli FA Tab. Spolcelligt leiomyosarkom med osäker malignitetspotential (STUMP), enl. WHO Tumörcellsnekros Måttlig-grav atyp Mitoser/10 Hpf Mitoser, medel hos recidiverande Andel med recidiv tumörer Nej Fokal/multifokal < ,6% (3/22 fall) Diffus < ,4% (7/67 fall) Ja Nej < ,7% (4/15 fall) Nej Nej 15 eller mer - 0%, 0/39 fall Tab. Diagnostiska kriterier för leiomyosarkom (LMS), baserat på subtyp. (ref. Nucci & Oliva, 2014) Spolcelligt LMS Epiteloitt LMS Myxoitt LMS Cytologisk atypi Måttlig-grav Måttlig till grav Lätt-grav Tumörcellsnekros +/- +/- +/- Mitoser/10 Hpf 10 eller fler 5 eller fler 2 eller mer* såvida nekros eller atypi inte ses, ffa i infiltrerande marginaler Om myxoitt LMS: mitoser, 2 eller mer* såvida nekros eller atypi inte ses, ffa i infiltrerande marginaler. Endast tumörer med mindre än 3 mitoser och utan cytologisk atypi skall tolkas som myxoitt leiomyom. 7
8 Regionalt vårdprogram för uterussarkom, version 1 mars a Låggradigt Endometriestromasarkom Klinik: Medel 53 år. Metastaser vanligast till lungor och ovarier. Metastaser vanligast till lungor och ovarier % engagerar ovarier resp. lymfkörtlar. Makroskopi: Endometriekomponenten är mjuk, beige, jämn. Polypoid, intramural växt dominerar ofta, kan följa större kärl. Initialt diffust förtjockat endometrium, senare nodulär härd, slutligen stor, dåligt avgränsad tumör. Histologi: Celler som vid endometriestroma i proliferationsfas, minimal atypi, Rikligt med tunnväggiga kärl som liknar spiralartärerna, jämnt fördelade. Svåravgränsad, invaderar ibland myometriet extensivt. Invasion av lymf- och kärlrum är karakteristiskt, därav det äldre namnet endolymfatisk stromamyos. Ibland spolcellig. I 20 % extensiv nekros. Hyaliniserade zoner och plack samt aggregat med skumceller eller foci med nekros kan ses. Deciduavandling kan ses, samt myxoida varianter. I % finns körtlar av endometrietyp, ofta prolifererande. Könstängsliknande områden kan också ses. Immunhistokemi: Positiva för vimentin och CD10), aktin- och desminpositivitet kan ses, och vanligen positiv för ER och PGR. Vanligen negativa för caldesmon utom i områden med glattmuskeldidfferentiering Genetik: Mutation av JAZF1-SUZ12 (formerly JAZF1-JJAZ1) fusion ses i en stor andel av LG- ESSs. Differentialdiagnoser: Jämn kant (pushing margin) vid stromal nodulus, diploida med låg S-fas. Körtelfattig adenomyos, framför allt hos äldre. Diffus stark infärgning för 2 glattmuskelmarkörer ex actin och desmin talar för leiomyomatös tumör, ex HCL (Highly Cellular Leiomyoma) eller leiomyosarkom, vanligen endast fokal positivitet i stromasarkom. Positiv CD10-färgning kan ses i leiomyosarkom (10). Kombinerad glattmuskel-stromatumör finns. Områden med sex-cord like elements kan vara positiva i inhibin, CD99, desmin och keratin-färgningar. Hemangiopericytom eller vaskulärt leiomyom (mindre celltätt) kan misstänkas vid riklig vaskularisering. 4.2b Höggradigt Endometriestromasarkom Klinik: år (medel 50 år). Onormal vaginal blödning, uterusförstoring eller bäckentumör. Makroskopi: Ofta polypoid eller intramural tumörmassa upp till 9 cm. Ofta extrauterin spridning vid diagnos. Beige-gul, fläskig snittyta. Ofta nekroser eller blödningar. Histologi: Kan ha typisk infiltration och kärlmönster som vid LgESS, men ofta konfluerade, destruerande växt. Varierande blandning av hypercellulära områden med höggradiga runda celler (ofta dominerande) med varierande, distinkt nukleol och måttlig eosinofil cytoplasma i nästen med finkalibriga kapillärer emellan. Vanligen > 10 mitoser/10 Hpf och nekroser. Typiskt är lymfovaskulär infiltration. I sällsynta fall ses samtidig LgESS. Immunhistokemi: Varierande positivitet för CD10 Svag positivitet eller negativitet för ER och PGR.
9 Regionalt vårdprogram för uterussarkom, version XXX Undergruppen med Y-FAM -translokation (se nedan) är CD10, ER och PGR negativa men visar stark CyklinD1-positivitet (>70% av kärnorna). Den höggradiga komponenten är c-kitpositiv och DOG1-negativ. Fokal positivitet för ActSM, desmin, EMA eller keratin kan ses. Genetik: En del av dessa har YWHEA-FAM22 fusion, vilket resulterar i t(10;17) (q22;p13). Prognos: Ofta recidiv inom ett år, sämre prognos är LgESS samt bättre än odifferentierat sarkom. 4.3 Adenosarkom En blandad tumör med benign epitelial och malign mesenkymal komponent huvudsakligen låggradig, men ca ¼ innehåller en höggradig sarkomatös del s.k. adenosarkom med sarkomatös överväxt. Majoriteten av patienterna (70 %) är postmenopausala, men även unga kvinnor kan drabbas. Makroskopi: Oftast polypoida kring 6 cm (1 20 cm) i diameter, beige-brun med multipla små hemorragier eller nekroser i 25 %, eventuellt små cystor % invaderar myometriet ibland med kärlinväxt. Vanligare än adenofibrom eller adenomyom. Histologi: Bild kan likna phyllodestumörer med dilaterade eller tilltryckta körtlar. Karakteristiskt är stromakondensation kring körtlar och klyftor och här ses den mest uttalade atypin och mitosrikedomen, detta skiljer adenosarkom från de flesta övriga blandtumörer. Här ses 2 20 mitoser/hpf, > 10 mitoser/10 Hpf i de hypercellulära områdena. Vanligen endast lätt cytologisk atypi, ibland måttlig. Fall med riklig fibros och bedrägligt benign bild i delar av tumören finns. Kan uppstå i ordinär corpuspolyp. Epitelet är vanligen av endometrioid typ. Benignt epitel eventuellt atypi OK men inte invasion. Ibland ses adenocarcinom i intilliggande endometrium. Sarcomatous overgrowth i 10 % med ren sarkomatös komponent utan körtlar, ofta höggradig, ses i mer än 25 % av den totala tumörvolymen, prognostiskt sämre med % recidiv (jfr % recidiv och % dödsfall). IHC: Fokalt CD10, mer positivitet vid låggradiga, varierande positivitet för glattmuskelmarkörer kan ses. Ki67 hög vid sarkomatös överväxt men ingen signifikant höjning vid låggradig. P53 kan vara positivt framför allt i höggradiga, negativt i endometriepolyper, endometrios, adenofibrom och ESS. Förlust av PGR vid sarkomatös överväxt. Differentialdiagnoser: Adenofibrom (kräver < 2 mitoser/10 Hpf, inte uttalad stromal cellularitet och inte mer än lätt cellatypi, AFIP s. 165), carcinosarkom. APA (Atpiskt Polypoidt Adenomyom), som ofta har rikligt med skivepitelmetaplasi (morula) kan ha mitoser i stromat, < 2/10 Hpf. Prognos: Recidiv ses i upp till 30 %, vanligast i vagina, pelvis och abdomen. Hematogen spridning är ovanligt. Metastasering ses mest vid sarkomatös överväxt. 4.4 Odifferentierat sarkom (inklusive höggradigt endometriestromasarkom) 9
10 Regionalt vårdprogram för uterussarkom, version 1 mars 2017 Ovanlig, vanligen postmenopausalt med medelålder på 60 år. 2/3 debuterar med blödning och spridning/högt stadium. Makroskopi: Ofta intraluminala polypoida och >10cm, med fläskig snittyta och nekros/blödning. Histologi: Heterogen grupp. Oftast > 10 mitoser/10 HPF. Subtypen höggradigt ESS kan men benämna fall som överlappar med områden med låggradig ESS. Stark positivitet för CD10 och frånvaro av (eller sparsam) positivitet för muskelmarkörer har också rekommenderats som diagnostiska för stromacellssarkom. Destruktiv infiltration med blödning och nekros samt inslag av stora bisarra, eventuellt multinukleära celler och foci med glattmuskel-differentiering kan ses. Heterolog komponent kan finnas Differentialdiagnoser: Andra mjukdelssarkom rhabdomyosarkom, osteosarkom, liposarkom, malignt fibröst histiocytom. Immunhistokemi: Positiv i Vimentin. Positivitet ses för CD10 framför allt i låggradiga ESS, ibland i höggradiga. Dessa kan också vara ER+. Negativ i EMA och caldesmon. Inhibin-negativ, men områden med sex-cord like elements kan vara positiva. Fokal keratinpositivitet har setts i ett fåtal fall. Ibland svag positivitet i desmin och aktin. CyklinD1 kan vara positiv men samtidig CD10-positivtet talar mot höggradigt stomasarkom av Y-FAM-typ. Prognos: Även vid Stadium I är dödligheten stor inom 2 år. 4.5 Heterologa sarkom Rhabdomyosarkom är det vanligaste rena heterologa sarkomet följt av kondrosarkom, osteosarkom, liposarkom eller med blandade komponenter 4.6 PECom (Perivaskulär Epiteloidcellstumör) (enl. WHO 2014, Nucci & Oliva 2014, Fadare 2008) Klinik: Mycket ovanlig mesenkymal tumör, med oklar histiogenes år, mest i perimenopausal ålder (medel år) Ibland associerad med Tuberös skleros komplexet (aut. dom TSC-mutation, 70 % nymutation), dock mindre ofta än vid extrauterina PECom. Makroskopi: 0,5->20 cm, oftast solitär. Mikroskopi: Kan ha en välavgränsad eller infiltrerande kant, ibland med tung-lika Infiltrationsområden. Cytoplasman är klar-fingrynigt eosinofil och kärnan är oval-rund, normokromatisk med liten nukleol. Blandning av epiteloida celler i nästen eller diffust och spolformade celler i korta fascikler och nästen. Varierande antal mitoser, oftast få. Ibland kan melaninpigment ses. Immunhistokemi: 92 % uttrycker HMB45, 72 % Melan A, 50 % MiTF, 80 % glattmuskelactin, och i färre fall 49 %, desmin- eller caldesmon-positivitet. Ofta ER och PGR-positiv. CD1a, kan vara +, liksom Masson för melanin.
11 Regionalt vårdprogram för uterussarkom, version XXX I vissa fall kan epiteloida, perivaskulära HMB45-positiva celler ses perivaskulärt i omgivande myometrium, ovarium, pelvin mjukvävnad och lymfkörtlar (PEComatos). Negativa i cytokeratiner, inhibin och CD34. Genetik: I sällsynta fall associerad med Lymfangioleiomyomatos (LAM) och Tuberös skleros komplexet (Hud- och hjärnförändringar (ex. subependymalt astrocytom), renalt angiomyolipom, rhabdomyom i hjärtmuskeln, pulmonell klarcellig sugar-tumor, cystor i lever, njure och pankreas). Inaktivering av TSC1 (9q43) eller TSC2 (16p13.3) genen kan ses sporadiskt eller som syndrom, med activering av mtor-pathwat. TFE3 gen-rearranemang utan någon inaktivering av TSC är ovanligt. Prognos: Tumörer med bara >5 cm i storlek eller höggradig kärnatypi (alt. mångkärniga jätteceller) klassificeras som osäker malignitetspotential. Två eller fler riskfaktorer, klassificeras som hög risk för aggressivt beteende, av även: Cellrikedom, mitoser>1/50 Hpf, nekros, infiltrativa marginaler och vaskulär infiltration. Spridning ses till lokalt, lunga, benmetastaser, sällan lymfkörtelmetastaser. Tumörer med inaktivering av TSC1 eller TCS2 kan svara på mtor-inihibitorer. Differentialdiagnoser: Epiteloid eller spolcellig, glattmuskeltumör Melan A-negativ. Epitelioid endometriestromatumör. Melanom eller pigmenterad nervskidetumör. UTROSCT. GIST, PSTT, Diffus LAM. 5. PROGNOSTISKA FAKTORER Den viktigaste prognostiska faktorn för samtliga sarkomtyper är stadium vid diagnos. Över 50 % av sarkomen upptäcks i stadium I. Spridningen sker både hematogent (framför allt LMS) och lymfogent (CS). Fjärrmetastasering sker främst till lungor samt till lymfkörtlar i bäckenet och paraaortalt. Vid recidiv är fjärrmetastasering vanligare än lokoregionala recidiv. 5- årsöverlevnaden för leiomyosarkom är %. Mycket högt antal mitoser (> 20 per 10 HPF) är förenat med sämre prognos men skall bedömas i relation till atypigraden (se ovan, kapitel Patologi). För ESS i stadium I är 5-årsöverlevnaden omkring 80 %. 6. KLINISKA SYMTOM OCH DIAGNOSTIK De vanligaste symtomen är blödningsrubbningar och lågt sittande buksmärtor. Uterus är nästan alltid förstorad vid leiomyosarkom och LMS kan inte kliniskt skiljas från benigna myom. Sarkom bör misstänkas hos en kvinna vars uterus tillväxer efter menopaus. Vid CS är uterus ofta normalstor och diagnosen kan ofta ställas med endometriebiopsi eller via abrasio. LMS diagnostiseras däremot sällan via endometriebiopsi/abrasio, eftersom tumören kan växa i uterusväggen utan att bryta igenom livmoderslemhinnan. Datortomografi av buk, bäcken och thorax skall ingå i den primära utredningen. Sarkomen sprids tidigt hematogent och små lungmetastaser kan upptäckas vid CT-undersökning. 11
12 Regionalt vårdprogram för uterussarkom, version 1 mars KIRURGISK BEHANDLING I stadium I kan kirurgi vara kurativ behandling. Optimal cytoreduktion i stadier med spridning utanför corpus uteri har evaluerats i endast ett fåtal studier och resultaten är inte entydiga. Det är inte heller klart definierat vad som är optimal cytoreduktion vid sarkom. 7.1 Leiomyosarkom Total hysterektomi, SOEB, buksköljvätska för cytologi, lymfadenektomi/biopsi av förstorade lymfkörtlar samt biopsi av metastassuspekta förändringar. Hos premenopausala kvinnor kan ovarierna kvarlämnas. Spridning till lymfkörtlar eller adnexa finns endast hos 3 % i tidigt stadium. Vare sig SOEB eller lymfkörtelutrymning har dock kunnat påvisas vara oberoende prognostiska faktorer för överlevnad. Postmenopausalt utföres oftast SOEB p g a att det trots allt finns en liten risk för metastasering. Dessutom förekommer låggradigt hormonkänsliga leiomyosarkom. 7.2 Endometriestromasarkom Adekvat hysterektomi, SOEB, buksköljvätska för cytologi, lymfadenektomi vid förstorade körtlar i cytoreducerande syfte samt biopsi av metastassuspekta förändringar % diagnosticeras i stadium I II % recidiverar och oftast i lilla bäckenet. Radikal hysterektomi göres vid flertal nordiska centra. Incidensen av lymfkörtelengagemang varierar från 0 33 %. Systematisk lymfkörtelutrymning har ej kunnat påvisas leda till förlängd överlevnad. 7.3 Odifferentierat sarkom Total hysterektomi, SOEB, buksköljvätska för cytologi, adenektomi/biopsi av förstorade lymfkörtlar samt biopsi av metastassuspekta förändringar. Få data finns angående incidens av lymfkörtelspridning. Ytterligare data behövs men hittills finns ej evidens för systematisk lymkörtelutrymning. 8. ADJUVANT TERAPI Någon överlevnadsvinst med adjuvant kemo- eller radioterapi vid uterussarkom har inte påvisats i randomiserade studier. Avsaknaden av överlevnadsvinst med adjuvant radioterapi vid LMS förklaras åtminstone delvis av att fjärrmetastasering är vanligare än lokoregionala recidiv. Adjuvant gestagenterapi har rekommenderats vid låggradigt ESS, men konklusiva studier saknas. 9. TERAPI VID METASTASERAD/RECIDIVERANDE SJUKDOM Vid recidiv av endometriestromasarkom skall aromatashämmare alternativt gestagenterapi övervägas i första hand beroende på den höga förekomsten av östrogen- respektive progesteronreceptorer. Vid metastaserande leiomyosarkom ges cytostatikabehandling och i
13 Regionalt vårdprogram för uterussarkom, version XXX terapival sker samarbete med kollegor inom allmänonkologin, vilka behandlar mjukdelssarkom. Fas 2-studier har visat en något förbättrad överlevnad med kombinationen gemcitabindocetaxel i såväl första som andra linjen vid recidiverande LMS, dock med påtaglig toxicitet. Fortfarande är dock kombinationen doxorubicin-ifosfamid att betrakta som förstaval givet i 4 6 cykler beroende på terapisvar. Strålbehandling används mot lokalrecidiv samt i palliativa situationer medan kirurgi kan övervägas exempelvis vid en enstaka lungmetastaser. 10. UPPFÖLJNING Alla patienter följs enligt samma schema som vid högrisk endometriecancer. Om radiologiska kontroller i det individuella fallet är indicerade, bör thorax inkluderas. 11. REFERENSER Amant F, Coosemans A, Debiec-Rychter M, Timmerman D, Vergote I. Clinical management of uterine sarcomas. The Lancet Oncology 2009; 12: Blackmon SH, Shah N, Roth JA et al. Resection of pulmonary and extrapulmonary sarcomatous metastases is associated with long-term survival. Ann Thorac Surg 2009; 88: Burch DM, Tavassoli FA. Myxoid leiomyosarcoma of the uterus. Histopathol 2011;59: Cancer Incidence in Sweden 2009: Socialstyrelsen Cohen I. Endometrial pathologies associated with postmenopausal tamoxifen treatment. Gynecol Oncol 2004; 94: Dinh TA, Olivia EA, Fuller Jr AF et al. The treatment of uterine leiomyosarcoma. Results from a 10 year experience ( ) at the Massachusetts General Hospital. Gynecol Oncol 2004; 92: DiSaia PJ, Percorelli S. Gynecological sarcomas. Semin Surg Oncol 1995; 10: Fadare O. perivascular epitheloid cell tumor (PEComa) of the uterus. Adv Anat Pathol 2008;15:63-75 Fang Z, Matsumoto S, Ae K et al. Postradiation soft tissue sarcoma: a multiinstitutional analysis of 14 cases in Japan. J Orthop Sci 2004; 9:242 Gadducci A. The management of patients with uterine sarcoma: A debated clinical challenge. Crit Rev Oncol Hematol 2008; 65:
14 Regionalt vårdprogram för uterussarkom, version 1 mars 2017 García-Martinez E, Prefasi LE, García-Donas J et al. Current management of uterine sarcomas. Clin Transl Oncol 2011; 13: Guintoli RL, Metzinger DS, DiMarco CS et al. Retrospective review of 208 patients with leiomyosarcoma of the uterus: prognostic indicators, surgical management, and adjuvant therapy. Gynecol Oncol 2003; 89: Hensley ML, Blessing JA et al. Fixed-dose rate gemcitabine plus docetaxel as first-line therapy for metastatic uterine leiomyosarcoma: a Gynecologic Oncology Group phase II trial. Gynecol Oncol 2008; 109: Jaffe ES, Harris NL, Stein H and Vardiman JW (eds.): WHO Classification of Tumours Pathology and Genetics of Tumours of the Breast and Female Genital Organs. IARC Press, Lyon 2003 Kanjeekal S, Chambers A, Fung Kee Fung M et al. Systemic therapy for advanced uterine sarcoma: A systematic review of the literature. Gynecol Oncol 2005; 97:624-6 Kapp DS, Shin JY, Chan JK. Prognostic factors and survival in 1396 patients with uterine leiomyosarcomas: emphasis on impact of lymphadenectomy and oophorectomy. Cancer 2008; 112: Kurman RJ, Carcangiu ML, Herrington S, Young RH (eds.) WHO Clissification of tumours of female reproductive organs. International Agency for Research on Cancer (IARC) Lyon, 2014 ISBN Memarzadeh S, Mundt A, Plaxe S, Goff B, Savarese D, Falk S. Uterine sarcoma: Staging and treatment. Up to Date Publication. Review. McCluggage WG. Uterine carcinosarcomas (malignant mixed Mullerian tumors) are metaplastic carcinomas. Int J Gynecol Oncol 2002; 12: McCluggage et al. CD10 is a sensitive and diagnostically useful immunohistochemical marker of normal endometrial stroma and of endometrial stromal neoplasms. Histopathol 2001 Sep; 39(3)273-8 Nucci M, Olia E. Diagnostic Pathology: Gynecological 2014 Amirsys Publishing Inc. ISBN: Oliva E, Young RH, Amin MB et al. An immunohistochemical analysis of endometrial stromal and smooth muscle tumors of the uterus. A study of 54 cases emphasizing the importance of using a panel of overlap in immunoreactivity for individual antibodies. Am J Surg Pathol 2002; 26: Prat J. FIGO staging for uterine sarcomas. Int J Gynaecol Obstet 2009; 104:
15 Regionalt vårdprogram för uterussarkom, version XXX Reich O, Regauer S. Hormonal therapy of endometrial stromal sarcoma. Curr Opin Oncol 2007; 19: Santos L, Garg K, Diaz J, Soslow R, Hensley M, Alektiar K, Barakat R, Leitao M. Incidence of lymf node and adnexal metastasis in endometrial stromal sarcoma. Gynecologic Oncology 2011; 121: Shah JP, Bryant CS, Kumar s et al. Lymphadenectomy and ovarian preservation in low-grade endometrial stromal sarcoma. Obstet Gynecol 2008; 112: Silverberg SG and Kurman RJ. Atlas of Tumor Pathology Third Series Fascicle 3. Tumors of the uterine corpus and gestational trophoblastic disease. Armed Forces Institute of Pathology, Washington D.C Sorbe B, Johansson B. Prophylactic pelvic irradiation as part of primary therapy in uterine sarcomas. Int J Oncol 2008; 32: Zagouri F, Dimopoulos A-M, Fotiou S et al. Treatment of early uterine sarcomas: disentangling adjuvant modalities. World J Surg Oncol 2009; 7: 38 15
16 Regionala cancercentrum landstingens och regionernas nationella samverkan inom cancervården. Med patienter och närstående för hela människan, i dagens och framtidens cancervård.
Vårdprogram för endometriecancer (corpuscancer) och uterussarkom
 Vårdprogram för endometriecancer (corpuscancer) och uterussarkom 2012 Vårdprogrammets giltighetstid: 2012-04-01--2014-12-31 www.ocsyd.se Versionshantering Datum 2012- Skapad Beskrivning av förändring Onkologiskt
Vårdprogram för endometriecancer (corpuscancer) och uterussarkom 2012 Vårdprogrammets giltighetstid: 2012-04-01--2014-12-31 www.ocsyd.se Versionshantering Datum 2012- Skapad Beskrivning av förändring Onkologiskt
Gynekologisk Cancer : Corpus
 Gynekologisk Cancer : Corpus Susanne Malander VO onkologi och strålningsfysik gyn-sektionen Christer Borgfeldt Kvinnokliniken Skånes Universitetssjukhus (SUS) Lund Corpuscancer Endometriecancer (Sarkom)
Gynekologisk Cancer : Corpus Susanne Malander VO onkologi och strålningsfysik gyn-sektionen Christer Borgfeldt Kvinnokliniken Skånes Universitetssjukhus (SUS) Lund Corpuscancer Endometriecancer (Sarkom)
Vid solitära recidiv kan kirurgi vara en botande behandling om man uppnår tumörfrihet.
 Regional medicinsk riktlinje Uterussarkom Fastställd av Hälso- och sjukvårdsdirektören (HS 2017-00942). Uppdaterad 2017-12-13. Giltig två år från uppdateringsdatum. Utarbetad av den Regionala patientprocessgruppen
Regional medicinsk riktlinje Uterussarkom Fastställd av Hälso- och sjukvårdsdirektören (HS 2017-00942). Uppdaterad 2017-12-13. Giltig två år från uppdateringsdatum. Utarbetad av den Regionala patientprocessgruppen
Epiteliala & Mesenkymala uterus tumörer Del 3
 Epiteliala & Mesenkymala uterus tumörer Del 3 April 2014 Anne-Marie Levin Jakobsen MD PhD MESENCHYMALA TUMÖRER WHO 2002 Stroma tumörer Endometrie stroma nodule låggradig endometrie stromasarkom (ESS) Odifferentierad
Epiteliala & Mesenkymala uterus tumörer Del 3 April 2014 Anne-Marie Levin Jakobsen MD PhD MESENCHYMALA TUMÖRER WHO 2002 Stroma tumörer Endometrie stroma nodule låggradig endometrie stromasarkom (ESS) Odifferentierad
Endometriebiopsi/skrap. Benignt Hyperplasi Cancer DNA
 Endometriebiopsi/skrap Benignt Hyperplasi Cancer DNA DNA-analys Inför OP endometriecancer Cancer av: Lågrisk- eller högrisktyp? Djupväxt > ½ myometriet? Avvikande DNA-innehåll? Diploid normal Non-diploid
Endometriebiopsi/skrap Benignt Hyperplasi Cancer DNA DNA-analys Inför OP endometriecancer Cancer av: Lågrisk- eller högrisktyp? Djupväxt > ½ myometriet? Avvikande DNA-innehåll? Diploid normal Non-diploid
Diana Zach
 Vulvacancer 2017-10-03 Diana Zach Bitr överläkare Gynekologisk onkologi Karolinska Universitetssjukhus Vad är vulvacancer? Vanligast histologisk typ: Skivepitelcancer 80-90% Ytterligare histologiska typer:
Vulvacancer 2017-10-03 Diana Zach Bitr överläkare Gynekologisk onkologi Karolinska Universitetssjukhus Vad är vulvacancer? Vanligast histologisk typ: Skivepitelcancer 80-90% Ytterligare histologiska typer:
ENDOMETRIECANCER -VAD HÄNDER EFTER KIRURGIN?
 Stadiefördelning 2015 Sverige INCA ENDOMETRIECANCER -VAD HÄNDER EFTER KIRURGIN? 70 60 50 40 Caroline Lundgren Överläkare, Med dr Radiumhemmet 30 20 10 0 59 23 6 3 1 2 2 2 1 Stad IA Stad IB Stad II Stad
Stadiefördelning 2015 Sverige INCA ENDOMETRIECANCER -VAD HÄNDER EFTER KIRURGIN? 70 60 50 40 Caroline Lundgren Överläkare, Med dr Radiumhemmet 30 20 10 0 59 23 6 3 1 2 2 2 1 Stad IA Stad IB Stad II Stad
Epiteliala & Mesenkymala uterus tumörer Del 1
 Epiteliala & Mesenkymala uterus tumörer Del 1 April 2014 Anne-Marie Levin Jakobsen MD PhD Histologiska typer-epiteliala WHO 2002 Endometrioid carcinom Varianter av endometrioid carcinom: Med skivepitelmetaplasi
Epiteliala & Mesenkymala uterus tumörer Del 1 April 2014 Anne-Marie Levin Jakobsen MD PhD Histologiska typer-epiteliala WHO 2002 Endometrioid carcinom Varianter av endometrioid carcinom: Med skivepitelmetaplasi
Stadieindelning enligt FIGO för ovarialcancer, endometriecancer, cervixcancer och sarkom
 Stadieindelning enligt FIGO för ovarialcancer, endometriecancer, cervixcancer och sarkom Kirurgisk stadieindelning av ovarialcancer enligt FIGO (1988) A B C I IA IB IC A B C V Tumören är begränsad till
Stadieindelning enligt FIGO för ovarialcancer, endometriecancer, cervixcancer och sarkom Kirurgisk stadieindelning av ovarialcancer enligt FIGO (1988) A B C I IA IB IC A B C V Tumören är begränsad till
Endometriecancer och uterussarkom. Henrik Falconer Överläkare, docent Kvinnokliniken, Karolinska Universitetssjukhuset
 Endometriecancer och uterussarkom Henrik Falconer Överläkare, docent Kvinnokliniken, Karolinska Universitetssjukhuset Endometriecancer i Sverige - Flera stora förändringar de senaste 5 åren Kraftig ökning
Endometriecancer och uterussarkom Henrik Falconer Överläkare, docent Kvinnokliniken, Karolinska Universitetssjukhuset Endometriecancer i Sverige - Flera stora förändringar de senaste 5 åren Kraftig ökning
Tillämpning av Nationellt vårdprogram Endometriecancer
 Regional medicinsk riktlinje Tillämpning av Nationellt vårdprogram Endometriecancer Fastställd av Hälso- och sjukvårdsdirektören (diarienr) giltig tom 2020-06-26. Utarbetad av Regional vårdprocessgrupp
Regional medicinsk riktlinje Tillämpning av Nationellt vårdprogram Endometriecancer Fastställd av Hälso- och sjukvårdsdirektören (diarienr) giltig tom 2020-06-26. Utarbetad av Regional vårdprocessgrupp
Vagina - patologi. Anna Måsbäck ST-kurs VT 2014
 Vagina - patologi Anna Måsbäck ST-kurs VT 2014 Skivepitelklädd Bakteriehämmande miljö Laktobaciller, lågt ph ca 4,6. Infektion vanligaste sjukdomen Kollaberat rör framför rektum och bakom urethra Fram-
Vagina - patologi Anna Måsbäck ST-kurs VT 2014 Skivepitelklädd Bakteriehämmande miljö Laktobaciller, lågt ph ca 4,6. Infektion vanligaste sjukdomen Kollaberat rör framför rektum och bakom urethra Fram-
Gynekologisk Cancer: cervix. Christer Borgfeldt Kvinnokliniken Susanne Malander SOK gyn-sektionen Skånes Universitetssjukhus (SUS) Lund
 Gynekologisk Cancer: cervix Christer Borgfeldt Kvinnokliniken Susanne Malander SOK gyn-sektionen Skånes Universitetssjukhus (SUS) Lund Vad vi skall tala om idag Cervix Ovariet Epiteliala tumörer Germinalcellstumörer
Gynekologisk Cancer: cervix Christer Borgfeldt Kvinnokliniken Susanne Malander SOK gyn-sektionen Skånes Universitetssjukhus (SUS) Lund Vad vi skall tala om idag Cervix Ovariet Epiteliala tumörer Germinalcellstumörer
Gynekologisk cancer Incidens, diagnostik, behandling och resultat
 Gynekologisk cancer Incidens, diagnostik, behandling och resultat T11-förel reläsning 27 Januari 2009 Preben Kjølhede Docent, överläkare Kvinnokliniken Universitetssjukhuset Linköping Innehåll Allmänt
Gynekologisk cancer Incidens, diagnostik, behandling och resultat T11-förel reläsning 27 Januari 2009 Preben Kjølhede Docent, överläkare Kvinnokliniken Universitetssjukhuset Linköping Innehåll Allmänt
Cervixcancer. Henrik Falconer, docent 2016
 Cervixcancer Henrik Falconer, docent 2016 Cervixcancer i världen Fjärde vanligaste kvinnliga cancern i världen Femte dödligaste cancern Ca 470000 fall 2008, 250000 dödsfall Globalt Sverige 1. Bröst 1.
Cervixcancer Henrik Falconer, docent 2016 Cervixcancer i världen Fjärde vanligaste kvinnliga cancern i världen Femte dödligaste cancern Ca 470000 fall 2008, 250000 dödsfall Globalt Sverige 1. Bröst 1.
Onkologisk behandling av Cervixcancer
 Onkologisk behandling av Cervixcancer Föreläsning ST-kurs 2017-10-03 Catharina Beskow Överläkare, Onkologiska kliniken Karolinska Universitetssjukhuset, Solna Utredning Välgrundad misstanke eller histologisk
Onkologisk behandling av Cervixcancer Föreläsning ST-kurs 2017-10-03 Catharina Beskow Överläkare, Onkologiska kliniken Karolinska Universitetssjukhuset, Solna Utredning Välgrundad misstanke eller histologisk
Riskfaktorer för lymfkörtelmetastaser (LNM) hos kvinnor med endometriecancer: en populationsbaserad nationell registerstudie.
 Riskfaktorer för lymfkörtelmetastaser () hos kvinnor med endometriecancer: en populationsbaserad nationell registerstudie. Stålberg K, Falconer H, Bjurberg M, Borgfeldt C, Dahm-Kähler P, Holmberg E, Kjølhede
Riskfaktorer för lymfkörtelmetastaser () hos kvinnor med endometriecancer: en populationsbaserad nationell registerstudie. Stålberg K, Falconer H, Bjurberg M, Borgfeldt C, Dahm-Kähler P, Holmberg E, Kjølhede
Ovarialcancer REGIONALT VÅRDPROGRAM FÖR EPITELIAL OVARIALCANCER, TUBAR- OCH PERITONEALCACNER GÄLLANDE FÖR SYDÖSTRA SJUKVÅRDSREGIONEN
 Ovarialcancer REGIONALT VÅRDPROGRAM FÖR EPITELIAL OVARIALCANCER, TUBAR- OCH PERITONEALCACNER GÄLLANDE FÖR SYDÖSTRA SJUKVÅRDSREGIONEN Giltighetstid 2013-06-01 2014-12-31 Regionala arbetsgruppen för Gynekologisk
Ovarialcancer REGIONALT VÅRDPROGRAM FÖR EPITELIAL OVARIALCANCER, TUBAR- OCH PERITONEALCACNER GÄLLANDE FÖR SYDÖSTRA SJUKVÅRDSREGIONEN Giltighetstid 2013-06-01 2014-12-31 Regionala arbetsgruppen för Gynekologisk
Corpuscancer ca 83% Cervixcancer ca 68% Ovarialcancer ca 42 % Corpuscancer ca Ovarialcancer ca 785. Cervixcancer ca 439
 Corpuscancer ca 1325 Ovarialcancer ca 785 Borderline 222 Cervixcancer ca 439 Vulvacancer ca 129 Vaginalcancer ca 40 Äggledarcancer (tubar) ca 42 Corpuscancer ca 83% Cervixcancer ca 68% Ovarialcancer ca
Corpuscancer ca 1325 Ovarialcancer ca 785 Borderline 222 Cervixcancer ca 439 Vulvacancer ca 129 Vaginalcancer ca 40 Äggledarcancer (tubar) ca 42 Corpuscancer ca 83% Cervixcancer ca 68% Ovarialcancer ca
Endometriecancer och Uterussarkom. Regional tillämpning av nationellt vårdprogram
 Endometriecancer och Uterussarkom Regional tillämpning av nationellt vårdprogram Januari 2014 Regionalt Cancercentrum Uppsala Örebro (RCC) Publiceras endast på RCC:s hemsida www.rccuppsalaorebro.se Regionalt
Endometriecancer och Uterussarkom Regional tillämpning av nationellt vårdprogram Januari 2014 Regionalt Cancercentrum Uppsala Örebro (RCC) Publiceras endast på RCC:s hemsida www.rccuppsalaorebro.se Regionalt
Modern Gynekologisk Ovarialcancer behandling
 Modern Gynekologisk Ovarialcancer behandling Pernilla Dahm Kähler Överläkare, Med Dr. Sektionschef Gynekologisk Tumörkirurgi Regional Processägare Ovarialcancer / Medlem Nationell Ovarialcancer VP Sahlgrenska
Modern Gynekologisk Ovarialcancer behandling Pernilla Dahm Kähler Överläkare, Med Dr. Sektionschef Gynekologisk Tumörkirurgi Regional Processägare Ovarialcancer / Medlem Nationell Ovarialcancer VP Sahlgrenska
Endometriecancer. Regional medicinsk riktlinje. Huvudbudskap. Utredning
 Regional medicinsk riktlinje Endometriecancer (kommer att) Fastställas av Hälso- och sjukvårdsdirektören (diarienr) giltigt till (2 år efter fastställandedatum) Utarbetad av vårdprocessgruppen för endometriecancer
Regional medicinsk riktlinje Endometriecancer (kommer att) Fastställas av Hälso- och sjukvårdsdirektören (diarienr) giltigt till (2 år efter fastställandedatum) Utarbetad av vårdprocessgruppen för endometriecancer
Lathund för handläggning av malignt melanom/dysplastisk naevus i Uppsala-Örebroregionen reviderad
 Lathund för handläggning av malignt melanom/dysplastisk naevus i Uppsala-Örebroregionen 2016-05-19 reviderad 2018-09-04 En pigmenterad förändring excideras med 2 mm klinisk marginal ned till ytliga subcutis
Lathund för handläggning av malignt melanom/dysplastisk naevus i Uppsala-Örebroregionen 2016-05-19 reviderad 2018-09-04 En pigmenterad förändring excideras med 2 mm klinisk marginal ned till ytliga subcutis
Epitelial ovarialcancer. Elisabet Hjerpe Överläkaregynekologisk onkologi Radiumhemmet
 Epitelial ovarialcancer Elisabet Hjerpe Överläkaregynekologisk onkologi Radiumhemmet Disposition 1 Epitelial ovarialcancer subtyper 2 Prognostiska faktorer 3 Icke- kirurgisk primärbehandling 4 Recidiv
Epitelial ovarialcancer Elisabet Hjerpe Överläkaregynekologisk onkologi Radiumhemmet Disposition 1 Epitelial ovarialcancer subtyper 2 Prognostiska faktorer 3 Icke- kirurgisk primärbehandling 4 Recidiv
TNM-klassifikation och stadieindelning
 1.1.1. TNM-klassifikation och stadieindelning Grunden för en stadieindelning är den histopatologiska undersökningen av primärtumören samt klinisk undersökning och vid behov ytterligare undersökningar.
1.1.1. TNM-klassifikation och stadieindelning Grunden för en stadieindelning är den histopatologiska undersökningen av primärtumören samt klinisk undersökning och vid behov ytterligare undersökningar.
Publicerat för enhet: Öron- Näsa- Hals- och Käkkirurgisk klinik gemensamt Version: 6
 Publicerat för enhet: Öron- Näsa- Hals- och Käkkirurgisk klinik gemensamt Version: 6 Innehållsansvarig: Aleksandar Pecanac, Specialistläkare, Öron- Näsa- Hals- och Käkkirurgisk klinik läkare (alepe1) Giltig
Publicerat för enhet: Öron- Näsa- Hals- och Käkkirurgisk klinik gemensamt Version: 6 Innehållsansvarig: Aleksandar Pecanac, Specialistläkare, Öron- Näsa- Hals- och Käkkirurgisk klinik läkare (alepe1) Giltig
VULVAKURSEN Noor, Knivsta. Cancer i vulva. Överläkare Olle Frankman (em) Konsult vid Ålands Centralsjukhus och Octaviakliniken
 VULVAKURSEN Noor, Knivsta. Cancer i vulva. Överläkare Olle Frankman (em) Konsult vid Ålands Centralsjukhus och Octaviakliniken Vulvacancer, historik. Stockholmsmetoden:elkoagulation från 1920 fram till
VULVAKURSEN Noor, Knivsta. Cancer i vulva. Överläkare Olle Frankman (em) Konsult vid Ålands Centralsjukhus och Octaviakliniken Vulvacancer, historik. Stockholmsmetoden:elkoagulation från 1920 fram till
Tumörmorfologiska grundbegrepp. Annika Dejmek T5 HT05
 Tumörmorfologiska grundbegrepp Annika Dejmek T5 HT05 Vad är en tumör? Tumor= eg. svullnad Neoplasi, neoplasm = äkta tumör Oncos - grekiska för tumör. Onkogen, onkologi, etc Terminologi - grundbegrepp -
Tumörmorfologiska grundbegrepp Annika Dejmek T5 HT05 Vad är en tumör? Tumor= eg. svullnad Neoplasi, neoplasm = äkta tumör Oncos - grekiska för tumör. Onkogen, onkologi, etc Terminologi - grundbegrepp -
Endometriecancer. Kristina Hellman, Onkologiska kliniken
 Endometriecancer Kristina Hellman, Onkologiska kliniken Onkologisk behandling Innehåll: Stadieindelning Postoperativa riskfaktorer Onkologisk behandling Biverkningar Uppföljning Recidiv Överlevnad Onkologisk
Endometriecancer Kristina Hellman, Onkologiska kliniken Onkologisk behandling Innehåll: Stadieindelning Postoperativa riskfaktorer Onkologisk behandling Biverkningar Uppföljning Recidiv Överlevnad Onkologisk
Gynekologisk Cancer: cervix
 Gynekologisk Cancer: cervix Susanne Malander VO onkologi och strålningsfysik gyn-sektionen Christer Borgfeldt Kvinnokliniken Skånes Universitetssjukhus (SUS) Lund Team work Diagnostik Kirurgi Radioterapi
Gynekologisk Cancer: cervix Susanne Malander VO onkologi och strålningsfysik gyn-sektionen Christer Borgfeldt Kvinnokliniken Skånes Universitetssjukhus (SUS) Lund Team work Diagnostik Kirurgi Radioterapi
Peniscancer- ovanligt
 Peniscancer- ovanligt 100 män per år får diagnosen invasiv peniscancer i Sverige. (+40 fall av carcinoma in situ). Över 9000 män får diagnosen prostatacancer. 21 män avlider i snitt varje år av peniscancer.
Peniscancer- ovanligt 100 män per år får diagnosen invasiv peniscancer i Sverige. (+40 fall av carcinoma in situ). Över 9000 män får diagnosen prostatacancer. 21 män avlider i snitt varje år av peniscancer.
ÄGGSTOCKSCANCER FAKTABLAD. Vad är äggstockscancer (ovarialcancer)?
 ÄGGSTOCKSCANCER FAKTABLAD Vad är äggstockscancer (ovarialcancer)? ENGAGe ger ut en serie faktablad för att öka medvetenheten om gynekologisk cancer och stödja sitt nätverk på gräsrotsnivå. Äggstockscancer
ÄGGSTOCKSCANCER FAKTABLAD Vad är äggstockscancer (ovarialcancer)? ENGAGe ger ut en serie faktablad för att öka medvetenheten om gynekologisk cancer och stödja sitt nätverk på gräsrotsnivå. Äggstockscancer
Icke epitelial ovarialcancer. Elisabet Hjerpe Sektionen för gynekologisk onkologi och bröstcancer Radiumhemmet
 Icke epitelial ovarialcancer Sektionen för gynekologisk onkologi och bröstcancer Radiumhemmet Disposition YST Epidemiologi Germinalcellstumörer GST Maligna könssträng- stromatumörer Ovanligare tumörer
Icke epitelial ovarialcancer Sektionen för gynekologisk onkologi och bröstcancer Radiumhemmet Disposition YST Epidemiologi Germinalcellstumörer GST Maligna könssträng- stromatumörer Ovanligare tumörer
UROGENITALA TUMÖRER. Nationellt vårdprogram Cancer i urinblåsa, njurbäcken, urinledare och urinrör maj 2013. Magdalena Cwikiel Lund VT 2015
 UROGENITALA TUMÖRER Nationellt vårdprogram Cancer i urinblåsa, njurbäcken, urinledare och urinrör maj 2013 Magdalena Cwikiel Lund VT 2015 Blåscancer Incidens Män 30/ 100 000 Kvinnor 10/100 000 Utgör sammanlagt
UROGENITALA TUMÖRER Nationellt vårdprogram Cancer i urinblåsa, njurbäcken, urinledare och urinrör maj 2013 Magdalena Cwikiel Lund VT 2015 Blåscancer Incidens Män 30/ 100 000 Kvinnor 10/100 000 Utgör sammanlagt
PET/CT och lungcancer. Bengt Bergman Lungmedicin Sahlgrenska Universitetssjukhuset
 PET/CT och lungcancer Bengt Bergman Lungmedicin Sahlgrenska Universitetssjukhuset Lungcancerincidens Sverige 1970-2012 Nya fall och mortalitet per 100 000 Trend 10 år: -1,4 %/år (M) +1,2 %/år (K) Källa:
PET/CT och lungcancer Bengt Bergman Lungmedicin Sahlgrenska Universitetssjukhuset Lungcancerincidens Sverige 1970-2012 Nya fall och mortalitet per 100 000 Trend 10 år: -1,4 %/år (M) +1,2 %/år (K) Källa:
VÅRDPROGRAM FÖR CANCER CORPORIS UTERI. Örebro/Uppsalaregionen
 VÅRDPROGRAM FÖR CANCER CORPORIS UTERI 1994 Örebro/Uppsalaregionen Innehållsförteckning Arbetsgruppen...3 I Bakgrund...4 Målsättning... 4 Epidemiologi... 4 Etiologi... 4 Prognos... 4 II Symptom och diagnostik...6
VÅRDPROGRAM FÖR CANCER CORPORIS UTERI 1994 Örebro/Uppsalaregionen Innehållsförteckning Arbetsgruppen...3 I Bakgrund...4 Målsättning... 4 Epidemiologi... 4 Etiologi... 4 Prognos... 4 II Symptom och diagnostik...6
Studiedagar 2007 Riksföreningen för Klinisk Cytologi - Åhus Strand
 Studiedagar 2007 Riksföreningen för Klinisk Cytologi - Åhus Strand Fallbeskrivningar 1-10 Kristianstad Sammanställt av Anneli Leksell Fall 1 Kvinna född 1975 VS 2004-maj Hälsoundersökning 8:e cykeldagen
Studiedagar 2007 Riksföreningen för Klinisk Cytologi - Åhus Strand Fallbeskrivningar 1-10 Kristianstad Sammanställt av Anneli Leksell Fall 1 Kvinna född 1975 VS 2004-maj Hälsoundersökning 8:e cykeldagen
Ortopedisk onkologi. cancer 50 000 metastaser 25 000. skelettmetastaser 10 000. skelettsarkom 60 mjukdelssarkom 150
 Ortopedisk onkologi cancer 50 000 metastaser 25 000 skelettmetastaser 10 000 skelettsarkom 60 mjukdelssarkom 150 57-årig frisk sjukvårdsbiträde 2 månaders anamnes på belastningssmärta vänster lår. finnålspunktion
Ortopedisk onkologi cancer 50 000 metastaser 25 000 skelettmetastaser 10 000 skelettsarkom 60 mjukdelssarkom 150 57-årig frisk sjukvårdsbiträde 2 månaders anamnes på belastningssmärta vänster lår. finnålspunktion
Nationellt vårdprogram för äggstockscancer
 Nationellt vårdprogram för äggstockscancer Presentation av huvuddragen SFOG-veckan Kristianstad 2012 Redaktionskommitten: Elisabeth Åvall Lundqvist Angelique Flöter Rådestad Bengt Tholander Bakgrund alla
Nationellt vårdprogram för äggstockscancer Presentation av huvuddragen SFOG-veckan Kristianstad 2012 Redaktionskommitten: Elisabeth Åvall Lundqvist Angelique Flöter Rådestad Bengt Tholander Bakgrund alla
TNM och lungcancer Vad tillför PET-CT? Cecilia Wassberg Överläkare, Bild och funktionsmedicin Akademiska Sjukhuset, Uppsala
 TNM och lungcancer Vad tillför PET-CT? Cecilia Wassberg Överläkare, Bild och funktionsmedicin Akademiska Sjukhuset, Uppsala ANATOMI FUNKTION 18 F- FDG- upptag i cancerceller Blodkärl G Cancercell FDG G
TNM och lungcancer Vad tillför PET-CT? Cecilia Wassberg Överläkare, Bild och funktionsmedicin Akademiska Sjukhuset, Uppsala ANATOMI FUNKTION 18 F- FDG- upptag i cancerceller Blodkärl G Cancercell FDG G
Susanne Fridsten Bitr Överläkare Röntgenkliniken Karolinska Universitetssjukhuset, Solna
 Susanne Fridsten Bitr Överläkare Röntgenkliniken Karolinska Universitetssjukhuset, Solna Disposition MRT Cervix DT Corpus PET/DT Vulva/Vagina Ultraljud Ovarier 2 MRT Fördelar Nackdelar Ingen joniserande
Susanne Fridsten Bitr Överläkare Röntgenkliniken Karolinska Universitetssjukhuset, Solna Disposition MRT Cervix DT Corpus PET/DT Vulva/Vagina Ultraljud Ovarier 2 MRT Fördelar Nackdelar Ingen joniserande
Labprocess. kolorektala cancerpreparat. Patrick Joost Processansvarig nedre GI patologi. patologi, Patologi Labmedicin Skåne
 Labprocess kolorektala cancerpreparat Patrick Joost Processansvarig nedre GI patologi patologi, Patologi Labmedicin Skåne Kolorektal cancer Labprocess Kolorektal cancer 617 operationspreparat i Region
Labprocess kolorektala cancerpreparat Patrick Joost Processansvarig nedre GI patologi patologi, Patologi Labmedicin Skåne Kolorektal cancer Labprocess Kolorektal cancer 617 operationspreparat i Region
Kliniska indikationer: När används PET/CT resp SPECT/CT? Peter Gjertsson Klinisk Fysiologi Sahlgrenska Universitetssjukhuset
 Kliniska indikationer: När används PET/CT resp SPECT/CT? Peter Gjertsson Klinisk Fysiologi Sahlgrenska Universitetssjukhuset PET/CT Innehåll Vanligaste onkologiska indikationerna Inflammation och infektion
Kliniska indikationer: När används PET/CT resp SPECT/CT? Peter Gjertsson Klinisk Fysiologi Sahlgrenska Universitetssjukhuset PET/CT Innehåll Vanligaste onkologiska indikationerna Inflammation och infektion
TILL DIG MED HUDMELANOM
 TILL DIG MED HUDMELANOM Hudmelanom är en typ av hudcancer Hudmelanom, basalcellscancer och skivepitelcancer är tre olika typer av hudtumörer. Antalet fall har ökat på senare år och sjukdomarna är nu bland
TILL DIG MED HUDMELANOM Hudmelanom är en typ av hudcancer Hudmelanom, basalcellscancer och skivepitelcancer är tre olika typer av hudtumörer. Antalet fall har ökat på senare år och sjukdomarna är nu bland
ONKOLOGISK BEHANDLING AV PRIMÄRA HJÄRNTUMÖRER. Katja Werlenius Onkologkliniken, SU/Sahlgrenska Hjärntumördagarna 25 aug 2011
 ONKOLOGISK BEHANDLING AV PRIMÄRA HJÄRNTUMÖRER Katja Werlenius Onkologkliniken, SU/Sahlgrenska Hjärntumördagarna 25 aug 2011 Disposition Introduktion Strålbehandling Cytostatika Kortfattat om onkologisk
ONKOLOGISK BEHANDLING AV PRIMÄRA HJÄRNTUMÖRER Katja Werlenius Onkologkliniken, SU/Sahlgrenska Hjärntumördagarna 25 aug 2011 Disposition Introduktion Strålbehandling Cytostatika Kortfattat om onkologisk
Fakta om GIST (gastrointestinala stromacellstumörer) sjukdom och behandling
 Fakta om GIST (gastrointestinala stromacellstumörer) sjukdom och behandling GIST en ovanlig magtumör GIST (gastrointestinala stromacellstumörer) är en ovanlig form av cancer i mag-tarmkanalen. I Sverige
Fakta om GIST (gastrointestinala stromacellstumörer) sjukdom och behandling GIST en ovanlig magtumör GIST (gastrointestinala stromacellstumörer) är en ovanlig form av cancer i mag-tarmkanalen. I Sverige
Uppföljning efter ovarialcancer vilken evidens finns? Dags att ändra kurs mot mer individualiserad uppföljning? SFOG, Stockholm 2017
 Uppföljning efter ovarialcancer vilken evidens finns? Dags att ändra kurs mot mer individualiserad uppföljning? SFOG, Stockholm 2017 Angelique Flöter Rådestad Docent, Lektor, KBH, KI Överläkare gynekologisk
Uppföljning efter ovarialcancer vilken evidens finns? Dags att ändra kurs mot mer individualiserad uppföljning? SFOG, Stockholm 2017 Angelique Flöter Rådestad Docent, Lektor, KBH, KI Överläkare gynekologisk
Innehållsförteckning. Cancer corpus uteri
 Innehållsförteckning Inledning... 3 Epidemiologi... 4 Ärftlighet och endometriecancer... 8 Precancerösa tillstånd... 10 Endometriehyperplasi histopatologi... 10 Endometriehyperplasi klinik... 12 Behandling...
Innehållsförteckning Inledning... 3 Epidemiologi... 4 Ärftlighet och endometriecancer... 8 Precancerösa tillstånd... 10 Endometriehyperplasi histopatologi... 10 Endometriehyperplasi klinik... 12 Behandling...
Kolorektal cancer. Man ska inte ha blod i avföringen eller anemi utan att veta varför!
 Kolorektal cancer Man ska inte ha blod i avföringen eller anemi utan att veta varför! 6100 fall av CRC/år i Sverige 3:e vanligaste cancerformen Kolorektal cancer Colon - rectum (15 cm från anus) Biologiskt
Kolorektal cancer Man ska inte ha blod i avföringen eller anemi utan att veta varför! 6100 fall av CRC/år i Sverige 3:e vanligaste cancerformen Kolorektal cancer Colon - rectum (15 cm från anus) Biologiskt
Pancreascancer -onkologisk behandling
 Pancreascancer -onkologisk behandling 140307 Margareta Heby Skånes onkologiska klinik Tumörer i pancreas Duktal pancreascancer > 90% Distal choledochuscancer Periampullär cancer Duodenal cancer Lymfom
Pancreascancer -onkologisk behandling 140307 Margareta Heby Skånes onkologiska klinik Tumörer i pancreas Duktal pancreascancer > 90% Distal choledochuscancer Periampullär cancer Duodenal cancer Lymfom
Germinalcellstumörer. Cecilia Petersen Sek3onen för barnonkologi Karolinska Universitetssjukhuset
 Germinalcellstumörer Cecilia Petersen Sek3onen för barnonkologi Karolinska Universitetssjukhuset Bakgrund GCT = stor varia3on De flesta är benigna teratom 20% är maligna =3% av all barncancer Incidens
Germinalcellstumörer Cecilia Petersen Sek3onen för barnonkologi Karolinska Universitetssjukhuset Bakgrund GCT = stor varia3on De flesta är benigna teratom 20% är maligna =3% av all barncancer Incidens
Gynekologisk cancer. Validering av Corpus- och Ovarialkvalitetsregistren. Diagnosår: 2011 och 2013
 Gynekologisk cancer av Corpus- och Ovarialkvalitetsregistren Diagnosår: 2011 och 2013 Beställningsadress alt cancercentrum väst Västra Sjukvårdsregionen Sahlgrenska Universitetssjukhuset SE-413 45 GÖTEBORG
Gynekologisk cancer av Corpus- och Ovarialkvalitetsregistren Diagnosår: 2011 och 2013 Beställningsadress alt cancercentrum väst Västra Sjukvårdsregionen Sahlgrenska Universitetssjukhuset SE-413 45 GÖTEBORG
Regionala tillämpningar för södra regionen av nationellt vårdprogram för ovarialcancer
 Regionala tillämpningar för södra regionen av nationellt vårdprogram för ovarialcancer Oktober 2015 Versionshantering Datum Beskrivning av förändring 2015-10-23 Slutlig version Tillämpningarna är utarbetade
Regionala tillämpningar för södra regionen av nationellt vårdprogram för ovarialcancer Oktober 2015 Versionshantering Datum Beskrivning av förändring 2015-10-23 Slutlig version Tillämpningarna är utarbetade
Lungcancer. Behandlingsresultat. Inna Meltser
 Lungcancer Behandlingsresultat Inna Meltser Förekomst Ca 3000 nya fall av lungcancer i Sverige per år, eller 7,25% av alla nya cancerfall 60 % är män Medianålder kring 70 år
Lungcancer Behandlingsresultat Inna Meltser Förekomst Ca 3000 nya fall av lungcancer i Sverige per år, eller 7,25% av alla nya cancerfall 60 % är män Medianålder kring 70 år
Lungcancerregistret användandet av kvalitetsregister i det regionala processarbetet
 Lungcancerregistret användandet av kvalitetsregister i det regionala processarbetet Annelie Behndig Överläkare Lungsektionen NUS Processledare för lungcancer RCC-norr Varför QR? Nationella riktlinjer-2011
Lungcancerregistret användandet av kvalitetsregister i det regionala processarbetet Annelie Behndig Överläkare Lungsektionen NUS Processledare för lungcancer RCC-norr Varför QR? Nationella riktlinjer-2011
Äggstockscancer. Regional tillämpning för södra sjukvårdsregionen av nationellt vårdprogram. Version: Version 2.0
 Äggstockscancer Regional tillämpning för södra sjukvårdsregionen av nationellt vårdprogram Version: 2018-01-08 Version 2.0 Versionshantering Datum Beskrivning av förändring 2015-10-23 Version 1.0 2018-01-08
Äggstockscancer Regional tillämpning för södra sjukvårdsregionen av nationellt vårdprogram Version: 2018-01-08 Version 2.0 Versionshantering Datum Beskrivning av förändring 2015-10-23 Version 1.0 2018-01-08
Endometriecancer Nationellt vårdprogram
 Landstingens och regionernas nationella samverkansgrupp inom cancervården Endometriecancer Nationellt vårdprogram Remissrunda 1 Versionshantering Datum ÅÅÅÅ-MM-DD Beskrivning av förändring Slutlig version
Landstingens och regionernas nationella samverkansgrupp inom cancervården Endometriecancer Nationellt vårdprogram Remissrunda 1 Versionshantering Datum ÅÅÅÅ-MM-DD Beskrivning av förändring Slutlig version
Kolorektal cancer. Man ska inte ha blod i avföringen eller anemi utan att veta varför!
 Kolorektal cancer Man ska inte ha blod i avföringen eller anemi utan att veta varför! 6100 fall av CRC/år i Sverige 3:e vanligaste cancerformen Kolorektal cancer Colon - rectum (15 cm från anus) Biologiskt
Kolorektal cancer Man ska inte ha blod i avföringen eller anemi utan att veta varför! 6100 fall av CRC/år i Sverige 3:e vanligaste cancerformen Kolorektal cancer Colon - rectum (15 cm från anus) Biologiskt
Lungcancer, radon och rökning
 Lungcancer, radon och rökning Karin Lindberg ST-läkare Onkologi Karolinska Doktorand KI Radon Lungcancer Stadier Typ av lungcancer Behandling Radon och uppkomst av lungcancer Cellpåverkan Genetiska förändringar
Lungcancer, radon och rökning Karin Lindberg ST-läkare Onkologi Karolinska Doktorand KI Radon Lungcancer Stadier Typ av lungcancer Behandling Radon och uppkomst av lungcancer Cellpåverkan Genetiska förändringar
THYREOIDEAPATOLOGI EQUALIS UTSKICK 2010-34
 THYREOIDEAPATOLOGI EQUALIS UTSKICK 2010-34 1 58-årig kvinna som upptäckte knöl i mittlinjen på halsen motsvarande isthmus. Högersidig lobektomi medtagande isthmus. Såväl höger lob som isthmus innehöll
THYREOIDEAPATOLOGI EQUALIS UTSKICK 2010-34 1 58-årig kvinna som upptäckte knöl i mittlinjen på halsen motsvarande isthmus. Högersidig lobektomi medtagande isthmus. Såväl höger lob som isthmus innehöll
Förslag till Nationellt Vårdprogram Gestationella trofoblastsjukdomar (GTD) Version 1.0-2014-05-14
 Förslag till Nationellt Vårdprogram Gestationella trofoblastsjukdomar (GTD) Version 1.0-2014-05-14 INNEHÅLLSFÖRTECKNING 1 Sammanfattning 2 Inledning 3 Mål med vårdprogrammet 4 Epidemiologi 5 Naturalhistoria
Förslag till Nationellt Vårdprogram Gestationella trofoblastsjukdomar (GTD) Version 1.0-2014-05-14 INNEHÅLLSFÖRTECKNING 1 Sammanfattning 2 Inledning 3 Mål med vårdprogrammet 4 Epidemiologi 5 Naturalhistoria
Ovarialcancer. Pernilla Dahm Kähler. Överläkare, Med.Dr. Sektionschef Gynekologisk Tumörkirurgi Sahlgrenska Universitetssjukhuset
 Ovarialcancer Pernilla Dahm Kähler Överläkare, Med.Dr. Sektionschef Gynekologisk Tumörkirurgi Sahlgrenska Universitetssjukhuset Patientfall 62 år Tidigare frisk 2-para Appendektomerad Hypertoni 4 månader
Ovarialcancer Pernilla Dahm Kähler Överläkare, Med.Dr. Sektionschef Gynekologisk Tumörkirurgi Sahlgrenska Universitetssjukhuset Patientfall 62 år Tidigare frisk 2-para Appendektomerad Hypertoni 4 månader
Råd angående handläggning av pat med BASALCELLSCANCER - Hudkliniken
 Vårdprogram Diarienr: Ej tillämpligt 1(5) Dokument ID: 09-40582 Fastställandedatum: 2016-09-13 Upprättare: Susanne I Vandell Uddströmer Giltigt t.o.m.: 2017-09-13 Fastställare: Kent Åhlenius Råd angående
Vårdprogram Diarienr: Ej tillämpligt 1(5) Dokument ID: 09-40582 Fastställandedatum: 2016-09-13 Upprättare: Susanne I Vandell Uddströmer Giltigt t.o.m.: 2017-09-13 Fastställare: Kent Åhlenius Råd angående
SCK Ortopedi. Sarkom Centrum Karolinska
 SCK Ortopedi Sarkom Centrum Karolinska Uppdrag Diagnostisera och behandla mesenkymala tumörer i rörelseapparaten thoraxväggen även barnen! ffa. maligna mesenkymala tumörer = sarkom SCK Ortopedi organisation
SCK Ortopedi Sarkom Centrum Karolinska Uppdrag Diagnostisera och behandla mesenkymala tumörer i rörelseapparaten thoraxväggen även barnen! ffa. maligna mesenkymala tumörer = sarkom SCK Ortopedi organisation
Corpuscancer ca 85% Cervixcancer ca 70% Ovarialcancer ca 40 % Corpuscancer ca 1300. Ovarialcancer ca 800 Borderline 200. Cervixcancer ca 450
 Corpuscancer ca 1300 Ovarialcancer ca 800 Borderline 200 Cervixcancer ca 450 Vulvacancer ca 125 Vaginalcancer ca 40 Äggledarcancer (tubar) ca 40 Corpuscancer ca 85% Cervixcancer ca 70% Ovarialcancer ca
Corpuscancer ca 1300 Ovarialcancer ca 800 Borderline 200 Cervixcancer ca 450 Vulvacancer ca 125 Vaginalcancer ca 40 Äggledarcancer (tubar) ca 40 Corpuscancer ca 85% Cervixcancer ca 70% Ovarialcancer ca
Äldre kvinnor och bröstcancer
 Äldre kvinnor och bröstcancer Det finns 674 000 kvinnor som är 70 år eller äldre i Sverige. Varje år får runt 2 330 kvinnor över 70 år diagnosen bröstcancer, det är 45 kvinnor i veckan. De får sin bröstcancer
Äldre kvinnor och bröstcancer Det finns 674 000 kvinnor som är 70 år eller äldre i Sverige. Varje år får runt 2 330 kvinnor över 70 år diagnosen bröstcancer, det är 45 kvinnor i veckan. De får sin bröstcancer
Livmoderhalscancer Regional nulägesbeskrivning VGR Standardiserat vårdförlopp
 Ett samarbete i Västra sjukvårdsregionen Livmoderhalscancer Regional nulägesbeskrivning VGR Standardiserat vårdförlopp Processägare Karin Bergmark och Pär Hellberg Februari 2017 Innehållsförteckning 1.
Ett samarbete i Västra sjukvårdsregionen Livmoderhalscancer Regional nulägesbeskrivning VGR Standardiserat vårdförlopp Processägare Karin Bergmark och Pär Hellberg Februari 2017 Innehållsförteckning 1.
Vulva patologi, forts. Anna Måsbäck ST-kurs VT 2014
 Vulva patologi, forts Anna Måsbäck ST-kurs VT 2014 Talg- och svettkörtlar, keratinisering Vulva Hud Vulva slemhinna ej keratiniserad Apokrina körtlar Histologi Urotel i urethra Labia majora (hud) fett
Vulva patologi, forts Anna Måsbäck ST-kurs VT 2014 Talg- och svettkörtlar, keratinisering Vulva Hud Vulva slemhinna ej keratiniserad Apokrina körtlar Histologi Urotel i urethra Labia majora (hud) fett
Endometrios. Ann-Kristin Örnö MD, PhD Department of Obstetrics and Gynecology, Clinical Sciences, Lund University, Lund, Sweden
 Endometrios Ann-Kristin Örnö MD, PhD Department of Obstetrics and Gynecology, Clinical Sciences, Lund University, Lund, Sweden Endometrium utanför uterus. Lokalisation; främst i lilla bäckenet nära uterus
Endometrios Ann-Kristin Örnö MD, PhD Department of Obstetrics and Gynecology, Clinical Sciences, Lund University, Lund, Sweden Endometrium utanför uterus. Lokalisation; främst i lilla bäckenet nära uterus
DUGGA 1. i patologi. för medicine studenter 18/3 2005
 KAROLINSKA INSTITUTET Institutionen för laboratoriemedicin Avdelningen för patologi DUGGA 1 i patologi för medicine studenter 18/3 2005 Totalt 50 poäng (minst 32 för G) Personnummer: Resultat: Stud. sign.
KAROLINSKA INSTITUTET Institutionen för laboratoriemedicin Avdelningen för patologi DUGGA 1 i patologi för medicine studenter 18/3 2005 Totalt 50 poäng (minst 32 för G) Personnummer: Resultat: Stud. sign.
Njurtumörer hos barn
 Njurtumörer hos barn De flesta är Wilms (men inte alla) Anna Nyström Röntgen Drottning Silvias Barn- och Ungdomssjukhus Sahlgrenska Universitetssjukhuset Göteborg Rtg pulm: Gosse född i v 35+5, FV 3195g.
Njurtumörer hos barn De flesta är Wilms (men inte alla) Anna Nyström Röntgen Drottning Silvias Barn- och Ungdomssjukhus Sahlgrenska Universitetssjukhuset Göteborg Rtg pulm: Gosse född i v 35+5, FV 3195g.
Rekommendationer för tidig upptäckt av gynekologisk cancer.
 Rekommendationer för tidig upptäckt av gynekologisk cancer. Enligt nationella cancerstrategin och regionala cancerplanen är det vårdprogramgruppernas uppgift att ta fram information till remitterande och
Rekommendationer för tidig upptäckt av gynekologisk cancer. Enligt nationella cancerstrategin och regionala cancerplanen är det vårdprogramgruppernas uppgift att ta fram information till remitterande och
Gunvald Larsson, 72 år
 Gunvald Larsson, 72 år Gunvald Larsson, 72 år, söker på hälsocentralen pga. vattenkastningsbesvär. Vid rektalpalpation känner läkaren ett fastare område till vänster i prostatan. P-PSA 15 (
Gunvald Larsson, 72 år Gunvald Larsson, 72 år, söker på hälsocentralen pga. vattenkastningsbesvär. Vid rektalpalpation känner läkaren ett fastare område till vänster i prostatan. P-PSA 15 (
Överblick. Punktion/dränage När? Invasiva ingrepp. Mellanålsbiopsi: Förberedelser utförande. Mellanålsbiopsi - ultraljudsledd 2016-01-24
 Ultraljud vid utredning av gynekologiska tumörer & invasiv diagnostik/terapi Elisabeth Epstein, Doc, Öl Karolinska Solna Stockholm, Sweden Överblick Invasiva ingrepp: Dränage abcess, cystpunktion, mellanålsbiopsi
Ultraljud vid utredning av gynekologiska tumörer & invasiv diagnostik/terapi Elisabeth Epstein, Doc, Öl Karolinska Solna Stockholm, Sweden Överblick Invasiva ingrepp: Dränage abcess, cystpunktion, mellanålsbiopsi
Nationellt Vårdprogram för Endometriecancer. Svenska Nationella Vårdprogramgruppen för Endometriecancer
 Nationellt Vårdprogram för Endometriecancer Svenska Nationella Vårdprogramgruppen för Endometriecancer Revision är planerad senast våren 2014 1 Regionalt cancercentrum väst Västra Sjukvårdsregionen Sahlgrenska
Nationellt Vårdprogram för Endometriecancer Svenska Nationella Vårdprogramgruppen för Endometriecancer Revision är planerad senast våren 2014 1 Regionalt cancercentrum väst Västra Sjukvårdsregionen Sahlgrenska
Del 8. Totalpoäng: 10p.
 Totalpoäng: 10p. En 66-årig kvinna söker på distriktsläkarmottagningen för problem med magen. Senaste tiden känt sig allmänt sjuk, periodvis illamående, tappat aptiten och fått problem med oregelbunden
Totalpoäng: 10p. En 66-årig kvinna söker på distriktsläkarmottagningen för problem med magen. Senaste tiden känt sig allmänt sjuk, periodvis illamående, tappat aptiten och fått problem med oregelbunden
F-FDG PET-CT i klinik. Cecilia Wassberg Överläkare, Bild och funktionsmedicin Akademiska Sjukhuset, Uppsala
 18 F-FDG PET-CT i klinik Cecilia Wassberg Överläkare, Bild och funktionsmedicin Akademiska Sjukhuset, Uppsala ANATOMI FUNKTION Positronannihila+on Positron 511 kev foton + 511 kev foton - - Elektron Coincidence
18 F-FDG PET-CT i klinik Cecilia Wassberg Överläkare, Bild och funktionsmedicin Akademiska Sjukhuset, Uppsala ANATOMI FUNKTION Positronannihila+on Positron 511 kev foton + 511 kev foton - - Elektron Coincidence
Hur vanligt är det med prostatacancer?
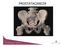 PROSTATACANCER Hur vanligt är det med prostatacancer? Ålder Cancer 20 30 30 40 40 50 50 60 70 80 2% 29% 32% 55% 64% Sakr et al. In Vivo 1994; 8: 439-43. Prostatacancer i Sverige Nya fall 9263 1 nytt fall
PROSTATACANCER Hur vanligt är det med prostatacancer? Ålder Cancer 20 30 30 40 40 50 50 60 70 80 2% 29% 32% 55% 64% Sakr et al. In Vivo 1994; 8: 439-43. Prostatacancer i Sverige Nya fall 9263 1 nytt fall
Vinster med ett palliativt förhållningssätt tidigt
 Vinster med ett palliativt förhållningssätt tidigt Bertil Axelsson Lungcancervård Shin J, Temel J. Integrating palliative care: When and how? Curr Opin Pulm Med 2013, 19:344 349 Upprepad genomgång av Smärtor
Vinster med ett palliativt förhållningssätt tidigt Bertil Axelsson Lungcancervård Shin J, Temel J. Integrating palliative care: When and how? Curr Opin Pulm Med 2013, 19:344 349 Upprepad genomgång av Smärtor
Mjukdelssarkom. Solida tumörsjukdomar hos barn och ungdomar april 2015 i Strängnäs
 Mjukdelssarkom Solida tumörsjukdomar hos barn och ungdomar 15-17 april 2015 i Strängnäs Gustaf Ljungman, doc, öl, barnonkolog gustaf.ljungman@kbh.uu.se Mjukdelssarkom Heterogen grupp 1/100 000 7% av all
Mjukdelssarkom Solida tumörsjukdomar hos barn och ungdomar 15-17 april 2015 i Strängnäs Gustaf Ljungman, doc, öl, barnonkolog gustaf.ljungman@kbh.uu.se Mjukdelssarkom Heterogen grupp 1/100 000 7% av all
Diagnos Kvalitetsregisterblankett Vanlig canceranmälan AML/AUL/ALL Nyupptäckta fall för patienter 16 år och äldre. Nyupptäckt primär PADverifierad
 Regelverk för anmälan via kvalitetsregisterblanketten eller via cancer anmälningsblanketten Anmälan om tumörer och tumörliknande tillstånd från klinisk verksamhet Nedanstående tabell anger inklusionskriterier
Regelverk för anmälan via kvalitetsregisterblanketten eller via cancer anmälningsblanketten Anmälan om tumörer och tumörliknande tillstånd från klinisk verksamhet Nedanstående tabell anger inklusionskriterier
Neuroendokrina buktumörer, inkl binjurecancer Regional nulägesbeskrivning VGR Standardiserat vårdförlopp
 Ett samarbete i Västra sjukvårdsregionen Neuroendokrina buktumörer, inkl binjurecancer Regional nulägesbeskrivning VGR Standardiserat vårdförlopp Processägare Viktor Johanson Januari 2018 Innehållsförteckning
Ett samarbete i Västra sjukvårdsregionen Neuroendokrina buktumörer, inkl binjurecancer Regional nulägesbeskrivning VGR Standardiserat vårdförlopp Processägare Viktor Johanson Januari 2018 Innehållsförteckning
Sarkom. Mjukdelssarkom
 2010SarkomMikaelE Sarkom Sarkom (av grekiskans sarx = kött, oma = svulst) är samlingsnamnet för maligna tumörer utgångna från skelett eller mjukdelar (fettväv, muskler, bindväv, nerver, kärl etc). Trots
2010SarkomMikaelE Sarkom Sarkom (av grekiskans sarx = kött, oma = svulst) är samlingsnamnet för maligna tumörer utgångna från skelett eller mjukdelar (fettväv, muskler, bindväv, nerver, kärl etc). Trots
Patologi en översikt VSTB. Strängnäs 2015 Bengt Sandstedt
 Patologi en översikt VSTB Strängnäs 2015 Bengt Sandstedt Patologi-ett ämne med foten kvar i 1800 talet Fortfarande gäller för 90%av diagnostiken: Ljusmikroskopi med bedömning av vävnadssnitt eller celler
Patologi en översikt VSTB Strängnäs 2015 Bengt Sandstedt Patologi-ett ämne med foten kvar i 1800 talet Fortfarande gäller för 90%av diagnostiken: Ljusmikroskopi med bedömning av vävnadssnitt eller celler
1.1 Ange tre möjliga differentialdiagnoser förutom bröstcancer. (1,5p)
 Du arbetar som underläkarvikarie på kirurgkliniken i Y-köping. Du träffar en 63-årig kvinna på mottagningen som känt en knöl i vänster bröst sedan ett par veckor. Hon är frisk i övrigt och tar inga mediciner.
Du arbetar som underläkarvikarie på kirurgkliniken i Y-köping. Du träffar en 63-årig kvinna på mottagningen som känt en knöl i vänster bröst sedan ett par veckor. Hon är frisk i övrigt och tar inga mediciner.
BRÖSTPATOLOGI FIBROADENOM I BRÖSTKÖRTELN
 BRÖSTPATOLOGI DSM054 (11i) FIBROADENOM I BRÖSTKÖRTELN Klinisk bakgrund: 25-årig kvinna, O-grav, O-para, äter p-piller. Upptäckte knöl i vänster bröst för fyra månader sedan som successivt vuxit. Mammografi
BRÖSTPATOLOGI DSM054 (11i) FIBROADENOM I BRÖSTKÖRTELN Klinisk bakgrund: 25-årig kvinna, O-grav, O-para, äter p-piller. Upptäckte knöl i vänster bröst för fyra månader sedan som successivt vuxit. Mammografi
KURSPLAN. Prevention, diagnostik samt behandling av livmoderhalscancer -från virusinfektion till allvarlig sjukdom med multimodel behandlingsstrategi
 080303 KURSPLAN Prevention, diagnostik samt behandling av livmoderhalscancer -från virusinfektion till allvarlig sjukdom med multimodel behandlingsstrategi Kursledare: Päivi Kannisto, docent, överläkare,
080303 KURSPLAN Prevention, diagnostik samt behandling av livmoderhalscancer -från virusinfektion till allvarlig sjukdom med multimodel behandlingsstrategi Kursledare: Päivi Kannisto, docent, överläkare,
VÅRDPROGRAM 2003 ENDOMETRIECANCER OCH UTERUSSARKOM. Diagnostik, behandling och uppföljning i Stockholm-Gotlandregionen ONKOLOGISKT CENTRUM STOCKHOLM
 VÅRDPROGRAM 2003 ENDOMETRIECANCER OCH UTERUSSARKOM Diagnostik, behandling och uppföljning i Stockholm-Gotlandregionen ONKOLOGISKT CENTRUM STOCKHOLM GOTLAND Beställningsadress Onkologiskt Centrum, M8:01
VÅRDPROGRAM 2003 ENDOMETRIECANCER OCH UTERUSSARKOM Diagnostik, behandling och uppföljning i Stockholm-Gotlandregionen ONKOLOGISKT CENTRUM STOCKHOLM GOTLAND Beställningsadress Onkologiskt Centrum, M8:01
Del 5_14 sidor_26 poäng
 _14 sidor_26 poäng En 35-årig kvinna söker akut pga hög feber sedan ett dygn tillbaka. Hon mår egentligen inte dåligt och har kunnat äta hela tiden. Har dock fått mera ont till vänster i buken nertill.
_14 sidor_26 poäng En 35-årig kvinna söker akut pga hög feber sedan ett dygn tillbaka. Hon mår egentligen inte dåligt och har kunnat äta hela tiden. Har dock fått mera ont till vänster i buken nertill.
NATIONELLT KVALITETSREGISTER FÖR KOLOREKTAL CANCER MANUAL FÖR UPPFÖLJNING
 NATIONELLT KVALITETSREGISTER FÖR KOLOREKTAL CANCER MANUAL FÖR UPPFÖLJNING (diagnostiserade alla år) Kriterier för uppföljningsinrapportering Riktlinjer för uppföljning Kvalitetsregistret för kolorektal
NATIONELLT KVALITETSREGISTER FÖR KOLOREKTAL CANCER MANUAL FÖR UPPFÖLJNING (diagnostiserade alla år) Kriterier för uppföljningsinrapportering Riktlinjer för uppföljning Kvalitetsregistret för kolorektal
Vårdprogram för endometriecancer (corpuscancer) och uterussarkom
 Vårdprogram för endometriecancer (corpuscancer) och uterussarkom Södra- och Sydöstra sjukvårsdregionen 2010 Vårdprogrammets giltighetstid: 2010 01 01 2012 12 31 www.ocsyd.se ISBN 91-85738-86-7 (pdf) Onkologiskt
Vårdprogram för endometriecancer (corpuscancer) och uterussarkom Södra- och Sydöstra sjukvårsdregionen 2010 Vårdprogrammets giltighetstid: 2010 01 01 2012 12 31 www.ocsyd.se ISBN 91-85738-86-7 (pdf) Onkologiskt
Vem skall operera kvinnan med ovarialcancer?
 Vem skall operera kvinnan med ovarialcancer? Pernilla Dahm Kähler (presenterad av Dr. P. Kölhede) Med.Dr. överläkare Sektionschef gynekologisk tumörkirurgi kvinnosjukvården Sahlgrenska Universitetssjukhuset
Vem skall operera kvinnan med ovarialcancer? Pernilla Dahm Kähler (presenterad av Dr. P. Kölhede) Med.Dr. överläkare Sektionschef gynekologisk tumörkirurgi kvinnosjukvården Sahlgrenska Universitetssjukhuset
KVAST-dokument för epitelial tumörer i ovarium, tuba uterina, peritoneum och de uterina ligamenten.
 A Måsbäck för Patologernas GYN-KVAST-grupp, Ovarialcancer, 2015/05/11 Sidan 1 KVAST-dokument för epitelial tumörer i ovarium, tuba uterina, peritoneum och de uterina ligamenten. I. Innehållsförteckning
A Måsbäck för Patologernas GYN-KVAST-grupp, Ovarialcancer, 2015/05/11 Sidan 1 KVAST-dokument för epitelial tumörer i ovarium, tuba uterina, peritoneum och de uterina ligamenten. I. Innehållsförteckning
Tidig upptäckt. Marcela Ewing. Spec. allmänmedicin/onkologi Regional processägare Tidig upptäckt Regionalt cancercentrum väst
 Tidig upptäckt Marcela Ewing Spec. allmänmedicin/onkologi Regional processägare Tidig upptäckt Regionalt cancercentrum väst Disposition av föreläsning Bakgrund Alarmsymtom och allmänna symtom Svårigheten
Tidig upptäckt Marcela Ewing Spec. allmänmedicin/onkologi Regional processägare Tidig upptäckt Regionalt cancercentrum väst Disposition av föreläsning Bakgrund Alarmsymtom och allmänna symtom Svårigheten
Okänd primärtumör. Ny medicinsk riktlinje
 Ny medicinsk riktlinje Definition En heterogen sjukdomsgrupp med histopatologiskt bekräftad metastatisk cancer där en sannolik primärtumör inte påvisats efter basal utredning Regional medicinsk riktlinje
Ny medicinsk riktlinje Definition En heterogen sjukdomsgrupp med histopatologiskt bekräftad metastatisk cancer där en sannolik primärtumör inte påvisats efter basal utredning Regional medicinsk riktlinje
Tumörregistret Rapport december 2011 Registrering t.o.m. 2010-12-31
 NATIONELLA KVALITETSREGISTRET INOM Tumörregistret Rapport december 2011 Registrering t.o.m. 2010-12-31 Thomas Högberg, Registerhållare för tumörregistret Avd för Cancerepidemiologi Lunds Universitet Innehållsförteckning
NATIONELLA KVALITETSREGISTRET INOM Tumörregistret Rapport december 2011 Registrering t.o.m. 2010-12-31 Thomas Högberg, Registerhållare för tumörregistret Avd för Cancerepidemiologi Lunds Universitet Innehållsförteckning
Kirurgisk behandling vid kolorektal cancer. Marie-Louise Lydrup Kolorektalteamet SUS
 Kirurgisk behandling vid kolorektal cancer Marie-Louise Lydrup Kolorektalteamet SUS Incidens kolorektal cancer 5900 fall / år i Sverige ca1100 fall / år i Sö sjukvårdsreg 400 fall / år i Malmö Medelålder
Kirurgisk behandling vid kolorektal cancer Marie-Louise Lydrup Kolorektalteamet SUS Incidens kolorektal cancer 5900 fall / år i Sverige ca1100 fall / år i Sö sjukvårdsreg 400 fall / år i Malmö Medelålder
Strategier som kan bidra till att minska ovarialcancer. Henrik Falconer, docent Karolinska Universitetssjukhuset
 Strategier som kan bidra till att minska ovarialcancer Henrik Falconer, docent Karolinska Universitetssjukhuset VECKAN 2017 Det finns inga intressekonflikter eller jäv att redovisa. Kan man förebygga ovarialcancer?
Strategier som kan bidra till att minska ovarialcancer Henrik Falconer, docent Karolinska Universitetssjukhuset VECKAN 2017 Det finns inga intressekonflikter eller jäv att redovisa. Kan man förebygga ovarialcancer?
Program. Bilddiagnostik vid prostatacancer PSMA PET for staging and restaging of. Validering av Bone Scan Index Bone Scan Index med skelettscintigrafi
 Program Bilddiagnostik vid prostatacancer PSMA PET for staging and restaging of prostate cancer Monte-Carlo Validering av Bone Scan Index Bone Scan Index med skelettscintigrafi Bone Scan Index med PET-CT
Program Bilddiagnostik vid prostatacancer PSMA PET for staging and restaging of prostate cancer Monte-Carlo Validering av Bone Scan Index Bone Scan Index med skelettscintigrafi Bone Scan Index med PET-CT
VSTB, register, rapportering, resultat, epidemiologi
 VSTB, register, rapportering, resultat, epidemiologi Solida tumörsjukdomar hos barn och ungdomar 15-17 april 2015 i Strängnäs Gustaf Ljungman, doc, öl, barnonkolog gustaf.ljungman@kbh.uu.se Organisation
VSTB, register, rapportering, resultat, epidemiologi Solida tumörsjukdomar hos barn och ungdomar 15-17 april 2015 i Strängnäs Gustaf Ljungman, doc, öl, barnonkolog gustaf.ljungman@kbh.uu.se Organisation
