Övningskompendium i organisk kemi för KEMA01
|
|
|
- Amanda Ivarsson
- för 8 år sedan
- Visningar:
Transkript
1 Övningskompendium i organisk kemi för KEMA01 Lunds Universtet, 2013 I detta kompendium finner du lämpliga övningsuppgifter för kuresn KEAMA01. Flera av uppgifter kommer att lösas under de schemalagda övningstillfällena, men alla kommer inte att hinnas med. Det är utmärkt om du själv försöker lösa de uppgifter som inte gås igenom på övningarna, och du är varmt välkommen att diskutera dina lösningar med kursens lärare! 1
2 Övning 1: Allmänna begrepp, formelskrivning och molekylorbitaler 1. Vilken är skillnaden mellan ønsteds syra-bas-begrepp och Lewisdefinition? Ange vilka av följande föreningar som är syror respektive baser enligt den senare definitionen: aceton vatten dimetylsulfid aluminiumtriklorid 2. Markera den suraste protonen i var och en av följande föreningar och ordna dessa efter ökande aciditet. C 3 C 2 FC 2 C 2 ClC 2 C 2 3. Välj ett bensenderivat med molekylformeln C 6 6. a) Rita det som Lewisstruktur. b) Rita det som skelettstruktur. 4. Rita och namnge isomererna med summaformeln C Till vilken substansklass hör följande molekyler? a) b) c) d) e) f) g) h) Cl 6. Ange trivialbnamnet för följande föreningar: a) b) c) d) e) Me 2 7. Rita fullständiga Kekulé-strukturer (s. 7 i McMurry) för: a) 4-hydroxibutansyra b) -metylanilin c) EtCC(Me)C 2 Me d) 5-(3-nitrophenyl)-5-oxopentanoic acid 2
3 8. amge följande föreningar: a) b) c) 2 9. Vad händer, eller händer inget? Förklara hur du resonerar! 10. Den här frågan rör molekylorbitaler (M). a) Rita ett orbitalkorrelationsdiagram för e. b) Kan denna molekyl, som ju är en jon, tänkas existera i yttre rymden? Förklara! 11. Väteperoxid, 1, har elektrofila egenskaper och kan i vissa sammanhang också fungera som oxidationsmedel. (Faktum är att koncentrerad väteperoxid tillsammans med organiska föreningar innebär en stor explosionsrisk!) Dimetyleter, 2, däremot är varken en elektrofil eller ett oxidationsmedel. 3 C C a) Ange LUM i båda föreningarna. b) Rita upp korrelationsdiagram som inbegriper LUM för såväl väteperoxid som dimetyleter. Ange de atomorbitaler som huvudsakligen ingår i de linjärkombinationer som ger LUM. c) Ange varför LUM är lägre för väteperoxd än för dimetyleter. d) Visa förenklat hur LUM ser ut för väteperoxid. 3
4 Övning 2: Alkener och konformationer 1. amnge föreningarna nedan entydigt. a) b) c) d) Cl Cl 2. Vad bildas? 3. Skriv en reaktionsformel för syntes av isopropanol (2-propanol) från propen och vatten i starkt sur miljö. 4. Redogör för mekanismen för reaktionen ovan och konstruera ett reaktionsenergidiagram. Markera vad som är intermediärer, övergångstillstånd och aktiveringsenergier. Vilket är det hastighetsbestämmande steget? Vilken biprodukt skulle man gissa bildas vid denna syntes? 5. a) Rita en ewmanprojektion som visar den stabilaste konformationen av 1- propanol. b) Illustrera meb hjälp av en ewmanprojektion vad en gauche-interaktion är. 6. Rita nedanstående substituerade cyklohexan, med alla vätena utsatta, i den mest gynnsamma stolformen. 5. Ekvivalent mängd av 2-metyl-2-buten och (E)-2-buten får reagera med en ekvivalent. Vad blir huvudprodukten. 6. Vilka är huvudprodukterna i nedanstående reaktioner? Stereokemin skall tydligt framgå i svaren! a) b) (E)-2-buten (Z)-3-hexen 2? C 2 Cl 2 2? C 2 Cl 2 4
5 Övning 3: Stereokemi 1. Rita strukturen för den mest stabila konformationen av cis- respektive trans-1,3- dimetylcyklohexan. Använd gärna molekylmodeller. 2. Rita de båda enantiomererna av 2-brombutan. Ange vilken som har S- respektive R-konfiguration. 3. Vilka av följande föreningar är kirala? Markera alla stereogena atomer. Ph 2 C 2 2 C 2 C 2 C 2 4. Tamiflu är det beryktade läkemedlet mot bl. a. fågelinfluensa som såldes slut på apoteket när medierna varnade för kommande pandemier. Strukturen ser du nedan. Tamiflu framställs ur shikiminsyra som är en naturprodukt med begränsad tillgång. Markera alla stereogena atomer i tamiflu och ange hur många stereoisomerer den har. C CEt Shikiminsyra C 3 C Tamiflu 2 5. Följande frågor gäller ( )-mentol, en naturligt förekommande substans som kan isoleras från pepparmintolja. ( )-mentol a) Rita den mest gynnade stolkonformationen för ( )-mentol. b) Fastställ absolutkonfigurationen för alla stereocentra i ( )-mentol. c) Rita enantiomeren av ( )-mentol. d) Rita en diastereomer till ( )-mentol. 5
6 6. Molekylen nedan kan existera som fyra olika stereoisomerer. Rita upp dessa, ange absolutkonfigurationen, samt hur de förhåller sig till varandra. Cl 7. I uppgift 7, övn. 3, analyserades produktutfallet vid addition av 2 till (E)- och (Z)-buten. u skall du reda ut det stereokemiska förhållandet mellan föreningarna! a) Ange absotutkonfigurationen för alla stereocentra. b) Ange realtionen mellan de olika stereoisomererna? c) ur många stereoisomerer har bildats i de två reaktionerna? Varför? 6
7 Övning 4: S 2, S 1, E2 och E1 1. Vilka av substraten nedan skulle reagera enligt S 1, S 2 eller inte alls med nukleofilen u -? Vad kan u - vara för någonting? I Cl 3 C- 2. Redogör för mekanismen för reaktionen mellan (S)-2-fenyl-2-brombutan och etanol i varm etanol (solvolys). 3. Välj från nedanstående lista den eller de alkylhalogenider som stämmer med respektive kriterium. a) 1-bromhexan b) 3-brom-3-metylpentan c) 1-brom-2,2-dimetylbutan d) 3-brom-2-metylpentan e) 2-brom-3-metylpentan f) bromcyklohexan i) som är kiral ii) som finns som diastereomerer iii) som reagerar snabbast vid S 2-reaktion med natriummetoxid i metanol iv) som inte reagerar nämvärt med S 2-reaktion med natriummetoxid i metanol v) som endast ger en alken vid E2-eliminering vi) som ger E2-eliminering men inte S 2-substitution vid reaktion med natriummetoxid i metanol. vii) Som reagerar snabbast vid S 1-reaktionen. 4. Ange huvudprodukt i följande reaktioner. Mekanism krävs ej.? S? 2? [lösningsmedel]? 5. ur kan man framställa nedanstående molekyl med hjälp av en E2-eliminering. 7
8 6. Vad sker när förening 1 behandlas med etoxid? De båda bromsubstituenterna på cyklohexanringen ser ut att ha lika omgivning, men en är betydligt mer reaktiv än den andra i den här reaktionen.? 1 a) Visa med en tydlig mekanism vad som händer! b) Varför, enligt den mekanism du föreslagit, uppvisar bromsubstituenterna olika reaktivitet? c) ur skulle man experimentellt kunna bevisa att din mekanismen är korrekt? d) Är förening 1 eller produkten kiral? 7) Förklara varför den relativa hastigheten mellan 1-brombutan azidjon ökar med en faktor 2800 när lösningsmedlet byts från metanol till DMF. 3 produkt 8. Vad sker? Diskutera alla tänkbara möjligheter och redogör varför bara ett av utfallen förefaller rimligt. Vilken substansklass tillhör produkten? 2 produkt 9. Enkla ("förenlade") orbitalresonemang gör det oftare lättare att förstå ett i övrigt så deskriptivt ämne som organisk kemi. Den härfrågan tar up orbitalperspektiv på nukleofiler, och grundregeln är att ju högre M ligger för en nukleofil desto mer benägen är nukleofilen att reagera med en elektrofil. edan förekommer fem par (mer eller mindre goda) nukleofiler. Ange nu med beteckning (t ex sp3 C, sp2 etc) vilket orbotal som är homo i var och en av nukleofilerna och markera inom varje par den M som har högst energi. En kort motivering skall ingå i denna rangodning. a) b) S c) P d) e) 8
9 Övning 5: Aromatiska föreningar 1. Definiera begreppet aromaticitet. Vilka av följande föreningar är aromatiska? Förklara. B C 3 2. Skriv upp all resonansformerna för följande joner. Vilken eller vilka bidrar mest till resonanshybriden? 3. Rita och namnge alla aromatiska föreningar med summaformeln a) C 7 7 b) C 8 10 som ger tre produkter vid elektrofil aromatisk monobromering. 4. Bensylkatjonen är resonansstabiliserad. Rita dess resonansstrukturer. Är aniliniumjonen stabiliserad på samma sätt? C Vi har tidigare diskuterat mekanismen för addition av till alkener samt olika substituenters effekt på aromatisk elektrofil substitution. u är det dags att kombinera dessa kunskaper! Vilken av följande föreningar reagerar snabbast med? Varför? Förklara med tydliga reaktionsmekanismer! Me
10 6. BT (butylhydroxitoluen) är en antioxidant som används som tillsattsmedel (E 321) i bl a tuggummi och kosmetika; dess främsta uppgift är att förhindra att fetter härsknar, vilket leder till missfärgning och oönskade lukter. BT framställs industriellt genom att reagera p-kresol med 2-metylpropen i sur miljö. 3 P 4 p-kresol BT a) Vad heter reaktionen? b) Förklara med en tydlig reaktionsmekanism hur BT bildas. [Det är ju även intressant att fundera på hur BT fungerar som antioxidant!] 10
11 Övning 6: ukleofil addition till aldehyder och ketoner 1. Vilka olika funktionella grupper innehållande karbonyl kan du finna i följande molekyler: C C vanillin C 3 C 3 C( 2 )CC 2 C alanylglycin retinal 2. Rita formler för följande föreningar: a) bromaceton b) 2-metylheptan-3-on c) butandial d) 6,6-dimetylcyklohexa-2,4-dienon e) 3-fenylpropenal f) 4-nitrobensenkarbaldehyd 3. För att undersöka en reaktions mekanism eller en substans metabolisering kan man märka in ovanliga isotoper i molekyler av intresse och sedan undersöka med t ex pektroskopiska metoder var isotoperna hamnar i produkterna. Föreslå en mekanism för hur vanlig aceton (i vilken syret är 16 ) kan inkorporera 18 genom behandling med vatten i sur miljö. SCC 3 ett kaliumsparande diuretikum Avgör om nedanstående föreningar är halvacetal, acetal eller imin. Ur vilka ämnen kan den första framställas? C 3 C 3 5. a) Vilka två isomera, cykliska acetaler kan bildas i den syrakatalyserade reaktionen mellan aceton och glycerol (1,2,3-propantriol)? b) Endast en bildas. Vilken är det om det visar sig att den kan spaltas i enantiomerer? 6 Kemisten Proton arbetade som utvecklingsansvarig på det förnämliga företaget Vallfart AB, och ville absolut framställa nedanstående substans F, för att utröna om densamma kunde vara lämplig som komponent i en ny komposition för den popolära "Kallas Guldvalla". ur han än försökte kunde Proton inte komma fram till rätt substans utan fick istället en närastående substans C som inte gick att använda till någonting. u är det din uppgift att förklara för Proton varför den syntesvägen inte fungerade och hur han skall lösa problemet. [Ledning: förklara vad som händer i de olika 11
12 reaktionsvägarna A B C och A D E F. Till din hjälp har du summaformlerna i respektive mellansteg. ab 4 C , 2 erhållen produkt A B C C 2 6 2, C ab 4 C7 14 3, 2 önskad produkt D E F 7. Ibland möter vi problem som i förstone förefaller nya och svåra, men som efter närmare analys kan brytas ner i enklare komponenter. Ett exempel är reaktionen mellan cyklopentanon och dimethylsulfoniummetylid (1) till epoxid 2. Vi har tidigare under kursen visat att epoxider är värdefulla intermediärer i organisk kemi. Det är nu din uppgift att ange en rimlig mekanism för reaktionen nedan! [Tips: börja med att identifiera vilketav startmaterialen som är nukleofil resp. elektrofil.] C 2 S DMS
13 Övning 7: Karboxylsyror och deras derivat 1. Enligt ett tabellverk gäller följande pk a -värden för några aromatiska syror: bensoesyra 4.20, p-metoxibensoesyra 4.47, p-cyanobensoesyra ur kan man föklara syrornas olika styrka? 2. Rangordna alkoholer, karboxylsyror och fenoler efter stigande aciditet (surhet). Förklara skillnaderna. 3. a) Vilka är karboxylderivaten, RCY? rdna dessa enligt ökande hydrolyshastighet. b) försök nu förklara varför du kom fram till rangordningen i uppgift a). En förenklad orbital/resonansargumentering är inte helt fel! 4. a) Redgör i detalj för mekanismen för framställning av estern mellan propionsyra och metanol i närvaro av lämplig katalysator. b) Denna reaktion är reversibel med K 4. ur kan man påverka jämviktsläget av ovanstående reaktion så att den önskade produkten erhålls i högt utbyte? 5. Redogör för mekanismen för den basinducerade hydrolysen av nedanstående ester. Asterisken anger att atomen är isotopmärkt. I svaret skall anges i vilken komponent i produkten isotopmärkningen återfinns. 6. En blandning av fenylacetat (estern mellan ättiksyra och fenol) och acetanilid (MeCPh) hydrolyseras med kokande natriumhydroxidlösning. ur kan man isolera de komponenter som finns i lösningen? 7. Det är möjligt att framställa antingen monoster 2 eller diester 3 från succinsyraanhydrid (1) enligt nedanstående schema. Varför ger ena metoden monoestern och den andra diestern? En tydlig reaktionsmekanism bör ingå i svaret. * Me Me Me Me Me Me
14 Övning 8: Kondensationsreaktioner 1. Formulera mekanismer för följande isomeriseringar. ur ligger respektive jämvikt förskjuten? 2. ur förklarar man, att aceton föreligger företrädesvis i ketoformen, medan 2,4- pentandion föreligger som enolform. 3. Skriv reaktionsformel för aldolkondensationen av propanal. 4. edanstående triketon kan undergå aldolkondensation i vilken anjonen av acetylgruppen i sidokedjan är nukleofil. Skriv strukturformler för produkterna som erhålles vid reaktion med var och en av de två karbonylgrupperna i ringen. Är produkterna identiska? m inte vilket är deras förhållande till varandra. 5. Claisenkondensationen är en effektiv metod för att framställa sexlediga heterocykler, och ett exempel visas nedan. I just detta fallet, där vi har ett symmetriskt startmaterial, spelar det ingen roll vilken estergrupp som enoliseras eftersom utfallet blir detsamma. Et 2 C C 2 Et 1. Et 2. värme -metyl-4- piperidon Men även i följande fall, där startmaterialet inte är symmetrisk, spelar det ingen roll vilken estergrupp som enoliseras. Produktutfallet blir detsamma! Förklara med en tydlig reaktionsmekanism hur detta är möjligt. Et 2 C C 2 Et 1. Et 2. värme -metyl-3- pyrrolidinon 7. a) Substrat 1 kan omvandlas till den niolediga strukturen 2 genom behandling med natriumetoxid. Visa med en tydlig mekanism hur detta sker. 14
15 b) Reaktionen startar med en enolisering. Substrat 1 innehåller tre sura metylenprotoner (i, ii ich iii) men bara en av dessa positioner reagerar vidare till produkt. Varför och hur avgörs selektiviteten? C 2 Et C 2 Et aet Et
16 Övning 10. Aminer och kolhydrater Dust, dirt and sand. The remains of greatness in history's hand. (Dartwill Aquila) 1. a) Ange strukturen för den öppna formen av D-ribos. b) m man löser 1 g α-d-glukopyranos i vatten och genast mäter vridningen av planpolariserat ljus erhålles värdet [α] = 113. Då man mäter på samma lösning efter endag erhålles [α] = 55. Förklara varför och ange mekanismen bakom detta fenomen. 2. Sätt rätt text i rätt ruta! anomer enantiomer diastereomer α-d-glukopyranos β-d-glukopyranos α-l-glukopyranos β-l-glukopyranos 3. rdna följande föreningar efter ökande basstyrka C C 3 4. Vilken av följande föreningar är mest basisk. Varför? 16
17 5. ur varierar C--bindningens längd i serien =C 2 C 3-2 C 2 =C- 2 17
18 Övning 6. Alkoholer, etrar, fenoler, tioler och sulfider. When they get you to believe their lies they think they've created a truth. (Dartwill Aquila) 1. Vad skiljer en fenol från en alkohol? ur kan följande föreningar separeras från varandra på ett enkelt sätt? 2. Bensyltiol får reagera med jod. Vad bildas? 3. En kemist skulle framställa t-butyl-metyleter och försökte då genomföra följande reaktion. C 3 a I Till sin förvåning fann kemisten dock en annan produkt, vilken? ur skulle du framställa t-butyl -metyleter? 4. ΔG o för nedanstående jämvikt är 3.4 kj/mol vid 25 o C. Vilken konformer är stabilast? Beräkna den procentuella fördelningen mellan konformererna vid denna temperaturen. 5. Etenoxid får reagera med metanol i sur miljö. Vad bildas? 18
Tentamen i Organisk kemi- grundkurs 7.5 hp (KEMA01),
 Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA0), 3-03-8 ) Molekylmodeller och är tillåtna hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA0), 3-03-8 ) Molekylmodeller och är tillåtna hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
H 3 C. 5. Förklara varför fenol (se ovan) är en starkare syra än cyklohexanol (pk a =18).
 Linköping 12-08-15 IFM/Kemi Linköpings universitet TFKE06/GAN-ss Efterarbete av föreläsningar inom rganisk kemi 2 Uppgifter kap. 1-3 1. Rita resonansformler för N,N-dimetyl-3-aminopropenal! 3 3 N 2. Ange
Linköping 12-08-15 IFM/Kemi Linköpings universitet TFKE06/GAN-ss Efterarbete av föreläsningar inom rganisk kemi 2 Uppgifter kap. 1-3 1. Rita resonansformler för N,N-dimetyl-3-aminopropenal! 3 3 N 2. Ange
Inga hjälpmedel är tillåtna. 100 poäng
 rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2017 Tid: 9:00-13:00 Hjälpmedel: Inga
rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2017 Tid: 9:00-13:00 Hjälpmedel: Inga
Tentamen i Organisk kemi- grundkurs 7.5 hp (KEMA01),
 Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA01), 13-08-19 1) Molekylmodeller är tillåtet hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA01), 13-08-19 1) Molekylmodeller är tillåtet hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
Svar: Tentamen i Organisk kemi 2, TFKE06, ,
 Svar: Tentamen i rganisk kemi 2, TFKE06, 2008-10-21, 1 a) Vilka av dessa heterocykliska föreningar är aromatiska? (2 p) S N N romatisk nti aromatisk nti aromatisk romatisk ückels regel: 4n + 2 elektroner
Svar: Tentamen i rganisk kemi 2, TFKE06, 2008-10-21, 1 a) Vilka av dessa heterocykliska föreningar är aromatiska? (2 p) S N N romatisk nti aromatisk nti aromatisk romatisk ückels regel: 4n + 2 elektroner
Inga hjälpmedel är tillåtna. 100 poäng
 rganisk kemi Provmoment: Ladokkod: Tentamen ges för: Tentamen A100TG Tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 15 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel är tillåtna
rganisk kemi Provmoment: Ladokkod: Tentamen ges för: Tentamen A100TG Tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 15 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel är tillåtna
TK061B Tillämpad bioteknik, antagna 2012, Inga hjälpmedel är tillåtna. 100 poäng
 Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Tillämpad bioteknik, antagna 2012, 2013 7,5 högskolepoäng TentamensKod: Tentamensdatum: 11 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel
Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Tillämpad bioteknik, antagna 2012, 2013 7,5 högskolepoäng TentamensKod: Tentamensdatum: 11 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel
1. P. Ange vilka av följande föreningar som är syror respektive baser enligt Lewis definition: aceton vatten dimetylsulfid AlCl 3
 KKA05/15 2014 utdelningsmtrl Övning 2 Kemisk bindning Instuderingsfrågor 1. 2.1.4 2. 2.1.5 3. 2.1.10 4. 2.1.11 5. Ange vad som menas med Brønstedsyra respektive bas, samt ge Lewis definition av syror och
KKA05/15 2014 utdelningsmtrl Övning 2 Kemisk bindning Instuderingsfrågor 1. 2.1.4 2. 2.1.5 3. 2.1.10 4. 2.1.11 5. Ange vad som menas med Brønstedsyra respektive bas, samt ge Lewis definition av syror och
Kapitel 2. Kovalent bindning
 Kapitel 2. Kovalent bindning 2.1 Instuderingsfrågor 2.1.1 Rangordna kväve, fluor, syre, kol och väte efter stigande elektronegativitet. 2.1.2 Vad menas med induktiv effekt? 2.1.3 Vad menas med dipolmoment?
Kapitel 2. Kovalent bindning 2.1 Instuderingsfrågor 2.1.1 Rangordna kväve, fluor, syre, kol och väte efter stigande elektronegativitet. 2.1.2 Vad menas med induktiv effekt? 2.1.3 Vad menas med dipolmoment?
Övning 1. Kemisk bindning. Instuderingsfrågor. Övningsuppgifter. Tentamensuppgift. KOKA05/ utdeldningsmtrl
 KKA05/15 2013 utdeldningsmtrl Övning 1 Kemisk bindning Instuderingsfrågor 1. 2.1.4 2. 2.1.5 3. 2.1.10 4. 2.1.11 5. Ange vad som menas med Brønstedsyra respektive bas, samt ge Lewis definition av syror
KKA05/15 2013 utdeldningsmtrl Övning 1 Kemisk bindning Instuderingsfrågor 1. 2.1.4 2. 2.1.5 3. 2.1.10 4. 2.1.11 5. Ange vad som menas med Brønstedsyra respektive bas, samt ge Lewis definition av syror
7,5 högskolepoäng. Organisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik.
 rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2018 Tid: 9:00-13:00 Hjälpmedel: Inga
rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2018 Tid: 9:00-13:00 Hjälpmedel: Inga
Inga hjälpmedel är tillåtna. För att få godkänd kurs måste man få minst 40 poäng på examen.
 Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Bt11-Bt2 7,5 högskolepoäng NAMN Personnummer Tentamensdatum: 28 augusti 2012 Tid: 09.00 13.00 Hjälpmedel: Inga hjälpmedel är tillåtna Totalt
Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Bt11-Bt2 7,5 högskolepoäng NAMN Personnummer Tentamensdatum: 28 augusti 2012 Tid: 09.00 13.00 Hjälpmedel: Inga hjälpmedel är tillåtna Totalt
1 Ange lämpliga reagens till följande reaktioner. Inga mekanismer behövs.
 Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 31 maj 2005, kl. 08.00-14.00 Tillåtna hjälpmedel: molekylmodeller, miniräknare (periodiskt system och tabeller med bindingsstyrkor och pk a -värden är bifogade
Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 31 maj 2005, kl. 08.00-14.00 Tillåtna hjälpmedel: molekylmodeller, miniräknare (periodiskt system och tabeller med bindingsstyrkor och pk a -värden är bifogade
Tentamen i Organisk kemi, 7.5 hp (KO3003) FACIT
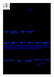 Tentamen i rganisk kemi, 7.5 hp (K3003) 1. (10 p) a) Ange om molekylerna 1 och/eller 2 är aromatiska. (1 p) b) Namnge föreningarna 1 och 2. (1 p) c) Vilken förening är starkast bas av 3 och 4? (2 p) d)
Tentamen i rganisk kemi, 7.5 hp (K3003) 1. (10 p) a) Ange om molekylerna 1 och/eller 2 är aromatiska. (1 p) b) Namnge föreningarna 1 och 2. (1 p) c) Vilken förening är starkast bas av 3 och 4? (2 p) d)
Föreläsning 16. Karbonylkolets kemi I Kapitel 16 F16
 Föreläsning 16 Karbonylkolets kemi I Kapitel 16 1) Introduktion 2) Addition av nukleofiler till karbonylgrupper A) Addition av hydridjoner B) Addition av metallorganiska reagens C) Addition av alkoholer
Föreläsning 16 Karbonylkolets kemi I Kapitel 16 1) Introduktion 2) Addition av nukleofiler till karbonylgrupper A) Addition av hydridjoner B) Addition av metallorganiska reagens C) Addition av alkoholer
Efterarbete: LÖSNINGSFÖRSLAG TILL UPPGIFTER - O +
 Linköping 10-03-15 IFM/Kemi Linköpings universitet TFKE51/GAN-SS Efterarbete: LÖSNINGSFÖRSLAG TILL UPPGIFTER Kap. 1-4 1. N - N + - + N - + N 2. Den första resonansstrukturen är stabilast. Kom ihåg: Ju
Linköping 10-03-15 IFM/Kemi Linköpings universitet TFKE51/GAN-SS Efterarbete: LÖSNINGSFÖRSLAG TILL UPPGIFTER Kap. 1-4 1. N - N + - + N - + N 2. Den första resonansstrukturen är stabilast. Kom ihåg: Ju
Kiralitet former som är spegelbilder av varandra men ej identiska. Jämför med händer.
 Organisk kemi i denna kurs KIRALITET NUKLEOFIL SUBSTITUTION Föreläsning v17 Nina Kann v16 karbonylgruppens kemi =O v17 nukleofil substitution (alkylhaliders reaktivitet), kiralitet v18 alkener, karbokatjoner,
Organisk kemi i denna kurs KIRALITET NUKLEOFIL SUBSTITUTION Föreläsning v17 Nina Kann v16 karbonylgruppens kemi =O v17 nukleofil substitution (alkylhaliders reaktivitet), kiralitet v18 alkener, karbokatjoner,
Tentamen i Organisk kemi AK 2/6 2005,
 Tentamen i rganisk kemi AK 2/6 2005, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: 3:a minst 40 poäng 4:a minst 55 poäng 5:a minst 75 poäng Skriv
Tentamen i rganisk kemi AK 2/6 2005, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: 3:a minst 40 poäng 4:a minst 55 poäng 5:a minst 75 poäng Skriv
Tentamen i Organisk kemi (KEGA01/KEGAH0/KEGAO0/KEGAOO/KEGAAK) (KEGL01/BIGLN3) 20 januari 2016, kl
 Institutionen för ingenjörs- och kemivetenskaper Karlstads universitet Tentamen i Organisk kemi (KEGA01/KEGAH0/KEGAO0/KEGAOO/KEGAAK) (KEGL01/BIGLN3) 20 januari 2016, kl 08.15 13.15 Betygsgränser: respektive:
Institutionen för ingenjörs- och kemivetenskaper Karlstads universitet Tentamen i Organisk kemi (KEGA01/KEGAH0/KEGAO0/KEGAOO/KEGAAK) (KEGL01/BIGLN3) 20 januari 2016, kl 08.15 13.15 Betygsgränser: respektive:
Föreläsning 10. Alkener I Kapitel 10 F10
 Föreläsning 10 Alkener I Kapitel 10 1) Introduktion 2) Monomolekylära eliminationer 3) Bimolekylära eliminationer 4) Alkyner 5) Sammanfattning av joniska reaktioner 6) Exempel 1. Introduktion Bimolekylär
Föreläsning 10 Alkener I Kapitel 10 1) Introduktion 2) Monomolekylära eliminationer 3) Bimolekylära eliminationer 4) Alkyner 5) Sammanfattning av joniska reaktioner 6) Exempel 1. Introduktion Bimolekylär
Tentamen i Organisk kemi 28/5 2013,
 Tentamen i rganisk kemi 28/5 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: Lycka till! /Ulf -fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p
Tentamen i rganisk kemi 28/5 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: Lycka till! /Ulf -fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p
TENTAMEN i FYSIKALISK-ORGANISK KEMI 7,5 hp, NKEC , kl
 TENTAMEN i FYSIKALISK-RGANISK KEMI 7,5 hp, NKEC63. 2008-05-30, kl. 08.00-13.00 1. Följande epoxider reagerar med de reagens som anges för reaktionerna A D och ger givna utbyten och produktförhållanden.
TENTAMEN i FYSIKALISK-RGANISK KEMI 7,5 hp, NKEC63. 2008-05-30, kl. 08.00-13.00 1. Följande epoxider reagerar med de reagens som anges för reaktionerna A D och ger givna utbyten och produktförhållanden.
Tentamen i Organisk kemi 16/ ,
 Tentamen i rganisk kemi 16/12 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p 5 75-90p 1) Besvara
Tentamen i rganisk kemi 16/12 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p 5 75-90p 1) Besvara
Tentamen i Organisk kemi 25/5 2011,
 Tentamen i rganisk kemi 25/5 2011, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak ECTS LT (T) G 40-59p E 40-41p 3 40-54p VG 60-90p D 42-50p
Tentamen i rganisk kemi 25/5 2011, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak ECTS LT (T) G 40-59p E 40-41p 3 40-54p VG 60-90p D 42-50p
Tentamen i organisk kemi, KOKA05, 5 hp, Måndagen den 1 juni 2009, 14.00-19.00.
 Tentamen i organisk kemi, KKA05, 5 hp, Måndagen den 1 juni 2009, 14.00-19.00. Molekylmodeller och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer
Tentamen i organisk kemi, KKA05, 5 hp, Måndagen den 1 juni 2009, 14.00-19.00. Molekylmodeller och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer
Totalt 10 uppgifter, vardera värd 10p (totalt 100p). För godkänt fordras minst 50p, för 4:a minst 66p och för 5:a minst 83p.
 Tentamen i rganisk Kemi 2 (3B1760) måndagen den 29 maj 2006, kl. 08.00-14.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor och pka-värden är bifogade efter frågorna
Tentamen i rganisk Kemi 2 (3B1760) måndagen den 29 maj 2006, kl. 08.00-14.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor och pka-värden är bifogade efter frågorna
Olika typer av kolväten
 INTDUKTIN TILL GANISK KEMI KABNYLGUPPSKEMI Föreläsning v16 Nina Kann lika typer av kolväten alifatiska - alkaner - alkener - alkyner aromatiska 1 Funktionella grupper alken alkohol l alkylhalid S tiol
INTDUKTIN TILL GANISK KEMI KABNYLGUPPSKEMI Föreläsning v16 Nina Kann lika typer av kolväten alifatiska - alkaner - alkener - alkyner aromatiska 1 Funktionella grupper alken alkohol l alkylhalid S tiol
2. SUBSTITUTION (Nukleofil substitution) S N 2
 . SUBSTITUTION (Nukleofil substitution) Alkylhalider är generellt reaktiva pga att den elektronegativa haliden gör att bindningen till kol polariseras, man får en dipol. Kolet blir elektrofilt (elektronfattigare
. SUBSTITUTION (Nukleofil substitution) Alkylhalider är generellt reaktiva pga att den elektronegativa haliden gör att bindningen till kol polariseras, man får en dipol. Kolet blir elektrofilt (elektronfattigare
TENTAMEN i ORGANISK KEMI 2 (TFKE06) ,
 TETAME i RGAISK KEMI 2 (TFKE06) 2012-10-23, 14.00-18.00 Lösningsförslag: 1. Vilken förening i respektive par a)-d) har surast väte? Ge kort förklaring till svaret. (10 p) a) b) F C 2 C Cl C 2 C c) d) 3
TETAME i RGAISK KEMI 2 (TFKE06) 2012-10-23, 14.00-18.00 Lösningsförslag: 1. Vilken förening i respektive par a)-d) har surast väte? Ge kort förklaring till svaret. (10 p) a) b) F C 2 C Cl C 2 C c) d) 3
TENTAMEN I ALLMÄN OCH ORGANISK KEMI
 KAROLINSKA INSTITUTET Biomedicinutbildningen TENTAMEN I ALLMÄN OCH ORGANISK KEMI FREDAGEN DEN 13 JANUARI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för
KAROLINSKA INSTITUTET Biomedicinutbildningen TENTAMEN I ALLMÄN OCH ORGANISK KEMI FREDAGEN DEN 13 JANUARI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för
Tentamen i Organisk Kemi (3B1760) Tisdagen den 30 augusti 2005, kl
 Tentamen i rganisk Kemi (3B1760) Tisdagen den 30 augusti 2005, kl. 08.00-14.00 Tillåtna hjälpmedel: molekylmodeller, miniräknare (periodiskt system och tabeller med bindingsstyrkor och pk a -värden är
Tentamen i rganisk Kemi (3B1760) Tisdagen den 30 augusti 2005, kl. 08.00-14.00 Tillåtna hjälpmedel: molekylmodeller, miniräknare (periodiskt system och tabeller med bindingsstyrkor och pk a -värden är
Tentamen i organisk kemi, KOKA05 Måndagen den 22 augusti 2011,
 Tentamen i organisk kemi, KKA05 Måndagen den 22 augusti 2011, 8.00-13.00. Molekylmod och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer på varje
Tentamen i organisk kemi, KKA05 Måndagen den 22 augusti 2011, 8.00-13.00. Molekylmod och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer på varje
Övningsfrågor inför dugga 3 och tentamen
 Övningsfrågor inför dugga 3 och tentamen Biomedicinare HT 006. MBB, K.I. Mats Hamberg Ge reaktionsformel för Fentonreaktionen! Följande frågor rör den nedan avbildade föreningen. a) Ange i vilken typ av
Övningsfrågor inför dugga 3 och tentamen Biomedicinare HT 006. MBB, K.I. Mats Hamberg Ge reaktionsformel för Fentonreaktionen! Följande frågor rör den nedan avbildade föreningen. a) Ange i vilken typ av
ALDEHYDER och KETONER Del D-2007
 ALDEYDE och KETNE Del D-2007 Karbonyl grupp: -# +# dipol, sp 2, 120 o vinkel Aldehyd ändelse: - al metanal formaldehyd 3 etanal acetaldehyd 3 2 propanal propionaldehyd bensaldehyd akrolein mrering av kolkedja:
ALDEYDE och KETNE Del D-2007 Karbonyl grupp: -# +# dipol, sp 2, 120 o vinkel Aldehyd ändelse: - al metanal formaldehyd 3 etanal acetaldehyd 3 2 propanal propionaldehyd bensaldehyd akrolein mrering av kolkedja:
Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor och pka-värden är bifogade efter frågorna
 Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 29 Augusti 2006, kl. 08.00-14.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor och pka-värden är bifogade efter
Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 29 Augusti 2006, kl. 08.00-14.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor och pka-värden är bifogade efter
Tentamen i organisk kemi, KEMB01, 15 hp, fredagen den 13 januari 2012,
 Tentamen i organisk kemi, KEMB01, 15 hp, fredagen den 13 januari 2012, 9.00-15.00. Molekylmodeller, miniräknare, punktgruppstabell och spektroskopibok får medtagas. Var vänlig besvara endast en uppgift
Tentamen i organisk kemi, KEMB01, 15 hp, fredagen den 13 januari 2012, 9.00-15.00. Molekylmodeller, miniräknare, punktgruppstabell och spektroskopibok får medtagas. Var vänlig besvara endast en uppgift
Ange längst upp på omslaget ett referensnummer (6 tecken, t.ex. bilnummer) om du vill kunna se resultatet på kurshemsidan när rättningen är klar.
 Tentamen i organisk kemi, KK05 nsdagen den 25 maj 2011, 8.00-13.00. nge längst upp på omslaget ett referensnummer (6 tecken, t.ex. bilnummer) om du vill kunna se resultatet på kurshemsidan när rättningen
Tentamen i organisk kemi, KK05 nsdagen den 25 maj 2011, 8.00-13.00. nge längst upp på omslaget ett referensnummer (6 tecken, t.ex. bilnummer) om du vill kunna se resultatet på kurshemsidan när rättningen
TENTAMEN I ALLMÄN OCH ORGANISK KEMI
 KARLINSKA INSTITUTET Biomedicinprogrammet TENTAMEN I ALLMÄN CH RGANISK KEMI NSDAGEN DEN 28 FEBRUARI 2007, 09.00-11.30 och 12.30-15.00. Tentamen är uppdelad i två pass med en uppsättning frågor för varje
KARLINSKA INSTITUTET Biomedicinprogrammet TENTAMEN I ALLMÄN CH RGANISK KEMI NSDAGEN DEN 28 FEBRUARI 2007, 09.00-11.30 och 12.30-15.00. Tentamen är uppdelad i två pass med en uppsättning frågor för varje
Lösningsförslag: Tentamen i Organisk kemi 2, TFKE06,
 Lösningsförslag: Tentamen i rganisk kemi 2, TFKE06, 2009-10-23 1.a) Vilken förening i följande par har surast väte? Ge kort förklaring till svaret. (2 p/delsvar) a) F 2 l 2 2 3 c) d) a) Fluoriden mer elektronegativ
Lösningsförslag: Tentamen i rganisk kemi 2, TFKE06, 2009-10-23 1.a) Vilken förening i följande par har surast väte? Ge kort förklaring till svaret. (2 p/delsvar) a) F 2 l 2 2 3 c) d) a) Fluoriden mer elektronegativ
Tentamen i organisk kemi, KOKA05 Tisdagen den 26 augusti 2010,
 Tentamen i organisk kemi, KKA05 Tisdagen den 26 augusti 2010, 8.00-13.00. Molekylmodeller och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer på varje
Tentamen i organisk kemi, KKA05 Tisdagen den 26 augusti 2010, 8.00-13.00. Molekylmodeller och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer på varje
1. Introduktion. Vad gör senapsgas så farlig?
 Föreläsning 9 Reaktionslära II Kapitel 9.1-9.6 1) Introduktion 2) Monomolekylära nukleofila substitutioner 3) Parametrar 4) Sammanfattning 5) Exempel 1. Introduktion Vad gör senapsgas så farlig? 2. Nukleofila
Föreläsning 9 Reaktionslära II Kapitel 9.1-9.6 1) Introduktion 2) Monomolekylära nukleofila substitutioner 3) Parametrar 4) Sammanfattning 5) Exempel 1. Introduktion Vad gör senapsgas så farlig? 2. Nukleofila
Kemiska reaktioner: Olika reaktionstyper och reaktionsmekanismer. Niklas Dahrén
 Kemiska reaktioner: Olika reaktionstyper och reaktionsmekanismer Niklas Dahrén 7 olika reaktionstyper 1. Substitutionsreaktioner 2. Additionsreaktioner 3. Eliminationsreaktioner 4. Kondensationsreaktioner
Kemiska reaktioner: Olika reaktionstyper och reaktionsmekanismer Niklas Dahrén 7 olika reaktionstyper 1. Substitutionsreaktioner 2. Additionsreaktioner 3. Eliminationsreaktioner 4. Kondensationsreaktioner
TENTAMEN I ALLMÄN OCH ORGANISK KEMI
 KAROLINSKA INSTITUTET Biomedicinprogrammet (Magister) TENTAMEN I ALLMÄN OCH ORGANISK KEMI FREDAGEN DEN 1 FEBRUARI 2008, 08.30-11.00 och 12.00-14.30 Tentamen är uppdelad i två pass med en uppsättning frågor
KAROLINSKA INSTITUTET Biomedicinprogrammet (Magister) TENTAMEN I ALLMÄN OCH ORGANISK KEMI FREDAGEN DEN 1 FEBRUARI 2008, 08.30-11.00 och 12.00-14.30 Tentamen är uppdelad i två pass med en uppsättning frågor
Lösning till Tentamen i Kemi (TFKE16),
 Lösning till Tentamen i Kemi (TFKE16), 091017. 1. a) KN Mn 2 b) krom(iii)sulfat alt. dikromtrisulfat (mindre bra) triarsenikpentanitrid alt. arsenik(v)nitrid c) +II +V +III +II 3 Fe 2+ + N 3 - + 4 + 3
Lösning till Tentamen i Kemi (TFKE16), 091017. 1. a) KN Mn 2 b) krom(iii)sulfat alt. dikromtrisulfat (mindre bra) triarsenikpentanitrid alt. arsenik(v)nitrid c) +II +V +III +II 3 Fe 2+ + N 3 - + 4 + 3
Valenselektroner = elektronerna i yttersta skalet visas nedan för några element ur grupperna
 Kapitel 9 är hittar du svar och lösningar till de övningsuppgifter som hänvisas till i inledningen. I vissa fall har lärobokens avsnitt Svar och anvisningar bedömts vara tillräckligt fylliga varför enbart
Kapitel 9 är hittar du svar och lösningar till de övningsuppgifter som hänvisas till i inledningen. I vissa fall har lärobokens avsnitt Svar och anvisningar bedömts vara tillräckligt fylliga varför enbart
Övningsuppgifter. till Ellervik, Sterner; Organisk Kemi. Studentlitteratur, 2004
 RGANISK KEMI Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Karolina Aplander, Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Jakob Nilsson,
RGANISK KEMI Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Karolina Aplander, Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Jakob Nilsson,
Föreläsning 17. Karbonylkolets kemi II Kapitel 17 F17
 Föreläsning 17 Karbonylkolets kemi II Kapitel 17 1) Introduktion 2) Addition av starka nukleofiler 3) Estrar 4) Amider 5) Nitriler 6) Syraklorider 7) Praktisk användning 1. Introduktion Aldehyder och ketoner
Föreläsning 17 Karbonylkolets kemi II Kapitel 17 1) Introduktion 2) Addition av starka nukleofiler 3) Estrar 4) Amider 5) Nitriler 6) Syraklorider 7) Praktisk användning 1. Introduktion Aldehyder och ketoner
Föreläsning 11. Alkener II Kapitel 11 F11
 Föreläsning 11 Alkener II Kapitel 11 1) Introduktion 2) Addition av elektrofila reagens 3) ydrogenering 4) ydroborering 5) Radikaladdition 6) Polymerisering 7) xidation 1. Introduktion ur gör man cancermedicinen
Föreläsning 11 Alkener II Kapitel 11 1) Introduktion 2) Addition av elektrofila reagens 3) ydrogenering 4) ydroborering 5) Radikaladdition 6) Polymerisering 7) xidation 1. Introduktion ur gör man cancermedicinen
Föreläsning 8. Reaktionslära I Kapitel
 Föreläsning 8 Reaktionslära I Kapitel 9.1-9.3 1) Introduktion 2) Nukleofila substitutioner 3) Parametrar 4) Praktisk användning 5) Elektrofiler och biologi 1. Introduktion Varför gråter vi när vi hackar
Föreläsning 8 Reaktionslära I Kapitel 9.1-9.3 1) Introduktion 2) Nukleofila substitutioner 3) Parametrar 4) Praktisk användning 5) Elektrofiler och biologi 1. Introduktion Varför gråter vi när vi hackar
STEREOKEMI B C. alla objekt har en spegelbild KOKA05/ många objekt är inte identiska med sin spegelbild. har ingen spegelbild
 TEREKEMI KK05/15 2012 alla objekt har en spegelbild har ingen spegelbild D C B B C D många objekt är inte identiska med sin spegelbild definition kiral ett objekt som inte är identiskt (kan bringas att
TEREKEMI KK05/15 2012 alla objekt har en spegelbild har ingen spegelbild D C B B C D många objekt är inte identiska med sin spegelbild definition kiral ett objekt som inte är identiskt (kan bringas att
KARBOKATJON KARBANJON
 EAKTINE: Generella typer : 1. Addition Fö D-2010 (rowe Kap 17-18) 2. Substitution 3. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME Z MLYS + Z ADIKALE Z ETELYS KABKATJN + Z Vanligast + Z KABANJN
EAKTINE: Generella typer : 1. Addition Fö D-2010 (rowe Kap 17-18) 2. Substitution 3. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME Z MLYS + Z ADIKALE Z ETELYS KABKATJN + Z Vanligast + Z KABANJN
Övningsuppgifter. till Ellervik, Sterner; Organisk Kemi. Studentlitteratur, 2004
 Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Karolina Larsson, Jakob Nilsson, Ulf Nilsson,
Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Karolina Larsson, Jakob Nilsson, Ulf Nilsson,
Organiska föreningar del 5: Rita och namnge alkoholer, karboxylsyror och estrar. Niklas Dahrén
 Organiska föreningar del 5: Rita och namnge alkoholer, karboxylsyror och estrar Niklas Dahrén Alkoholer är organiska ämnen med en eller flera OH-grupper Alkoholer innehåller OH-grupper: Alkoholer är organiska
Organiska föreningar del 5: Rita och namnge alkoholer, karboxylsyror och estrar Niklas Dahrén Alkoholer är organiska ämnen med en eller flera OH-grupper Alkoholer innehåller OH-grupper: Alkoholer är organiska
Organiska föreningar del 6: Rita och namnge etrar, aldehyder, ketoner, tioler och disulfider. Niklas Dahrén
 Organiska föreningar del 6: Rita och namnge etrar, aldehyder, ketoner, tioler och disulfider Niklas Dahrén Etrar Etrar har en etergrupp (eterbindning): R-grupperna är två identiska eller två olika kolvätegrupper/kolvätekedjor
Organiska föreningar del 6: Rita och namnge etrar, aldehyder, ketoner, tioler och disulfider Niklas Dahrén Etrar Etrar har en etergrupp (eterbindning): R-grupperna är två identiska eller två olika kolvätegrupper/kolvätekedjor
Datum Tid Anmärkning Lokal UndervTyp. 12/ F1 OW V:A Intro/grundläggande begrepp. 13/ F2 OW DC:lhö Termodynamik och jämvikt
 Medicin och Teknik 2012 LV1 Datum Tid Anmärkning Lokal UndervTyp 12/3 08.00-10.00 F1 W V:A Intro/grundläggande begrepp 13/3 08.00-10.00 F2 W DC:lhö Termodynamik och jämvikt 13/3 10.00-12.00 F3 W Gen: Aula
Medicin och Teknik 2012 LV1 Datum Tid Anmärkning Lokal UndervTyp 12/3 08.00-10.00 F1 W V:A Intro/grundläggande begrepp 13/3 08.00-10.00 F2 W DC:lhö Termodynamik och jämvikt 13/3 10.00-12.00 F3 W Gen: Aula
http://www.naturvetenskap.org/index.php?option=com_content&view=article&id=226&itemi d=236
 http://sv.wikipedia.org/wiki/petroleum http://www.naturvetenskap.org/index.php?option=com_content&view=article&id=226&itemi d=236 Alkaner C n H 2n+2 metan etan propan butan pentan hexan heptan oktan nonan
http://sv.wikipedia.org/wiki/petroleum http://www.naturvetenskap.org/index.php?option=com_content&view=article&id=226&itemi d=236 Alkaner C n H 2n+2 metan etan propan butan pentan hexan heptan oktan nonan
2. Transitions state theory för att jämföra relativa reaktiviteten hos olika substrat
 2. Transitions state theory för att jämföra relativa reaktiviteten hos olika substrat Ex: baskatalyserad hydrolys av en ester jmf substraten p-nitrofenylacetat och fenylacetat OH - attackerar karbonylkolet
2. Transitions state theory för att jämföra relativa reaktiviteten hos olika substrat Ex: baskatalyserad hydrolys av en ester jmf substraten p-nitrofenylacetat och fenylacetat OH - attackerar karbonylkolet
Tentamensuppgifter moment 2, organisk kemi.
 UMEÅ UIVERSITET TETAME Kemiska Institutionen Tentamensdatum 2012-01-19 BE, KP Studiekurs: Kemi för miljö- och hälsoskyddsområdet, 15 hp. Kurskod: KE004 Tentamen: Moment 2, organisk kemi (sid 1-3) och Moment
UMEÅ UIVERSITET TETAME Kemiska Institutionen Tentamensdatum 2012-01-19 BE, KP Studiekurs: Kemi för miljö- och hälsoskyddsområdet, 15 hp. Kurskod: KE004 Tentamen: Moment 2, organisk kemi (sid 1-3) och Moment
Reaktionsmekanismer. Kap 6
 Reaktionsmekanismer Kap 6 Rep. Kemiska reaktioner https://laughingsquid.com/a-ted-ed-animation-explaining-howall-sorts-of-different-chemical-reactions-are-triggered/ Karbokatjoner är elektrofila intermediärer
Reaktionsmekanismer Kap 6 Rep. Kemiska reaktioner https://laughingsquid.com/a-ted-ed-animation-explaining-howall-sorts-of-different-chemical-reactions-are-triggered/ Karbokatjoner är elektrofila intermediärer
Kap 2 McMurry Viktiga Begrepp
 Kap 2 McMurry Viktiga Begrepp Funktionella grupper Alkaner Isomerer Nomenklatur Konformerer Sågbocks- och Newmanprojektioner Cykloalkaner Cis- och trans- Axiell och ekvatoriell Funktionella grupper En
Kap 2 McMurry Viktiga Begrepp Funktionella grupper Alkaner Isomerer Nomenklatur Konformerer Sågbocks- och Newmanprojektioner Cykloalkaner Cis- och trans- Axiell och ekvatoriell Funktionella grupper En
Organisk kemi AK KOK Ulf Ellervik
 rganisk kemi AK KK012 2013-01-29 Ulf Ellervik Föreläsning 3 Kolvätens egenskaper Kapitel 4 1) Introduktion 2) Konformationsanalys 3) Sura kolväten 4) Kolvätens reaktioner 1. Introduktion Vad händer egentligen
rganisk kemi AK KK012 2013-01-29 Ulf Ellervik Föreläsning 3 Kolvätens egenskaper Kapitel 4 1) Introduktion 2) Konformationsanalys 3) Sura kolväten 4) Kolvätens reaktioner 1. Introduktion Vad händer egentligen
Namnge och rita organiska föreningar - del 4 Alkoholer, karboxylsyror och estrar. Niklas Dahrén
 Namnge och rita organiska föreningar - del 4 Alkoholer, karboxylsyror och estrar Niklas Dahrén Alkoholer är kolväten med en eller flera OH-grupper Alkoholer innehåller OH-grupper: Om man byter ut en av
Namnge och rita organiska föreningar - del 4 Alkoholer, karboxylsyror och estrar Niklas Dahrén Alkoholer är kolväten med en eller flera OH-grupper Alkoholer innehåller OH-grupper: Om man byter ut en av
Skrivning i Oorganisk och organisk kemi för Bt3 och K2, KOK080
 Kemi- och bioteknik, CT 12 mars, 2011 1(16) Skrivning i organisk och organisk kemi för Bt3 och K2, KK080 Tid: Lördagen den 19 mars 2011, kl 14-18. Plats: V Lärare: Nina Kann, tel: 0705 162172 eller anknytning
Kemi- och bioteknik, CT 12 mars, 2011 1(16) Skrivning i organisk och organisk kemi för Bt3 och K2, KK080 Tid: Lördagen den 19 mars 2011, kl 14-18. Plats: V Lärare: Nina Kann, tel: 0705 162172 eller anknytning
Föreläsning 12. Alkener III Kapitel 12 F12
 Föreläsning 12 Alkener III Kapitel 12 1) Introduktion 2) Allyliska system 3) Fleromättade kolväten 4) Färg och seende 5) Reaktioner 6) Sammanfattning och framåtblick 1. Introduktion Varför ser man bättre
Föreläsning 12 Alkener III Kapitel 12 1) Introduktion 2) Allyliska system 3) Fleromättade kolväten 4) Färg och seende 5) Reaktioner 6) Sammanfattning och framåtblick 1. Introduktion Varför ser man bättre
REAKTIONER : A. ADDITION Crowe p REAKTIONER: Del D-2009 Generella typer : 1. Addition 2. Substitution 3. Elimination 4.
 EAKTINE: Del D-009 Generella typer : 1. Addition. Substitution. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME rowe 1.-1. MYS ETEYS KABKATJN KABANJN eaktioner innebär att kovalenta bindningar
EAKTINE: Del D-009 Generella typer : 1. Addition. Substitution. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME rowe 1.-1. MYS ETEYS KABKATJN KABANJN eaktioner innebär att kovalenta bindningar
1. Ett grundämne har atomnummer 82. En av dess isotoper har masstalet 206.
 1. Ett grundämne har atomnummer 82. En av dess isotoper har masstalet 206. a) Antalet protoner är., antalet neutroner är. och antalet elektroner. hos atomer av isotopen. b) Vilken partikel bildas om en
1. Ett grundämne har atomnummer 82. En av dess isotoper har masstalet 206. a) Antalet protoner är., antalet neutroner är. och antalet elektroner. hos atomer av isotopen. b) Vilken partikel bildas om en
1 a) Namnge följande strukturer med gängse trivialnamn eller enligt IUPAC (1p per struktur)
 Tentamen i rganisk Kemi 2 (KD1100/3B1760) Torsdagen den 28 augusti 2008, kl. 08.00-13.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och MR-skift
Tentamen i rganisk Kemi 2 (KD1100/3B1760) Torsdagen den 28 augusti 2008, kl. 08.00-13.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och MR-skift
TENTAMEN I ALLMÄN OCH ORGANISK KEMI
 KALISKA ISTITUTET Biomedicinutbildningen TETAME I ALLMÄ GAISK KEMI FAIT FEDAGE DE 13 JAUAI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för varje pass. Dessa
KALISKA ISTITUTET Biomedicinutbildningen TETAME I ALLMÄ GAISK KEMI FAIT FEDAGE DE 13 JAUAI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för varje pass. Dessa
FUNKTIONELLA GRUPPER (Ämnesklasser) Fö
 FUNKTINELLA GUPPE (Ämnesklasser) Fö 3 2010 Ex. 32-l + 2 32- + l Kloretan Etanol Generellt: -l - = - Z = generell kolvätekedja (alkyl) Z= Funktionell grupp, Ex. -l, -, -, -N2 m.fl. 1. Föreningars egenskaper
FUNKTINELLA GUPPE (Ämnesklasser) Fö 3 2010 Ex. 32-l + 2 32- + l Kloretan Etanol Generellt: -l - = - Z = generell kolvätekedja (alkyl) Z= Funktionell grupp, Ex. -l, -, -, -N2 m.fl. 1. Föreningars egenskaper
Reaktionsmekanismer. Kap 6
 Reaktionsmekanismer Kap 6 Karbokatjoner är elektrofila intermediärer Innehåll Kvalitativa resonemang hur och varför kemiska reaktioner sker Exempel på energiomsättningar vid olika slags organiska reaktioner.
Reaktionsmekanismer Kap 6 Karbokatjoner är elektrofila intermediärer Innehåll Kvalitativa resonemang hur och varför kemiska reaktioner sker Exempel på energiomsättningar vid olika slags organiska reaktioner.
Totalt 10 uppgifter, vardera värd 10p (totalt 100p). För godkänt fordras minst 50p, för 4:a minst 66p och för 5:a minst 83p.
 Tentamen i rganisk Kemi 2 (3B1760) nsdagen den 23 maj 2007, kl. 08.00-13.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och M-skift är bifogade
Tentamen i rganisk Kemi 2 (3B1760) nsdagen den 23 maj 2007, kl. 08.00-13.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och M-skift är bifogade
Namnge och rita organiska föreningar - del 5
 Namnge och rita organiska föreningar - del 5 Etrar, aldehyder, ketoner, tioler, fenoler, nitroföreningar, aminer, amider Niklas Dahrén Etrar Etrar har en etergrupp: Vid namngivning lägger man till ändelsen
Namnge och rita organiska föreningar - del 5 Etrar, aldehyder, ketoner, tioler, fenoler, nitroföreningar, aminer, amider Niklas Dahrén Etrar Etrar har en etergrupp: Vid namngivning lägger man till ändelsen
Tentamen i Organisk Kemi 2 (KD1100/3B1760) Torsdagen den 27 augusti, kl Tillåtet hjälpmedel: molekylmodeller
 Tentamen i rganisk Kemi 2 (KD1100/3B1760) Torsdagen den 27 augusti, kl 14.00-19.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och MR-skift är
Tentamen i rganisk Kemi 2 (KD1100/3B1760) Torsdagen den 27 augusti, kl 14.00-19.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och MR-skift är
Totalt 10 uppgifter, vardera värd 10p (totalt 100p). För godkänt fordras minst 50p, för 4:a minst 66p och för 5:a minst 83p.
 Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 28 augusti 2007, kl. 08.00-13.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och M-skift är bifogade
Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 28 augusti 2007, kl. 08.00-13.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och M-skift är bifogade
Hans Adolfsson - Organisk Kemi Stockholms Universitet
 ans Adolfsson - rganisk Kemi Stockholms Universitet Stereocenter och kiralitet ans Adolfsson, Stockholms universitet Stereocenter i molekylernas värld Vad är kiralitet? Ett föremål är kiralt om det inte
ans Adolfsson - rganisk Kemi Stockholms Universitet Stereocenter och kiralitet ans Adolfsson, Stockholms universitet Stereocenter i molekylernas värld Vad är kiralitet? Ett föremål är kiralt om det inte
Föreläsning 13. Aromater I Kapitel 13 F13. 1) Introduktion 2) Bensens struktur och egenskaper 3) Aromaticitet 4) Aromatiska föreningar
 Föreläsning 13 Aromater I Kapitel 13 1) Introduktion 2) Bensens struktur och egenskaper 3) Aromaticitet 4) Aromatiska föreningar 1. Introduktion π-system ger stabilisering allyliska radikaler och karbokatjoner
Föreläsning 13 Aromater I Kapitel 13 1) Introduktion 2) Bensens struktur och egenskaper 3) Aromaticitet 4) Aromatiska föreningar 1. Introduktion π-system ger stabilisering allyliska radikaler och karbokatjoner
Föreläsning 3. Kolvätens egenskaper! Kapitel 3 och 4
 Kolvätens egenskaper Kapitel 3 och 4 Föreläsning 3 1) Introduktion 2) Mättade kolväten 3) Konformationsanalys 4) Omättade kolväten 5) Reaktivitet 1. Introduktion Vad händer egentligen här? Vad har det
Kolvätens egenskaper Kapitel 3 och 4 Föreläsning 3 1) Introduktion 2) Mättade kolväten 3) Konformationsanalys 4) Omättade kolväten 5) Reaktivitet 1. Introduktion Vad händer egentligen här? Vad har det
4. Organiska föreningars struktur
 4. Organiska föreningars struktur Organisk kemi Alla föreningar i den levande naturen är uppbyggda av kol (C). Många innehåller dessutom väte (H), syre (O), kväve (N), fosfor (P) och svavel (S). Den levande
4. Organiska föreningars struktur Organisk kemi Alla föreningar i den levande naturen är uppbyggda av kol (C). Många innehåller dessutom väte (H), syre (O), kväve (N), fosfor (P) och svavel (S). Den levande
TENTAMEN I ALLMÄN OCH ORGANISK KEMI: FACIT
 KALINSKA INSTITUTET Biomedicinutbildningen TENTAMEN I ALLMÄN C GANISK KEMI: FACIT MÅNDAGEN DEN 12 JANUAI 2004, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för
KALINSKA INSTITUTET Biomedicinutbildningen TENTAMEN I ALLMÄN C GANISK KEMI: FACIT MÅNDAGEN DEN 12 JANUAI 2004, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för
Organiska ämnen (2) s
 Organiska ämnen (2) s126-154 Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar lätt med andra ämnen. (p g a den elektronegativa halogenatomen) används
Organiska ämnen (2) s126-154 Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar lätt med andra ämnen. (p g a den elektronegativa halogenatomen) används
Alla papper, även kladdpapper lämnas tillbaka.
 Maxpoäng 66 g 13 vg 28 varav 4 p av uppg. 18,19,20,21 mvg 40 varav 9 p av uppg. 18,19,20,21 Alla papper, även kladdpapper lämnas tillbaka. 1 (2p) En oladdad atom innehåller 121 neutroner och 80 elektroner.
Maxpoäng 66 g 13 vg 28 varav 4 p av uppg. 18,19,20,21 mvg 40 varav 9 p av uppg. 18,19,20,21 Alla papper, även kladdpapper lämnas tillbaka. 1 (2p) En oladdad atom innehåller 121 neutroner och 80 elektroner.
Organiska ämnen (2) s
 Organiska ämnen (2) s126-154 Organiska stamträdet Ämnesklasser- reaktionstyper/reaktionsvägar) Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar
Organiska ämnen (2) s126-154 Organiska stamträdet Ämnesklasser- reaktionstyper/reaktionsvägar) Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar
Reaktionsmekanismer. Niklas Dahrén
 Reaktionsmekanismer Niklas Dahrén 7 olika reaktionstyper 1. Subs'tu'onsreak'oner 2. Addi'onsreak'oner 3. Elimina'onsreak'oner 4. Syra-bas-reak'oner 5. Kondensa'onsreak'oner 6. Hydrolysreak'oner 7. Redoxreak'oner
Reaktionsmekanismer Niklas Dahrén 7 olika reaktionstyper 1. Subs'tu'onsreak'oner 2. Addi'onsreak'oner 3. Elimina'onsreak'oner 4. Syra-bas-reak'oner 5. Kondensa'onsreak'oner 6. Hydrolysreak'oner 7. Redoxreak'oner
LARS ERIK ANDREAS EHNBOM
 GAISK KEMI FÖELÄSIGA T 06 LAS EIK ADEAS EBM rganisk kemi - kolföreningarnas kemi * kan framställas från organismer (1828) * behövdes ingen livskraft (1860) Kolföreningar består av ett kolskelett Grupp,
GAISK KEMI FÖELÄSIGA T 06 LAS EIK ADEAS EBM rganisk kemi - kolföreningarnas kemi * kan framställas från organismer (1828) * behövdes ingen livskraft (1860) Kolföreningar består av ett kolskelett Grupp,
Mål och betygskriterier för kemi
 Mål och betygskriterier för kemi För att bli GODKÄND på samtliga kurser skall du: Kunna skyddsföreskrifter inom NO-institutionen, samt veta var skydds- och nödutrustning finns Kunna handha den laboratorieutrustning
Mål och betygskriterier för kemi För att bli GODKÄND på samtliga kurser skall du: Kunna skyddsföreskrifter inom NO-institutionen, samt veta var skydds- och nödutrustning finns Kunna handha den laboratorieutrustning
Föreläsning 4. Substituerade kolväten Kapitel 5
 Föreläsning 4 Substituerade kolväten Kapitel 5 1) Introduktion 2) eteroatomer 3) Nomenklatur 4) Krafter mellan molekyler 5) Elektroniska modeller 6) Egenskaper hos molekyler 1. Introduktion Det afrikanska
Föreläsning 4 Substituerade kolväten Kapitel 5 1) Introduktion 2) eteroatomer 3) Nomenklatur 4) Krafter mellan molekyler 5) Elektroniska modeller 6) Egenskaper hos molekyler 1. Introduktion Det afrikanska
Tentamen för KEMA02 lördag 14 april 2012, 08-13
 Lunds Universitet, Kemiska Institutionen Tentamen för KEMA02 lördag 14 april 2012, 08-13 Tillåtna hjälpmedel är utdelat formelblad och miniräknare. Redovisa alla beräkningar. Besvara varje fråga på ett
Lunds Universitet, Kemiska Institutionen Tentamen för KEMA02 lördag 14 april 2012, 08-13 Tillåtna hjälpmedel är utdelat formelblad och miniräknare. Redovisa alla beräkningar. Besvara varje fråga på ett
SAMMANFATTNING AV NOMENKLATUR
 SAMMAFATTG AV MEKLATUR REGLER FÖR SYSTEMATSK AMGVG: Kolvätekedjan: 1. Längsta kolkedjan bildar basnamn. 2. Kolatomerna numreras från den ände ssom ger lägst nummer åt första substituenten. 3. Substituent
SAMMAFATTG AV MEKLATUR REGLER FÖR SYSTEMATSK AMGVG: Kolvätekedjan: 1. Längsta kolkedjan bildar basnamn. 2. Kolatomerna numreras från den ände ssom ger lägst nummer åt första substituenten. 3. Substituent
Rättningstiden är i normalfall 15 arbetsdagar, annars är det detta datum som gäller:
 Kemi Bas 1 Provmoment: Ladokkod: Tentamen ges för: TentamensKod: Tentamen 40S01A KBAST och KBASX 7,5 högskolepoäng Tentamensdatum: 2016-10-27 Tid: 09:00-13:00 Hjälpmedel: papper, penna, radergummi, kalkylator
Kemi Bas 1 Provmoment: Ladokkod: Tentamen ges för: TentamensKod: Tentamen 40S01A KBAST och KBASX 7,5 högskolepoäng Tentamensdatum: 2016-10-27 Tid: 09:00-13:00 Hjälpmedel: papper, penna, radergummi, kalkylator
TENTAMEN I KEMI TFKE16 (4 p)
 Linköpings Universitet IFM-Kemi. Kemi för Y, M. m. fl. (TFKE16) TENTMEN I KEMI TFKE16. 2007-10-16 Lokal: TER2. Skrivtid: 14.00 18.00 nsvariga lärare: Nils-la Persson, tel. 1387, alt 070-517 1088. Stefan
Linköpings Universitet IFM-Kemi. Kemi för Y, M. m. fl. (TFKE16) TENTMEN I KEMI TFKE16. 2007-10-16 Lokal: TER2. Skrivtid: 14.00 18.00 nsvariga lärare: Nils-la Persson, tel. 1387, alt 070-517 1088. Stefan
Kursplan för kurs på grundnivå
 Kursplan för kurs på grundnivå Organisk kemi I Organic Chemistry I 7.5 Högskolepoäng 7.5 ECTS credits Kurskod: KO2003 Gäller från: HT 2017 Fastställd: 2016-11-21 Ändrad: 2017-08-18 Institution Institutionen
Kursplan för kurs på grundnivå Organisk kemi I Organic Chemistry I 7.5 Högskolepoäng 7.5 ECTS credits Kurskod: KO2003 Gäller från: HT 2017 Fastställd: 2016-11-21 Ändrad: 2017-08-18 Institution Institutionen
Tentamen i KEMI del B för Basåret GU (NBAK10) kl Institutionen för kemi, Göteborgs universitet
 Tentamen i KEMI del B för Basåret GU (NBAK10) 2007-03-23 kl. 08.30-13.30 Institutionen för kemi, Göteborgs universitet Lokal: örsalslängan A1, B1, B4 jälpmedel: Räknare valfri Ansvarig lärare: Leif olmlid
Tentamen i KEMI del B för Basåret GU (NBAK10) 2007-03-23 kl. 08.30-13.30 Institutionen för kemi, Göteborgs universitet Lokal: örsalslängan A1, B1, B4 jälpmedel: Räknare valfri Ansvarig lärare: Leif olmlid
dess energi ökar (S blir mer instabilt) TS sker tidigare i reaktionen strukturen på TS blir mer lik S (2p).
 Dugga 1 TFE44 2012 1. Vad innebär the Hammond postulate - om det finns ett instabilt intermediat under reaktionen, kommer transition state att likna strukturen av intermediatet (1p). Vad menas med the
Dugga 1 TFE44 2012 1. Vad innebär the Hammond postulate - om det finns ett instabilt intermediat under reaktionen, kommer transition state att likna strukturen av intermediatet (1p). Vad menas med the
TENTAMEN I ALLMÄN OCH ORGANISK KEMI
 KAROLINSKA INSTITUTET Bi omedic inutb ildningen TENTAMEN I ALLMÄN OCH ORGANISK KEMI TORSDAGEN DEN 20 december 2001, 08.30-11.00 och 12.00-14.30 Tentamen är uppdelad i två pass med en uppsättning frågor
KAROLINSKA INSTITUTET Bi omedic inutb ildningen TENTAMEN I ALLMÄN OCH ORGANISK KEMI TORSDAGEN DEN 20 december 2001, 08.30-11.00 och 12.00-14.30 Tentamen är uppdelad i två pass med en uppsättning frågor
Organiska föreningar Struktur- och stereoisomerer. Niklas Dahrén
 Organiska föreningar Struktur- och stereoisomerer Niklas Dahrén Olika typer av isomerer Kedjeisomerer ü Isomerer: Isomerer är ämnen som har samma summaformel/molekylformel men där molekylstrukturen skiljer
Organiska föreningar Struktur- och stereoisomerer Niklas Dahrén Olika typer av isomerer Kedjeisomerer ü Isomerer: Isomerer är ämnen som har samma summaformel/molekylformel men där molekylstrukturen skiljer
Skrivning i Oorganisk och organisk kemi för Bt3 och K2 KOK080, ,
 Kemi- och bioteknik, T 2012-03-07 1(14) Skrivning i organisk och organisk kemi för Bt3 och K2 KK080, 120310, 14.00-18.00 Lärare: Lars Öhrström, 2871, Jerker Mårtensson, Nina Kann jälpmedel: Molekylmodeller
Kemi- och bioteknik, T 2012-03-07 1(14) Skrivning i organisk och organisk kemi för Bt3 och K2 KK080, 120310, 14.00-18.00 Lärare: Lars Öhrström, 2871, Jerker Mårtensson, Nina Kann jälpmedel: Molekylmodeller
Kemiolympiaden 2014 En tävling i regi av Svenska Kemistsamfundet
 KEMILYMPIADE SVERIGE Kemiolympiaden 2014 En tävling i regi av Svenska Kemistsamfundet Till alla elever u är det dags för årets kemiolympiad. Kemiolympiaden är en tävling för gymnasieelever som inte fyllt
KEMILYMPIADE SVERIGE Kemiolympiaden 2014 En tävling i regi av Svenska Kemistsamfundet Till alla elever u är det dags för årets kemiolympiad. Kemiolympiaden är en tävling för gymnasieelever som inte fyllt
Namnge och rita organiska föreningar - del 2 Alkaner, alkener, alkyner. Niklas Dahrén
 Namnge och rita organiska föreningar - del 2 Alkaner, alkener, alkyner Niklas Dahrén Alkaner Alkaner är s.k. mättade kolväten vilket betyder att de har fullt med väteatomer (och därför enbart enkelbindningar).
Namnge och rita organiska föreningar - del 2 Alkaner, alkener, alkyner Niklas Dahrén Alkaner Alkaner är s.k. mättade kolväten vilket betyder att de har fullt med väteatomer (och därför enbart enkelbindningar).
TENTAMEN I ALLMÄN OCH ORGANISK KEMI: FACIT
 KALISKA ISTITUTET Biomedicinprogrammet TETAME I ALLMÄ GAISK KEMI: FAIT SDAGE DE 15 FEBUAI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för varje pass. Dessa
KALISKA ISTITUTET Biomedicinprogrammet TETAME I ALLMÄ GAISK KEMI: FAIT SDAGE DE 15 FEBUAI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för varje pass. Dessa
