Efterarbete: LÖSNINGSFÖRSLAG TILL UPPGIFTER - O +
|
|
|
- Gunnar Hermansson
- för 6 år sedan
- Visningar:
Transkript
1 Linköping IFM/Kemi Linköpings universitet TFKE51/GAN-SS Efterarbete: LÖSNINGSFÖRSLAG TILL UPPGIFTER Kap N - N N - + N 2. Den första resonansstrukturen är stabilast. Kom ihåg: Ju fler kovalenta bindningar ju stabilare. Strukturer där alla atomer har full oktett är särskilt stabila. Laddningsseparation minskar stabiliteten N 2 3 Övriga ej markerade har laddning = 0 Viktigt att: Rita korrekta Lewisstrukturer och att bokföra atomers formella laddning! 4. Att 4-metylfenol är en svagare syra än fenol kan förklaras med hjälp av induktiv effekt. Den induktiva effekten kan vara både elektronsugande och elektrondonerande. Metylgruppen i 4-metylfenol är svagt elektrondonerande och förstärker således elektrondensiteten i -bindningen. Starkare bindningen ger en svagare syra! Metylgruppen har också en destabiliserande effekt på anjonen I cyklohexanol är kolet som bär hydroxylgruppen sp 3 -hybridiserat. I fenol är motsvarande kol sp 2 -hybridiserat. sp 2- ybridiserade kolatomer är mer elektronegativa än sp 3 -hybridiserade kolatomer (har mer s-karaktär). Bensenringen i fenol är elektronsugande (induktiv effekt) vilket medför ökande syrastyrka (bindningen till protonen försvagas). Med resonans visas hur syret i fenol blir positivt.
2 Genom resonans stabiliseras anjonen av fenol (fenoxidjonen). Enligt resonansteorin stabiliseras anjonen mer av resonans än fenol. Något som stabiliserar anjonen gör syran surare! För cyklohexanol kan ingen resonans ritas! Resonansstrukturformler för fenoxidjonen: 6. ring-flip 3 cis-1,2-dimetylcyklohexan De båda stolkonformationerna ovan kommer ha samma potentiella energi, dvs vara lika stabila. I varje konformation sitter en metyl axiellt och en ekvatoriellt. Notera att cis betyder att substituenterna skall peka åt samma håll. Vid ring-flip behålls cis. Axiell blir ekvatoriell och tvärtom. 7. 1,3-diaxiell interaktion cis-1-tert-butyl-2-metylcyklohexan När tert-butyl gruppen sitter axiellt blir den 1,3-diaxiella interaktionen stor. Få molekyler är i den här konformationen. 1 ring-flip Stabilast av steriska skäl (utrymmes skäl)! ar den största substituenten i ekvatoriell position. Den steriska interaktionen minimeras.
3 8. Kap. 6 ring-flip Stabilase konformationen av trans - Mindre stabil konformation 1,2-dimetylcyklohexan. De båda då båda metylgrupperna sitter metylgrupperna sitter i ekvatoriell position. i axiell position. Större 1,3-diaxiell interaktion. Trans betyder att substituenterna skall peka åt motsatt håll. Konformationerna har inte samma energi Konformationerna har inte samma potentiella energi! Br N N 2 ( S ) ( S ) ( R ) Svårt att ta ut R och S när gruppen med lägst prioritet inte pekar in i papperet? är kommer ett tips! Antag att Du har följande stereoisomer av uppritad och skall bestämma R eller S Steg 2: Byt plats på två grupper = vi får spegelbilden. Byt så att pekar in i papperet. Inversion. Steg 3: För att få tillbaka den ursprungliga strukturen måste vi byta plats på ytterligare två grupper. Inversion. Två inversioner = retention, dvs tillbaka där vi startade. Steg 1: Prioritera atomerna runt stereocentret efter ökande atomnummer Vi får absolutkonfigurationen : R
4 2. 3. N (R) 4. a. 2,3-dibrombutan Finns som meso-form (se nedan) b. 2,3-dibrompentan Nej finns ej som meso-form c. 2,4-dibrompentan Finns som meso-form (se nedan) Nl (R) 2 2 5a. A Br Br Br Br A A oh finns i meso-form b. Enantiomerer (spegelbilder): A och B. Diastereomerer (stereoisomerer som inte är enantiomerer): A och eller B och. Mesoform: (har ett inre spegelplan). Racemisk blandning: en 50/50-blandning av enantiomerer A och B. Kap Alkohol Y kan erhållas från 2-metyl-2-buten genom addition av vatten till kol-kol dubbelbindningen under syrakatalys. Additionen följer Markovnikovs regel! Reaktionen går via den stabilaste karbokatjonen. Mekanism: Dubbelbindningen ("källa av elektroner") angriper ett väte. Vätet går till det alkenkol som redan har flest väten. Den stabilaste karbokatjonen bildas (här en tertiär). Vatten agerar sedan nukleofil med sitt syre (har två fria elektronpar) på det elektrofila kolet. En oxoniumjon bildas som till sist förlorar ett väte.
5 Alkohol X är en anti-markovnikov produkt. Den kan framställas genom en hydroborering/oxidation av 2-metyl-2-buten. Mekanism (BS! Ej fullständig). 2.
6 Kap. 5 Bensenringen som sitter direkt bunden till syreatomen kommer att reagera snabbast. Syreatomen verkar aktiverande på bensenringen och kan donera ett av sina fria elektronpar till ringen och stabilisera den intermediära areniumjon som bildas när attack sker i orto-och para-position.. För att lättare komma ihåg vilken position i bensenringen som skall reagera kan man med resonans visa vilka positioner på ringen som är elektronrika och alltså kan reagera med en elektrofil. 2. Monobromering ger följande produkter: 2 N Br Br Br + + Br 2 Br N 3. Av de givna föreningarna är fenol (se nedan) mest reaktiv i EAS. = Mest reaktiv = Minst reaktiv 4. Fenyl är inte meta-dirigerande. 5.
7 Kap ( ) 3 Br I Jodidjon är en mycket bra nukleofil (har negativ polariserande laddning. Reaktionen är av S N 2-typ. ( ) 3 I + Br Substratet är en sekundär alkylhalid. Brom är en bra lämnande grupp. Bindningen -Br är polariserad, vilket ger elektofilt kol för nuleofilen jodidjon att attackera. Produkten ritad i stabilaste konformation. I S N 2 attackerar Nu det elektronfattiga kolet från motsatt håll som lämnande grp. 2. Två mekanismer är inblandade! Tert-butylbromid kan bilda en stabil karbokatjon och bör alltså reagera enligt en S N 1. Karbokatjonen reagerar sedan med nukleofilen. De andra alkylhaliderna reagerar enligt en S N 2 mekanism där liten sterisk hindring i transition state är gynnsamt. Således reagerar metylbromid snabbare än etylbromid som i sin tur reagerar snabbare än isopropylbromid. Att denna substitutionsreaktion är långsammare än S N 1 kan förklaras med att nukleofilen är svag (dålig). I en S N 2 spelar nukleofilen en viktig roll när den sparkar ut lämnande gruppen från substratet och åstadkommer ett utbyte vid kol. 3. Polärt aprotiskt lösningsmedel är lämpligt att använda. Ett sådant lösningsmedel solvatiserar nukleofilens motjon (katjon) vilket innebär att nukleofilen blir fri att reagera (har inte sin negativa laddning upptagen i interaktioner med lösningsmedlet). Exempel på polära aprotiskt lösningsmedel är aceton och N,N-dimetylformamid (DMF). NaBr i aceton Katjonen solvatiseras Na Br Bromidjonen friare att agera som nukleofil 4. Reaktionshastigheten är endast beroende av konc. tert-butylbromid. Unimolekylär substitutionsreaktion S N 1. v = k [ tert-butylbromid ] Mekansim: 3 3 Br 3 + Br 3 3 Plan karbokatjon
8 5. E2 reaktionen kräver ett antiperiplant transition state där vätet som rycks av basen och L- gruppen (brom) sitter trans-diaxiellt. Det antiperiplana transition statet är staggered och har därmed lägre energi. I molekylen ovan finns således endast ett möjligt transdiaxiellt väte för basen att rycka och en produkt bildas. 6. Reaktion (b) kommer att gå bäst! Reaktionen är en S N 2. Substratet skall vara så litet som möjligt (liten sterisk hindring i transition state gynnsamt). Reaktion (a) kan ge betydande elimination enligt en E2 mekanism (natriummetoxid är en stark bas och substratet är grenat). Mekanism: Kap Trans-2-buten ger två signaler och etanol ger tre signaler i 1 -nmr. 2. (l 2 b ) 3 a Föreningen innehåller två kemiskt icke ekvivalenta väten ( a och b ) och ger alltså två signaler. a som har tre vätegrannar ger upphov till en kvartett och b (tre ekvivalenta väten) som har en vätegranne ger upphov till en dublett. (Signal splittning kap. 9.9). Då vätena b sitter vid två stycken elektronegativa kloratomer kommer signalen för b att ligga downfield (vid ett större värde på δ-skalan) medan signalen för a kommer att ligga upfield (vid ett mindre värde på δ-skalan 3. Du har erhållit följande spektroskopiska data av förening P (med summaformeln ). Summaformeln ger antal omättnader fem stycken IR absorption vid 1740 cm -1 Närvaro av karbonylgrupp (fig 13.7)
9 1 -nmr: δ (ppm) Splittning Antal och typ av 1.2 triplett har två grannar 3 är en som har en 2 till granne 3.5 singlett- har inga grannar 2 är en kvartett har tre grannar 2 är en 2 som sitter nära elektronegativ atom (syre). ar en 7.3 multiplett antal grannar svårt att bestämma Fragment: Ph-, - 2 -, - 2 och = till granne. 5 är aromatväten på monosubstituerad bensenring Svar: Förening P är etyl-2-fenyletanoat. Ph fenyletanol innehåller sex kemiskt icke ekvivalenta kolatomer och bör alltså ge upphov till sex signaler i ett 13 -nmr. I bensenringen finns fyra olika kol och i kolkedjan två olika. Kap Två faktorer spelar roll: a) Aldehydens karbonylkol är mer elektrofilt (elektronfattigt) än ketonens. Det beror på att ketonen har två alkylgrupper som genom induktiv effekt donerar elektrondensitet mot karbonylkolet medan aldehyden endast har en alkylgrupp som utövar induktiv effekt. Ketonen är av samma orsak stabilare än aldehyden. b) Steriska skäl. Karbonylkolet går från sp 2 till sp 3 vilket leder till trängsel i transition state vid addition. Aldehyden som har ett väte som en av grupperna runt kol gynnas även av steriska skäl. 2.
10 3.
11 Kap. 10 och Förening G med summaformeln har tio stycken omättnader. Givna startmaterial i uppgiften är bensaldehyd och fenylacetaldehyd. Reaktionsbetingelserna är natriumhydroxidlösning och rumstemperatur (25 o ). är gäller det att rita upp startmaterialen och se vad som kan hända. Identifiera eventuella nukleofiler och elektrofiler. Antal omättnader antyder två bensenringar (åtta omättnader), en karbonyl (eftersom vi har ett syre med i summaformeln) och en dubbelbindning. Mekanismen i ord: 1) ydroxidjonen rycker ett surt α väte i fenylacetaldehyd och en resonansstabiliserad enolatanjon (kolnukleofil) bildas. 2) Enolatanjonen angriper det elektrofila karbonylkolet i bensaldehyd och en alkoxidanjon bildas. 3) Alkoxidjonen (stark bas) rycker ett väte från vatten och en aldol bildas. 4) ydroxidjonen rycker till slut ett sista α väte, en dubbelbindning bildas mellan α och β kolet och hydroxidjon agerar lämnande grupp. En α,β omättad aldehyd bildas.
12 2. Rita upp estern och identifiera reaktionstypen! Svar: Produkterna är etanol och natriumpropanoat. Mekanismen i ord: 1) ydroxidjon (nukleofil) angriper det elektrofila karbonylkolet i estern - addition. 2) Karbonylkolet tillbakabildas under utspark av esterns lämnande grupp (alkoxidjonen) - elimination. Totalt en substitution vid acylkolet. 3) Alkoxidjonen (stark bas) rycker karboxylsyrans sura väte och en resonansstabiliserad karboxylatanjon och en alkohol bildas. 3. Etylacetoacetat kan användas när man vill framställa metylketoner (derivat av aceton). Syntesen utnyttjar β-ketoesterns sura α-väte/en för att bilda en anjon som kan mono -eller dialkyleras. Man säger att anjonen av etylacetoacetat är en syntetekvivalent till anjonen av aceton. Några problem med att använda aceton som startmeterial är bland annat att det åtgår en starkare bas för att bilda anjonen och att det finns risk för självkondensation. Etylacetoacetat framställs enkelt genom en självkondensation av etylacetat (kap. 11).
13 4. Dietylmalonat kan användas för att syntetisera substituerad ättiksyra. Anjonen av dietylmalonat är syntetekvivalent till esterenolaten av ättiksyra eller dianjonen av ättiksyra. Syntesen bygger på samma principer som uppgiften 3) ovan.
H 3 C. 5. Förklara varför fenol (se ovan) är en starkare syra än cyklohexanol (pk a =18).
 Linköping 12-08-15 IFM/Kemi Linköpings universitet TFKE06/GAN-ss Efterarbete av föreläsningar inom rganisk kemi 2 Uppgifter kap. 1-3 1. Rita resonansformler för N,N-dimetyl-3-aminopropenal! 3 3 N 2. Ange
Linköping 12-08-15 IFM/Kemi Linköpings universitet TFKE06/GAN-ss Efterarbete av föreläsningar inom rganisk kemi 2 Uppgifter kap. 1-3 1. Rita resonansformler för N,N-dimetyl-3-aminopropenal! 3 3 N 2. Ange
2. SUBSTITUTION (Nukleofil substitution) S N 2
 . SUBSTITUTION (Nukleofil substitution) Alkylhalider är generellt reaktiva pga att den elektronegativa haliden gör att bindningen till kol polariseras, man får en dipol. Kolet blir elektrofilt (elektronfattigare
. SUBSTITUTION (Nukleofil substitution) Alkylhalider är generellt reaktiva pga att den elektronegativa haliden gör att bindningen till kol polariseras, man får en dipol. Kolet blir elektrofilt (elektronfattigare
KARBOKATJON KARBANJON
 EAKTINE: Generella typer : 1. Addition Fö D-2010 (rowe Kap 17-18) 2. Substitution 3. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME Z MLYS + Z ADIKALE Z ETELYS KABKATJN + Z Vanligast + Z KABANJN
EAKTINE: Generella typer : 1. Addition Fö D-2010 (rowe Kap 17-18) 2. Substitution 3. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME Z MLYS + Z ADIKALE Z ETELYS KABKATJN + Z Vanligast + Z KABANJN
REAKTIONER : A. ADDITION Crowe p REAKTIONER: Del D-2009 Generella typer : 1. Addition 2. Substitution 3. Elimination 4.
 EAKTINE: Del D-009 Generella typer : 1. Addition. Substitution. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME rowe 1.-1. MYS ETEYS KABKATJN KABANJN eaktioner innebär att kovalenta bindningar
EAKTINE: Del D-009 Generella typer : 1. Addition. Substitution. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME rowe 1.-1. MYS ETEYS KABKATJN KABANJN eaktioner innebär att kovalenta bindningar
Tentamen i Organisk kemi AK 2/6 2005,
 Tentamen i rganisk kemi AK 2/6 2005, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: 3:a minst 40 poäng 4:a minst 55 poäng 5:a minst 75 poäng Skriv
Tentamen i rganisk kemi AK 2/6 2005, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: 3:a minst 40 poäng 4:a minst 55 poäng 5:a minst 75 poäng Skriv
Kemiska reaktioner: Olika reaktionstyper och reaktionsmekanismer. Niklas Dahrén
 Kemiska reaktioner: Olika reaktionstyper och reaktionsmekanismer Niklas Dahrén 7 olika reaktionstyper 1. Substitutionsreaktioner 2. Additionsreaktioner 3. Eliminationsreaktioner 4. Kondensationsreaktioner
Kemiska reaktioner: Olika reaktionstyper och reaktionsmekanismer Niklas Dahrén 7 olika reaktionstyper 1. Substitutionsreaktioner 2. Additionsreaktioner 3. Eliminationsreaktioner 4. Kondensationsreaktioner
Kiralitet former som är spegelbilder av varandra men ej identiska. Jämför med händer.
 Organisk kemi i denna kurs KIRALITET NUKLEOFIL SUBSTITUTION Föreläsning v17 Nina Kann v16 karbonylgruppens kemi =O v17 nukleofil substitution (alkylhaliders reaktivitet), kiralitet v18 alkener, karbokatjoner,
Organisk kemi i denna kurs KIRALITET NUKLEOFIL SUBSTITUTION Föreläsning v17 Nina Kann v16 karbonylgruppens kemi =O v17 nukleofil substitution (alkylhaliders reaktivitet), kiralitet v18 alkener, karbokatjoner,
1. Introduktion. Vad gör senapsgas så farlig?
 Föreläsning 9 Reaktionslära II Kapitel 9.1-9.6 1) Introduktion 2) Monomolekylära nukleofila substitutioner 3) Parametrar 4) Sammanfattning 5) Exempel 1. Introduktion Vad gör senapsgas så farlig? 2. Nukleofila
Föreläsning 9 Reaktionslära II Kapitel 9.1-9.6 1) Introduktion 2) Monomolekylära nukleofila substitutioner 3) Parametrar 4) Sammanfattning 5) Exempel 1. Introduktion Vad gör senapsgas så farlig? 2. Nukleofila
Inga hjälpmedel är tillåtna. 100 poäng
 rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2017 Tid: 9:00-13:00 Hjälpmedel: Inga
rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2017 Tid: 9:00-13:00 Hjälpmedel: Inga
Reaktionsmekanismer. Kap 6
 Reaktionsmekanismer Kap 6 Karbokatjoner är elektrofila intermediärer Innehåll Kvalitativa resonemang hur och varför kemiska reaktioner sker Exempel på energiomsättningar vid olika slags organiska reaktioner.
Reaktionsmekanismer Kap 6 Karbokatjoner är elektrofila intermediärer Innehåll Kvalitativa resonemang hur och varför kemiska reaktioner sker Exempel på energiomsättningar vid olika slags organiska reaktioner.
Föreläsning 10. Alkener I Kapitel 10 F10
 Föreläsning 10 Alkener I Kapitel 10 1) Introduktion 2) Monomolekylära eliminationer 3) Bimolekylära eliminationer 4) Alkyner 5) Sammanfattning av joniska reaktioner 6) Exempel 1. Introduktion Bimolekylär
Föreläsning 10 Alkener I Kapitel 10 1) Introduktion 2) Monomolekylära eliminationer 3) Bimolekylära eliminationer 4) Alkyner 5) Sammanfattning av joniska reaktioner 6) Exempel 1. Introduktion Bimolekylär
Kap 2 McMurry Viktiga Begrepp
 Kap 2 McMurry Viktiga Begrepp Funktionella grupper Alkaner Isomerer Nomenklatur Konformerer Sågbocks- och Newmanprojektioner Cykloalkaner Cis- och trans- Axiell och ekvatoriell Funktionella grupper En
Kap 2 McMurry Viktiga Begrepp Funktionella grupper Alkaner Isomerer Nomenklatur Konformerer Sågbocks- och Newmanprojektioner Cykloalkaner Cis- och trans- Axiell och ekvatoriell Funktionella grupper En
Valenselektroner = elektronerna i yttersta skalet visas nedan för några element ur grupperna
 Kapitel 9 är hittar du svar och lösningar till de övningsuppgifter som hänvisas till i inledningen. I vissa fall har lärobokens avsnitt Svar och anvisningar bedömts vara tillräckligt fylliga varför enbart
Kapitel 9 är hittar du svar och lösningar till de övningsuppgifter som hänvisas till i inledningen. I vissa fall har lärobokens avsnitt Svar och anvisningar bedömts vara tillräckligt fylliga varför enbart
TENTAMEN i ORGANISK KEMI 2 (TFKE06) ,
 TETAME i RGAISK KEMI 2 (TFKE06) 2012-10-23, 14.00-18.00 Lösningsförslag: 1. Vilken förening i respektive par a)-d) har surast väte? Ge kort förklaring till svaret. (10 p) a) b) F C 2 C Cl C 2 C c) d) 3
TETAME i RGAISK KEMI 2 (TFKE06) 2012-10-23, 14.00-18.00 Lösningsförslag: 1. Vilken förening i respektive par a)-d) har surast väte? Ge kort förklaring till svaret. (10 p) a) b) F C 2 C Cl C 2 C c) d) 3
Tentamen i Organisk kemi, 7.5 hp (KO3003) FACIT
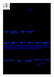 Tentamen i rganisk kemi, 7.5 hp (K3003) 1. (10 p) a) Ange om molekylerna 1 och/eller 2 är aromatiska. (1 p) b) Namnge föreningarna 1 och 2. (1 p) c) Vilken förening är starkast bas av 3 och 4? (2 p) d)
Tentamen i rganisk kemi, 7.5 hp (K3003) 1. (10 p) a) Ange om molekylerna 1 och/eller 2 är aromatiska. (1 p) b) Namnge föreningarna 1 och 2. (1 p) c) Vilken förening är starkast bas av 3 och 4? (2 p) d)
Olika typer av kolväten
 INTDUKTIN TILL GANISK KEMI KABNYLGUPPSKEMI Föreläsning v16 Nina Kann lika typer av kolväten alifatiska - alkaner - alkener - alkyner aromatiska 1 Funktionella grupper alken alkohol l alkylhalid S tiol
INTDUKTIN TILL GANISK KEMI KABNYLGUPPSKEMI Föreläsning v16 Nina Kann lika typer av kolväten alifatiska - alkaner - alkener - alkyner aromatiska 1 Funktionella grupper alken alkohol l alkylhalid S tiol
FUNKTIONELLA GRUPPER (Ämnesklasser) Fö
 FUNKTINELLA GUPPE (Ämnesklasser) Fö 3 2010 Ex. 32-l + 2 32- + l Kloretan Etanol Generellt: -l - = - Z = generell kolvätekedja (alkyl) Z= Funktionell grupp, Ex. -l, -, -, -N2 m.fl. 1. Föreningars egenskaper
FUNKTINELLA GUPPE (Ämnesklasser) Fö 3 2010 Ex. 32-l + 2 32- + l Kloretan Etanol Generellt: -l - = - Z = generell kolvätekedja (alkyl) Z= Funktionell grupp, Ex. -l, -, -, -N2 m.fl. 1. Föreningars egenskaper
Föreläsning 11. Alkener II Kapitel 11 F11
 Föreläsning 11 Alkener II Kapitel 11 1) Introduktion 2) Addition av elektrofila reagens 3) ydrogenering 4) ydroborering 5) Radikaladdition 6) Polymerisering 7) xidation 1. Introduktion ur gör man cancermedicinen
Föreläsning 11 Alkener II Kapitel 11 1) Introduktion 2) Addition av elektrofila reagens 3) ydrogenering 4) ydroborering 5) Radikaladdition 6) Polymerisering 7) xidation 1. Introduktion ur gör man cancermedicinen
Lösningsförslag: Tentamen i Organisk kemi 2, TFKE06,
 Lösningsförslag: Tentamen i rganisk kemi 2, TFKE06, 2009-10-23 1.a) Vilken förening i följande par har surast väte? Ge kort förklaring till svaret. (2 p/delsvar) a) F 2 l 2 2 3 c) d) a) Fluoriden mer elektronegativ
Lösningsförslag: Tentamen i rganisk kemi 2, TFKE06, 2009-10-23 1.a) Vilken förening i följande par har surast väte? Ge kort förklaring till svaret. (2 p/delsvar) a) F 2 l 2 2 3 c) d) a) Fluoriden mer elektronegativ
Svar: Tentamen i Organisk kemi 2, TFKE06, ,
 Svar: Tentamen i rganisk kemi 2, TFKE06, 2008-10-21, 1 a) Vilka av dessa heterocykliska föreningar är aromatiska? (2 p) S N N romatisk nti aromatisk nti aromatisk romatisk ückels regel: 4n + 2 elektroner
Svar: Tentamen i rganisk kemi 2, TFKE06, 2008-10-21, 1 a) Vilka av dessa heterocykliska föreningar är aromatiska? (2 p) S N N romatisk nti aromatisk nti aromatisk romatisk ückels regel: 4n + 2 elektroner
Reaktionsmekanismer. Kap 6
 Reaktionsmekanismer Kap 6 Rep. Kemiska reaktioner https://laughingsquid.com/a-ted-ed-animation-explaining-howall-sorts-of-different-chemical-reactions-are-triggered/ Karbokatjoner är elektrofila intermediärer
Reaktionsmekanismer Kap 6 Rep. Kemiska reaktioner https://laughingsquid.com/a-ted-ed-animation-explaining-howall-sorts-of-different-chemical-reactions-are-triggered/ Karbokatjoner är elektrofila intermediärer
Reaktionsmekanismer. Niklas Dahrén
 Reaktionsmekanismer Niklas Dahrén 7 olika reaktionstyper 1. Subs'tu'onsreak'oner 2. Addi'onsreak'oner 3. Elimina'onsreak'oner 4. Syra-bas-reak'oner 5. Kondensa'onsreak'oner 6. Hydrolysreak'oner 7. Redoxreak'oner
Reaktionsmekanismer Niklas Dahrén 7 olika reaktionstyper 1. Subs'tu'onsreak'oner 2. Addi'onsreak'oner 3. Elimina'onsreak'oner 4. Syra-bas-reak'oner 5. Kondensa'onsreak'oner 6. Hydrolysreak'oner 7. Redoxreak'oner
Inga hjälpmedel är tillåtna. För att få godkänd kurs måste man få minst 40 poäng på examen.
 Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Bt11-Bt2 7,5 högskolepoäng NAMN Personnummer Tentamensdatum: 28 augusti 2012 Tid: 09.00 13.00 Hjälpmedel: Inga hjälpmedel är tillåtna Totalt
Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Bt11-Bt2 7,5 högskolepoäng NAMN Personnummer Tentamensdatum: 28 augusti 2012 Tid: 09.00 13.00 Hjälpmedel: Inga hjälpmedel är tillåtna Totalt
7,5 högskolepoäng. Organisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik.
 rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2018 Tid: 9:00-13:00 Hjälpmedel: Inga
rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2018 Tid: 9:00-13:00 Hjälpmedel: Inga
Inga hjälpmedel är tillåtna. 100 poäng
 rganisk kemi Provmoment: Ladokkod: Tentamen ges för: Tentamen A100TG Tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 15 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel är tillåtna
rganisk kemi Provmoment: Ladokkod: Tentamen ges för: Tentamen A100TG Tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 15 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel är tillåtna
TK061B Tillämpad bioteknik, antagna 2012, Inga hjälpmedel är tillåtna. 100 poäng
 Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Tillämpad bioteknik, antagna 2012, 2013 7,5 högskolepoäng TentamensKod: Tentamensdatum: 11 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel
Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Tillämpad bioteknik, antagna 2012, 2013 7,5 högskolepoäng TentamensKod: Tentamensdatum: 11 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel
Föreläsning 16. Karbonylkolets kemi I Kapitel 16 F16
 Föreläsning 16 Karbonylkolets kemi I Kapitel 16 1) Introduktion 2) Addition av nukleofiler till karbonylgrupper A) Addition av hydridjoner B) Addition av metallorganiska reagens C) Addition av alkoholer
Föreläsning 16 Karbonylkolets kemi I Kapitel 16 1) Introduktion 2) Addition av nukleofiler till karbonylgrupper A) Addition av hydridjoner B) Addition av metallorganiska reagens C) Addition av alkoholer
LARS ERIK ANDREAS EHNBOM
 GAISK KEMI FÖELÄSIGA T 06 LAS EIK ADEAS EBM rganisk kemi - kolföreningarnas kemi * kan framställas från organismer (1828) * behövdes ingen livskraft (1860) Kolföreningar består av ett kolskelett Grupp,
GAISK KEMI FÖELÄSIGA T 06 LAS EIK ADEAS EBM rganisk kemi - kolföreningarnas kemi * kan framställas från organismer (1828) * behövdes ingen livskraft (1860) Kolföreningar består av ett kolskelett Grupp,
Namnge och rita organiska föreningar - del 5
 Namnge och rita organiska föreningar - del 5 Etrar, aldehyder, ketoner, tioler, fenoler, nitroföreningar, aminer, amider Niklas Dahrén Etrar Etrar har en etergrupp: Vid namngivning lägger man till ändelsen
Namnge och rita organiska föreningar - del 5 Etrar, aldehyder, ketoner, tioler, fenoler, nitroföreningar, aminer, amider Niklas Dahrén Etrar Etrar har en etergrupp: Vid namngivning lägger man till ändelsen
Tentamen i Organisk kemi 28/5 2013,
 Tentamen i rganisk kemi 28/5 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: Lycka till! /Ulf -fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p
Tentamen i rganisk kemi 28/5 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: Lycka till! /Ulf -fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p
Föreläsning 8. Reaktionslära I Kapitel
 Föreläsning 8 Reaktionslära I Kapitel 9.1-9.3 1) Introduktion 2) Nukleofila substitutioner 3) Parametrar 4) Praktisk användning 5) Elektrofiler och biologi 1. Introduktion Varför gråter vi när vi hackar
Föreläsning 8 Reaktionslära I Kapitel 9.1-9.3 1) Introduktion 2) Nukleofila substitutioner 3) Parametrar 4) Praktisk användning 5) Elektrofiler och biologi 1. Introduktion Varför gråter vi när vi hackar
Tentamen i Organisk kemi 16/ ,
 Tentamen i rganisk kemi 16/12 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p 5 75-90p 1) Besvara
Tentamen i rganisk kemi 16/12 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p 5 75-90p 1) Besvara
ALDEHYDER och KETONER Del D-2007
 ALDEYDE och KETNE Del D-2007 Karbonyl grupp: -# +# dipol, sp 2, 120 o vinkel Aldehyd ändelse: - al metanal formaldehyd 3 etanal acetaldehyd 3 2 propanal propionaldehyd bensaldehyd akrolein mrering av kolkedja:
ALDEYDE och KETNE Del D-2007 Karbonyl grupp: -# +# dipol, sp 2, 120 o vinkel Aldehyd ändelse: - al metanal formaldehyd 3 etanal acetaldehyd 3 2 propanal propionaldehyd bensaldehyd akrolein mrering av kolkedja:
Tentamen i Organisk kemi 25/5 2011,
 Tentamen i rganisk kemi 25/5 2011, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak ECTS LT (T) G 40-59p E 40-41p 3 40-54p VG 60-90p D 42-50p
Tentamen i rganisk kemi 25/5 2011, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak ECTS LT (T) G 40-59p E 40-41p 3 40-54p VG 60-90p D 42-50p
Organiska ämnen (2) s
 Organiska ämnen (2) s126-154 Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar lätt med andra ämnen. (p g a den elektronegativa halogenatomen) används
Organiska ämnen (2) s126-154 Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar lätt med andra ämnen. (p g a den elektronegativa halogenatomen) används
Föreläsning 12. Alkener III Kapitel 12 F12
 Föreläsning 12 Alkener III Kapitel 12 1) Introduktion 2) Allyliska system 3) Fleromättade kolväten 4) Färg och seende 5) Reaktioner 6) Sammanfattning och framåtblick 1. Introduktion Varför ser man bättre
Föreläsning 12 Alkener III Kapitel 12 1) Introduktion 2) Allyliska system 3) Fleromättade kolväten 4) Färg och seende 5) Reaktioner 6) Sammanfattning och framåtblick 1. Introduktion Varför ser man bättre
Organisk kemi AK KOK Ulf Ellervik
 rganisk kemi AK KK012 2013-01-29 Ulf Ellervik Föreläsning 3 Kolvätens egenskaper Kapitel 4 1) Introduktion 2) Konformationsanalys 3) Sura kolväten 4) Kolvätens reaktioner 1. Introduktion Vad händer egentligen
rganisk kemi AK KK012 2013-01-29 Ulf Ellervik Föreläsning 3 Kolvätens egenskaper Kapitel 4 1) Introduktion 2) Konformationsanalys 3) Sura kolväten 4) Kolvätens reaktioner 1. Introduktion Vad händer egentligen
Föreläsning 4. Substituerade kolväten Kapitel 5
 Föreläsning 4 Substituerade kolväten Kapitel 5 1) Introduktion 2) eteroatomer 3) Nomenklatur 4) Krafter mellan molekyler 5) Elektroniska modeller 6) Egenskaper hos molekyler 1. Introduktion Det afrikanska
Föreläsning 4 Substituerade kolväten Kapitel 5 1) Introduktion 2) eteroatomer 3) Nomenklatur 4) Krafter mellan molekyler 5) Elektroniska modeller 6) Egenskaper hos molekyler 1. Introduktion Det afrikanska
Kapitel 2. Kovalent bindning
 Kapitel 2. Kovalent bindning 2.1 Instuderingsfrågor 2.1.1 Rangordna kväve, fluor, syre, kol och väte efter stigande elektronegativitet. 2.1.2 Vad menas med induktiv effekt? 2.1.3 Vad menas med dipolmoment?
Kapitel 2. Kovalent bindning 2.1 Instuderingsfrågor 2.1.1 Rangordna kväve, fluor, syre, kol och väte efter stigande elektronegativitet. 2.1.2 Vad menas med induktiv effekt? 2.1.3 Vad menas med dipolmoment?
Organiska ämnen (2) s
 Organiska ämnen (2) s126-154 Organiska stamträdet Ämnesklasser- reaktionstyper/reaktionsvägar) Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar
Organiska ämnen (2) s126-154 Organiska stamträdet Ämnesklasser- reaktionstyper/reaktionsvägar) Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar
Omättade kolväten med dubbelbindning Generell formel: CnH2n Ändelsen -an ändras till -en
 ALKENER mättade kolväten med dubbelbindning Generell formel: n2n Ändelsen -an ändras till -en Del B ETEN (etylen) Plan struktur med 120 o vinkel sp 2 -hybridisering av 2s 2px 2py 3 st. sp 2 -orbitaler
ALKENER mättade kolväten med dubbelbindning Generell formel: n2n Ändelsen -an ändras till -en Del B ETEN (etylen) Plan struktur med 120 o vinkel sp 2 -hybridisering av 2s 2px 2py 3 st. sp 2 -orbitaler
2. Transitions state theory för att jämföra relativa reaktiviteten hos olika substrat
 2. Transitions state theory för att jämföra relativa reaktiviteten hos olika substrat Ex: baskatalyserad hydrolys av en ester jmf substraten p-nitrofenylacetat och fenylacetat OH - attackerar karbonylkolet
2. Transitions state theory för att jämföra relativa reaktiviteten hos olika substrat Ex: baskatalyserad hydrolys av en ester jmf substraten p-nitrofenylacetat och fenylacetat OH - attackerar karbonylkolet
Namnge och rita organiska föreningar - del 4 Alkoholer, karboxylsyror och estrar. Niklas Dahrén
 Namnge och rita organiska föreningar - del 4 Alkoholer, karboxylsyror och estrar Niklas Dahrén Alkoholer är kolväten med en eller flera OH-grupper Alkoholer innehåller OH-grupper: Om man byter ut en av
Namnge och rita organiska föreningar - del 4 Alkoholer, karboxylsyror och estrar Niklas Dahrén Alkoholer är kolväten med en eller flera OH-grupper Alkoholer innehåller OH-grupper: Om man byter ut en av
KEMA00. Magnus Ullner. Föreläsningsanteckningar och säkerhetskompendium kan laddas ner från
 KEMA00 Magnus Ullner Föreläsningsanteckningar och säkerhetskompendium kan laddas ner från http://www.kemi.lu.se/utbildning/grund/kema00/dold Användarnamn: Kema00 Lösenord: DeltaH0 Repetition F2 Vågfunktion
KEMA00 Magnus Ullner Föreläsningsanteckningar och säkerhetskompendium kan laddas ner från http://www.kemi.lu.se/utbildning/grund/kema00/dold Användarnamn: Kema00 Lösenord: DeltaH0 Repetition F2 Vågfunktion
Lösning till Tentamen i Kemi (TFKE16),
 Lösning till Tentamen i Kemi (TFKE16), 091017. 1. a) KN Mn 2 b) krom(iii)sulfat alt. dikromtrisulfat (mindre bra) triarsenikpentanitrid alt. arsenik(v)nitrid c) +II +V +III +II 3 Fe 2+ + N 3 - + 4 + 3
Lösning till Tentamen i Kemi (TFKE16), 091017. 1. a) KN Mn 2 b) krom(iii)sulfat alt. dikromtrisulfat (mindre bra) triarsenikpentanitrid alt. arsenik(v)nitrid c) +II +V +III +II 3 Fe 2+ + N 3 - + 4 + 3
Föreläsning 5. Molekylers rymdgeometri, Dipolmoment, VSEPR-teori och hybridisering
 Föreläsning 5 Molekylers rymdgeometri, Dipolmoment, VSEPR-teori och hybridisering Fleratomiga molekylers geometri. (Kap. 8.1-4) Molekyler eller joner av typ XY n, där X = centralatom, Y = ligand Alla Y
Föreläsning 5 Molekylers rymdgeometri, Dipolmoment, VSEPR-teori och hybridisering Fleratomiga molekylers geometri. (Kap. 8.1-4) Molekyler eller joner av typ XY n, där X = centralatom, Y = ligand Alla Y
TENTAMEN I ALLMÄN OCH ORGANISK KEMI
 KAROLINSKA INSTITUTET Biomedicinprogrammet (Magister) TENTAMEN I ALLMÄN OCH ORGANISK KEMI FREDAGEN DEN 1 FEBRUARI 2008, 08.30-11.00 och 12.00-14.30 Tentamen är uppdelad i två pass med en uppsättning frågor
KAROLINSKA INSTITUTET Biomedicinprogrammet (Magister) TENTAMEN I ALLMÄN OCH ORGANISK KEMI FREDAGEN DEN 1 FEBRUARI 2008, 08.30-11.00 och 12.00-14.30 Tentamen är uppdelad i två pass med en uppsättning frågor
VIKTIGT ATT DU FYLLER I DETTA PÅ SAMTLIGA SIDOR SOM LÄMNAS IN!
 1. Vilket grundämne har följande elektroniska konfiguration: Which element has the following ground-state electronic configuration: 1s 2 2s 2 2p x 2p y 2p z? 1 kol / carbon kväve / nitrogen syre / oxygen
1. Vilket grundämne har följande elektroniska konfiguration: Which element has the following ground-state electronic configuration: 1s 2 2s 2 2p x 2p y 2p z? 1 kol / carbon kväve / nitrogen syre / oxygen
Föreläsning 14. Aromater II - elektrofil aromatisk substitution Kapitel 14 F14
 Föreläsning 14 Aromater II - elektrofil aromatisk substitution Kapitel 14 1) Introduktion 2) Generell reaktion 3) Framställning av elektrofiler 4) Påverkan av substituenter 5) Praktiska aspekter 1. Introduktion
Föreläsning 14 Aromater II - elektrofil aromatisk substitution Kapitel 14 1) Introduktion 2) Generell reaktion 3) Framställning av elektrofiler 4) Påverkan av substituenter 5) Praktiska aspekter 1. Introduktion
Föreläsning 3. Kolvätens egenskaper! Kapitel 3 och 4
 Kolvätens egenskaper Kapitel 3 och 4 Föreläsning 3 1) Introduktion 2) Mättade kolväten 3) Konformationsanalys 4) Omättade kolväten 5) Reaktivitet 1. Introduktion Vad händer egentligen här? Vad har det
Kolvätens egenskaper Kapitel 3 och 4 Föreläsning 3 1) Introduktion 2) Mättade kolväten 3) Konformationsanalys 4) Omättade kolväten 5) Reaktivitet 1. Introduktion Vad händer egentligen här? Vad har det
1 Ange lämpliga reagens till följande reaktioner. Inga mekanismer behövs.
 Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 31 maj 2005, kl. 08.00-14.00 Tillåtna hjälpmedel: molekylmodeller, miniräknare (periodiskt system och tabeller med bindingsstyrkor och pk a -värden är bifogade
Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 31 maj 2005, kl. 08.00-14.00 Tillåtna hjälpmedel: molekylmodeller, miniräknare (periodiskt system och tabeller med bindingsstyrkor och pk a -värden är bifogade
Kolföreningar. Oändliga variationsmöjligheter
 Kolföreningar Oändliga variationsmöjligheter 1 Mål med avsnittet När vi är färdiga med detta avsnitt skall du kunna: Förklara följande begrepp: alkaner, alkener, alkyner, cykloalkaner, arenor, substituenter
Kolföreningar Oändliga variationsmöjligheter 1 Mål med avsnittet När vi är färdiga med detta avsnitt skall du kunna: Förklara följande begrepp: alkaner, alkener, alkyner, cykloalkaner, arenor, substituenter
8.1 Se lärobokens svar och anvisningar. 8.2 Se lärobokens svar och anvisningar. 8.3 a) Skrivsättet innebär följande strukturformel
 Kapitel 8 är hittar du svar och lösningar till de övningsuppgifter som hänvisas till i inledningen. I vissa fall har lärobokens avsnitt Svar och anvisningar bedömts vara tillräckligt fylliga varför enbart
Kapitel 8 är hittar du svar och lösningar till de övningsuppgifter som hänvisas till i inledningen. I vissa fall har lärobokens avsnitt Svar och anvisningar bedömts vara tillräckligt fylliga varför enbart
TENTAMEN I ALLMÄN OCH ORGANISK KEMI: FACIT
 KALISKA ISTITUTET Biomedicinprogrammet TETAME I ALLMÄ GAISK KEMI: FAIT SDAGE DE 15 FEBUAI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för varje pass. Dessa
KALISKA ISTITUTET Biomedicinprogrammet TETAME I ALLMÄ GAISK KEMI: FAIT SDAGE DE 15 FEBUAI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för varje pass. Dessa
Tentamen i Organisk kemi (KEGA01/KEGAH0/KEGAO0/KEGAOO/KEGAAK) (KEGL01/BIGLN3) 20 januari 2016, kl
 Institutionen för ingenjörs- och kemivetenskaper Karlstads universitet Tentamen i Organisk kemi (KEGA01/KEGAH0/KEGAO0/KEGAOO/KEGAAK) (KEGL01/BIGLN3) 20 januari 2016, kl 08.15 13.15 Betygsgränser: respektive:
Institutionen för ingenjörs- och kemivetenskaper Karlstads universitet Tentamen i Organisk kemi (KEGA01/KEGAH0/KEGAO0/KEGAOO/KEGAAK) (KEGL01/BIGLN3) 20 januari 2016, kl 08.15 13.15 Betygsgränser: respektive:
Organiska föreningar del 5: Rita och namnge alkoholer, karboxylsyror och estrar. Niklas Dahrén
 Organiska föreningar del 5: Rita och namnge alkoholer, karboxylsyror och estrar Niklas Dahrén Alkoholer är organiska ämnen med en eller flera OH-grupper Alkoholer innehåller OH-grupper: Alkoholer är organiska
Organiska föreningar del 5: Rita och namnge alkoholer, karboxylsyror och estrar Niklas Dahrén Alkoholer är organiska ämnen med en eller flera OH-grupper Alkoholer innehåller OH-grupper: Alkoholer är organiska
Övningsuppgifter. till Ellervik, Sterner; Organisk Kemi. Studentlitteratur, 2004
 Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Karolina Larsson, Jakob Nilsson, Ulf Nilsson,
Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Karolina Larsson, Jakob Nilsson, Ulf Nilsson,
Namnge och rita organiska föreningar - del 3 Halogenalkaner, cykliska kolväten och arener. Niklas Dahrén
 Namnge och rita organiska föreningar - del 3 Halogenalkaner, cykliska kolväten och arener Niklas Dahrén Halogenalkaner (alkylhalogenider) En halogenalkan är en alkan där en eller flera av väteatomerna
Namnge och rita organiska föreningar - del 3 Halogenalkaner, cykliska kolväten och arener Niklas Dahrén Halogenalkaner (alkylhalogenider) En halogenalkan är en alkan där en eller flera av väteatomerna
Skrivning i Oorganisk och organisk kemi för Bt3 och K2 KOK081, , Lärare: Lars Öhrström, 2871, Jerker Mårtensson, Nina Kann
 Kemi- och bioteknik, T 2013-03-16 1(15) Skrivning i organisk och organisk kemi för Bt3 och K2 KK081, 130316, 08.30-12.30 Lärare: Lars Öhrström, 2871, Jerker Mårtensson, Nina Kann jälpmedel: Molekylmodeller
Kemi- och bioteknik, T 2013-03-16 1(15) Skrivning i organisk och organisk kemi för Bt3 och K2 KK081, 130316, 08.30-12.30 Lärare: Lars Öhrström, 2871, Jerker Mårtensson, Nina Kann jälpmedel: Molekylmodeller
Organiska ämnen (2) s
 Organiska ämnen (2) s126-154 Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar lätt med andra ämnen. (p g a den elektronegativa halogenatomen) används
Organiska ämnen (2) s126-154 Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar lätt med andra ämnen. (p g a den elektronegativa halogenatomen) används
Övningsuppgifter. till Ellervik, Sterner; Organisk Kemi. Studentlitteratur, 2004
 RGANISK KEMI Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Karolina Aplander, Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Jakob Nilsson,
RGANISK KEMI Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Karolina Aplander, Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Jakob Nilsson,
Kemisk bindning I, Chemical bonds A&J kap. 2
 Kemisk bindning I, Chemical bonds A&J kap. 2 Dagens Olika bindningstyper - Jonbindning - Kovalent bindning - Polär kovalent bindning - Metallbindning Elektronegativitet - Jonbindning eller kovalent bindning?
Kemisk bindning I, Chemical bonds A&J kap. 2 Dagens Olika bindningstyper - Jonbindning - Kovalent bindning - Polär kovalent bindning - Metallbindning Elektronegativitet - Jonbindning eller kovalent bindning?
ORGANISK KEMI. Enkel Dubbel Trippel. En liten jämförelse mellan:
 ORGANISK KEMI Fö12-2013/TFKE52 KOLFÖRENINGANRNAS KEMI Varför Organisk kemi? Alla växter och djur är uppbyggda av kemiska föreningar som innehåller grundämnet kol. För att kunna undersöka och förstå hur
ORGANISK KEMI Fö12-2013/TFKE52 KOLFÖRENINGANRNAS KEMI Varför Organisk kemi? Alla växter och djur är uppbyggda av kemiska föreningar som innehåller grundämnet kol. För att kunna undersöka och förstå hur
Tentamen i Organisk kemi- grundkurs 7.5 hp (KEMA01),
 Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA01), 13-08-19 1) Molekylmodeller är tillåtet hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA01), 13-08-19 1) Molekylmodeller är tillåtet hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
4. Organiska föreningars struktur
 4. Organiska föreningars struktur Organisk kemi Alla föreningar i den levande naturen är uppbyggda av kol (C). Många innehåller dessutom väte (H), syre (O), kväve (N), fosfor (P) och svavel (S). Den levande
4. Organiska föreningars struktur Organisk kemi Alla föreningar i den levande naturen är uppbyggda av kol (C). Många innehåller dessutom väte (H), syre (O), kväve (N), fosfor (P) och svavel (S). Den levande
Föreläsning 13. Aromater I Kapitel 13 F13. 1) Introduktion 2) Bensens struktur och egenskaper 3) Aromaticitet 4) Aromatiska föreningar
 Föreläsning 13 Aromater I Kapitel 13 1) Introduktion 2) Bensens struktur och egenskaper 3) Aromaticitet 4) Aromatiska föreningar 1. Introduktion π-system ger stabilisering allyliska radikaler och karbokatjoner
Föreläsning 13 Aromater I Kapitel 13 1) Introduktion 2) Bensens struktur och egenskaper 3) Aromaticitet 4) Aromatiska föreningar 1. Introduktion π-system ger stabilisering allyliska radikaler och karbokatjoner
Föreläsning 15. Aromater III - andra reaktioner Kapitel 15
 Föreläsning 15 Aromater III - andra reaktioner Kapitel 15 1) Introduktion 2) Sammanfattning av EAS 3) Aromatiska alkholer - fenoler 4) Aromatiska aminer 5) Aromatiska halider 6) Andra reaktioner 7) Praktiska
Föreläsning 15 Aromater III - andra reaktioner Kapitel 15 1) Introduktion 2) Sammanfattning av EAS 3) Aromatiska alkholer - fenoler 4) Aromatiska aminer 5) Aromatiska halider 6) Andra reaktioner 7) Praktiska
Organiska föreningar del 7: Rita och namnge fenoler, nitroföreningar och aminer. Niklas Dahrén
 Organiska föreningar del 7: Rita och namnge fenoler, nitroföreningar och aminer Niklas Dahrén Fenoler Fenoler är föreningar som har minst en OH-grupp (hydroxylgrupp/hydroxigrupp) bunden direkt till en
Organiska föreningar del 7: Rita och namnge fenoler, nitroföreningar och aminer Niklas Dahrén Fenoler Fenoler är föreningar som har minst en OH-grupp (hydroxylgrupp/hydroxigrupp) bunden direkt till en
Tentamen i organisk kemi, KOKA05, 5 hp, Måndagen den 1 juni 2009, 14.00-19.00.
 Tentamen i organisk kemi, KKA05, 5 hp, Måndagen den 1 juni 2009, 14.00-19.00. Molekylmodeller och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer
Tentamen i organisk kemi, KKA05, 5 hp, Måndagen den 1 juni 2009, 14.00-19.00. Molekylmodeller och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer
STEREOKEMI B C. alla objekt har en spegelbild KOKA05/ många objekt är inte identiska med sin spegelbild. har ingen spegelbild
 TEREKEMI KK05/15 2012 alla objekt har en spegelbild har ingen spegelbild D C B B C D många objekt är inte identiska med sin spegelbild definition kiral ett objekt som inte är identiskt (kan bringas att
TEREKEMI KK05/15 2012 alla objekt har en spegelbild har ingen spegelbild D C B B C D många objekt är inte identiska med sin spegelbild definition kiral ett objekt som inte är identiskt (kan bringas att
ALKOHOLER Del C Metanol. Etanol. 2-propanol isopropanol
 ALKLE Del C-2007 - Funktionell grupp - (alifatisk bunden) Derivat av kolväte där - byts ut mot - amnges genom att -ol läggs till motsvarande kolväte (-an -anol) C 3 Metanol C 3 C 2 C 3 C C 3 Etanol 2-propanol
ALKLE Del C-2007 - Funktionell grupp - (alifatisk bunden) Derivat av kolväte där - byts ut mot - amnges genom att -ol läggs till motsvarande kolväte (-an -anol) C 3 Metanol C 3 C 2 C 3 C C 3 Etanol 2-propanol
Vätebindningar och Hydro-FON-regeln. Niklas Dahrén
 Vätebindningar och Hydro-FON-regeln Niklas Dahrén Indelning av kemiska bindningar Jonbindning Bindningar mellan jonerna i en jonförening (salt) Kemiska bindningar Metallbindning Kovalenta bindningar Bindningar
Vätebindningar och Hydro-FON-regeln Niklas Dahrén Indelning av kemiska bindningar Jonbindning Bindningar mellan jonerna i en jonförening (salt) Kemiska bindningar Metallbindning Kovalenta bindningar Bindningar
Konc. i början 0.1M 0 0. Ändring -x +x +x. Konc. i jämvikt 0,10-x +x +x
 Lösning till tentamen 2013-02-28 för Grundläggande kemi 10 hp Sid 1(5) 1. CH 3 COO - (aq) + H 2 O (l) CH 3 COOH ( (aq) + OH - (aq) Konc. i början 0.1M 0 0 Ändring -x +x +x Konc. i jämvikt 0,10-x +x +x
Lösning till tentamen 2013-02-28 för Grundläggande kemi 10 hp Sid 1(5) 1. CH 3 COO - (aq) + H 2 O (l) CH 3 COOH ( (aq) + OH - (aq) Konc. i början 0.1M 0 0 Ändring -x +x +x Konc. i jämvikt 0,10-x +x +x
TENTAMEN i FYSIKALISK-ORGANISK KEMI 7,5 hp, NKEC , kl
 TENTAMEN i FYSIKALISK-RGANISK KEMI 7,5 hp, NKEC63. 2008-05-30, kl. 08.00-13.00 1. Följande epoxider reagerar med de reagens som anges för reaktionerna A D och ger givna utbyten och produktförhållanden.
TENTAMEN i FYSIKALISK-RGANISK KEMI 7,5 hp, NKEC63. 2008-05-30, kl. 08.00-13.00 1. Följande epoxider reagerar med de reagens som anges för reaktionerna A D och ger givna utbyten och produktförhållanden.
Tentamen i organisk kemi, KEMB01, 15 hp, fredagen den 13 januari 2012,
 Tentamen i organisk kemi, KEMB01, 15 hp, fredagen den 13 januari 2012, 9.00-15.00. Molekylmodeller, miniräknare, punktgruppstabell och spektroskopibok får medtagas. Var vänlig besvara endast en uppgift
Tentamen i organisk kemi, KEMB01, 15 hp, fredagen den 13 januari 2012, 9.00-15.00. Molekylmodeller, miniräknare, punktgruppstabell och spektroskopibok får medtagas. Var vänlig besvara endast en uppgift
Tentamen i Organisk kemi- grundkurs 7.5 hp (KEMA01),
 Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA0), 3-03-8 ) Molekylmodeller och är tillåtna hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA0), 3-03-8 ) Molekylmodeller och är tillåtna hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
Kapitel 1. Kemisk bindning
 Övningar Övningar Övningsuppgifterna följer läroboken. Till varje kapitel finns ett antal instuderingsfrågor. Exempel: 2.1.1. Efter instuderingsfrågorna kommer ett antal övningsuppgifter. Exempel: 2.2.1.
Övningar Övningar Övningsuppgifterna följer läroboken. Till varje kapitel finns ett antal instuderingsfrågor. Exempel: 2.1.1. Efter instuderingsfrågorna kommer ett antal övningsuppgifter. Exempel: 2.2.1.
TENTAMEN I ALLMÄN OCH ORGANISK KEMI: FACIT
 KALINSKA INSTITUTET Biomedicinutbildningen TENTAMEN I ALLMÄN C GANISK KEMI: FACIT MÅNDAGEN DEN 12 JANUAI 2004, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för
KALINSKA INSTITUTET Biomedicinutbildningen TENTAMEN I ALLMÄN C GANISK KEMI: FACIT MÅNDAGEN DEN 12 JANUAI 2004, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för
Vanliga flervärdiga alkoholer. 1,2,3-Propantriol Glycerol Ingår i fett (ogiftig) Etandiol Etylenglykol Antifrysvätska (giftig)
 Funktionella grp med Syre. Fö 6-2010 ALKLE - Funktionell grupp - (alifatisk bunden) Derivat av kolväte där - byts ut mot - Namnges genom att -ol läggs till motsvarande kolväte (-an -anol) 3 Metanol Träsprit
Funktionella grp med Syre. Fö 6-2010 ALKLE - Funktionell grupp - (alifatisk bunden) Derivat av kolväte där - byts ut mot - Namnges genom att -ol läggs till motsvarande kolväte (-an -anol) 3 Metanol Träsprit
Förslag på svar till skrivning i oorganisk och organisk kemi för Bt3 och K2, KOK080
 Kemi- och bioteknik, CT 10 mars, 2009 1(15) Förslag på svar till skrivning i oorganisk och organisk kemi för Bt3 och K2, KK080 Tid: Fredagen den 13 mars 2009, 14 00-18 00. Plats: Lärare:. Tel: 772 3071
Kemi- och bioteknik, CT 10 mars, 2009 1(15) Förslag på svar till skrivning i oorganisk och organisk kemi för Bt3 och K2, KK080 Tid: Fredagen den 13 mars 2009, 14 00-18 00. Plats: Lärare:. Tel: 772 3071
Efternamn:...Mapp nr.. OBS! TEXTA TYDLIGT! Förnamn:... Personnr:... Totalsumma: Resultat: OBS! MYCKET VIKTIGT!! FÖRSE VARJE SIDA MED MAPP NUMMER!
 KARLINSKA INSTITUTET Biomedicinprogrammet ALLMÄN RGANISK KEMI SKRIFTLIG RESTDUGGA 1 TISDAG DEN 12 NVEMBER 2012, KL. 8.30-10.00 Skrivningen ska inlämnas senast kl. 10.00. Efternamn:...Mapp nr.. BS! TEXTA
KARLINSKA INSTITUTET Biomedicinprogrammet ALLMÄN RGANISK KEMI SKRIFTLIG RESTDUGGA 1 TISDAG DEN 12 NVEMBER 2012, KL. 8.30-10.00 Skrivningen ska inlämnas senast kl. 10.00. Efternamn:...Mapp nr.. BS! TEXTA
Skrivning i Oorganisk och organisk kemi för Bt3 och K2, KOK080
 Kemi- och bioteknik, CT 12 mars, 2011 1(16) Skrivning i organisk och organisk kemi för Bt3 och K2, KK080 Tid: Lördagen den 19 mars 2011, kl 14-18. Plats: V Lärare: Nina Kann, tel: 0705 162172 eller anknytning
Kemi- och bioteknik, CT 12 mars, 2011 1(16) Skrivning i organisk och organisk kemi för Bt3 och K2, KK080 Tid: Lördagen den 19 mars 2011, kl 14-18. Plats: V Lärare: Nina Kann, tel: 0705 162172 eller anknytning
ORGANISK KEMI Fö
 KOLFÖRENINGANRNAS KEMI ORGANISK KEMI Fö 1-2 2010 Förr ansågs organiska föreningar vara sådana som endast kunde fås från växt-och djurriket. En speciell levande kraft ansågs råda s.k. vitalism, vilket gjorde
KOLFÖRENINGANRNAS KEMI ORGANISK KEMI Fö 1-2 2010 Förr ansågs organiska föreningar vara sådana som endast kunde fås från växt-och djurriket. En speciell levande kraft ansågs råda s.k. vitalism, vilket gjorde
F1 F d un t amen l a s KEMA00
 F1 F d t l F1 Fundamentals KEMA00 A Materia och Energi SI-enheter Mätosäkerhet Potentiell energi Ep = mgh Coulombs lag q1 q2 4 r E p 0 B Grundämnen och atomer Atomnummer z (antal atomer i kärnan) Masstal
F1 F d t l F1 Fundamentals KEMA00 A Materia och Energi SI-enheter Mätosäkerhet Potentiell energi Ep = mgh Coulombs lag q1 q2 4 r E p 0 B Grundämnen och atomer Atomnummer z (antal atomer i kärnan) Masstal
Organiska föreningar del 6: Rita och namnge etrar, aldehyder, ketoner, tioler och disulfider. Niklas Dahrén
 Organiska föreningar del 6: Rita och namnge etrar, aldehyder, ketoner, tioler och disulfider Niklas Dahrén Etrar Etrar har en etergrupp (eterbindning): R-grupperna är två identiska eller två olika kolvätegrupper/kolvätekedjor
Organiska föreningar del 6: Rita och namnge etrar, aldehyder, ketoner, tioler och disulfider Niklas Dahrén Etrar Etrar har en etergrupp (eterbindning): R-grupperna är två identiska eller två olika kolvätegrupper/kolvätekedjor
Polära och opolära ämnen, lösningsmedel och löslighet. Niklas Dahrén
 Polära och opolära ämnen, lösningsmedel och löslighet Niklas Dahrén Polära och opolära ämnen Polära ämnen/molekyler (dipoler): Polära ämnen är (i de flesta fall) dipoler, vilket innebär att en sida/del
Polära och opolära ämnen, lösningsmedel och löslighet Niklas Dahrén Polära och opolära ämnen Polära ämnen/molekyler (dipoler): Polära ämnen är (i de flesta fall) dipoler, vilket innebär att en sida/del
Tentamensuppgifter moment 2, organisk kemi.
 UMEÅ UIVERSITET TETAME Kemiska Institutionen Tentamensdatum 2012-01-19 BE, KP Studiekurs: Kemi för miljö- och hälsoskyddsområdet, 15 hp. Kurskod: KE004 Tentamen: Moment 2, organisk kemi (sid 1-3) och Moment
UMEÅ UIVERSITET TETAME Kemiska Institutionen Tentamensdatum 2012-01-19 BE, KP Studiekurs: Kemi för miljö- och hälsoskyddsområdet, 15 hp. Kurskod: KE004 Tentamen: Moment 2, organisk kemi (sid 1-3) och Moment
1.1.3 Hur många valenselektroner har kol, kväve, syre, fluor och neon? Vad menas med att ett system är kinetiskt stabilt?
 Övningar Övningar Övningsuppgifterna följer läroboken. Till varje kapitel finns ett antal instuderingsfrågor. Exempel: 2.1.1. Efter instuderingsfrågorna kommer ett antal övningsuppgifter. Exempel: 2.2.1.
Övningar Övningar Övningsuppgifterna följer läroboken. Till varje kapitel finns ett antal instuderingsfrågor. Exempel: 2.1.1. Efter instuderingsfrågorna kommer ett antal övningsuppgifter. Exempel: 2.2.1.
CH 3 N. metylamin dimetylamin trimetylamin tetrametylammonium jon primär sekundär!!!!!!!!!!!!! tertiär!!!!!!!!!!!kvartenär
 Funktionella grp med kväve, Fö 7-2010 AMIE - 2 amnges med alkyl följt av ordet amin. Indelning: metylamin dimetylamin trimetylamin tetrametylammonium jon primär sekundär!!!!!!!!!!!!! tertiär!!!!!!!!!!!kvartenär
Funktionella grp med kväve, Fö 7-2010 AMIE - 2 amnges med alkyl följt av ordet amin. Indelning: metylamin dimetylamin trimetylamin tetrametylammonium jon primär sekundär!!!!!!!!!!!!! tertiär!!!!!!!!!!!kvartenär
FUNKTIONELLA GRUPPER (Ämnesklasser)
 FUKTIELLA GUPPE (Ämnesklasser) Fö2-2011/EMM Ex. 32-l + 2 32- + l Kloretan Etanol Generellt: -l - = - Z = generell kolvätekedja (alkyl) eller Ar = aromat Z= Funktionell grupp, Ex. -l, -, -, -2 m.fl. 1.
FUKTIELLA GUPPE (Ämnesklasser) Fö2-2011/EMM Ex. 32-l + 2 32- + l Kloretan Etanol Generellt: -l - = - Z = generell kolvätekedja (alkyl) eller Ar = aromat Z= Funktionell grupp, Ex. -l, -, -, -2 m.fl. 1.
Alla papper, även kladdpapper lämnas tillbaka.
 Maxpoäng 66 g 13 vg 28 varav 4 p av uppg. 18,19,20,21 mvg 40 varav 9 p av uppg. 18,19,20,21 Alla papper, även kladdpapper lämnas tillbaka. 1 (2p) En oladdad atom innehåller 121 neutroner och 80 elektroner.
Maxpoäng 66 g 13 vg 28 varav 4 p av uppg. 18,19,20,21 mvg 40 varav 9 p av uppg. 18,19,20,21 Alla papper, även kladdpapper lämnas tillbaka. 1 (2p) En oladdad atom innehåller 121 neutroner och 80 elektroner.
Aromatiska föreningar
 Aromatiska föreningar och aromaticitet tiitt Dan Johnels Kemiska Institutionen Aromatiska föreningar och aromaticitet Vi har lärt oss att konjugation i linjära system alltid leder till stabilisering Om
Aromatiska föreningar och aromaticitet tiitt Dan Johnels Kemiska Institutionen Aromatiska föreningar och aromaticitet Vi har lärt oss att konjugation i linjära system alltid leder till stabilisering Om
TENTAMEN I ALLMÄN OCH ORGANISK KEMI
 KALISKA ISTITUTET Biomedicinutbildningen TETAME I ALLMÄ GAISK KEMI FAIT FEDAGE DE 13 JAUAI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för varje pass. Dessa
KALISKA ISTITUTET Biomedicinutbildningen TETAME I ALLMÄ GAISK KEMI FAIT FEDAGE DE 13 JAUAI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för varje pass. Dessa
ATOMENS BYGGNAD. En atom består av : Kärna ( hela massan finns i kärnan) Positiva Protoner Neutrala Neutroner. Runt om Negativa Elektroner
 periodiska systemet ATOMENS BYGGNAD En atom består av : Kärna ( hela massan finns i kärnan) Positiva Protoner Neutrala Neutroner Runt om Negativa Elektroner En Elektron har en negativt laddning. Och elektronerna
periodiska systemet ATOMENS BYGGNAD En atom består av : Kärna ( hela massan finns i kärnan) Positiva Protoner Neutrala Neutroner Runt om Negativa Elektroner En Elektron har en negativt laddning. Och elektronerna
Föreläsning 17. Karbonylkolets kemi II Kapitel 17 F17
 Föreläsning 17 Karbonylkolets kemi II Kapitel 17 1) Introduktion 2) Addition av starka nukleofiler 3) Estrar 4) Amider 5) Nitriler 6) Syraklorider 7) Praktisk användning 1. Introduktion Aldehyder och ketoner
Föreläsning 17 Karbonylkolets kemi II Kapitel 17 1) Introduktion 2) Addition av starka nukleofiler 3) Estrar 4) Amider 5) Nitriler 6) Syraklorider 7) Praktisk användning 1. Introduktion Aldehyder och ketoner
Intermolekylära krafter
 Intermolekylära krafter Medicinsk Teknik KTH Biologisk kemi Vt 2011 Märit Karls Intramolekylära attraktioner Atomer hålls ihop av elektrostatiska krafter mellan protoner och.elektroner Joner hålls ihop
Intermolekylära krafter Medicinsk Teknik KTH Biologisk kemi Vt 2011 Märit Karls Intramolekylära attraktioner Atomer hålls ihop av elektrostatiska krafter mellan protoner och.elektroner Joner hålls ihop
Syror, baser och ph-värde. Niklas Dahrén
 Syror, baser och ph-värde Niklas Dahrén Syror är protongivare Syror kännetecknas av följande: 1. De har förmåga att avge vätejoner, H + (protoner), vilket leder till en ph-sänkning. 2. De ger upphov till
Syror, baser och ph-värde Niklas Dahrén Syror är protongivare Syror kännetecknas av följande: 1. De har förmåga att avge vätejoner, H + (protoner), vilket leder till en ph-sänkning. 2. De ger upphov till
Totalt 10 uppgifter, vardera värd 10p (totalt 100p). För godkänt fordras minst 50p, för 4:a minst 66p och för 5:a minst 83p.
 Tentamen i rganisk Kemi 2 (3B1760) måndagen den 29 maj 2006, kl. 08.00-14.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor och pka-värden är bifogade efter frågorna
Tentamen i rganisk Kemi 2 (3B1760) måndagen den 29 maj 2006, kl. 08.00-14.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor och pka-värden är bifogade efter frågorna
Kap. 8. Bindning: Generella begrepp, fortsättning
 Kap. 8. Bindning: Generella begrepp, fortsättning 8.5 Energieffekter i binära joniska föreningar Faktorer som påverkar stabiliteten och strukturen för fasta binära joniska ämnen. Coulomb (elektrostatisk)
Kap. 8. Bindning: Generella begrepp, fortsättning 8.5 Energieffekter i binära joniska föreningar Faktorer som påverkar stabiliteten och strukturen för fasta binära joniska ämnen. Coulomb (elektrostatisk)
http://www.naturvetenskap.org/index.php?option=com_content&view=article&id=226&itemi d=236
 http://sv.wikipedia.org/wiki/petroleum http://www.naturvetenskap.org/index.php?option=com_content&view=article&id=226&itemi d=236 Alkaner C n H 2n+2 metan etan propan butan pentan hexan heptan oktan nonan
http://sv.wikipedia.org/wiki/petroleum http://www.naturvetenskap.org/index.php?option=com_content&view=article&id=226&itemi d=236 Alkaner C n H 2n+2 metan etan propan butan pentan hexan heptan oktan nonan
