Aminkatalyserad asymmetrisk Friedel-Crafts-alkylering
|
|
|
- Andreas Håkansson
- för 10 år sedan
- Visningar:
Transkript
1 Aminkatalyserad asymmetrisk Friedel-Crafts-alkylering Mika Berg Pro gradu Helsingfors Universitet Kemiska Institutionen Laboratoriet för svenskspråkig undervisning Februari 2014
2 Tiedekunta/Osasto Fakultet/Sektion Faculty Matematisk-naturvetenskapliga fakulteten Tekijä/Författare Author Laitos/Institution Department Kemiska institutionen Mika Berg Työn nimi / Arbetets titel Title Aminkatalyserad asymmetrisk Friedel-Crafts-alkylering Oppiaine /Läroämne Subject Organisk kemi Työn laji/arbetets art Level Pro gradu avhandling Tiivistelmä/Referat Abstract Aika/Datum Month and year Februari 2014 Sivumäärä/ Sidoantal Number of pages 77 Organokatalytisk asymmetrisk Friedel-Crafts-alkylering av olika aromatiska och heteroaromatiska nukleofiler med -omättade aldehyder och ketoner har visat sig vara en effektiv metod för att syntetisera olika grundstrukturer för viktiga biologiskt aktiva föreningar. Under det senaste årtiondet har forskningen inom detta område gått framåt med stora steg. Det var David W. C. MacMillan som startade utvecklingen av organokatalytisk asymmetrisk F-Calkylering då han presenterade den LUMO-sänkande iminaktiveringsmekanismen för första gången. Dessutom introducerade han första generationens imidazolidinon vilken visade hög katalytisk aktivitet i alkyleringsreaktioner av pyrroler med enaler. Trots detta fungerade katalysatorn inte vid indolalkylering p.g.a. steriska hinder vilket ledde till att en serie av förbättrade och nya katalysatorer har utvecklats. Andra generationens imidazolidinon och diarylprolinoletrar har alla visat sig vara bra och effektiva alternativ för asymmetriska F-C-alkyleringar av indoler med enaler. Förutom indoler har dessa använts för att katalysera också reaktioner med aniliner, naftoler och furanderivat. Resultaten har varit mycket bra både med avseende på utbyte och enantioselektivitet. En annan typ av katalysatorer som härstammar från de naturligt förekommande cinkona-alkaloiderna har också introducerats. Dessa primära aminer är speciellt användbara i reaktioner där mera sterisk hindrande -omättade ketoner används istället för aldehyder. Resultaten var även i dessa reaktioner bra och riktgivande för vidare forskning. Andra mindre undersökta och använda organokatalysatorer är bl. a. imidazoltioner och (3-metylaziridin-2-yl)-difenylmetanoler. I framtiden kommer organokatalysatorer att användas allt mer i asymmetriska F-C-reaktioner. Resultaten som erhållits så här långt ger möjlighet att kombinera dessa nya billigare alternativ till de tidigare använda dyra instabila metallkomplexen. Detta minskar på användningen av de svårhanterliga toxiska metallföreningarna och gör synteserna miljövänligare. Organokatalysatorerna är stabila och icke-toxiska vid rumsbetingelser och därmed lätt att använda i alkyleringsreaktioner. Detta är speciellt viktigt vid syntes av läkemedelsderivat och naturprodukter. Detta kommer att vara ett av de viktigaste tillämpningsområdena där organokatalytisk F-C-alkylering används. Avainsanat Nyckelord Keywords Organokatalytisk, Asymmetrisk, Friedel-Crafts-alkylering, Imidazolidinoner, LUMO-sänkande, Iminaktivering Säilytyspaikka Förvaringställe Where deposited Kemiska institutionen, Laboratoriet för svenskspråkig undervisning Muita tietoja Övriga uppgifter Additional information Handledare: Bertel Westermark
3 Innehållsförteckning 1. Inledning Olika organokatalysatorer Imidazolidinoner Derivat av prolin Derivat av cinkona-alkaloider Friedel-Crafts-alkyleringar av olika aromatiska nukleofiler Alkylering av pyrroler Alkylering av indoler Alkylering av aniliner Alkylering av naftoler, bensofuraner och furaner Experiment Syntesrutt Synteser och karaktärisering Resultat och diskussion Sammanfattning Förkortningar och akronymer Referenser...72
4 1. Inledning Friedel-Crafts-alkylering (F-C) är en av de äldsta organiska syntesmetoderna som fortfarande används. F-C-reaktionen uppfanns år 1877 och har sedan dess använts för att bilda viktiga organiska byggklossar inom synteskemin. Denna metod är ett av de mest kraftfulla sätten att bilda nya C-C-bindningar till -aromatiska och heteroaromatiska föreningar. 1 Till en början utfördes reaktionen i närvaro av en stökiometrisk mängd Lewissyra. Senare har man försökt hitta mildare och miljövänligare metoder. Det tog ca. hundra år innan man upptäckte de första katalytiska och asymmetriska varianterna av denna reaktion. I mitten av 1980-talet presenterades de första metallkatalyserade F-Creaktionerna där aromatiska föreningar adderades till elektronfattiga -system, se bild 1. Efter det har man försökt hitta nya och effektivare sätt att göra samma omvandlingar. 2 Bild 1. Metall- och organokatalyserad asymmetrisk Friedel-Crafts-alkylering. David W. C. MacMillan var den som år 2001 gjorde genombrottet inom organokatalytisk asymmetrisk F-C-alkylering, bild 1, då han alkylerade pyrrol med krotonaldehyd där en sekundär amin, imidazolidinon, fungerade som katalysator. Imidazolidinonen uppvisade en stark katalytisk aktivitet i dessa alkyleringsreaktioner 3. Detta krävde dock en djupare insikt i aktiveringsmekanismen. Pionjären MacMillan hade ett år tidigare presenterat en LUMOsänkande iminaktiveringsmekanism i organokatalytiska Diels-Alder-cykloadditioner 4. Mekanismen baserar sig på reversibel bildning av en iminiumintermediär där aminkatalysatorn aktiverar den -omättade karbonylföreningen. Därmed sänks iminiumintermediärens energinivå för den lägsta obesatta molekylorbitalen (LUMO). Efter att addition av nukleofilen till iminiumintermediären har skett kan katalysatorn dissocieras från produkten och återanvändas. Samma mekanism har tillämpats på de organokatalytiska 1
5 F-C-alkyleringarna med stor framgång. Denna upptäckt var ett stort framsteg för de metallfria asymmetriska F-C-alkyleringarna. Då utbytena samt selektiviteterna visat sig vara höga och jämförbara med motsvarande resultat från de metallkatalyserade alkyleringsreaktionerna kan den metallkatalyserade reaktionen till en del ersättas med den organokatalytiska metoden. Forskningen inom detta område har under senare år gått framåt med stora steg och i dag har metoden använts i många olika alkyleringsreaktioner 3. Under det senaste årtiondet har förutom MacMillans imidazolidinoner också andra organiska katalysatorer introducerats 5, se bild 2. Bild 2. Olika organokatalysatorer. Speciellt användbara är diarylprolinoletrarna 1 och derivat av de naturligt förekommande cinkona-alkaloiderna 1. Gemensamt för alla katalysatorer är grundaktiveringen som följer den LUMO-sänkande iminbildningsmekanismen. Jämfört med metallkatalysatorerna är fördelen med alla dessa organiska katalysatorer deras stabilitet i aerobiska förhållanden och fuktiga lösningsmedel 3. Dessutom är dessa icke-toxiska organokatalysatorer betydligt billigare och stabilare än de flesta metallkatalysatorerna 6. Imidazolidinonerna och diarylprolinoletrarna har använts i olika F-C-alkyleringar av aromatiska föreningar med -omättade aldehyder, medan cinkona-alkaloidderivaten har använts i reaktioner med -omättade ketoner 7. Till en början gjordes alkyleringsreaktionerna endast på de mest reaktiva aromatiska nukleofilerna, pyrrolerna. När processen utvecklats har valmöjligheten av nukleofilen också ökat. 2
6 De -aromatiska och heteroaromatiska föreningarna beter sig som C-nukleofiler och deltar i organokatalytisk asymmetrisk Friedel-Crafts-substitution med enaler och enoner. Speciellt viktiga och mycket undersökta är pyrrolernas och indolernas alkyleringar 8. Pyrrol- och indolstrukturen är grundbyggstenar i många kirala biologiskt aktiva föreningar och läkemedel. Detta skapar ett behov av att utveckla den metallfria enantioselektiva metoden för framställning av dessa syntoner 9. Senare har man tillämpat den organokatalytiska F-C-alkyleringen också på andra nukleofiler som aniliner, naftoler, furaner och bensofuraner. Resultaten har varit lovande. Metoden kommer säkert att förbättras och utvecklas i framtiden. 3
7 2. Olika organokatalysatorer I detta kapitel diskuteras olika primära samt sekundära amin- och diaminkatalysatorer. Dessutom presenteras katalysatorernas aktiveringsmekanismer i de asymmetriska Friedel- Crafts-alkyleringarna. De viktigaste aminkatalysatorerna i dessa omvandlingar är MacMillans imidazolidinoner, diarylprolinoletrarna samt derivat av cinkona-alkaloiderna. Den vanligaste mekanismen i F-C-reaktionerna är den LUMO-sänkande iminaktiveringen. Den har senare utvecklats för imidazolidinoner till en imin/enamin kaskadaktivering för att kunna framställa mera komplicerade slutprodukter. Diarylprolinoleterkatalyserade F-Creaktionerna aktiveras med en bifunktionell mekanism där vätebindning kombineras med den LUMO-sänkande iminaktiveringen. Detta förbättrar reaktionens resultat genom förhöjt utbyte och selektivitet. 2.1 Imidazolidinoner Imidazolidinonerna är heterocykliska föreningar som kan framställas från olika aminosyror. Två olika katalysatorer som härstammar från aminosyran L-fenylalanin har introducerats: MacMillans första, 1, och andra, 2, generationens imidazolidinon, se bild Bild 3. MacMillans imidazolidinonkatalysatorer. Imidazolidinonerna har utnyttjats vid olika asymmetriska transformationer t.ex. i Friedel- Crafts-alkyleringar. Katalysatorns, 3, uppgift är att aktivera elektrofilen, den -omättade aldehyden, genom att bilda en iminiumintermediär, 4. Kokatalysatorn X, ofta en syra, bör vara närvarande för att aktiveringen skall kunna ske. Intermediären 4 kan sedan attackeras selektivt av en aromatiska nukleofil för att bilda enaminintermediären 5 och vidare iminiumintermediären 6. Den slutliga enantiomert rena F-C-alkyleringsprodukten, 7, bildas efter hydrolys av intermediären 6. Denna mekanism, se schema 1, kallas för LUMO- 4
8 sänkande iminaktivering och har senare blivit ett viktigt koncept inom hela organokatalysatorkemin. 8 Schema 1 Selektiviteten i alkyleringen beror främst på iminiumintermediärens struktur och valet av nukleofil. Speciellt avgörande är intermediärens C2- och C5-substituenter som härstammar från ursprungskatalysatorn. Då imidazolidinonen 1 används i F-C-alkylering av pyrroler med -omättade aldehyder bildas först iminiumintermediärens (E)-isomer. Pyrrolen kan därefter attackera intermediärens -position från den öppna Re-sidan. Si-sidan är blockerad av imidazolidinonens C5-bensylgrupp vilket leder till att en hög stereoselektivitet för produkten kan uppnås 10. Dålig reaktivitet erhölls då nukleofilen byttes ut till de mindre reaktiva och steriskt mera hindrade indolerna. Detta beror på att gemmetylgruppen i 1 steriskt hindrar addition av indolen till iminiumintermediärens - position. MacMillans grupp gjorde modifikationer på första generationens katalysator och syntetiserade 2 där C2- och C5-substituenterna är på samma sida. Detta innebär att ingen steriskt repulsion mellan C2-substituenten och nukleofilen förekommer. Indolalkyleringsprodukterna kan alltså fås i höga utbyten och enantioselektiviteter när man 5
9 använde MacMillans förbättrade andra generationens imidazolidinonkatalysator 11. Olika imidazolidinonananloger, imidazoltioner 8 och 5-indolylimidazolidinoner 9, se bild 4, har senare framställts för att undersöka och hitta katalysatorer med ännu högre aktivitet och selektivitet i de olika F-C-alkyleringarna. Bild 4. Modifierade imidazolidinonkatalysatorer. MacMillans forskningsgrupp 12 utvecklade år 2005 en ny s.k. kaskadreaktion där den från tidigare kända iminaktiveringen kombineras med ett nytt HOMO-höjande enaminsteg, se schema 2. Den första alkyleringsprodukten aktiveras av katalysatorn och bildar en nukleofil enamin med höjd energinivå för den högsta besatta molekylorbitalen (HOMO). Efter funktionalisering av enaminens -position med en elektrofil kan katalysatorn dissocieras och den slutliga kaskadprodukten fås. Denna uppfinning ger möjlighet att framställa mera komplicerade slutprodukter genom att införa olika elektrofiler i alkyleringsprodukternas -position. Alkyleringsprodukten 7, som bildats efter den första katalytiska cykeln, aktiveras på nytt av katalysatorn 3 och bildar intermediären 6. Intermediären omvandlas till enamin 10 varefter en elektrofil införs och iminiumintermediär 11 bildas. Efter hydrolys av 11 bildas de nya diastereoselektiva kaskadprodukterna 12 i bra utbyten samt höga enantio- och diastereoselektiviteter. Detta kräver dock ett väl planerat val av katalysator för att ha en bra kontroll över selektiviteterna i reaktionerna. Imidazolidinoner kan delta i båda aktiveringscyklerna utan större begränsningar vilket möjliggör att kaskadprodukter med höga ee- och dr-värden kan erhållas. Man kan också kontrollera reaktionerna genom att välja skilda katalysatorer för de olika aktiveringssätten och på så sätt uppnå ännu högre selektiviteter för produkterna. Denna tillämpning med cykelspecifika katalysatorer är ett potentiellt sätt att göra andra asymmetriska synteser som inte tidigare varit möjliga. 6
10 Schema 2 MacMillans koncept där kirala sekundära aminkatalysatorer aktiverar karbonylföreningar via LUMO-sänkande iminbildning har senare varit basmekanismen för de flesta organokatalytiska asymmetriska omvandlingarna Derivat av prolin Diarylprolinoletrarna 14c och 14d är derivat av den väl kända aminosyran prolin, 13, se bild 5. Prolin har tidigare använts som organokatalysator i olika asymmetriska omvandlingar. Den har ofta visat hög aktivitet men låg stereokontroll i reaktionerna. Detta har väckt forskarnas intresse för att förbättra katalysatorns effektivitet i reaktionerna genom att derivatisera den. 13 7
11 Bild 5. Prolin och dess derivat. Difenylprolinolen 14b har tidigare använts som kiral hjälpare 14 och som ligand i reaktioner med Lewissyror 15. År 2005 presenterade Jørgensen et al. 16, 17 och Hayashi et al. 18 första gången användningen av diarylprolinoler som organiska katalysatorer i asymmetriska synteser. I organokatalytiska asymmetriska omvandlingar har 14b visat en betydligt bättre stereokontroll än 14a vilket beror på den steriskt styrande -hydroxigruppen i 14b. Däremot har utbytena i dessa asymmetriska omvandlingar där katalysator 14b använts varit låga. Jørgensens grupp påstod att den fria hydroxigruppen i 14b bildar en stabil och oreaktiv hemiaminalintermediär, 15 bild 6, som leder till att utbytet i reaktionerna blir låga. Genom att skydda hydroxigruppen i 14b med trimetylsilyl (TMS) undviks bildning av hemiaminal 15 och därmed uppnås en högre reaktivitet för den maskerade katalysatorn 14c. 13 Bild 6. Hemiaminala jämvikten för katalysator 14b. År 2009 var Wang et al. 19 de första som använde sig av den maskerade difenyltrimetylsilyletern 14c i asymmetriska Friedel-Crafts-alkyleringar. Den diarylprolinoleterkatalyserade alkyleringsprocessen baserar sig på den LUMO-sänkande iminaktiveringsmekanismen, se schema 1 på sidan 5, som MacMillan tidigare presenterat för imidazolidinoner. Som kokatalysator används i detta fall en bas. Basens uppgift är att höja nukleofilens nukleofilicitet genom att vätebindas till den. Därmed förskjuts elektroner mot nukleofilen och dess HOMO-nivå höjs vilket leder till starkare nukleofilattack. Bindning av protonen kan också uppnås utan bas genom att istället använda ett protiskt 8
12 lösningsmedel. Kombinationen av MacMillans LUMO-sänkande iminaktiveringen och den HOMO-höjande vätebindningen kan sägas vara en ny typ av bifunktionell mekanism, se bild 7. Denna skall dock inte förväxlas med MacMillans kaskadmekanism. Bild 7. Den bifunktionella aktiveringsmekanismen. Även med diarylprolinolkatalyserade asymmetriska F-C-alkyleringar kan en stark stereokontroll uppnås. Den bildade iminiumintermediärens Si-sida blockeras av prolinoleterns arylgrupper vilket resulterar i nukleofil attack från den ohindrade Re-sidan. Därmed erhålls kontroll över reaktionens stereoselektivitet Derivat av cinkona-alkaloider Gemensamt för de sekundära aminkatalysatorerna är deras ineffektivitet i F-C-reaktioner där mera steriskt hindrade elektrofiler används. Speciellt alkylering av aromatiska nukleofiler med enoner leder till låga utbyten och selektiviteter. År 2005 presenterades användningen av primära aminer, cinkona-alkaloidderivat, som organokatalysatorer i asymmetriska F-C-reaktioner 20. Cinkona-alkaloiderna är naturligt förekommande små och enkla organiska föreningar. De kan lätt omvandlas t.ex. med en Mitsunobureaktion till olika derivat som kan katalysera asymmetriska omvandlingar. De vanligaste cinkonaalkaloidderivaten som används har erhållits från de naturligt förekommande alkaloiderna kinin, cinkonin, kinidin och cinkonidin. Kinin- och cinkoninderivaten är kinidinrespektive cinkonidinderivatens enantiomerer, se bild
13 Bild 8. Derivat av cinkona-alkaloider. Dessa primära aminkatalysatorer aktiverar elektrofilen i F-C-reaktioner enligt samma mekanism som de sekundära, se schema 1 på sidan Skillnaden mellan de primära och sekundära aminkatalysatorerna är aminogruppens steriska frihet. De primära aminkatalysatorerna har mera rum vid kvävet, som skall aktivera den -omättade karbonylföreningen. Detta leder till en snabbare iminbildning med mera hindrade elektrofiler än för de sekundära katalysatorerna, se bild Bild 9. De primära och sekundära aminkatalysatorernas skillnader i iminaktiverinssteget. År 2007 presenterade både Chen 22 och Melchiorre 23 de första lyckade asymmetriska F-Calkyleringarna av indoler med enoner där dessa alkaloidderivat användes som katalysatorer tillsammans med syror som kokatalysatorer. 10
14 3. F-C-alkyleringar av olika aromatiska nukleofiler Organokatalytiska F-C-alkyleringar av olika aromatiska nukleofiler med -omättade aldehyder och ketoner presenteras i detta kapitel. De viktigaste och mest undersökta F-Calkyleringarna är reaktionerna med indoler. Indolstrukturen finns i många olika biologiskt aktiva naturprodukter och har därmed ett omfattande användningsområde. I dessa asymmetriska F-C-alkyleringar har främst de katalysatorer som introducerats i kapitel 2 i denna avhandling använts med några specialfall som undantag. 3.1 Alkylering av pyrroler I början av 2000-talet användes MacMillans imidazolidinonkatalysatorer första gången i asymmetriska LUMO-sänkande iminaktiverade Friedel-Crafts-alkyleringar av pyrroler med -omättade aldehyder. År 2001 presenterade MacMillans grupp 3 alkylering av N- metylpyrrol med (E)-kanelaldehyd där MacMillans första generationens benzylimidazolidinon*tfa salt, 1, fungerade som katalysator, se schema 3. Produkterna, -pyrrolylaldehyderna 18, är viktiga syntoner för framställningen av olika biomediciner 24. Schema 3 Alkyleringsprodukterna erhölls i höga utbyten och selektiviteter vid låga temperaturer mellan -30 och -60. Variationer i pyrrol- eller aldehydstrukturen förändrade inte märkbart reaktionens utbyte eller selektivitet, se tabell 1. Reaktionen tål bra förändringar i pyrrolens N-substituent (ansatserna 1 3). Då C2-alkylsubstituerade pyrroler alkyleras med kanelaldehyd fås de disubstituerade alkyleringsprodukterna i höga utbyten och selektiviteter (ansats 5). Användningen av C3-substituerad pyrrol, 16d, resulterar i regioselektiv alkylering av C2-positionen. Organokatalytisk F-C-alkylering av N- 11
15 metylpyrrol med olika -omättade aldehyder presenteras också i tabell 1. Både alifatiska- och aromatiska -substituenter på olefinen kan användas utan utbytesförlust eller försämrad selektivitet (ansatserna 1 och 2). Den elektronfattiga aldehyden 17c ger i reaktion med N-metylindol 16a, -pyrrolylaldehyden 18d i högt, 90 %, enantiomeröverskott. Däremot sjunker utbytet till 72 %. Med denna reaktion har MacMillan visat att man kan göra både symmetriska och osymmetriska 2,5-disubstituerade pyrroler. Dessa 2,5-disubstituerade pyrroler kan fungera som utgångsämne vid framställning av kirala organometallkatalysatorers ligander. 3 Tabell 1. Imidazolidinonkatalyserade F-C-alkyleringar av pyrroler med aldehyder -omättade Ansats Pyrrol Aldehyd Produkt Utbyte ee 1 R 1 = Me, R 2,R 3 = H (16a) R= Me (17a) 18a R 1 = Me, R 2,R 3 = H (16a) R= Ph (17b) 18b R 1 = Allyl, R 2,R 3 = H (16b) R= Ph (17b) 18c R 1 = Me, R 2,R 3 = H (16a) R= CO 2 Me (17c) 18d R 2 = Bu, R 1,R 3 = H (16c) R= Ph (17b) 18e R 3 = Pr, R 1,R 2 = H (16d) R= Ph (17b) 18f Efter MacMillans pionjärarbete inom detta område har ett antal andra grupper undersökt olika organokatalytiska asymmetriska Friedel-Crafts-reaktioner av pyrroler. Su et al. 25 har gjort derivat av MacMillans första generationens katalysator genom att förändra imidazolidinonens amidstruktur till tioamid. Dessa nya imidazoltioner har en styvare struktur vilket förbättrar geometrin för den aktiverade iminiumintermediären och höjer därmed reaktionens stereoselektivitet. Dessa imidazoltioner har framställts från motsvarande imidazolidinoner med P 2 S 5 /Al 2 O 3 som svavelkälla. 12
16 Schema 4 De fann att denna typ av katalysator, 8a, med TFA som kokatalysator har utmärkt aktivitet i asymmetriska F-C-alkyleringar speciellt i reaktioner mellan N-metylpyrrol, 19a, och krotonaldehyd, 20d. Utmärkt selektivitet, ee = 98 %, erhölls vilket var högre än MacMillans resultat från motsvarande imidazolidinonkatalyserade reaktion. Sus grupp varierade både på pyrrolens och aldehydens struktur för att se hur reaktiviteten och selektiviteten förändrades. Då N-metylpyrrol alkylerades med den p-substituerade aromatiska aldehyden 20a erhölls högre utbyten och ee-värden än med de o- och m- substituerade aromatiska aldehyderna 20b och 20c. Alkylering av osubstituerad pyrrol ledde däremot till problem vid isoleringen av alkyleringsprodukten. Su löste detta genom att modifiera imidazoltionens, 8a, struktur. Den nya spirosubstituerade imidazoltionkatalysatorn 8b gav bra utbyten och utmärkta selektiviteter speciellt då pyrrol alkylerades med krotonaldehyd (ansats 7). Aromatiska omättade aldehyder gav betydligt sämre utbyten och ee-värden än alifatiska aldehyder (ansatserna 5 och 6). Su undersökte också lösningsmedlets inverkan på reaktionen. Reaktionerna utförda i DCM, i-proh eller THF gav låga utbyten och dåliga selektiviteter. Både utbytena och selektiviteterna höjdes märkbart då THF/H 2 O- eller DCM/i-PrOH-blandningar användes som lösningsmedel. De högsta värdena erhölls i THF/H 2 O-lösning (85:15) vid Samma grupp har senare introducerat imidazoltioner i asymmetriska F-C-reaktioner av indoler, se sid
17 Tabell 2. Imidazoltionkatalyserade F-C-alkyleringar av pyrroler med aldehyder -omättade Ansats Pyrrol Aldehyd Produkt Utbyte ee 1 R 1 =Me, R 2,R 3 = H (19a) R= p-clc 6 H 4 (20a) 21a R 1 = Me, R 2,R 3 = H (19a) R= o-meoc 6 H 5 (20b) 21b R 1 = Me, R 2,R 3 = H (19a) R= m-clc 6 H 4 (20c) 21c R 1 = Me, R 2,R 3 = H (19a) R= Me (20d) 21d R 1,R 2,R 3 = H (19b) R= p-clc 6 H 4 (20a) 21e R 1,R 2,R 3 = H (19b) R= C 6 H 5 (20b) 21f R 1,R 2,R 3 = H (19b) R= Me (20d) 21g Då resultaten av Macmillans imidazolidinonkatalyserade F-C-reaktioner av pyrroler med -omättade aldehyder var lovande skapades ett intresse för att undersöka andra iminaktiverande aminkatalysatorer i samma omvandlingar. År 2006 introducerade Hedenström et al. 26 pyrrolidiniumsaltet, 24, som katalysator för alkylering av N- metylpyrrol, 22, med cyklopent-1-en-karbaldehyd 23, se schema 5. Schema 5 Den cykliska -omättade aldehyden ger efter reduktion med NaBH 4 upphov till en mera komplicerad alkyleringsprodukt, 25, med två nya stereocentra. Första försöket med pyrrolidiniumkloridsaltet som katalysator gav bra enantioselektiviteter men cis/transförhållandet var nästan 50:50. För att förbättra selektiviteten varierade Hedenströms grupp på olika faktorer som temperatur, mängden vatten i reaktionen samt kokatalysatorn och dess mängd. Nedkylning av reaktionsblandningen förändrade inte märkbart på selektiviteten. Kokatalysatorns inverkan var däremot stor. Pyrrolidiniumjodidsaltet höjde 14
18 cis/trans-förhållandet till 9:91. Fördubblad ekvivalentmängd HI höjde förhållandet ytterligare till 3:97. Dessutom förbättrades enantioselektiviteten för båda diastereoisomererna. När 40 H 2 O tillsatts gav reaktionerna de bästa selektiviteterna. Det har tidigare noterats att tillsats av 20 mol% vatten tillsammans med katalysatorn och kokatalysatorn försnabbar iminiumjonens hydrolys och förbättrar därmed reaktionens selektivitet. 26 Samma år som Hedenström gjorde sina framsteg inom området presenterade Bonini och medarbetare 27 en ny typ av organokatalysator, (3-metylaziridin-2-yl)-difenylmetanol. De använde dessa små organiska föreningar i asymmetriska Friedel-Crafts-reaktioner av N- metylpyrrol, 22, med krotonaldehyd, 26a, och kanelaldehyd, 26b, vilket visas i schema 6. Schema 6 Aziridinkatalysatorernas struktur ger upphov till en hög ringspänning och det är därmed osäkert om dessa kan bilda stabila iminiumintermediärer. Bonini kom fram till att speciellt aziridinmetanol, 27, gav bra utbyten och selektiviteter i F-C-reaktionerna av N-metylpyrrol med krotonaldehyd (51 %, ee = 75 %) och kanelaldehyd (55 %, ee = 74 %) vid 40. Resultaten visar att aziridinmetanoler kan bilda stabila iminiumintermediärer i organokatalytiska asymmetriska F-C-reaktioner av pyrroler. 27 Senare har samma katalysator, 27, använts vid motsvarande elektrofila substitution av N-metylindol, se sid 35. ( )-Rhazinilam, 34, är en tetracyklisk alkaloid som isolerats från både mellanösternväxten Rhazya stricta och malesiska växten Kopsia singapurensis vilka tillhör växtfamiljen, Apocynaceae. 28, 29, 30. Rhazinilam är ett gift som effektivt hindrar bildning av nya celler genom att avbryta den normala celldelningen, mitosen. ( )-Rhazinilam kan därmed klassificeras som ett potentiellt antitumörmedel. Andra viktiga och med ( )-Rhazinilam 15
19 nära besläktade alkaloider är ( )-Rhazinal 33, ( )-leuconolam 35 och ( )-epi-leuconolam 36. Alla dessa alkaloider kan framställas med syntesmetoden som Banwell et al. 31 har utvecklat. I deras metod tillämpas intramolekylär imidazolidinonkatalyserad asymmetrisk Friedel-Crafts-alkylering av pyrrol, 31, för att bilda mellanprodukt 32. Mellanprodukten kan omvandlas via olika antal mellansteg till alkaloiderna, 33 36, se schema 7. Schema 7 4,7-Dihydroindolerna är intressanta föreningar som lätt kan oxideras till motsvarande indoler. Wang et al. 32 alkylerade 4,7-dihydroindolerna, 37, med de -omättade aldehyderna, 38a-f, för att få de förväntade 2-substituerade pyrrolprodukterna 40a-f, se schema 8. Wang kom fram till att 20 mol% av både katalysator 14c och Et 3 N i MTBE gav de bästa utbytena och selektiviteterna för alkyleringarna. Alkyleringen följer den bifunktionella mekanismen som tidigare presenterats på sidan 9. De 2-substituerade pyrrolprodukterna kan sedan oxideras till motsvarande 2-substituerade indoler, 41, m.h.a. 16
20 p-bensokinon. Denna omvandling är speciellt viktig då man kan få de med F-C-reaktioner svåråtkomliga icke-traditionella 2-substituerade indolerna som slutprodukter. Schema 8 Wnags forskningsgrupp undersökte alkyleringssteget främst med avseende på enalens - substituent, se tabell 3. 4,7-Dihydroindolens 37a reaktioner med både steriskt och elektroniskt olika aromatiska enaler (ansatserna 1 3) gav i allmänhet högre utbyten än alifatiska enaler (ansats 4). Selektiviteterna var utmärka i alla försök. Bra resultat erhölls också då 4,7-dihydro-5-metoxiindol, 37b, fick reagera med olika -omättade aldehyder (ansatserna 5 och 6). 32 Tabell 3. Difenylprolinoltrimetylsilyleterkatalyserade F-C-alkyleringar av 4,7- dihydroindoler med -omättade aldehyder. Ansats 4,7-Dihydroindol Aldehyd Produkt Utbyte ee 1 R= H (37a) R 1 = Ph, R 2 = H (38a) 40a R= H (37a) R 1 = 2-ClPh, R 2 = H (38b) 40b R= H (37a) R 1 = 4-NO 2 Ph, R 2 = H (38c) 40c R= H (37a) R 1 = Me, R 2 = H (38d) 40d R= MeO (37b) R 1 = Pr, R 2 = H (38e) 40e R= MeO (37b) R 1 = 4-ClPh, R 2 = H (38f) 40f
21 Wangs grupp 33 har senare undersökt alkyleringar av 4,7-dihydroindolerna, 37, med - omättade ketonerna, 38g-k, se schema 8. Efter oxidation av alkyleringsprodukterna, 40g-k, med p-bensokinon fås de 2-substituerade indolerna, 41. Gruppen använde sig inledningsvis av samma alkyleringsförhållanden som tidigare för aldehyderna. Utbytena och selektiviteterna för produkterna, -pyrrolylketonerna, var dock låga vilket beror på att ketoner har lägre aktivitet för iminbildning än aldehyder. Katalysator, 14c, är därmed inte en lämplig och tillräckligt starkt aktiverande katalysator för detta ändamål. Gruppen gjorde grundliga undersökningar och prövade olika primära och sekundära aminkatalysatorers inverkan på reaktionens resultat. De kom fram till att primära aminer med högre sterisk frihet vid kvävet aktiverar ketoner bättre i dessa F-C-reaktioner. Speciellt diaminen 39 med både primär och sekundär aminogrupp gav de bästa resultaten. Mekanismen följer en bifunktionell dubbelaktivering, se bild 10, där den primära aminogruppen binder enonen via den LUMO-sänkande iminbildningen och den sekundära aminogruppen växelverkar med indolens N-H via en HOMO-höjande vätebindning. Bild 10. Aktiveringsmekanismen för en diaminkatalysator med både primär och sekundär aminogrupp. Reaktionen gav bra utbyten och höga selektiviteter då 4,7-dihydroindol fick reagera med steriskt och elektroniskt olika enoner, se tabell 4. 18
22 Tabell 4. Diaminkatalyserade F-C-alkyleringar av 4,7-dihydroindoler ketoner. -omättade Ansats 4,7-Dihydroindol Keton Produkt Utbyte ee 1 R= H (37a) R 1 = Ph, R 2 = Me (38g) 40g R= H (37a) R 1 = 4-ClPh, R 2 = Me (38h) 40h R= H (37a) R 1 = Ph, R 2 = Ph (38i) 40i R= H (37a) R 1,2 = -(CH 2 ) 3 - (38j) 40j R= MeO (37b) R 1 = Ph, R 2 = Me (38k) 40k Speciellt intressant resultat erhölls då elektrofilen var chalkon 38i. Chalkon som är ett krångligt substrat för iminaktiverande katalysatorer gav i detta fall en överraskande hög optisk renhet för produkten, 85 %. Å andra sidan erhölls endast moderata ee-värden för cykliska enoner (ansats 4). Substitution av 4,7-dihydroindolen inverkade inte märkbart på produktens utbyte eller ee-värde (ansats 5). Ett undantag var N-substitution som hindrar vätebindning mellan 4,7-dihydroindolen och katalysatorn vilket leder till att utbytena blir väldigt låga. Detta stöder mekanismen i bild 10 där den sekundära aminen vätebinds till 4,7-dihydroindolen, vilket ökar nukleofiliciteten. Organokatalytisk asymmetrisk F-Calkylering av 4,7-dihydroindoler följt av alkyleringsproduktens oxidation med p- bensokinon är en innovativ och användbar metod för att framställa de icke-traditionella 2- substituerade indolerna Alkylering av indoler Då försöken att enantioselektivt alkylera pyrroler med LUMO-sänkande iminaktiverande organokatalysatorer var framgångsrika, ökade intresset för att göra samma omvandlingar på andra elektronrika substrat, speciellt indoler. Indolstrukturen är den viktigaste heterocykeln i naturen och kan identifieras i en hel del biologiskt aktiva naturprodukter. Dessutom har många indolderivat förmågan att bindas till olika receptorer vilket gör dem till intressanta föreningar inom läkemedelskemin. Till skillnad från pyrroler har funktionalisering av indoler varit ett problem genom tiderna. Den pyrrollika 19
23 indolstrukturen har p.g.a. bensenringen ett svagare -system och därmed minskad förmåga 34, 35 att delta i elektrofil substitution. MacMillan et al. 11 fortsatte sina undersökningar genom att försöka utnyttja första generationens imidazolidinonkatalysator i asymmetriska F-C-reaktioner av indoler med -omättade aldehyder. Resultaten för indolakyleringarna var avsevärt sämre än för pyrrolalkyleringarna. Efter teoretiska undersökningar av organokatalysatorns effekter på reaktionen kan antingen iminbildningen eller bildningen av den nya C-C-bindningen anses vara det hastighetsbestämmande steget i alkyleringsprocesserna. För att höja katalysatoreffektiviteten böt MacMillan ut första generationens imidazolidinon mot en förbättrad andra generationens imidazolidinonkatalysator, 2, där C2- och C5- substituenterna sitter på samma sida. Förhöjd reaktivitet och selektivitet kunde uppnås vid alkylering av indoler med andra generationens MacMillan-katalysator. Resultatet inspirerade MacMillans grupp till att variera indolens, 42, och den -omättade aldehydens, 43, struktur i de asymmetriska F-C-reaktionerna, se schema Schema 9 Reaktionen tolererade bra de olika förändringarna i indolstrukturen. N-substituerade indoler gav höga utbyten och selektiviteter i reaktion med krotonaldehyd (ansats 6). En förändring av indolens steriska eller elektroniska egenskaper genom insättning av en alkyleller alkoxisubstituent i C4-position kan utföras utan förlust i reaktivitet och selektivitet (ansatserna 7 och 8). Halogensubstituerade indoler är viktiga derivat för olika organometallreaktioner, t.ex. Stille-kopplingar. Utbytet och ee-värdet för den 6- klorsubstituerade indolprodukten 44i var 73 % respektive 97 %. Variationer av - substituenten på den -omättade aldehyden kunde göras utan större förluster i selektiviteten. Reaktionen visade bra utbyten och höga selektiviteter för steriskt olika aldehyder (ansats 2). Dessutom erhölls höga selektiviteter både för elektronfattiga, R 2 = 20
24 CO 2 Me, och iminstabiliserande, R 2 = Ph, aldehyder. De två sistnämnda resultaten är intressanta då reaktanterna vanligtvis inte beter sig lika. 11 Tabell 5. Imidazolidinonkatalyserade F-C-alkyleringar av indoler med olika aldehyder -omättade Ansats Indol Aldehyd Produkt Utbyte ee 1 R 1 = Me, X= H (42a) R 2 = Me (43a) 44a R 1 = Me, X= H (42a) R 2 = CH 2 OBz (43b) 44b R 1 = Me, X= H (42a) R 2 = Ph (43c) 44c R 1 = Me, X= H (42a) R 2 = CO 2 Me (43d) 44d R 1 = H, X= H (42b) R 2 = Me (43a) 44e R 1 = Allyl, X= H (42c) R 2 = Me (43a) 44f R 1 = H, X= 4-Me (42d) R 2 = Me (43a) 44g R 1 = Me, X= 4-MeO (42e) R 2 = Me (43a) 44h R 1 = H, X= 6-Cl (42f) R 2 = Me (43a) 44i År 2005 började MacMillans grupp 12 syntetisera andra mera substituerade alkyleringsprodukter genom att införa elektrofiler i produktens -position. Gruppen använde sig av den tidigare diskuterade kaskadmekanismen (se sidorna 6 och 7) för att förstå bildningen av de mera komplicerade slutprodukterna. Samtidigt tog de i bruk den nyutvecklade imidazolidinonkatalysatorn, 12. Kaskadmekanismen har tillämpats vid t.ex. alkylering av N-metylindol, 45, med kanelaldehyd, 46a, eller -isopropylakrolein, 46b, för att bilda alkyleringsprodukterna 48a och 48b. Efter att en elektrofil, Cl +, adderats till alkyleringsprodukterna erhölls de slutliga kaskadprodukterna 49a och 49b i utbyten på 83 % respektive 67 %, se schema 10. Som elektrofildonerande reagens användes i detta fall 2,3,4,5,6,6-hexaklorcyklohexa-2,4-dienon
25 Schema 10 Produkternas ee/dr var 99/9:1 respektive >99/12:1. Dessutom har N-bensylindol alkylerats med krotonaldehyd. Produktens utbyte var 75 % och ee/dr >99/12:1. Alla produkter är syn vilket beror på katalysatorselektiviteten i enaminaktiveringssteget. Fördelen med detta kaskadkatalysatorsystem är att man framgångsrikt kan göra nya asymmetriska omvandlingar som inte tidigare har lyckats. 12 Senare har gruppen använt kaskadmetoden vid alkylering av andra nukleofiler som furaner, se sid 57. MacMillans goda resultat vid asymmetrisk alkylering av indoler har varit riktgivande för ytterligare forskning inom området. Metoden har senare tillämpats vid framställning av olika enantiomert rena naturprodukter och läkemedelsderivat där indolstrukturen är stommen för den slutliga föreningen. Samma grupp 12 har presenterat en tvåstegsreaktion för framställningen av en COX-2- inhibitor, indolylbutansyra 52, där deras egen metod tillämpades på ett enkelt sätt, se schema 11. COX-2 är ett enzym som producerar prostaglandiner. Prostaglandinerna motverkar inflammationer och smärtor i kroppen. Inhibitorernas uppgift är att reglera enzymets beteende då det fungerar felaktigt och på så sätt verka som ett läkemedel
26 Schema 11 Senare har MacMillan och medarbetare 37 tillämpat denna enantioselektiva metod vid framställningen av olika pyrrolindoliner från tryptaminer, se schema 12. De använde olika modifikationer av andra generationens imidazolidinonsalt, 53, som katalysatorer i F-Creaktionerna. Efter att tryptaminen, 56, attackerat den aktiverade iminen, 55, bildas en intermediär, indoliumjon 57, som intramolekylärt ringsluts till den aktiverade pyrrolindolinen 58. Efter hydrolys av 58 bildas den slutliga pyrrolindolinen
27 Schema 12 Reaktionen tål en hel del förändringar i tryptaminstrukturen, se tabell 6. Substitution av tryptaminens N1-position med elektrondonerande grupper som allyl och bensyl ger höga utbyten, %, och selektiviteter, %, i reaktion med akrolein (ansatserna 1 3). Nästan samma resultat erhölls då N10-positionen substituerats med olika stora alkylgrupper (ansatserna 1 och 2). Då den -metoxikarbonylsubstituerade akroleinen, 61b, används som aldehyd höjs både utbytet och enantioselektiviteten för de diastereoselektiva pyrrolindolinerna, 62d-h, som bildas (ansatserna 4 8). Produkternas diastereoselektiva förhållande varierar stort från 10:1 till 50:1. Det högsta dr-värdet erhölls för C5- metylsubstituerade tryptaminen 60d (ansats 5). Utmärkt utbyte och enantioselektivitet gav tryptaminen 60g, men det diastereoselektiva förhållandet var endast 17:1 (ansats 8). Den C6-halogensubstituerade tryptaminen 60f gav lägre utbyte (ansats 7) än andra tryptaminer med substituenter på indolringen
28 Tabell 6. Imidazolidinonkatalyserade F-C-alkyleringar av tryptaminer med aldehyder -omättade Ansats Indol Aldehyd Produkt Utbyte ee dr 1 R 1 = Allyl, R 2 = t-bu, R 3 = H (61a) 62a * - X= H (60a) 2 R 1 = Allyl, R 2 = Et, R 3 = H (61a) 62b * - X= H (60b) 3 R 1 = Bensyl, R 2 = t-bu, R 3 = H (61a) 62c * - X= H (60c) 4 R 1 = Allyl, R 2 = t-bu, R 3 = CO 2 Me 62d :1 ** X= H (60a) (61b) 5 R 1 = Allyl, R 2 = t-bu, R 3 = CO 2 Me 62e :1 ** X= 5-Me (60d) (61b) 6 R 1 = Allyl, R 2 = t-bu, R 3 = CO 2 Me 62f :1 ** X= 5-MeO (60e) (61b) 7 R 1 = Allyl, R 2 = t-bu, R 3 = CO 2 Me 62g :1 ** X= 6-Br (60f) (61b) 8 R 1 = Allyl, R 2 = t-bu, R 3 = CO 2 Me 62h :1 ** X= 7-Me (60g) (61b) *= utfört med katalysator I **= utfört med katalysator II Pyrrolindolinerna är substrat med en alkaloidlik basstruktur och hör till familjen polyindoliska alkaloider. Dessa har isolerats från amfibier, växter och havsalger 38. I allmänhet har denna basstruktur uppvisat biologisk aktivitet och därmed har pyrrolindolinerna blivit viktiga mellanprodukter vid syntes av olika naturprodukter. 25
29 MacMillans grupp 37 har presenterat en totalsyntes av alkaloiden ( )-flustramin B, 66, där asymmetrisk F-C-alkylering tillämpas på 6-bromtryptamin, 63, se schema 13. Flustraminer hör till gruppen havsalkaloider, som första gången isolerades i slutet på 1970-talet från mossdjuret Flusta foliacea 39. Flustramin B blockerar spänningsaktiverade kaliumkanaler 40 och har muskelavslappnande egenskaper 41. Schema 13 King och Meng et al. 42 har rapporterat en kort men effektiv framställningsmetod för 3- ((1R,2S)-2-((dimetylamino)metyl)cyklopentyl)-indol-5-karbonitril, som är en selektiv serotoninåterupptagningsinhibitor (SSRI). Möjliga användningsområden för dessa inhibitorer är behandling av depression och andra mentala sjukdomar 43, 44. King och Meng tillämpade MacMillans sätt att F-C-alkylera indol 67 med den -förgrenade -omättade aldehyden 23 där imidazolidinon 68 fungerade som katalysator, se schema 14. Denna modifierade andra generationens imidazolidinonkatalysator gav högt utbyte och bra selektivitet med den -förgrenade cyklopent-1-enkarbaldehyden vid -25 (utbyte = % och ee-värde = 84 %). Aldehydprodukten som bildades vid alkyleringen var den mera oväntade (S)-enantiomeren, 69. Detta kan förklaras genom att betrakta mekanismen för iminbildningen. Sterisk växelverkan mellan cyklopentenens C5-metylengrupp och imidazolidinonens bensylgrupp minimeras. Dessutom har katalysatorns 5-metylfurylgrupp det längsta avståndet till cyklopentengruppen vilket är energetiskt mest gynnsamt. Båda faktorerna bidrar till att trans-(z)-iminiumintermediären och som en följd av det att den 26
30 oväntade (S)-enantiomeren av aldehyd 69 bildas. Då aldehyden sedan reduktivt amineras och därpå cyaneras bildas slutligen homotryptamin, SSRI:n 70, i bra utbyte, %. 42 Schema 14 Efter MacMillans, Kings och Mengs framgångar i imidazolidinonkatalyserade Friedel- Crafts-alkyleringar av indoler med -omättade aldehyder har andra grupper undersökt alternativa aminkatalysatorer för alkyleringsprocesserna. Jørgensen 16, 17 och Hayashi 18 har tidigare presenterat diarylprolinolsilyletrar som effektiva organokatalysatorer i ett antal asymmetriska omvandlingar. Detta väckte forskarnas intresse för att utnyttja kiral difenylprolinoltrimetylsilyleter, 14c, i asymmetriska F-C-reaktioner av indoler. Wang et al. 19 presenterade alkylering av indoler, 71, med -omättade aldehyder, 72, där 14c fungerade som katalysator, se schema 15. Alkyleringsmekanismen följer den bifunktionella LUMO-sänkande och HOMO-höjande aktiveringen. Difenylprolinoltrimetylsilyletern aktiverar den -omättade aldehyden och bildar en iminiumjon. Lewisbasen som tillsätts vätebinds till indolens N-proton. Detta ökar indolens nukleofilicitet och höjer därmed reaktionshastigheten. Flera baser prövades men Wangs grupp kom fram till att 50 mol% trietylamin, Et 3 N, gav de högsta utbytena och selektiviteterna för reaktionerna. Lösningsmedlets och temperaturens inverkan på reaktionen undersöktes också. Etrarna, av vilka metyl(tert-butyl)eter (MTBE) visade lovande resultat, var de bästa alternativen som lösningsmedel. Då temperaturen sänktes blev utbytet för reaktionen lägre men å andra sidan höjdes ee-värdet. 27
31 Schema 15 Tabell 7 visar hur variationer i både indolens och aldehydens struktur påverkar utbyten och selektiviteter för de asymmetriska F-C-alkyleringarna. Reaktioner med kanelaldehyd 72b som elektrofil tolererar olika substituerade indoler (utbyte = % och ee-värde = %). Elektrondonerande och -attraherande grupper i indolens C5-position ger höga utbyten (ansatserna 5 och 6) medan en alkylgrupp i C7-position ger endast ett moderat utbyte (ansats 7). Selektiviteten är utmärkt i alla försök. Enda begränsningen är att N- substitution av indolen förhindrar vätebindningen och leder därmed till ett nästan obefintligt utbyte av produkten. I reaktion med indol gav både alkyl- och arylsubstituerade -omättade aldehyder bra utbyten och höga ee:n. Förändringar i de arylsubstituerade aldehydernas steriska eller elektroniska egenskaper kunde göras utan större förluster i reaktivitet eller selektivitet
32 Tabell 7. Difenylprolinoltrimetylsilyleterkatalyserade F-C-alkyleringar av indoler med -omättade aldehyder Ansats Indol Aldehyd Produkt Utbyte ee 1* X= H (71a) R 1 = Me (72a) 73a * X= H (71a) R 1 = Ph (72b) 73b * X= H (71a) R 1 = 2-ClC 6 H 4 (72c) 73c * X= H (71a) R 1 = 3-MeOC 6 H 4 (72d) 73d * X= 5-MeO (71b) R 1 = Ph (72b) 73e * X= 5-Br (71c) R 1 = Ph (72b) 73f * X= 7-Me (71d) R 1 = Ph (72b) 73g * X= H (71a) R 1 = Ph (72b) 73h ** X= H (71a) R 1 = 2-ClC 6 H 4 (72c) 73i ** X= H (71a) R 1 = 4-MeOC 6 H 4 (72e) 73j ** X= 5-MeO (71b) R 1 = Ph (72b) 73k ** X= 5-Me (71e) R 1 = Ph (72b) 73l ** X= 5-O 2 N (71f) R 1 = Ph (72b) 73m * Wang et al. ** Bao et al. Bao och medarbetare 45 undersökte samma F-C-alkyleringar som Wang gjort tidigare. Baos grupp har använt samma difenylprolinoltrimetylsilyleter 14c som katalysator men till skillnad från Wangs arbete tillsatte de inte en Lewisbas, se schema 15 på sida 30. Därför bör reaktionsbetingelserna förändras för att få reaktionen att lyckas. Bao undersökte lösningsmedlets effekt på reaktionen och kom fram till att användning av etrar, som tidigare gett bra resultat och speciellt höga selektiviteter, ledde till endast moderata utbyten och selektiviteter. Metanol som är ett polärt protiskt lösningsmedel visade sig vara det bästa mediet att utföra reaktionerna i. Detta kan bero på att MeOH kan vätebindas till nukleofilen och på så sätt underlätta reaktionens gång. Trots alla förändringar i reaktionsförhållandena är Baos resultat för F-C-reaktioner av substituerade indoler med kanelaldehydderivat sämre än Wangs. Små förluster i selektiviteten kan noteras. Bao märkte också att N-substituerade indoler inte reagerade med kanelaldehyder. Detta beror på att N-substituerade indolers nukleofilicitet inte kan höjas genom att bilda en 29
33 vätebindning. Därmed minskar reaktiviteten mellan indolen och iminiumjonen vilket leder till utbytesförluster. Ett annat intressant fenomen som Baos grupp märkte var att -alkyl -omättade aldehyder, t.ex. krotonaldehyd, reagerade inte med indoler under dessa reaktionsbetingelser. Baos resultat visade att de utvecklat ett annat sätt att alkylera indoler med kanelaldehydderivat där difenylprolinoltrimetylsilyleter fungerade som katalysator. 45 Organokatalytisk asymmetrisk Friedel-Crafts-alkylering av indoler, 74, med 4-hydroxi-2- butenal, 75, är ett sätt att framställa kirala -substituerade -laktoler, 76. Dessa kan oxideras vidare med PCC till -substituerade- -laktoner, 77, som är viktiga prekursorer vid syntes av olika biologiskt aktiva naturprodukter. 46, 47 Laktolerna 76 kan också reduceras för att bilda kirala 3-substituerade tetrahydrofuraner, 78. Strukturen i förening 78 är viktig då den förekommer i många biologiskt aktiva föreningar t.ex. i diazonimider 48 och leptofuraner 49. Kim et al. 50 har rapporterat framställning av olika -substituerade- - laktoler där imidazolidinon 2 fungerar som katalysator i F-C-reaktionerna. Dessutom har oxidations- och reduktionsreaktionen av -laktolerna till motsvarande -laktoner respektive tetrahydrofuraner presenterats, se schema 16. Schema 16 30
34 Substituentförändringar på indolens N-position kunde utföras utan förluster i utbyte eller selektivitet. Substitution av indolens C5-position med en elektrondonerande grupp gav högt utbyte och utmärkt ee-värde (ansats 3) medan en elektronattraherande grupp i samma position resulterade i betydligt sämre utbyten (ansats 4), se tabell Tabell 8. Imidazolidinonkatalyserade F-C-alkyleringar av indoler med 4-hydroxi-2-butenal Ansats Indol Produkt Utbyte ee 1 R= Me, X= H (74a) 76a R= CH 2 Ph, X= H (74b) 76b R= CH 2 Ph, X= 5-MeO (74c) 76c R= CH 2 Ph, X= 5-Br (74d) 76d Kim använde samma alkyleringsmetod förutom på indoler också på andra nukleofiler som tryptaminer och tryptofol. Alkyleringsprodukterna erhölls dock i låga utbyten samt med dålig selektivitet. 50 Zhang och Zhang et al. 51 har presenterat en ny förbättrad organisk katalysator för asymmetriska Friedel-Craft-transformationer, N-isopropylbipyrrolidin 81. Denna har hög aktivitet som katalysator i alkyleringsreaktioner av indoler, 79, med -omättade aldehyder, 80, se schema 17. Schema 17 Produkterna, 3-alkylerade indoler 82, erhölls i höga utbyten och enantioselektiviteter, se tabell 9. Även små mängder katalysator bidrog till utmärkta resultat. Zhang och Zhang kom fram till att de optimala reaktionsbetingelserna fordrar att förutom katalysatorn också 31
35 trifluormetansulfonsyra (TfOH) som kokatalysator och MeOH som lösningsmedel. Dessutom bör reaktionerna utföras i låga temperaturer (-45 ) för att uppnå de bästa resultaten. Utbytet var högst men selektiviteten lägst för reaktionen när indol 79a alkylerades med krotonaldehyd 80a (ansats 1). Då aldehyden har en större -substituent, t.ex. CH 2 OBz, sjunker utbytet för reaktionen vilket beror på steriska faktorer (ansats 2). Däremot stiger ee-värdet för produkten. Goda utbyten och utmärkta selektiviteter fås också då substituerade indoler alkyleras med 2-hexenal (ansatserna 3 4). En elektronattraherande grupp i indolens C5-position leder till en utbytesförlust medan selektiviteten är hög (ansats 5). 51 Tabell 9. Bipyrrolidinkatalyserade F-C-alkyleringar av indoler med aldehyder -omättade Ansats Indol Aldehyd Produkt Utbyte ee 1 R 1 = H, X= H (79a) R 2 = Me (80a) 82a R 1 = H, X= H (79a) R 2 = CH 2 OBz (80b) 82b R 1 = Bn, X= H (79b) R 2 = npr (80c) 82c R 1 = H, X= 5-MeO (79c) R 2 = npr (80c) 82d R 1 = H, X= 5-Br (79d) R 2 = npr (80c) 82e Kroman är en viktig basstruktur för föreningar som motverkar tillväxten av olika virus, tumörer och mikroorganismer i biologiska system 52, 53, 54, 55. Speciellt indolsubstituerade kromanderivat är synnerligen viktiga föreningar då de innehåller två olika grupper som visat biologisk aktivitet, nämligen indol och kroman. De indolsubstituerade kromanerna kan bildas från kirala 4-indol-2-kromanoler via en ringslutning. Kim och medarbetare 56 har rapporterat en framställningsmetod för kirala 4-indolyl-2-kromanolerna där MacMillans imidazolidinonkatalyserade asymmetriska Friedel-Crafts-alkylering tillämpas på ett lämpligt sätt. Gruppen har alkylerat indoler, 83, med olika o-hydroxikanelaldehyder, 84. Efter cyklisering av alkyleringsprodukterna, 85, bildas de kirala 4-indolyl-2-kromanolerna, 86, i bra utbyten och höga selektiviteter, se schema 18 och tabell
36 Schema 18 Reaktionen undersöktes både från indolens och aldehydens perspektiv. Utbytena och selektiviteterna för reaktionerna av olika N-substituerade indoler med o- hydroxikanelaldehyd var moderata. Då man införde en elektrondonerande grupp i indolens C5-position höjdes selektiviteten (ansats 3). För att undersöka aldehydberoendet lät man N-bensylindol reagera med olika 4- och 5-substituerade 2-hydroxikanelaldehyder. Utbytena och ee-värdena var i allmänhet bra. Elektronattraherande grupper i 4-position bidrog till höga utbyten (ansats 6). 2-Hydroxi-3-nitrokanelaldehyd 84e gav det högsta utbytet, 85 %, för alkyleringsprodukten (ansats 7)
37 Tabell 10. Imidazolidinonkatalyserade F-C-alkyleringar av indoler med olika o- hydroxikanelaldehyder Ansats Indol Aldehyd Produkt Utbyte ee 1 R= Me, X= H (83a) Y= H (84a) 86a R= Bn, X= H (83b) Y= H (84a) 86b R= Bn, X= MeO (83c) Y= H (84a) 86c R= Bn, X= H (83b) Y= 4-Me (84b) 86d R= Bn, X= H (83b) Y= 5-MeO (84c) 86e R= Bn, X= H (83b) Y= 4-Cl (84d) 86f R= Bn, X= H (83b) Y= 4-NO 2 (84e) 86g Imidazoltionerna som visat hög aktivitet i alkyleringsreaktioner av pyrroler, se sid 12, har också framgångsrikt använts av Su et al. som katalysator i reaktioner med indoler. 57 De imidazoltionkatalyserade Friedel-Crafts-alkyleringarna av indoler med -omättade aldehyder presenteras i schema 19. Fördelen med imidazoltionerna är att alkyleringsreaktionerna kan utföras vid högre temperaturer (-25 ) än med MacMillans imidazolidinoner (< -60 ). Schema 19 Resultaten från Sus försök att asymmetriskt alkylera indoler med olika -omättade aldehyder var utmärkta, se tabell 11. Både alifatiska och aromatiska -omättade aldehyder reagerade bra med N-metylindol 87a och gav de 3-substituerade indolerna 89 i höga utbyten och utmärka ee-värden. Speciellt krotonaldehyd 88c var en bra elektrofil inte bara med N-metylindol utan också med andra substituerade indoler (ansatserna 3 5). 34
38 Endast moderata selektiviteter uppnåddes då indol 87d och 5-bromindol 87e fick reagera med aromatiska -omättade aldehyder (ansatserna 6 och 7). De låga ee-värdena kan förklaras med reaktionens reversibilitet eller för att en racemisering kan ske. 57 Tabell 11. Imidazoltionkatalyserade F-C-alkyleringar av indoler med aldehyder -omättade Ansats Indol Aldehyd Produkt Utbyte ee 1 R 1 = Me, X= H (87a) R 2 = m-clc 6 H 4 (88a) 89a R 1 = Me, X= H (87a) R 2 = C 6 H 5 (88b) 89b R 1 = Me, X= H (87a) R 2 = Me (88c) 89c R 1 = H, X= 2-Me (87b) R 2 = Me (88c) 89d R 1 = H, X= 5-MeO (87c) R 2 = Me (88c) 89e R 1 = H, X= H (87d) R 2 = m-mec 6 H 4 (88d) 89f R 1 = H, X= 5-Br (87e) R 2 = m-clc 6 H 4 (88a) 89g Hedenström och medarbetare 26 har år 2006 presenterat asymmetrisk alkylering av förutom N-metylpyrrol (se sid 15) också N-metylindol, 45, med -omättade aldehyder, 26a och 26b, se schema 20. Som katalysator användes (3-metylaziridin-2-yl)-difenylmetanol, 27. Den har visats bilda den aktiverade iminiumintermediären trots den höga ringspänningen som existerar. Resultaten för indolalkyleringen var väldigt varierande och temperaturberoende. Gruppen kom fram till att då N-metylindol fick reagera med krotonaldehyd vid -10 bildas alkyleringsprodukten med ett utbyte på 30 % och ee-värde på 58 %. Ifall temperaturen höjdes steg utbytet till 85 % medan ee-värdet sjönk till 40 %. Samma trend kunde ses då N-metylindol alkylerades med kanelaldehyd. Utbytena och selektiviteterna varierade mellan % respektive %. Resultaten är sämre än för N-metylpyrrolalkyleringarna, vilket var förväntat då indol är en svagare nukleofil. 35
39 Schema 20 År 2007 presenterade Xiao et al. 58 de första intramolekylära organokatalytiska asymmetriska Friedel-Crafts-alkyleringarna av 2-substituerade indoler, 91, där MacMillans andra generationens imidazolidinon, 2, fungerade som katalysator. De polycykliska tetrahydropyran[3,4-b]indolerna (THP-indolerna), 92, erhölls i bra utbyten och höga selektiviteter då man använde 20 mol% av katalysatorn i form av 3,5-dinitrobensoatsalt, se schema 21. Schema 21 THP-indolstrukturen är vanlig i biologiskt aktiva föreningar 59, 60. Olika substituenter på indolringen hade ingen större inverkan på reaktionens selektivitet. Däremot varierar utbytena något mera. Utbytena och selektiviteterna för steriskt och elektroniskt olika substituenter på indolen presenteras i tabell
40 Tabell 12. Resultaten från de intramolekylära ringslutnings-f-c-alkyleringarna av indoler till THP-indoler Ansats Indol Produkt Utbyte ee 1 R= Bn, R 1 = 5-Me, X= O (91a) 92a R= Bn, R 1 = 5-MeO, X= O (91b) 92b R= Bn, R 1 = 5-F, X= O (91c) 92c R= Me, R 1 = 7-Cl, X= O (91d) 92d R= Me, R 1 = H, X= O (91e) 92e R= DMB, R 1 = H, X= O (91f) 92f Metylsubstituerade indolen 91a gav högt utbyte och ee-värde. Metoxi, en mesomert elektrondonerande grupp, i samma position visade sig ha lika bra selektivitet men gav sämre utbyte än metylgruppen (ansats 2). Indoler med elektronattraherande grupper i 5- eller 7-positon duger också bra som utgångssubstrat för den intramolekylära alkyleringen (ansatserna 3 och 4). Speciellt värdefullt utgångsämne är den halogensubstituerade indolen 91d. Den bildar den klorerade THP-indolen 92d, som kan delta i olika organometallreaktioner 61, 62, 63. Fluorerade THP-indolen 92c kan användas som substrat inom läkemedels- eller materialkemin 64. Varierande utbyten och selektiviteter erhölls då de olika N-substituerade indolerna 91e och 91f alkylerades intramolekylärt. N-Metylindolen 91e gav alkyleringsprodukten 92e i både högt utbyte och ee-värde (ansats 5). Dessutom kan indoler där X=NTs också alkyleras intramolekylärt med denna metod. Produkterna som då bildas är tetrahydro- -karboliner. Xiaos grupp visade också att alkyleringsmetoden kan tillämpas på olika aniliner för att bilda 4-kromanylacetaldehyder, se sid Två år senare rapporterade Xiao et al. 65 en imidazolidinonkatalyserad asymmetrisk F-Calkylering av indoler, 93, med (E)-dialkyl-3-oxoprop-1-enylfosfonater, 94, se schema 22. Produkterna, -indolylfosfonaterna 95, erhölls i bra utbyten och höga selektiviteter efter reduktion av alkyleringsprodukterna med NaBH 4. 37
41 Schema 22 De enantiomert rena produkterna har visat en anmärkningsvärt hög biologisk aktivitet och har därför väckt forskarnas intresse. -Substituerade fosfonaterna har ett omfattande användningsområde inom medicin och läkemedelskemin bl.a. som enzyminhibitorer 66, 67, som antibakteriella medel 68, 69 och som anti-hiv-medel 70, 71. Alkyleringsreaktionen är starkt beroende av både indolens, 93, och fosfonatens, 94, struktur, se tabell 13. Tabell 13. Imidazolidinonkatalyserade F-C-alkyleringar av indoler med olika fosfonater Ansats Indol Aldehyd Produkt Utbyte ee 1 R= Allyl, R 1 = 5-I (93a) R 2 = Me (94a) 95a R= Allyl, R 1 = 6-Cl (93b) R 2 = Me (94a) 95b R= Allyl, R 1 = 5-CO 2 Me (93c) R 2 = Me (94a) 95c R= Allyl, R 1 = 5-MeO (93d) R 2 = Me (94a) 95d R= Allyl, R 1 = 5-Me (93e) R 2 = Me (94a) 95e R= Allyl, R 1 = H (93f) R 2 = Me (94a) 95f R= Me, R 1 = H (93g) R 2 = Et (94b) 95g R= Me, R 1 = H (93h) R 2 = Me (94a) 95h Elektronattraherande grupper i indolens 5- och 6-posititon gav moderata utbyten och eevärden (ansatserna 1 och 2). Av de halogensubstituerade indolerna gav 6-klorindol, 93b, det högsta utbytet. Selektiviteterna var ungefär lika i alla försök. Utbytena för de 5- metoxikarbonyl-, 5-metoxi- och 5-metylsubstituerade indolerna, 93c-e, sjönk i denna ordning. 5-Metylsubstituerade indolen hade däremot den högsta selektiviteten (ansats 5). Av indolerna gav i allmänhet de N-Allylsubstituerade högre utbyten än de N- metylsubstituerade. Dietyl-3-oxoprop-1-enylfosfonat, 94b, där R 2 =Et sänkte selektiviteten 38
42 för reaktionen jämfört med fosfonaten 94a. Utbytena var i båda fallen endast moderata (ansatserna 7 och 8). 65 För att visa metodens användbarhet har Xiaos grupp alkylerat också aniliner med fosfonater, se sid 50. År 2011 presenterade Hanessian och medarbetare 72 en organokatalytisk alkylering av 5- bromindol, 98, med en ny typ av elektrofil, 3-aminokrotonaldehyd, 97. I schema 23 presenteras framställningen av (S)-5-brom-3-(1-metylpyrrolidin-3-yl)indol, 100, där den asymmetriska Friedel-Crafts-alkyleringen är ett viktigt mellansteg. Schema 23 (S)-3-(1-metylpyrrolidin-3-yl)indol är en viktig basstruktur för olika potentiella läkemedelsmolekyler, som kunde användas för att bota olika neurodegenererande sjukdomar 73. Ett av enzymen som ansvarar för den neurologiska kväveoxidsyntasen är nnos. nnos-enzymet fungerar i hjärnan och producerar den viktiga signalmolekylen kväveoxid. Speciellt förening, 101, har uppvisat inhibitoraktivitet mot detta enzym. Hanessians grupp undersökte noggrannare alkyleringssteget för 5- och 6-bromindol med olika 3-aminokrotonaldehyder, se tabell
43 Tabell 14. Alkyleringssteget av 5- och 6-bromindol med olika 3-aminokrotonaldehyder Ansats Indol Aldehyd Produkt Utbyte ee 1 5-Br (103a) R= Me, Pg= Boc (102a) 104a kvant Br (103a) R= Me, Pg= CO 2 Me (102b) 104b 97 95,5 3 6-Br (103b) R= PMB, Pg= Boc (102c) 104c 65 90,5 4 5-Br (103a) R= H, Pg= Boc (102d) 104d i.r.* - * i.r. = ingen reaktion Utbytena och selektiviteterna var i allmänhet höga. Förändring av kvävets skyddsgrupp i aminokrotonaldehyden ledde inte till större avvikelser i utbyte och ee-värde (ansatserna 1 och 2). Variationer i aldehydens andra N-substituent inverkar däremot drastiskt på reaktionen. Den N-p-metoxibensylsubstituerade aldehyden 102c gav ett utbyte på endast 65 % för reaktionen med 6-bromindol (ansats 3). Aldehyd, 102d, där R= H kräver en helt annan syntesrutt för att bilda den motsvarande 3-pyrrolidinylindolen. Hanessian påstår att denna metod kan i framtiden utnyttjas vid syntes av alkaloider eller andra kväveföreningar av medicinskt intresse. 72 För att överkomma den traditionella Friedel-Crafts regiospecificiteten, 3-substitution, måste man införa en aktiverande grupp på indolen. Petasis et al. 75, 76 har visat att B(OR) 2 - substituenter är bra aktiverande grupper i asymmetriska additionsreaktioner. En utvecklad BF - 3 (K + )-substituent har senare introducerats av Molander 77 och Vedejs 78. MacMillan et al. kom år 2007 fram till att både B(OH) 2 - och speciellt den utvecklade BF - 3 (K + )-substituenten aktiverar indolens 2-position i alkyleringsreaktioner. Boransubstituenten styr därmed alkyleringens regioselektivitet vilket leder till att de 2-substituerade indolprodukterna kan erhållas i höga ee-värden. I schema 24 presenteras en totalsyntes av indolderivatet, deoxifrondosin B 79, (R)-108, där 2-BF - 3 (K + )-substituerad N-boc-indol, 105, alkyleras med 40
44 krotonaldehyd, 51, i ett mellansteg. Vid addition av 107 till alkyleringsprodukten 106 följt av en syrakatalyserad ringslutningsreaktion bildas 108. Det regiospecifika alkyleringssteget visas som en intermediär. Schema 24 Denna metod har senare tillämpats på benzofuraner för att åstadkomma de mindre vanliga 2-substituerade slutprodukterna, se sid 55. I tidigare avsnitt visades att asymmetrisk F-C-alkylering av olika indoler med - omättade aldehyder där sekundära aminer använts som katalysatorer är en effektiv och mångsidig metod för att framställa -indolsubstituerade aldehdyder. Xiaos 80 försök att använda en av dessa sekundära aminkatalysatorer vid alkylering av indol med en svagare elektrofil, -omättad keton, resulterade i ett dåligt utbyte på 52 % och ett ee-värde på 28 %. Chen och medarbetare 22 fann att sekundära aminkatalysatorer i allmänhet har en dålig aktiveringshastighet vid alkylering av indoler med -omättade ketoner. Detta ledde till att Chens grupp introducerade primära aminkatalysatorer som ett bättre alternativ för alkyleringarna. De primära aminerna har en större sterisk frihet vid aminogruppen vilket höjer deras aktivitet mot enoner. Detta underlättar bildningen av ketiminkatjonen och 41
45 sänker intermediärens LUMO-energi. Inspirerade av detta syntetiserade Chens grupp två diaminer som härstammar från den naturligt förekommande cinkoninen. Dessa diaminer, speciellt 111 i kombination med TfOH som kokatalysator, har visat lovande katalytisk aktivitet i F-C-alkyleringar av indoler, 109, med -omättade ketoner, 110, se schema 25. Schema 25 Produkterna, 112, erhölls i väldigt varierande utbyten och selektiviteter, se tabell 15. Moderata utbyten och selektiviteter erhölls då indol alkylerades med alifatiska eller aromatiska enoner (ansatserna 1 2). Då 5-metoxiindolen 109b alkylerades med de aromatiska enonerna 110e och 110f erhölls utmärkta utbyten, över 93 %. Endast dåliga till moderata selektiviteter erhölls (ansatserna 6 och 7). Höga selektiviteter men låga utbyten erhölls då etylenoner användes som elektrofiler i F-C-alkyleringarna (ansatserna 3 och 9). När den 2-metylsubstituerade indolen 109d alkylerades med enonen 110a blev utbytet för alkyleringsprodukten utmärkt, 99 %, medan selektiviteten blev endast moderat, 65 %. Elektronattraherande grupper i indolens C5-position kan införas utan förlust i utbyte (ansats 10). Selektiviteten sjunker dock lite. Reaktionerna som utfördes vid högre temperaturer gav betydligt bättre utbyten, men selektiviteterna sjönk en aning
46 Tabell 15. Resultaten från F-C-alkyleringarna av indoler med katalysator 111 användes -omättade ketoner där Ansats Indol Keton Produkt Utbyte ee 1 X= H (109a) R 1 = n-pr, R 2 = Me (110a) 112a X= H (109a) R 1 = Ph, R 2 = Me (110b) 112b X= H (109a) R 1 = Ph, R 2 = Et (110c) 112c X= 5-MeO (109b) R 1 = n-pr, R 2 = Me (110a) 112d 74 * 78 5 X= 5-MeO (109b) R 1 = n-pr, R 2 = Me (110a) 112d 43 ** 84 6 X= 5-MeO (109b) R 1 = p-cl-ph, R 2 = Me (110d) 112e X= 5-MeO (109b) R 1 = p-meo-ph, R 2 = Me 112f (110e) 8 X= 5-MeO (109b) R 1 = 2-tienyl, R 2 = Me (110f) 112g X= 5-MeO (109b) R 1 = p-cl-ph, R 2 = Et (110g) 112h X= 5-Br (109c) R 1 = n-pr, R 2 = Me (110a) 112i X= 2-Me (109d) R 1 = n-pr, R 2 = Me (110a) 112j * Utfört vid -10 ** Utfört vid -20 Melchiorre et al. 23 undersökte samma alkyleringsprocess som Chens grupp hade gjort tidigare. Skillnaden var att Melchiorre introducerade en kiral kokatalysator för att försöka förbättra utbytena och ee-värdena för reaktionerna. Olika maskerade och omaskerade L- fenylglycinderivat tillsammans med katalysator 115 prövades för att optimera F-Calkyleringen av indol med kanelaldehyd. Speciellt L-fenylglycinderivatets N-skyddsgrupp hade en stor inverkan på reaktiviteten. Omaskerad L-fenylglycin ledde till en misslyckad reaktion. En avsevärd förbättring uppnåddes då N-boc-maskerad kokatalysator användes. Produktens utbyte var då 16 % och ee-värdet 90 %. Det bästa resultatet, utbyte över 95 % och ee-värdet 87 %, erhölls trots allt med den motsatta enantiomeren, D-N-bocfenylglycin, av den maskerade kokatalysatorn vid 70. Alkyleringsprodukten som erhölls var förvånande nog samma enantiomer som erhölls vid reaktion med L-N-boc-fenylglycin. De Friedel-Crafts-alkyleringar av indoler, 113, med -omättade ketoner, 114, där katalysator 115 i form av D-N-boc-fenylglycinsalt användes presenteras i schema
47 Schema 26 Melchiorres resultat var i allmänhet bättre än Chens, vilket tyder på att särskilt bytet av kokatalysator inverkar drastiskt på reaktionen. Den kirala motjonen bidrar till ett höjt utbyte och ee-värde i de flesta försöken, se tabell 16. Alkylering av indol 113a tolererar steriska och elektroniska förändringar i enonens -substituent. Forskningsgruppen kom också fram till samma slutsats som Chen nämligen att etylketoner bidrar till högre enantioselektiviteter än motsvarande metylketoner. Indol har också framgångsrikt alkylerats med aromatiska omättade ketoner där R 2 =Ph (ansats 6) vilket är värt att notera. Förändringar i indolstrukturen kan också göras utan större förluster i selektiviteterna. Enda begränsningen var de N-substituerade indolerna, som gav alkyleringsprodukter i lågt utbyte. Detta har redan tidigare förklarats m.h.a. den bifunktionella aktiveringsmekanismen
48 Tabell 16. Resultaten från F-C-alkyleringarna av indoler med katalysator 115 användes -omättade ketoner där Ansats Indol Keton Produkt Utbyte ee 1 X= H (113a) R 1 = Ph, R 2 = Me (114a) 116a X= H (113a) R 1 = 2-tienyl, R 2 = Me (114b) 116b X= H (113a) R 1 = Me, R 2 = Me (114c) 116c X= H (113a) R 1 = CH 3 (CH 2 ) 4, R 2 = Me 116d (114d) 5 X= H (113a) R 1 = Ph, R 2 = Et (114e) 116e X= H (113a) R 1 = Ph, R 2 = Ph (114f) 116f X= 5-Cl (113b) R 1 = CH 3 (CH 2 ) 4, R 2 = Me (114d) 8 X= 5-MeO (113c) R 1 = CH 3 (CH 2 ) 4, R 2 = Me (114d) 9 X= 2-Me (113d) R 1 = CH 3 (CH 2 ) 4, R 2 = Me (114d) 116g h i Kwiatkowski et al. 81 har fortsatt att förbättra och utveckla Chens och Melchiorres metoder för alkylering av indoler, 117, med -omättade ketoner. Kwiatkowski anpassade metoden även till mindre reaktiva -disubstituerade enoner, 118, genom att utföra reaktionen vid högt hydrostatiskt tryck, se schema 27. Reaktionshastigheten ökar då man kombinerar ett högt tryck med den bifunktionella katalysatorn, 119. Produkten som bildas har ett kvaternärt stereocentrum vilket inte kan erhållas med Chens eller Melchiorres metoder. Dessutom räcker det med en mindre mängd katalysator (10 mol%). 45
49 Schema 27 Indolylprodukterna, 120, bildas i moderata utbyten och enantioselektiviteter, se tabell 17. Med -disubstituerade enoner erhölls ee-värden upp till 80 % (ansatserna 1 3). Cykliska -substituerade enonen 118d kan också användas, men reaktionens selektivitet sjunker då till 48 %. Resultaten visar att Kwiatkowskis metod kan användas vid framställning av mera komplicerade alkyleringsprodukter. 81 Tabell 17. Resultaten från F-C-alkyleringarna av indoler med höga tryck där katalysator 119 användes -omättade ketoner vid Ansats Keton Produkt Utbyte ee 1 R 1 = Et, R 2 = CO 2 Et, R 3 = Me (118a) 120a R 1 = Me, R 2 = CO 2 Et, R 3 = Bu (118b) 120b R 1 = Ph(CH 2 ) 2, R 2 = CO 2 Et, R 3 =Me (118c) 120c R 1,3 = -(CH 2 ) 3 -, R 2 = Me (118d) 120d Alkylering av aniliner Aniliner är aminosubstituerade aromatiska föreningar som gärna deltar i elektrofila aromatiska substitutionsreaktioner, t.ex. F-C-alkyleringar. Det var MacMillans grupp 3 som utvecklade också den organokatalytiska asymmetriska F-C-alkyleringen av aniliner med -omättade aldehyder. Alkyleringsprodukterna har bensyliska stereocentra som förekommer i många isolerbara naturprodukter och läkemedel t.ex. Paxil 82, Detrol 83 (Tolterodin) och Zoloft 84. MacMillan användede sin för heteroaromatiska nukleofiler effektiva LUMO-sänkande iminaktiveringsmekanism också på F-C-reaktioner av aniliner. Gruppen utnyttjade andra generationens imidazolidinonkatalysator, 2, och märkte att 46
50 aniliner, 121, kan alkyleras stereoselektivt med 28. -omättade aldehyder, 122, se schema Schema 28 Utbytena var höga och selektiviteterna utmärkta för alkyleringsprodukterna då olika aniliner alkylerades med enaler, se tabell 18. Enalens -substituent kan varieras både med avseende på steriska och elektroniska faktorer utan att förorsaka en större utbytesförlust eller mindre selektivitet. Resultaten för reaktionerna med -aromatiska omättade aldehyder (ansatserna 2 och 4) var särskilt lovande då den bildade produkten innehåller ett bisbensyliskt stereocentrum. Denna struktur är viktig då den förekommer i potentiella läkemedelsföreningar. Förändringar i anilinstrukturen kan också göras utan problem. Då olika N-substituerade aniliner alkyleras med enal 122c fås p-substituerade produkter i höga selektiviteter. Orto- och metasubstituerade aniliner kan också delta i alkyleringar med samma enal 122c för att bilda trisubstituerade alkyleringsprodukter. Dessutom kan 1- naftylaminer också delta i F-C-alkyleringar med enaler och bilda produkter i högt utbyte och god selektivitet (ansats 7). Alkylering av m-kloranilin, 121h, med metyl-4- oxobutenoat, 122c, bildar en viktig halogensubstituerad produkt, 123h, i bra utbyte (73 %) och högt ee-värde (93 %). Den kan användas som utgångssubstrat för olika metallkatalyserade omvandlingar, t.ex. Stille- eller Suzukikopplingar. Reaktionerna som utfördes vid rumstemperatur gav produkter med lite lägre utbyten och ee-värden, men reaktionstiderna var märkbart kortare. 3 47
51 Tabell 18. Imidazolidinonkatalyserade F-C-alkyleringar av aniliner med aldehyder -omättade Ansats Anilin Aldehyd Produkt Utbyte ee 1 R 1 = Me, R 2 = Me, R 3 = Me (122a) 123a X= H, Y= MeO (121a) 2 R 1,2 = -(CH 2 ) 4 -, X= H, R 3 = Ph (122b) 123b Y= MeO (121b) 3 R 1 = Me, R 2 = Me, R 3 = CO 2 Me (122c) 123c X= H, Y= MeO (121c) 4 R 1,2 = -(CH 2 ) 4 -, X= H, R 3 = p-no 2 -Ph (122d) 123d Y= H (121d) 5 R 1 = Bn, R 2 = Bn, X= H, R 3 = CO 2 Me (122c) 123e Y= H (121e) 6 R 1,2 = -(CH 2 ) 4 -, X= Ph, R 3 = CO 2 Me (122c) 123f Y= H (121f) 7 R 1 = Me, R 2 = Me, R 3 = CO 2 Me (122c) 123g X, Y= -CH=CH- CH=CH- (121g) 8 R 1 = Me, R 2 = Me, R 3 = CO 2 Me (122c) 123h 73 93* X= H, Y= Cl (121h) 9 R 1 = Me, R 2 = Me, R 3 = CO 2 Me (122c) 123h 66 86** X= H, Y= Cl (121h) * utfört i -20, 80 h ** utfört i 20, 12 h MacMillans grupp 85 har senare använt sin organokatalytiska asymmetriska anilinalkylering för att framställa (R)-tolterodin (Detrol är Pfizers varumärke), 127, se schema 29. (R)- Tolterodin är ett välkänt läkemedel mot urininkontinens. Föreningen påverkar muskarinreceptorn, som styrr de icke-viljestyrda kroppsfunktionerna
52 Schema 29 Kim et al. 87 har år 2005 rapporterat en totalsyntes av (+)-kurkufenol, 131, där MacMillans sätt att asymmetriskt alkylera aniliner användes, se schema 30. Huvudstegen i syntesen är den imidazolidinonkatalyserade F-C-reaktionen, diazotering/sandmeyers reaktion och organometallkoppling av Negishi-typ med dimetylzink. Schema 30 49
53 S-(+)-Kurkufenol är en biologiskt aktiv seskviterpenfenol som kan isoleras från havssvamparna Didiscus flavus och Epipolasis. Föreningen uppvisar antimykotikumaktivitet mot svamparten Candida albicans, antitumöraktivitet mot cancercellinjer och antimalariaaktivitet mot parasiten Plasmodium falciparium 88, 89. Dessutom inhiberar den proton-kalium ATP-syntasen 90. Den andra enantiomeren, R-( )- kurkufenol, som isolerats från hornkorallen Pseudopterogorgia rigida, har helt andra egenskaper och aktiviteter. Den har antibakteriella aktiviteter mot Staphylococcus aureus samt Vibrio anguillarum 91. Förutom -alkyl- och -arylsubstituerade -omättade aldehyder har också fosfor- och kvävesubstituerade enaler använts för att asymmetriskt alkylera aniliner, se schema 31. Xiao och medarbetare 65 presenterade en imidazolidinonkatalyserad alkylering av olika N,N-dimetylaniliner, 132, med dimetyl-3-oxoprop-1-enylfosfonat, 133. Efter reduktion av alkyleringsprodukterna bildades hydroxipropylfosfonaterna 134 i höga utbyten och eevärden, % respektive %. Produkt 134a, som har visat sig vara ett potentiellt antimalariamedel, hör till familjen -arylsubstituerade fosmidomycinanaloger 92. Hanessian et al. 72 visade att den kvävesubstituerade -omättade aldehyden deltar också i F-C-alkyleringar av aniliner. Alkyleringsprodukten 137 bildas i ett högt, 82 %, enantiomeröverskott då m-pyrrolidinylanisol 135 får reagera med enal 136. Schema 31 50
54 Även intramolekylär asymmetrisk Friedel-Crafts-alkylering av aniliner har gjorts. Xiaos grupp 58 rapporterade en imidazolidinonkatalyserad ringslutning av (E)-5-(3- (dimetylamino)fenoxi)pent-2-enal, 138. Den bildade kroman-4-ylacetaldehyden, 139, erhölls i högt utbyte (88 %) och ee (90 %), se schema 32. Schema Alkylering av naftoler, bensofuraner och furaner Förutom aniliner har andra aromatiska föreningar med starkt elektrondonerande substituenter, t.ex. naftoler, visat sig vara bra F-C-donorer med ett antal olika elektrofiler 93, 94. Trots detta har de inte tidigare använts i enantioselektiva Friedel-Crafts-alkyleringar. Wang et al. 95 har rapporterat en asymmetrisk diarylprolinoleterkatalyserad F-C-alkylering av naftoler med -omättade aldehyder för att bilda olika bensokromanderivat, se schema 33. Dessa strukturer förekommer i olika naturprodukter som har en hög biologisk aktivitet 96. Naftoler är utöver C- också bra O-nukleofiler vilket kan leda till problem vid de organokatalytiska asymmetriska F-C-reaktionerna 97. Wangs grupp 95 kom fram till att difenylprolinoltrimetylsilyleter 14c som 2-nitrobensoesyrasalt har den högsta katalysatoraktiviteten och styr reaktionerna så att C-alkylerade produkter bildas. Utbytena för produkterna var till en början låga p.g.a. iminiumintermediärens relativa stabilitet. Vatten tillsattes för att underlätta hydrolys av intermediären och på så sätt höja produktutbytena. Resultaten från F-C-reaktionerna med naftoler, 140, och -omättade aldehyder, 141, var bra, se tabell
55 Schema 33 Bensokromanderivaten 142 bildades i höga utbyten och utmärkta enantioselektiviteter. Produkternas diastereoselektiviteter var i allmänhet bra. Då 1-naftol fick reagera med olika substituerade kanelaldehyder erhölls produkterna i % utbyte och % ee. Kanelaldehyden 141b med en elektronattraherande substituent gav högre utbyten och eevärden än de med elektrondonerande 141c eller neutrala 141d substituenter. Dessutom var reaktionen med 1-naftol framgångsrik då mindre reaktiva alkyl- och heteroaromatsubstituerade enaler användes (ansatserna 4 och 5). Utbytena och ee-värdena var trots allt lägre än för reaktionerna med kanelaldehyderna. Förändringar i naftolstrukturen kunde också göras utan problem. Goda utbyten och selektiviteter erhölls. Utöver alkylering av naftol med -omättade aldehyder utfördes reaktionen också på fenol men låga (<10 %) produktutbyten erhölls. 95 Tabell 19. Difenylprolinoltrimetylsilyleterkatalyserade F-C-alkyleringar av naftoler med -omättade aldehyder Ansats Naftol Aldehyd Produkt Utbyte ee dr 1 R= H (140a) R 1 = Ph (141a) 142a :2 2 R= H (140a) R 1 = m-cl-ph (141b) 142b :1 3 R= H (140a) R 1 = m-meo-ph (141c) 142c :1 4 R= H (140a) R 1 = 2-furyl (141d) 142d :2 5 R= H (140a) R 1 = Me (141e) 142e :1 6 R= 4-Cl (140b) R 1 = Ph (141a) 142f :1 7 R= 5-MeO (140c) R 1 = Ph (141a) 142g :1 52
56 Senare har Bencivenni och medarbetare 98 asymmetriskt alkylerat naftoler med cykliska -omättade ketoner. Man vet redan från tidigare att då enoner används som elektrofiler vid F-C-alkyleringar behövs en primär amin som katalysator för att reaktionen skall ske. Bencivenni utnyttjade detta och presenterade katalysator 145 i alkylering av - och - naftoler (143 och 147) med olika cykliska -omättade ketoner (144 och 148). Alkyleringarna följdes av en acetalisering varefter makrocyklerna 146 och 149 bildades, se schema 34. Schema 34 Makrocyklerna 146 och 149 är nära besläktade med enokipodin A och C, se bild 9. Enokipodinerna är föreningar med antimikrobiell aktivitet och hör till gruppen seskviterpenoider av typen -kuparenon 99. Bild 9. Strukturerna för -kuparenon samt enokipodin A och C. 53
57 Själva alkyleringsreaktionerna gav varierande resultat, se tabell 20. I reaktion med cyklohex-2-enon 148a kunde -naftolen substitueras med olika grupper utan större förluster i produktens optiska renhet. Då cyklohept-2-enon 148b fick reagera med - naftoler sjönk utbytena en aning men selektiviteten var nästan oförändrad (ansats 12). Reaktion med en racemisk blandning av 4-etylcyklohex-2-enon 148c ledde till att endast den ena diasteroisomera alkyleringsprodukten 149f bildades i lågt utbyte, 16 %. Bencivennis grupp påstår att endast (S)-enantiomeren av 148c reagerade och bildade produkten. 98 Tabell 20. Resultaten från F-C-alkyleringarna av - och -naftoler med cykliska ketoner där katalysator 145 användes -omättade Ansats Naftol Keton n Produkt Utbyte ee 1* R= H (143a) R 1 = H, R 2 = H (144a) 1 146a * R= 4-Cl (143b) R 1 = H, R 2 = H (144a) 1 146b * R= 4-MeO (143c) R 1 = H, R 2 = H (144a) 1 146c * R= 4-NHBoc (143d) R 1 = H, R 2 = H (144a) 1 146d * R= H (143a) R 1 = H, R 2 = H (144b) 2 146e * R= H (143a) R 1 = Et, R 2 = H (144c) 1 146f * R= H (143a) R 1 = H, R 2 = Ph (144d) 1 146g ** R= H (147a) R 1 = H (148a) 1 149a ** R= 5-Br (147b) R 1 = H (148a) 1 149b ** R= 6-MeO (147c) R 1 = H (148a) 1 149c ** R= 2-NHBoc (147d) R 1 = H (148a) 1 149d ** R= H (147a) R 1 = H (148b) 2 149e ** R= H (147a) R 1 = Et (148c) 1 149f * -naftol användes ** -naftol användes Samma sak sker då en racemisk blandning av den cykliska ketonen 144c får reagera med -naftol. I övriga fall betedde sig -naftolerna annorlunda. Selektiviteten var bättre än för alkyleringar med -naftolerna. Ett intressant resultat erhölls då en racemisk blandning av 5-fenylcyklohex-2-enon 144d fick reagera med -naftol. Båda enantiomererna reagerade 54
58 och bildade två olika produkter. (S)-enantiomeren gav den acetaliserade produkten 146g medan (R)-enantiomeren bildade endast den icke-acetaliserade alkyleringsprodukten som vanligtvis bildas i F-C-reaktioner. En icke-acetaliserad alkyleringsprodukt erhölls också då cyklopent-2-enon, 144, användes. Stora otympliga inden-1-oner har också adderats till olika substituerade - och -naftoler, se tabell 21. Goda utbyten och höga ee-värden erhölls för produkterna i alla försök. 98 Tabell 21. Resultaten och schema för F-C-alkyleringarna av - och -naftoler med olika inden-1-oner där katalysator 145 användes Ansats Naftol Keton Produkt Utbyte ee 1* R= H (150a) R 1 = H (152a) 153a * R= H (150a) R 1 = 6-Me (152b) 153b * R= Br (150b) R 1 = 5-F (152c) 153c * R= MeO (150c) R 1 = 5-Cl (152d) 153d ** R= Cl (151a) R 1 = 5-F (152c) 154a ** R= MeO (151b) R 1 = 6-Me (152b) 154b ** R= MeO (151b) R 1 = 5-Cl (152d) 154c * -naftol användes ** -naftol användes 55
59 Bensofuraner är aromatiska föreningar med indollika egenskaper. Bensofuranerna såväl som indolerna föredrar substitution av 3-positionen vid F-C-alkyleringar med - omättade aldehyder. För att uppnå 2-substituerade bensofuraner, som är icke-traditionella Friedel-Crafts-produkter, bör man införa en aktiverande grupp i utgångssubstratets 2- position. Både BF - 3 (K + ) och B(OH) 2 har av MacMillan et al. 74, 79 visats fungera bra som aktiverande grupper. I schema 35 presenteras de 2-bensofuranylboranernas, 155, imidazolidinonkatalyserade asymmetriska alkyleringar med krotonaldehyd, 51. Selektiviteterna för alkyleringsprodukterna, 156, var höga, %. Utbytena var beroende av aktiverande gruppen. Bensofuraner med en BF - 3 (K + )-substituent, 155a, gav utbyten över 90 % medan den med en B(OH) 2 -substituent, 155b, gav endast utbytet 52 %. Schema 35 MacMillan 79 har senare tillämpat denna metod för att framställa (+)-frondosin B och dess analoger. Frondosin B är en seskviterpenoid som har isolerats från havssvampen Dysidea frondosa av Freyers grupp i Mikronesien år , 101. Föreningen är en mikromolär inhibitor mot interleukin-8 (IL-8) och protein kinas C (PKC) 101. IL-8 aktiverar neutrofiler som ökar bildningen av monocytsuperoxidanjoner. Denna ökning har implicerats i olika sjukdomar som psoriasis, reumatoid artrit och artros. Utveckling av cancertumörer kan också bero på neutrofilaktiveringen av IL-8. Frondosin är därmed ett potentiellt antiinflammatoriskt och antitumörmedel 102, 103. Själva framställningen av (+)-frondosin B bestod av F-C-alkylering av bensofuran 157 med krotonaldehyd 51, vinylering av bildade aldehyden 158 och ringslutning via allylisk substitution/isomerisering av dubbelbindningen. Denna korta och effektiva totalsyntes för att bilda (+)-frondosin B, 160, och dess analog, 159, schema 36, presenterades av MacMillans grupp
60 Schema 36 Furan som har en pyrrollik struktur föredrar 2-substitution i alkyleringsreaktioner. 2- Metylfuran, 161, har asymmetriskt alkylerats med olika -omättade aldehyder, 162, se schema 37, via den bicykliska kaskadmekanismen som MacMillan 12 rapporterade år 2005, se sidorna 6 och 7. Kinon 47 användes som elektrofildonerande reagens. Kaskadprodukterna, 163, erhölls i höga utbyten (74 86 %), enantioselektiviteter (ee 99 %) och diastereoselektiviteter (dr = 11:1 22:1) beroende på vilken omättad aldehyd som användes. 2-Metylfuran har senare kombinerats med 3-aminokrotonaldehyd av Hanessian et al. 72 Alkyleringsprodukten erhölls i 88 % utbyte och 96 % enantiomeröverskott. Dessutom erhölls alkyleringsprodukten i högt utbyte, 85 %, och utmärkt ee-värde, 95 %, då 2-formylfuran alkyleras med krotonaldehyd. Schema 37 57
61 4. Experiment Syftet med denna experimentella del i pro gradu arbetet var att försöka syntetisera en ny kiral imidazolidinonkatalysator, 165, och undersöka dess aktivitet i olika asymmetriska Friedel-Crafts-alkyleringar. F-C-alkylering av indol, 164, och N-metylpyrrol, 22, med krotonaldehyd, 51, valdes för aktivitetsbestämningen, se schema 38. Schema 38 Meningen var att jämföra de för alkyleringsprodukterna, 166 och 167, erhållna utbytena och ee-värdena med referensvärden och på så sätt bestämma den nya katalysatorns aktivitet i dessa asymmetriska F-C-reaktioner. 4.1 Syntesrutt Imidazolidinonen som skulle framställas var 2-(t-butyl)-5-isobutyl-3-metyl-imidazolidin-4- on hydroklorid 165. Vi valde att utgå från den lättillgängliga aminosyran L-leucin, 168, och att främst följa den framställningsmetod av imidazolidinoner som MacMillan 104 föreslagit år Efter att katalysatorn framställts derivatiserades den genom bensoylering för att få en produkt, 172, med känt -värde. Genom att jämföra referensvärdet med det uppmätta -värdet för den bensoylerade produkten kan dess och därmed också katalysatorns optiska renhet bestämmas. I schema 39 presenteras den 58
62 retrosyntetiska modellen för framställning av katalysatorn 165 och dess derivat 172. Reaktionstegen är enkla organiska basreaktioner som inte kräver användning av skyddsgrupper. Schema 39 Framställning av den nya katalysatorn består av fyra steg. Först esterifierar man L-leucin, 168, genom att återloppskoka den i MeOH och SOCl Andra steget innebär en amidering av estern 169 med 33 %-ig metylamin-/etoh-lösning vid rumstemperatur. För att omvandla den primära aminen till en imin låter man 170 reagera med egenframställd pivalaldehyd (2,2-dimethylpropanal) och Et 3 N. Katalysatorn erhölls efter cyklisering av iminen 171, som sker genom tilldroppning av acetylklorid vid låg temperatur 104. Den isolerade katalysatorn 165 omvandlades till derivatet 172 genom tillsättning av bensoylklorid och Et 3 N under magnetomrörning vid 0. Derivatets D-värde mättes för att bestämma dess optiska renhet 106. I schema 40 presenteras de fullständiga reaktionsförhållandena vid totalsyntesen av katalysatorn och dess derivat. Schema 40 59
63 Pivalaldehyden 175, som är ett av utgångsämnena i det tredje reaktionsskedet, var egenframställd. Vi beslöt att utgå från pivaloylklorid, 173, och göra en kombinerad reduktions/oxidationsreaktion, se schema 41. Reduktion av pivaloylkloriden med 0,5 ekv. 2 M LAH-lösning i THF vid 0 bildar en alkoxialuminiumintermediär, 174, som utan mellanisolering kan oxideras vidare med PCC i rumstemperatur till pivalaldehyd. Denna metod har trots allt två nackdelar. Reduktionsmedlet LAH är en krånglig förening att handskas med och dessutom är upparbetningen efter oxidationen väldigt obekväm. 107 Schema 41 Detta ledde till att andra syntesvägar för pivalaldehyd beaktades. Två välkända namnreaktioner där pivalaldehyden görs från den lätt tillgängliga t-butylkloriden, 176, ansågs vara användbara. Vi följde både Bouveaults och Bodroux-Chichibabins aldehydsynteser som båda baserar sig på grignardering med t-butylmagnesiumklorid, 177, se schema 42. Schema 42 I båda metoderna bildades grignardreagenset, t-butylmagnesiumklorid, genom att svagt återloppskoka t-butylklorid och Mg-spån i nydestillerad Et 2 O 108, 109. Efter det skiljer sig metoderna från varandra. I Bouveault-metoden formyleras grignardreagenset med en N,Ndisubstituerad formamid t.ex. DMF eller N-fenyl-N-metylformamid (N-metylformanilid) till en hemiaminal, 178. Med sur upparbetning hydrolyserades hemiaminalen till pivalaldehyd 110, 111. I Bodroux-Chichibabin-metoden omvandlas grignardreagenset till en acetal, 179, genom att införa trietylortoformat och återloppskoka blandningen. Acetalen 60
64 hydrolyserades med koncentrerad svavelsyra till pivalaldehyd 111, 112. I schema 43 presenteras reaktionsförhållandena för båda aldehydsynteserna. Schema 43 Efter att katalysatorn framställts och identifierats användes den i asymmetriska Friedel- Crafts-reaktioner. Reaktionerna som valdes var från tidigare kända alkyleringar där MacMillans första och andra generationens katalysatorer använts. Detta ger möjlighet att jämföra vår nya imidazolidinonkatalysators aktivitet i asymmetriska F-C-alkyleringar med MacMillans motsvarande. Vi valde att alkylera indol, 164, med krotonaldehyd, 51, där den nya imidazolidinonen 165 fungerade som katalysator. Alkyleringsprodukten 166 är en relativt instabil aldehyd i aerobiska förhållanden vilket gjorde identifieringen av den krånglig. Vi beslöt att oxidera aldehyden till motsvarande karboxylsyra, 180, för att kunna bestämma den optiska renheten. I schema 44 presenteras den retrosyntetiska modellen för alkyleringen och oxidationen. Schema 44 Alkyleringen utfördes genom att låta indol reagera med krotonaldehyd i närvaro av katalysatorn 165 och kokatalysatorn TFA vid låga temperaturer 113. För att oxidera den bildade aldehyden infördes en katalytisk mängd AgNO 3. Sedan tillsattes H 2 O 2 och 61
65 blandningen uppvärmdes till 50 schema varefter den eftertraktade karboxylsyran bildades, se Schema Synteser och karaktärisering Reagensen som användes var lätt tillgängliga kommersiella föreningar. Syntesernas fortskridande följdes med tunnskiktskromatografi (TLC kiselgelplattor 60 F 254 ). Detektionen gjordes med en UV-ljuskälla (Spectroline, 254 nm). Syntesprodukterna renades med pelarkromatografi (kiselgel 60, 0,063 0,200 mm) eller omkristallisation. Produkterna karaktäriserades med FT-IR-spektrometer (PerkinElmer, Spectrum 100). Dessutom gjordes en elementäranalys (Elementar, vario micro cube) och smältpunktsbestämningar (Stuart Scientific, melting point SMP10) på produkterna. Polarimetriska bestämningar (Jasco DIP-1000, kyvett 10 cm) för att erhålla -värden för produkterna gjordes också. L-leucinmetylester hydroklorid (169): L-Leucin, 15 g, och MeOH, 210 ml, infördes i en 500 ml:s tvåhalskolv försedd med dropptratt och återloppskylare försedd med gasfälla. I dropptratten infördes 20,65 ml (2,45 ekv.) SOCl 2 som tilldroppades reaktionsblandningen under magnetomrörning och nedkylning (0 ) med isbad. Efter halva tillsatsen löste sig den heterogena blandningen helt och en klar lösning erhölls. Tillsatsen slutfördes på 30 min varefter isbadet avlägsnades och lösningen återloppskokades i 3 h. Uppvärmningen avslutades och lösningen omrördes i rumstemperatur över natten. Reaktionen avslutades och lösningsmedlet indunstades med en rotationsindunstare (Büchi rotavapor R-205). Toluen, 20 ml, infördes och indunstades för att försöka avlägsna det mesta av lösningsmedlet som en azeotrop. Detta upprepades fyra gånger. Produkten renades genom omkristallisation med MeOH/Et 2 O vid 0. Ett vitt fast ämne erhölls som ytterligare 62
66 torkades i en vakuumugn (Heraeus, 50 ) i 1,5 h. Utbytet var 20 g (96,7 %) och ee = 95,5 %. Smp: 151. IR (cm -1 ): 2845, 2050, 1736, 1590, 1507, 1452, 1225, Elementäranalys: N= 7,7 %, C= 46,1 %, H= 8,7 %. [ ]= +16,8. IR- och [ ]-värdena stämmer bra överens med litteraturvärdena 115, 116. L-leucin-N-metylamid hydroklorid (170): I en 100 ml:s tvåhalskolv försedd med torkrör och septum med injektionsnål infördes 10,3 ml (3,5 ekv.) MeNH 2 -lösning i EtOH. Lösningen omrördes magnetiskt under argonatmosfär och kolven sänktes ned i ett rumstempererat vattenbad. L-leucinmetylester hydroklorid, 4,29 g, tillsattes MeNH 2 - lösningen som omrördes i ytterligare 12 h. Reaktionen avslutades och lösningsmedlet indunstades med en rotationsindunstare. Ett klibbigt fast ämne erhölls. Toluen, 20 ml, tillsattes och indunstades för att försöka avlägsna det mesta av lösningsmedlet som en azeotrop. Detta upprepades några gånger varefter det torkade fasta ämnet dekanterades med 2 20 ml Et 2 O. Detta avlägsnar den eterlösliga fria aminamiden och den i esterifieringen bildade biprodukten, dimetylsulfiten. Produkten torkades ytterligare i vakuumugn (40 ) i 1,5 h. t-butylmagnesiumklorid (grignardreagens) (177): I en 250 ml:s trehalskolv försedd med septum med injektionsnål, återloppskylare med torkrör och dropptratt med torkrör infördes 3,62 g Mg-spån och en jodkristall. En lösning av 80 ml torr Et 2 O och 20ml nydestillerad t-bucl framställdes. Av denna lösning togs 10 ml och infördes i kolven med Mg-spånen under magnetomrörning i argonatmosfär. En kraftig reaktion skedde omedelbart och blandningen började svagt återloppskoka. Efter några minuter tillsattes 30 ml torr eter under konstant omrörning och argonatmosfär. I dropptratten infördes 70 ml av den kvarblivna t-bucl/et 2 O-lösningen. Lösningen tilldroppades reaktionsblandningen med en hastighet på 1 droppe/sek. Efter att tillsatsen slutförts fortsattes omrörningen i argonatmosfär och en ny utspädd lösning gjordes under tiden. Den kvarblivna t- BuCl/Et 2 O-lösningen, 20 ml, utspäddes med 50 ml torr eter och infördes i dropptratten. Den utspädda lösningen tilldroppades reaktionsblandningen med samma hastighet som tidigare. Reaktionsblandningen fick återloppskoka svagt och omröras i ytterligare 1 h efter den sista tillsatsen. Det bildade grignardreagenset användes vidare oisolerat och orenat för framställning av pivalaldehyd. 63
67 Pivalaldehyd (175): Kolven med den tidigare framställda grignardreagenslösningen kyldes till -20 med en CO 2 -is/aceton-blandning. Återloppskylaren avlägsnades och ersattes med en termometer. Ny DMF, 12,4 ml, löstes i 16,1 ml Et 2 O. Denna lösning infördes i en dropptratt och tilldroppades grignardreagenset under omrörning i argonatmosfär. Tillsatsen slutfördes på 50 min dock så att temperaturen inte överskred -15. En grå fällning bildades vilken försvann efter en tid. Till reaktionsblandningen tilldroppades snabbt ytterligare 12,4 ml DMF vid -8. Fem minuter senare tillsattes 0,08 g hydrokinon varefter en vit lösning med grå fällning erhölls. Kolven hölls nedkyld och 40 ml 4 M HCl tillsattes försiktigt. En kraftig reaktion skedde då vätgas bildades. Lösningen infördes i en skiljetratt och eterskiktet (moderlösningen) separerades. Vattenfasen extraherades med 3 10 ml Et 2 O. Eterskikten separerades och kombinerades med moderlösningen. Lösningen torkades med MgSO 4 och filtrerades. Lösningsmedlet fraktionsdestillerades försiktigt bort. Destillationen fortsattes och pivalaldehyden kom över vid 70. Utbytet var 2,91 ml. Kp: 70. IR (cm -1 ): 2956, 2926, 2854, 1733, 1461, 1365, 1284, 1151, 989. IR-värden stämmer bra överens med litteraturvärden 117. (S,E)-2-(2,2-dimetylpropylidenamin)-4-metyl-N-metylpentanamid (171): I en 100 ml:s tvåhalskolv försedd med torkrör och septum med injektionsnål infördes 3,14 g L-leucin-Nmetylamid hydroklorid, 15 ml DCM och 4 g MgSO 4. Kolven sattes i ett rumstempererat vattenbad och omrördes magnetiskt i argonatmosfär. Et 3 N, 3,63 ml och pivalaldehyd, 2,1 ml tillsattes den väl omrörda reaktionsblandningen. Omrörningen fortsattes i 12 h och reaktionens fortskridande följdes med TLC (eluent: EtOAc-EtOH 5:1). Ytterligare pivalaldehyd, 0,22 ml, och MgSO 4, 1 g, tillsattes. 30 minuter efter tillsatsen byttes torkröret ut mot en dropptratt i vilken 20 ml toluen infördes. Toluenet tilldroppades på 10 min varefter reaktionsblandningen omrördes i 15 min. MgSO 4 och den bildade trietylaminhydrokloriden filtrerades bort och tvättades med 3 5 ml toluen. Filtratet koncentrerades med en rotationsindunstare och ytterligare trietylamin hydroklorid föll ut. Toluen, 10 ml, tillsattes och filtreringsprocessen, tvätten och indunstningen upprepades. En gul olja som torkades i en vakuumugn (20, 12 h) erhölls. Produkten sattes i frysen där den kristalliserades till ett vitgult fast ämne. Utbytet var 2,4 g (65 %). Smp: 45. IR (cm -1 ): 3345, 2952, 1663, 1520, 1469, 1406, 1316, 1254, 1158, 928. Elementäranalys: N= 12,9 %, C= 66,3 %, H= 11 %. [ ]= -2,2. 64
68 (2R, 5S)-2-(t-butyl)-5-isobutyl-3-metyl-imidazolidin-4-on hydroklorid (165): EtOH, 2,4 ml, infördes i en trehalskolv försedd med termometer, tryckutjämnande dropptratt och septum med injektionsnål. Kolven kyldes ner till 1 3 med ett isbad och lösningen magnetomrördes. I dropptratten infördes 0,37 ml acetylklorid. Acetylkloriden tilldroppades på 15 min vilket ledde till en temperaturhöjning på ca. 15. Kolven kyldes på nytt ner till 5 varefter orenad imin, 1 g, tillsattes. Kolven som innehållit iminen sköljdes med EtOH och tvättlösningen tilldroppades reaktionsblandningen via dropptratten. Isbadet avlägsnades och lösningen uppvärmdes till 70. Uppvärmningen avslutades och lösningen omrördes 12 h vid rumstemperatur. Reaktionen avslutades och lösningsmedlet indunstades med en rotationsindunstare. En vitgul produkt kristalliserade och renades genom omkristallisation med EtOH/Et 2 O. Vit fast imidazolidinon hydroklorid, 620 mg (53,9 %) erhölls. Smp: 197. IR (cm -1 ): 2960, 2873, 2511, 1705, 1400, 1369, 1312, 1261, 1079, 997. Elementäranalys: N= 11,2 %, C= 57,7 %, H= 9,8 %. [ ]= -48,9. (2R, 5S)-1-bensoyl-2-(t-butyl)-5-isobutyl-3-metylimidazolidin-4-on (172): Imidazolidinon hydroklorid, 400 mg, löstes i 5 ml DCM och infördes i en 50 ml:s tvåhalskolv. Kolven kyldes till 0 med ett isbad varefter 0,19 ml bensoylklorid och 0,45 ml Et 3 N tillsattes under omrörning. Isbadet avlägsnades och lösningen omrördes i ytterligare 12 h. Reaktionen avslutades och lösningen utspäddes med 10 ml Et 2 O. Den utspädda lösningen infördes i en skiljetratt och tvättades med 2 10 ml 2 M Na 2 CO 3 och 2 5 ml H 2 O. Den organiska fasen separerades och torkades med MgSO 4. Torkmedlet filtrerades bort och lösningsmedlet indunstades med rotationsindunstare. En gul olja erhölls som kristalliserade i frysen. Produkten renades genom omkristallisation med Et 2 O/hexan. Utbytet var 50 mg och ee = 97,6 %. Smp: 114. IR (cm -1 ): 2959, 2869, 1627, 1449, 1363, 1314, 1256, 1203, 1097, 872. Elementäranalys: N= 8,8 %, C= 71 %, H= 8,8 %. [ ]= +16,9. Det uppmätta [ ]-värdet stämmer bra överens med litteraturvärdet 118. (2R, 5S)-2-(t-butyl)-5-isobutyl-3-metylimidazolidin-4-on: (2R, 5S)-2-(t-butyl)-5- isobutyl-3-metyl-imidazolidin-4-on hydroklorid, 50 mg, löstes i 5 droppar H 2 O. Vattenlösningen gjordes starkt basisk med 0,1 M NaOH och extraherades med DCM. Den organiska fasen separerades och torkades med MgSO 4. Efter filtrering och indunstning av lösningsmedlet erhölls 47 mg (88,5 %) av den frigjorda imidazolidinonkatalysatorn. 65
69 (R)-3-(indol-3-yl)butanal (166): I ett provrör infördes 47 mg frigjord imidazolidinon. Provröret kyldes till -60 varefter 16,9 l TFA, 129,7 mg indol, 2 ml DCM och 0,2 ml isopropanol tillsattes. Reaktionsblandningen omrördes nedkyld i 5 min. Krotonaldehyd, 91,7 l, tillsattes och lösningen omrördes i 19 h vid -60. Reaktionens fortskridande följdes med TLC (eluent: hexan-etoac 1:1). Reaktionen avslutades och lösningen filtrerades genom ett sinter med 1 cm kiselgel. Kiselgelen sköljdes med Et 2 O varefter filtratet koncentrerades med rotationsindunstare. Produkten renades med pelarkromatografi (eluent: hexan-etoac 1:1). Produkt erhölls 150 mg och användes oisolerat och orenat vidare. (R)-3-(indol-3-yl)smörsyra (180): I en 100 ml:s tvåhalskolv försedd med återloppskylare och septum med injektionsnål infördes 13,6 mg AgNO 3, 150 mg (R)-3-(indol-3-yl)-butanal och 2 ml MeCN. Lösningen omrördes magnetiskt varefter 0,4 ml 30 %-tig H 2 O 2 tillsattes reaktionsblandningen. Blandningen uppvärmdes långsamt till 50. Reaktionen avslutades efter 3,5 h och en upparbetning gjordes. 10 %-tig Na 2 S 2 O 3 tillsattes tills ph för lösningen överskred 7. För att försäkra sig om att produkten hölls i vattenfasen tillsattes en liten mängd mättad NaHCO 3. Organiska föroreningar extraherades med DCM varefter vattenfasen surgjordes med 2 M HCl och tvättades med DCM. DCM-faserna separerades, torkades med MgSO 4 och indunstades med en rotationsindunstare. Ingen produkt kunde dock identifieras. 4.3 Resultat och diskussion Syntesrutten för framställningen av den nya imidazolidinonen fungerade relativt bra. Slutprodukten, katalysatorn, kunde erhållas i ett tillräckligt högt utbyte för att kunna användas vidare för asymmetrisk F-C-alkylering av indol. Själva alkyleringsreaktionen var inte lyckad. Framställningen av pivalaldehyd var möjligt men inte rekommenderbart p. g. a. det låga utbytet som erhölls. Esterifieringen av L-leucin med tionylklorid i MeOH gav ett högt utbyte och relativt ren produkt. I reaktionen bildades det en oönskad biprodukt, dimetylsulfit. Dimetylsulfiten störde inte nästa reaktionssteg vilket betyder att man kunde använda estern som sådan efter omkristallisation. Ifall man lät estern stå tillräckligt länge i öppet kärl indunstade dimetylsulfiten mycket långsamt. 66
70 Det andra reaktionssteget gick också väldigt bra i form av högt utbyte. Produkten, amidhydrokloriden, var en extremt klibbig förening och därmed svår att hantera. Detta kunde bero på att den innehöll förutom amidhydroklorid också fri amid och dimetylsulfit från esterifieringen. De två sistnämnda kunde avskaffas genom att dekantera produktblandningen med Et 2 O. Detta gjorde också amidhydrokloridens konsistens mera kristallin och lättare att använda för vidare reaktioner. Pivalaldehyden som behövdes för att iminera amidhydrokloriden var svår att framställa. Reduktions-oxidationsmetoden hade en otäckt upparbetning då PCC:n bildade flera olika kromkomplex som var svåra att avskaffa. Bäst fungerade Bouveault-syntesen speciellt med DMF. Utbytet var trots allt väldigt lågt. Det påstås att högre utbyten fås då DMF byts ut mot N-metylformanilid men inga förbättringar uppnåddes. Den tredje metoden för att framställa pivalaldehyd, Bodroux-Chichibabins syntes med trietylortoformat, misslyckades. Upparbetningen var krånglig och innehöll många mellanskeden. Reaktionerna i de olika framställningsmetoderna var i allmänhet kraftiga men problemen uppstod i upparbetningarna. Imineringen av amidhydrokloriden med pivalaldehyd lyckades och moderata utbyten erhölls. Iminprodukten kristalliserar först i nedkylda förhållanden. Liknande resultat kunde uppnås då isobutyraldehyd användes. En begränsning som noterades var användningen av aromatiska aldehyder. Aromatiska aldehyder som har högre kokpunkter än alifatiska kan vara svåra att avskaffa i upparbetningsskedet. De alifatiska aldehyderna försvinner då lösningsmedlet indunstas med rotationsindunstaren. P.g.a. aromatiska aldehyders höga kokpunkter bör respektive iminer renas på ett annat sätt nämligen med pelarkromatografi. Ingen bra eluent som skulle ha separerat tillräckligt den aromatiska aldehyden från iminen hittades. Detta är ett problem som bör lösas före man kan iminera amidhydroklorider med aromatiska aldehyder. Ringslutningsreaktionen av iminen till imidazolidinonhydrokloriden gick bra. Efter omkristallisation erhölls ett rent vitt fast ämne i moderata utbyten. Kristallisationsprocessen är väldigt långsam vilket bör beaktas för att få bra utbyte. Iminen hydrolyseras relativt lätt i aeroba förhållanden vilket betyder att den bör förvaras under argon i kylskåp. I reaktionen bildades förutom produkt fri imidazolidinon. Dessutom kunde oreagerat utgångsämne hittas vilket skulle tyda på en för kort reaktionstid eller att acetylklorid använts i underskott. 67
71 Då imidazolidinonen skulle bensoyleras uppstod stora problem då det efter omkristallisation förekom endast en liten mängd av rätt produkt. Vi vet inte vad som kunde vara orsaken till detta. Någon typ av orenheter kunde observeras i IR-spektret som kördes men inget specifikt kan sägas. Alkyleringen av indol med krotonaldehyd i närvaro av den nya imidazolidinonhydrokloriden var inte så lyckad. Då katalysatorn frigjorts och TFA införts som kokatalysator kunde möjligtvis en aldehydpik identifieras i IR-spektret men p. g. a. att oxideringen till karboxylsyra misslyckades kan inget säkert sägas. En förklaring till detta kan man finna genom att se på katalysatorns stereokemi. Vår katalysator har en motsvarande stereokemi som MacMillans första generationens imidazolidinon där C2- och C5-substituenterna sitter på olika sidor. Detta blockerar addition av den relativt stora och inte så starka nukleofilen, indolen, till den aktiverade iminiumintermediärens -position och leder därmed till låg reaktivitet och dåliga utbyten. Ett bättre resultat kunde ha uppnåtts om alkyleringen hade gjorts på den starkare nukleofilen, N-metylpyrrol. Både alkyleringen och oxideringen kräver optimering för att få bättre resultat. 68
72 5. Sammanfattning Organokatalytisk asymmetrisk F-C-alkylering av olika aromatiska och heteroaromatiska nukleofiler är ett intressant alternativ som framställningsmetod för föreningar av biologiskt intresse. Imidazolidinonerna och diarylprolinoletrarna är väl undersökta katalysatorer som har visat sig vara effektiva och selektiva i de asymmetriska omvandlingar där - omättade aldehyder använts som elektrofiler. Katalysatorerna, imidazoltionerna och bipyrrolidinerna, har gett utmärkta resultat men är relativt lite undersökta. Dessa katalysatorer kunde vara värda att utvecklas för att uppnå ännu bättre resultat. Aziridin-2- ylmetanolerna är däremot inte tillräckligt effektiva och därmed ointressanta för vidare undersökningar. Resultaten från de asymmetriska F-C-alkyleringarna där aromatiska nukleofilerna alkyleras med enoner kräver i framtiden förbättringar. Cinkonaalkaloidderivaten har uppvisat bra resultat i dessa alkyleringar men nya katalysatorer bör hittas. Olika diaminer kunde vara bättre alternativ som effektiva katalysatorer för alkyleringarna med enoner. Resultaten har varit goda och kommer att förbättras i framtiden. Katalysatorerna utvecklas och mildare reaktionsförhållandena används vilket leder till att synteserna blir allt mer ekonomiskt fördelaktiga. Mindre mängd och svagare kokatalysatorer kan användas och reaktionerna kan utföras i rumstemperatur. Dessutom kommer valet av både nukleofilen och elektrofilen att utvidgas. Detta öppnar nya möjligheter att tillämpa denna organokatalytiska metod i allt fler synteser och på så sätt framställa intressantare slutprodukter. 69
73 6. Förkortningar och akronymer ATP Boc COX-2 DBA DCA DCM DMB DME DMF (D)-N-Boc-Phg-OH dr ee F-C- HIV HOMO IL-8 IR LAH LUMO MTBE nnos Adenosintrifosfat tert-butoxikarbonyl Cyklooxygenas-2 Dibensylidenaceton Dikloretan Diklormetan Dimetoxibensyl 1,2-Dimetoxietan Dimetylformamid (D)-N-(tert-butoxikarbonyl)- fenylglycin Diastereoisomera förhållandet Enantiomeröverskott Friedel-Crafts- Humant immunbristvirus Högsta besatta molekylorbitalen Interleukin-8 Infraröd Litiumaluminiumhydrid Lägsta obesatta molekylorbitalen Metyl(tert-butyl)eter Neurologisk kväveoxidsyntas 70
74 OTMS PCC PKC PMB p-tsa rt SSRI STAB TFA TfOH THF THP- TLC UV 5-NO 2 -SA Trimetylsilyleter Pyridinklorkromat Protein kinas C para-metoxibensyl para-toluensulfonsyra rumstemperatur Selektiv serotoninåterupptagningsinhibitor Natriumtriacetoxiborhydrid Trifluorättiksyra Trifluormetansulfonsyra Tetrahydrofuran Tetrahydropyran[3,4-b]- Tunnskiktskromatografi Ultraviolett 5-Nitrosalicylsyra 71
75 7. Referenser 1. Terrasson, V., de Figueiredo, R. M. och Campagne, J. M., Eur. J. Org. Chem. (2010) Bigi, F., Casiraghi, G., Casnati, G. och Sartori, G., J. Org. Chem. 50 (1985) Paras, N. A. och MacMillan, D. W. C., J. Am. Chem. Soc. 123 (2001) Northrup, A. B. och MacMillan, D. W. C., J. Am. Chem. Soc. 124 (2002) Erkkilä, A., Majander, I. och Pihko, P. M., Chem. Rev. 107 (2007) MacMillan, D. W. C., Nature 455 (2008) Lelais, G. och MacMillan, D. W. C., Aldrichim. Acta 39 (2006) Almasi, D., Alonso, D. A. och Nájera, C., Tetrahedron: Asymmetry 18 (2007) de Figueiredo, R. M. och Christmann, M., Eur. J. Org. Chem. (2007) Lee, S., Development of iminium-activation technologies and the total synthesis of (+)- frondosin B, doktorsavhandling, California institute of technology, California, Austin, J. F. och MacMillan, D. W. C., J. Am. Chem. Soc. 124 (2001) Huang, Y., Walji, A. M., Larsen, C. H. och MacMillan, D. W. C., J. Am. Chem. Soc. 127 (2005) Galzerano, P., New organocatalytic asymmetric strategies: simple catalysts for complex molecules, doktorsavhandling, University of Bologna, Bologna, Enders, D., Kipphardt, H., Gerdes, P., Breña-Valle, L. J. och Bhushan, V., Bull. Soc. Chim. Belg. 100 (1988) Corey, E. J., Shibata, T. och Lee, T. W., J. Am. Chem. Soc. 124 (2002) Marigo, M., Wabnitz, T. C., Fielenbach, D. och Jørgensen, K. A., Angew. Chem. Int. Ed. 44 (2005) Marigo, M., Fielenbach, D., Braunton, A., Kjærsgaard, A. och Jørgensen, K. A., Angew. Chem. Int. Ed. 44 (2005) Hayashi, Y., Gotoh, H., Hayashi, T. och Shoji, M., Angew. Chem. Int. Ed. 44 (2005) Hong, L., Wang, L., Chen, C., Zhang, B. och Wang, R., Adv. Synth. Catal. 351 (2009) Török, B., Abid, M., London, G., Esquibel, J., Török, M., Mhadgut, S. C., Yan, P. och Prakash, G. K. S., Angew. Chem. Int. Ed. 44 (2005) Bartoli, G. och Melchiorre, P., Synlett 12 (2008)
76 22. Chen, W., Du, W., Yue, L., Li, R., Wu, Y., Ding, L-S. och Chen, Y-C., Org. Biomol. Chem. 5 (2007) Bartoli, G., Bosco, M., Carlone, A., Pesciaioli, F., Sambri, L. och Melchiorre, P., Org. Lett. 9 (2007) Gusman, A., Yuste, F., Toscano R. A. och Young, J. M., J. Med. Chem. 29 (1986) Liang, X., Fan, J., Shi, F. och Su, W., Tetrahedron Lett. 51 (2010) Breistein, P., Karlsson, S. och Hedenström, E., Tetrahedron: Asymmetry 17 (2006) Bonini, B. F., Capitò, E., Comes-Franchini, M., Fochi, M., Ricci, A. och Zwanenburg, B., Tetrahedron: Asymmetry 17 (2006) David, B., Sévenet, T., Thoison, O., Awang, K., Païs, M., Wright, M. och Guénard, D., Bioorg. Med. Chem. Lett. 7 (1997) Baudoin, O., Claveau, F., Thoret, S., Herrbach, A., Guénard, D. och Guéritte, F., Bioorg. Med. Chem. 10 (2002) Bowie Jr., A. L., Hughes, C. C. och Trauner, D., Org. Lett. 7 (2005) Banwell, M. G., Beck, D. A. S. och Willis, A. C., ARKIVOC (iii) (2006) Hong, L., Sun, W., Liu, C., Wang, L., Wong, K. och Wang, R., Chem. Eur. J. 15 (2009) Hong, L., Liu, C., Sun, W., Wang, L., Wong, K. och Wang, R., Org. Lett. 11 (2009) Bandini, M. och Eichholzer, A., Angew. Chem. Int. Ed. 48 (2009) Bartoli, G., Bencivenni, G. och Dalpozzo, R., Chem. Soc. Rev. 39 (2010) Masferrer, J. L., Zweifel, B. S., Manning, P. T., Hauser, S. D., Leahy, K. M., Smith, W. G., Isakson, P. C. och Seibert, K., Proc. Natl. Acad. Sci. 91 (1994) Austin, J. F., Kim, S-G., Sinz, C. J., Xiao, W-J. och MacMillan, D. W. C., PNAS 101 (2004) Kobayashi, J. och Ishibashi, M., The Alkaloids: Chemistry and Pharmacology 41 (1992) Wulff, P., Carle, J. S. och Christophersen, C., Comp. Biochem. Physiol. B Biochem. Mol. Biol. 71 (1982) Peters, L., Konig, G. M., Terlau, H. och Wright, A. D., J. Nat. Prod. 65 (2002) Sjöblom, T., Bohlin, L. och Christophersen, C., Acta Pharm. Suec. 20 (1983)
77 42. King, H. D., Meng, Z., Denhart, D., Mattson, R., Kimura, R., Wu, D., Gao, Q. och Macor, J. E., Org. Lett. 7 (2005) Baldwin, D. S., Hum. Psychopharmacol. 16 (2001) S93 S Spinks, D. och Spinks, G., Curr. Med. Chem. 9 (2002) Yang, J-G., Jin, J., Lv, X. och Bao, W., Synthesis 23 (2009) Collins, I., Contemp. Org. Synth. 4 (1997) Sefkow, M., Top. Curr. Chem. 243 (2005) Nicolaou, K. C., Huang, X., Guiseppone, N., Eheema Rao, P., Bella, M., Reddy, M. V. och Snyder, S. A., Angew. Chem. Int. Ed. 40 (2001) Marshall, J. A. och Schaaf, G. M., J. Org. Chem. 68 (2003) Kim, S-G., Bull. Korean Chem. Soc. 30 (2009) Jin, S., Li, C., Ma, Y., Kan, Y., Zhang, Y. J. och Zhang, W., Org. Biomol. Chem. 8 (2010) Hoettecke, N., Rotzoll, S., Albrecht, U., Lalk, M., Fischer, C. och Langer, P., Bioorg. Med. Chem. 16 (2008) Koufaki, M., Kiziridi, C., Alexi, X. och Alexi, M. N., Bioorg. Med. Chem. 17 (2009) Dong, Y., Nakagawa-Goto, K., Lai, C.-Y., Morris-Natschke, S. L., Bastow, K. F. och Lee, K.-H., Bioorg. Med. Chem. Lett. 20 (2010) Kraus, G. A., Mengwasser, J., Maury, W. och Oh, C., Bioorg. Med. Chem. Lett. 21 (2011) Gwon, S. H., Kim, S. och Kim, S-G., Bull. Korean Chem. Soc. 32 (2011) Liang, X., Li, S. och Su, W., Tetrahedron Lett. 53 (2012) Li, C-F., Liu, H., Liao, J., Cao, Y-J., Liu, X-P. och Xiao, W-J., Org. Lett. 9 (2007) Sundberg, R. J., Indoles, Academic Press: San Diego, Larghi, E. L. och Kaufman, T. S., Synthesis 2 (2006) Wolfe, J. P. och Buchwald, S. L., Angew. Chem. Int. Ed. 38 (1999) Hartwig, J. F., Acc. Chem. Res. 31 (1998) Stille, J. K., Angew. Chem. Int. Ed. Engl. 25 (1986) Ma, J.-A. och Cahard, D., Chem. Rev. 104 (2004) Guo, Y-C., Li, D-P., Li, Y-L., Wang, H-M. och Xiao, W-J., Chirality 21 (2009)
78 66. Allen, M. C., Fuhrer, W., Tuck, B., Wade, R. och Wood, J. M., J. Med. Chem. 32 (1989) Smith, W. W. och Bartlett, P. A., J. Am. Chem. Soc. 120 (1998) Allen, J. G., Atherton, F. R., Hall, M. J., Hassall, C. H., Holmes, S. W., Lambert, R. W., Nisbet, L. J. och Ringrose, P. S., Nature 272 (1978) Atherton, F. R., Hassall, C. H. och Lambert, R. W., J. Med. Chem. 29 (1986) Alonso, E., Solis, A. och Pozo, C. D., Synlett 5 (2000) Camp, N. P., Hawkins, P. C. D., Hitchcock, P. B. och Gani, D., Bioorg. Med. Chem. Lett. 2 (1992) Hanessian, S., Stoffman, E., Mi, X. och Renton, P., Org. Lett. 13 (2011) Ji, H., Stanton, B. Z., Igarashi, J., Li, H., Martásek, P., Roman, L. J., Poulos, T. L., och Silverman, R. B., J. Am. Chem. Soc. 130 (2008) Lee, S. och MacMillan, D. W. C., J. Am. Chem. Soc. 129 (2007) Petasis, N. A. och Akritpoulou, I., Tetrahedron Lett. 34 (1999) Petasis, N. A. och Zavialov, I. A., J. Am. Chem. Soc. 119 (1997) Molander, G. A. och Fumagalli, T., J. Org. Chem. 71 (2006) Vedejs, E., Chapman, R. W., Fields, S. C., Lin, S. och Schrimpf, M. R., J. Org. Chem. 60 (1995) Reiter, M., Torssell, S., Lee, S. och MacMillan, D. W. C., Chem. Sci. 1 (2010) Li, D-P., Guo, Y-C., Ding, Y. och Xiao, W-J., Chem. Commun. 7 (2006) Łyżwa, D., Dudziński, K. och Kwiatkowski, P., Org. Lett. 14 (2012) Heydorn, W. E., Expert Opin. Invest. Drugs 8 (1999) Hills, C. J., Winter, S. A. och Balfour, J. A., Drugs 55 (1998) McRae, A. L. och Brady, K. T., Expert Opin. Pharmacotherapy 2 (2001) Paras, N. A., Simmons, B. och MacMillan, D. W. C., Tetrahedron 65 (2009) De Castro, K. A., Ko, J., Park, D., Park, S. och Rhee, H., Org. Process Res. Dev. 11 (2007) Kim, S-G., Kim, J. och Jung, H., Tetrahedron Lett. 46 (2005) Wright, A. E., Pomponi, S. A., McConnell, O. J., Kohmoto, S. och McCarthy, P. J., J. Nat. Prod. 50 (1987) Fusetini, N., Sugano, M., Matsunaga, S. och Hashimoto, K., Experientia 43 (1987)
79 90. Sayed, K. A. E., Yousaf, M., Hamann, M. T., Avery, M. A., Kelly, M. och Wipf, P., J. Nat. Prod. 65 (2002) McEnroe, F. J. och Fenical, W., Tetrahedron 34 (1978) Haemers, T., Wiesner, J., Busson, R., Jomaa, H. och Calenbergh, S. V., Eur, J. Org. Chem. (2006) Kidwai, M., Saxena, S., Khan, M. K. och Thukral, S. S., Bioorg. Med. Chem. Lett. 15 (2005) Aoki, S., Amamoto, C., Oyamada, J. och Kitamura, T., Tetrahedron 61 (2005) Hong, L., Wang, L., Sun, W., Wong, K. och Wang, R., J. Org. Chem. 74 (2009) Horton, D. A., Boume, G. T. och Smythe, M. L., Chem. Rev. 103 (2003) Bertelsen, S., DinMr, P., Johansen, R. L. och Jørgensen, K. A., J. Am. Chem. Soc. 129 (2007) Paradisi, E., Righi, P., Mazzanti, A., Ranieri, S. och Bencivenni, G., Chem. Commun. 48 (2012) Ishikawa, N. K., Fukushi, Y., Yamaji, K., Tahara, S. och Takahashi, K., J. Nat. Prod. 64 (2001) Patil, A. D., Freyer, A. J., Kilmer, L., Offen, P., Carte, B., Jurewicz, A. J. och Johnsson, R. K., Tetrahedron 53 (1997) Hallock, Y. F., Cardellina, J. H. och Boyd, M. R., Nat. Prod. Lett. 11 (1998) Seitz, M., Dewald, B., Gerber, N. och Baggiolini, M., J. Clin. Invest. 11 (1998) Brat, D. J., Bellail, A. C. och Van Meir, E. G., Neuro-Oncology 7 (2005) Graham, T. H., Horning, B. D. och MacMillan, D. W. C., Org. Synth. 88 (2011) Elders, N., Schmitz, R. F., de Kanter, F. J. J., Ruijter, E., Groen, M. B. och Orru, R. V. A., J. Org. Chem. 72 (2007) Naef, R. och Seebach, D., Helv. Chim. Acta 68 (1985) Cha, J. S. och Chun, J. H., Bull. Korean Chem. Soc. 21 (2000) Whitmore, F. C. och Houk, A. L., J. Am. Chem. Soc. 54 (1932) Whitmore, F. C. och Badertscher, D. E., J. Am. Chem. Soc. 55 (1933) Nazarski, R. B., Tasz, M. K. och Skowroński, R., Bull. Soc. Chim. Belg. 101 (1992)
80 111. Smith, L. I. och Bayliss, M., J. Org. Chem. 6 (1941) Furniss, B. S., Hannaford, A. J., Smith, P. W. G. och Tatchell, A. R., Vogel s textbook of practical organic chemistry, 5 ed., Longman Group UK Limited, Storbritannien, 1989, kap. 5, Ref. 11, tillägsinfo Chakraborty, D., Gowda, R. R. och Malik, P., Tetrahedron Lett. 50 (2009) Zhang, Y.-M., Liu, P. och Zhang, H.-L., J. Chem. Res. 11 (2009) Tao, G.-H., He, L., Sun, N. och Kou, Y., Chem. Commun. (2005) Crowder, G. A., J. Chem. Soc. Perkin Trans. 2 (1973) Adamson, G. A., Beckwith, A. L. J. och Chai, C. L. L., Aust. J. Chem. 57 (2004)
1. Introduktion. Vad gör senapsgas så farlig?
 Föreläsning 9 Reaktionslära II Kapitel 9.1-9.6 1) Introduktion 2) Monomolekylära nukleofila substitutioner 3) Parametrar 4) Sammanfattning 5) Exempel 1. Introduktion Vad gör senapsgas så farlig? 2. Nukleofila
Föreläsning 9 Reaktionslära II Kapitel 9.1-9.6 1) Introduktion 2) Monomolekylära nukleofila substitutioner 3) Parametrar 4) Sammanfattning 5) Exempel 1. Introduktion Vad gör senapsgas så farlig? 2. Nukleofila
1 Ange lämpliga reagens till följande reaktioner. Inga mekanismer behövs.
 Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 31 maj 2005, kl. 08.00-14.00 Tillåtna hjälpmedel: molekylmodeller, miniräknare (periodiskt system och tabeller med bindingsstyrkor och pk a -värden är bifogade
Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 31 maj 2005, kl. 08.00-14.00 Tillåtna hjälpmedel: molekylmodeller, miniräknare (periodiskt system och tabeller med bindingsstyrkor och pk a -värden är bifogade
KARBOKATJON KARBANJON
 EAKTINE: Generella typer : 1. Addition Fö D-2010 (rowe Kap 17-18) 2. Substitution 3. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME Z MLYS + Z ADIKALE Z ETELYS KABKATJN + Z Vanligast + Z KABANJN
EAKTINE: Generella typer : 1. Addition Fö D-2010 (rowe Kap 17-18) 2. Substitution 3. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME Z MLYS + Z ADIKALE Z ETELYS KABKATJN + Z Vanligast + Z KABANJN
Föreläsning 11. Alkener II Kapitel 11 F11
 Föreläsning 11 Alkener II Kapitel 11 1) Introduktion 2) Addition av elektrofila reagens 3) ydrogenering 4) ydroborering 5) Radikaladdition 6) Polymerisering 7) xidation 1. Introduktion ur gör man cancermedicinen
Föreläsning 11 Alkener II Kapitel 11 1) Introduktion 2) Addition av elektrofila reagens 3) ydrogenering 4) ydroborering 5) Radikaladdition 6) Polymerisering 7) xidation 1. Introduktion ur gör man cancermedicinen
H 3 C. 5. Förklara varför fenol (se ovan) är en starkare syra än cyklohexanol (pk a =18).
 Linköping 12-08-15 IFM/Kemi Linköpings universitet TFKE06/GAN-ss Efterarbete av föreläsningar inom rganisk kemi 2 Uppgifter kap. 1-3 1. Rita resonansformler för N,N-dimetyl-3-aminopropenal! 3 3 N 2. Ange
Linköping 12-08-15 IFM/Kemi Linköpings universitet TFKE06/GAN-ss Efterarbete av föreläsningar inom rganisk kemi 2 Uppgifter kap. 1-3 1. Rita resonansformler för N,N-dimetyl-3-aminopropenal! 3 3 N 2. Ange
Föreläsning 10. Alkener I Kapitel 10 F10
 Föreläsning 10 Alkener I Kapitel 10 1) Introduktion 2) Monomolekylära eliminationer 3) Bimolekylära eliminationer 4) Alkyner 5) Sammanfattning av joniska reaktioner 6) Exempel 1. Introduktion Bimolekylär
Föreläsning 10 Alkener I Kapitel 10 1) Introduktion 2) Monomolekylära eliminationer 3) Bimolekylära eliminationer 4) Alkyner 5) Sammanfattning av joniska reaktioner 6) Exempel 1. Introduktion Bimolekylär
Föreläsning 14. Aromater II - elektrofil aromatisk substitution Kapitel 14 F14
 Föreläsning 14 Aromater II - elektrofil aromatisk substitution Kapitel 14 1) Introduktion 2) Generell reaktion 3) Framställning av elektrofiler 4) Påverkan av substituenter 5) Praktiska aspekter 1. Introduktion
Föreläsning 14 Aromater II - elektrofil aromatisk substitution Kapitel 14 1) Introduktion 2) Generell reaktion 3) Framställning av elektrofiler 4) Påverkan av substituenter 5) Praktiska aspekter 1. Introduktion
Tentamen i Organisk kemi 28/5 2013,
 Tentamen i rganisk kemi 28/5 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: Lycka till! /Ulf -fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p
Tentamen i rganisk kemi 28/5 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: Lycka till! /Ulf -fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p
Tentamen i Organisk kemi 25/5 2011,
 Tentamen i rganisk kemi 25/5 2011, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak ECTS LT (T) G 40-59p E 40-41p 3 40-54p VG 60-90p D 42-50p
Tentamen i rganisk kemi 25/5 2011, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak ECTS LT (T) G 40-59p E 40-41p 3 40-54p VG 60-90p D 42-50p
Föreläsning 17. Karbonylkolets kemi II Kapitel 17 F17
 Föreläsning 17 Karbonylkolets kemi II Kapitel 17 1) Introduktion 2) Addition av starka nukleofiler 3) Estrar 4) Amider 5) Nitriler 6) Syraklorider 7) Praktisk användning 1. Introduktion Aldehyder och ketoner
Föreläsning 17 Karbonylkolets kemi II Kapitel 17 1) Introduktion 2) Addition av starka nukleofiler 3) Estrar 4) Amider 5) Nitriler 6) Syraklorider 7) Praktisk användning 1. Introduktion Aldehyder och ketoner
2. SUBSTITUTION (Nukleofil substitution) S N 2
 . SUBSTITUTION (Nukleofil substitution) Alkylhalider är generellt reaktiva pga att den elektronegativa haliden gör att bindningen till kol polariseras, man får en dipol. Kolet blir elektrofilt (elektronfattigare
. SUBSTITUTION (Nukleofil substitution) Alkylhalider är generellt reaktiva pga att den elektronegativa haliden gör att bindningen till kol polariseras, man får en dipol. Kolet blir elektrofilt (elektronfattigare
Olika typer av kolväten
 INTDUKTIN TILL GANISK KEMI KABNYLGUPPSKEMI Föreläsning v16 Nina Kann lika typer av kolväten alifatiska - alkaner - alkener - alkyner aromatiska 1 Funktionella grupper alken alkohol l alkylhalid S tiol
INTDUKTIN TILL GANISK KEMI KABNYLGUPPSKEMI Föreläsning v16 Nina Kann lika typer av kolväten alifatiska - alkaner - alkener - alkyner aromatiska 1 Funktionella grupper alken alkohol l alkylhalid S tiol
Föreläsning 8. Reaktionslära I Kapitel
 Föreläsning 8 Reaktionslära I Kapitel 9.1-9.3 1) Introduktion 2) Nukleofila substitutioner 3) Parametrar 4) Praktisk användning 5) Elektrofiler och biologi 1. Introduktion Varför gråter vi när vi hackar
Föreläsning 8 Reaktionslära I Kapitel 9.1-9.3 1) Introduktion 2) Nukleofila substitutioner 3) Parametrar 4) Praktisk användning 5) Elektrofiler och biologi 1. Introduktion Varför gråter vi när vi hackar
REAKTIONER : A. ADDITION Crowe p REAKTIONER: Del D-2009 Generella typer : 1. Addition 2. Substitution 3. Elimination 4.
 EAKTINE: Del D-009 Generella typer : 1. Addition. Substitution. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME rowe 1.-1. MYS ETEYS KABKATJN KABANJN eaktioner innebär att kovalenta bindningar
EAKTINE: Del D-009 Generella typer : 1. Addition. Substitution. Elimination 4. Kondensation EAKTINSINTEMEDIÄE och MEKANISME rowe 1.-1. MYS ETEYS KABKATJN KABANJN eaktioner innebär att kovalenta bindningar
Reaktionsmekanismer. Kap 6
 Reaktionsmekanismer Kap 6 Karbokatjoner är elektrofila intermediärer Innehåll Kvalitativa resonemang hur och varför kemiska reaktioner sker Exempel på energiomsättningar vid olika slags organiska reaktioner.
Reaktionsmekanismer Kap 6 Karbokatjoner är elektrofila intermediärer Innehåll Kvalitativa resonemang hur och varför kemiska reaktioner sker Exempel på energiomsättningar vid olika slags organiska reaktioner.
Kemiska reaktioner: Olika reaktionstyper och reaktionsmekanismer. Niklas Dahrén
 Kemiska reaktioner: Olika reaktionstyper och reaktionsmekanismer Niklas Dahrén 7 olika reaktionstyper 1. Substitutionsreaktioner 2. Additionsreaktioner 3. Eliminationsreaktioner 4. Kondensationsreaktioner
Kemiska reaktioner: Olika reaktionstyper och reaktionsmekanismer Niklas Dahrén 7 olika reaktionstyper 1. Substitutionsreaktioner 2. Additionsreaktioner 3. Eliminationsreaktioner 4. Kondensationsreaktioner
Föreläsning 16. Karbonylkolets kemi I Kapitel 16 F16
 Föreläsning 16 Karbonylkolets kemi I Kapitel 16 1) Introduktion 2) Addition av nukleofiler till karbonylgrupper A) Addition av hydridjoner B) Addition av metallorganiska reagens C) Addition av alkoholer
Föreläsning 16 Karbonylkolets kemi I Kapitel 16 1) Introduktion 2) Addition av nukleofiler till karbonylgrupper A) Addition av hydridjoner B) Addition av metallorganiska reagens C) Addition av alkoholer
Namnge och rita organiska föreningar - del 5
 Namnge och rita organiska föreningar - del 5 Etrar, aldehyder, ketoner, tioler, fenoler, nitroföreningar, aminer, amider Niklas Dahrén Etrar Etrar har en etergrupp: Vid namngivning lägger man till ändelsen
Namnge och rita organiska föreningar - del 5 Etrar, aldehyder, ketoner, tioler, fenoler, nitroföreningar, aminer, amider Niklas Dahrén Etrar Etrar har en etergrupp: Vid namngivning lägger man till ändelsen
Kiralitet former som är spegelbilder av varandra men ej identiska. Jämför med händer.
 Organisk kemi i denna kurs KIRALITET NUKLEOFIL SUBSTITUTION Föreläsning v17 Nina Kann v16 karbonylgruppens kemi =O v17 nukleofil substitution (alkylhaliders reaktivitet), kiralitet v18 alkener, karbokatjoner,
Organisk kemi i denna kurs KIRALITET NUKLEOFIL SUBSTITUTION Föreläsning v17 Nina Kann v16 karbonylgruppens kemi =O v17 nukleofil substitution (alkylhaliders reaktivitet), kiralitet v18 alkener, karbokatjoner,
Tentamen i Organisk Kemi (3B1760) Tisdagen den 30 augusti 2005, kl
 Tentamen i rganisk Kemi (3B1760) Tisdagen den 30 augusti 2005, kl. 08.00-14.00 Tillåtna hjälpmedel: molekylmodeller, miniräknare (periodiskt system och tabeller med bindingsstyrkor och pk a -värden är
Tentamen i rganisk Kemi (3B1760) Tisdagen den 30 augusti 2005, kl. 08.00-14.00 Tillåtna hjälpmedel: molekylmodeller, miniräknare (periodiskt system och tabeller med bindingsstyrkor och pk a -värden är
ALDEHYDER och KETONER Del D-2007
 ALDEYDE och KETNE Del D-2007 Karbonyl grupp: -# +# dipol, sp 2, 120 o vinkel Aldehyd ändelse: - al metanal formaldehyd 3 etanal acetaldehyd 3 2 propanal propionaldehyd bensaldehyd akrolein mrering av kolkedja:
ALDEYDE och KETNE Del D-2007 Karbonyl grupp: -# +# dipol, sp 2, 120 o vinkel Aldehyd ändelse: - al metanal formaldehyd 3 etanal acetaldehyd 3 2 propanal propionaldehyd bensaldehyd akrolein mrering av kolkedja:
Övningsfrågor inför dugga 3 och tentamen
 Övningsfrågor inför dugga 3 och tentamen Biomedicinare HT 006. MBB, K.I. Mats Hamberg Ge reaktionsformel för Fentonreaktionen! Följande frågor rör den nedan avbildade föreningen. a) Ange i vilken typ av
Övningsfrågor inför dugga 3 och tentamen Biomedicinare HT 006. MBB, K.I. Mats Hamberg Ge reaktionsformel för Fentonreaktionen! Följande frågor rör den nedan avbildade föreningen. a) Ange i vilken typ av
TK061B Tillämpad bioteknik, antagna 2012, Inga hjälpmedel är tillåtna. 100 poäng
 Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Tillämpad bioteknik, antagna 2012, 2013 7,5 högskolepoäng TentamensKod: Tentamensdatum: 11 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel
Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Tillämpad bioteknik, antagna 2012, 2013 7,5 högskolepoäng TentamensKod: Tentamensdatum: 11 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel
Tentamen i organisk kemi, KEMB01, 15 hp, fredagen den 13 januari 2012,
 Tentamen i organisk kemi, KEMB01, 15 hp, fredagen den 13 januari 2012, 9.00-15.00. Molekylmodeller, miniräknare, punktgruppstabell och spektroskopibok får medtagas. Var vänlig besvara endast en uppgift
Tentamen i organisk kemi, KEMB01, 15 hp, fredagen den 13 januari 2012, 9.00-15.00. Molekylmodeller, miniräknare, punktgruppstabell och spektroskopibok får medtagas. Var vänlig besvara endast en uppgift
Hans Adolfsson - Organisk Kemi Stockholms Universitet
 ans Adolfsson - rganisk Kemi Stockholms Universitet Stereocenter och kiralitet ans Adolfsson, Stockholms universitet Stereocenter i molekylernas värld Vad är kiralitet? Ett föremål är kiralt om det inte
ans Adolfsson - rganisk Kemi Stockholms Universitet Stereocenter och kiralitet ans Adolfsson, Stockholms universitet Stereocenter i molekylernas värld Vad är kiralitet? Ett föremål är kiralt om det inte
Totalt 10 uppgifter, vardera värd 10p (totalt 100p). För godkänt fordras minst 50p, för 4:a minst 66p och för 5:a minst 83p.
 Tentamen i rganisk Kemi 2 (3B1760) måndagen den 29 maj 2006, kl. 08.00-14.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor och pka-värden är bifogade efter frågorna
Tentamen i rganisk Kemi 2 (3B1760) måndagen den 29 maj 2006, kl. 08.00-14.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor och pka-värden är bifogade efter frågorna
2. Transitions state theory för att jämföra relativa reaktiviteten hos olika substrat
 2. Transitions state theory för att jämföra relativa reaktiviteten hos olika substrat Ex: baskatalyserad hydrolys av en ester jmf substraten p-nitrofenylacetat och fenylacetat OH - attackerar karbonylkolet
2. Transitions state theory för att jämföra relativa reaktiviteten hos olika substrat Ex: baskatalyserad hydrolys av en ester jmf substraten p-nitrofenylacetat och fenylacetat OH - attackerar karbonylkolet
Energi, katalys och biosyntes (Alberts kap. 3)
 Energi, katalys och biosyntes (Alberts kap. 3) Introduktion En cell eller en organism måste syntetisera beståndsdelar, hålla koll på vilka signaler som kommer utifrån, och reparera skador som uppkommit.
Energi, katalys och biosyntes (Alberts kap. 3) Introduktion En cell eller en organism måste syntetisera beståndsdelar, hålla koll på vilka signaler som kommer utifrån, och reparera skador som uppkommit.
Framställning av flersubstituerade azulenderivat med fokus på positionerna 1, 2 och 6
 Framställning av flersubstituerade azulenderivat med fokus på positionerna 1, 2 och 6 Niklas Johansson Pro gradu Helsingfors Universitet Kemiska Institutionen Laboratoriet för svenskspråkig undervisning
Framställning av flersubstituerade azulenderivat med fokus på positionerna 1, 2 och 6 Niklas Johansson Pro gradu Helsingfors Universitet Kemiska Institutionen Laboratoriet för svenskspråkig undervisning
Proteiner. Biomolekyler kap 7
 Proteiner Biomolekyler kap 7 Generna (arvsanlagen) (och miljön) bestämmer hur en organism skall se ut och fungera. Hur? En gen är en ritning för hur ett protein skall se ut. Proteiner får saker att hända
Proteiner Biomolekyler kap 7 Generna (arvsanlagen) (och miljön) bestämmer hur en organism skall se ut och fungera. Hur? En gen är en ritning för hur ett protein skall se ut. Proteiner får saker att hända
Tentamen i Organisk kemi- grundkurs 7.5 hp (KEMA01),
 Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA01), 13-08-19 1) Molekylmodeller är tillåtet hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA01), 13-08-19 1) Molekylmodeller är tillåtet hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
O O EtOAc. anilin bensoesyraanhydrid N-fenylbensamid bensoesyra
 Linköping 2009-10-25 IFM/Kemi Linköpings universitet För NKEA07 ht2009 SS Syntes av N-fenylbensamid Inledning: Amider, som tillhör gruppen karboxylsyraderivat, kan framställas från aminer och syraanhydrider.
Linköping 2009-10-25 IFM/Kemi Linköpings universitet För NKEA07 ht2009 SS Syntes av N-fenylbensamid Inledning: Amider, som tillhör gruppen karboxylsyraderivat, kan framställas från aminer och syraanhydrider.
TENTAMEN i ORGANISK KEMI 2 (TFKE06) ,
 TETAME i RGAISK KEMI 2 (TFKE06) 2012-10-23, 14.00-18.00 Lösningsförslag: 1. Vilken förening i respektive par a)-d) har surast väte? Ge kort förklaring till svaret. (10 p) a) b) F C 2 C Cl C 2 C c) d) 3
TETAME i RGAISK KEMI 2 (TFKE06) 2012-10-23, 14.00-18.00 Lösningsförslag: 1. Vilken förening i respektive par a)-d) har surast väte? Ge kort förklaring till svaret. (10 p) a) b) F C 2 C Cl C 2 C c) d) 3
Selektiv och katalytisk hydrogenering av 4-vinylcyklohexen
 Selektiv och katalytisk hydrogenering av 4-vinylcyklohexen Simon Pedersen 27 februari 2012 Chalmers Tekniska Högskola Institutionen för Kemi och Bioteknik Oorganisk och Organisk Kemi Handledare Andreas
Selektiv och katalytisk hydrogenering av 4-vinylcyklohexen Simon Pedersen 27 februari 2012 Chalmers Tekniska Högskola Institutionen för Kemi och Bioteknik Oorganisk och Organisk Kemi Handledare Andreas
Lite basalt om enzymer
 Enzymer: reaktioner, kinetik och inhibering Biokatalysatorer Reaktion: substrat omvandlas till produkt(er) Påverkar reaktionen så att jämvikten ställer in sig snabbare, dvs hastigheten ökar Reaktionen
Enzymer: reaktioner, kinetik och inhibering Biokatalysatorer Reaktion: substrat omvandlas till produkt(er) Påverkar reaktionen så att jämvikten ställer in sig snabbare, dvs hastigheten ökar Reaktionen
TENTAMEN I ALLMÄN OCH ORGANISK KEMI
 KAROLINSKA INSTITUTET Biomedicinprogrammet (Magister) TENTAMEN I ALLMÄN OCH ORGANISK KEMI FREDAGEN DEN 1 FEBRUARI 2008, 08.30-11.00 och 12.00-14.30 Tentamen är uppdelad i två pass med en uppsättning frågor
KAROLINSKA INSTITUTET Biomedicinprogrammet (Magister) TENTAMEN I ALLMÄN OCH ORGANISK KEMI FREDAGEN DEN 1 FEBRUARI 2008, 08.30-11.00 och 12.00-14.30 Tentamen är uppdelad i två pass med en uppsättning frågor
FUNKTIONELLA GRUPPER (Ämnesklasser) Fö
 FUNKTINELLA GUPPE (Ämnesklasser) Fö 3 2010 Ex. 32-l + 2 32- + l Kloretan Etanol Generellt: -l - = - Z = generell kolvätekedja (alkyl) Z= Funktionell grupp, Ex. -l, -, -, -N2 m.fl. 1. Föreningars egenskaper
FUNKTINELLA GUPPE (Ämnesklasser) Fö 3 2010 Ex. 32-l + 2 32- + l Kloretan Etanol Generellt: -l - = - Z = generell kolvätekedja (alkyl) Z= Funktionell grupp, Ex. -l, -, -, -N2 m.fl. 1. Föreningars egenskaper
Tentamen i Organisk kemi, 7.5 hp (KO3003) FACIT
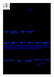 Tentamen i rganisk kemi, 7.5 hp (K3003) 1. (10 p) a) Ange om molekylerna 1 och/eller 2 är aromatiska. (1 p) b) Namnge föreningarna 1 och 2. (1 p) c) Vilken förening är starkast bas av 3 och 4? (2 p) d)
Tentamen i rganisk kemi, 7.5 hp (K3003) 1. (10 p) a) Ange om molekylerna 1 och/eller 2 är aromatiska. (1 p) b) Namnge föreningarna 1 och 2. (1 p) c) Vilken förening är starkast bas av 3 och 4? (2 p) d)
Kapitel Repetition inför delförhör 2
 Kapitel 12-18 Repetition inför delförhör 2 Kapitel 1 Innehåll Kapitel 12 Kapitel 13 Kapitel 14 Kapitel 15 Kapitel 16 Kapitel 17 Kapitel 18 Kemisk kinetik Kemisk jämvikt Syror och baser Syra-basjämvikter
Kapitel 12-18 Repetition inför delförhör 2 Kapitel 1 Innehåll Kapitel 12 Kapitel 13 Kapitel 14 Kapitel 15 Kapitel 16 Kapitel 17 Kapitel 18 Kemisk kinetik Kemisk jämvikt Syror och baser Syra-basjämvikter
Reaktionsmekanismer. Kap 6
 Reaktionsmekanismer Kap 6 Rep. Kemiska reaktioner https://laughingsquid.com/a-ted-ed-animation-explaining-howall-sorts-of-different-chemical-reactions-are-triggered/ Karbokatjoner är elektrofila intermediärer
Reaktionsmekanismer Kap 6 Rep. Kemiska reaktioner https://laughingsquid.com/a-ted-ed-animation-explaining-howall-sorts-of-different-chemical-reactions-are-triggered/ Karbokatjoner är elektrofila intermediärer
Kapitel Kapitel 12. Repetition inför delförhör 2. Kemisk kinetik. 2BrNO 2NO + Br 2
 Kapitel 1-18 Repetition inför delförhör Kapitel 1 Innehåll Kapitel 1 Kemisk kinetik Redoxjämvikter Kapitel 1 Definition Kapitel 1 Området inom kemi som berör reaktionshastigheter Kemisk kinetik Kapitel
Kapitel 1-18 Repetition inför delförhör Kapitel 1 Innehåll Kapitel 1 Kemisk kinetik Redoxjämvikter Kapitel 1 Definition Kapitel 1 Området inom kemi som berör reaktionshastigheter Kemisk kinetik Kapitel
CH 3 N. metylamin dimetylamin trimetylamin tetrametylammonium jon primär sekundär!!!!!!!!!!!!! tertiär!!!!!!!!!!!kvartenär
 Funktionella grp med kväve, Fö 7-2010 AMIE - 2 amnges med alkyl följt av ordet amin. Indelning: metylamin dimetylamin trimetylamin tetrametylammonium jon primär sekundär!!!!!!!!!!!!! tertiär!!!!!!!!!!!kvartenär
Funktionella grp med kväve, Fö 7-2010 AMIE - 2 amnges med alkyl följt av ordet amin. Indelning: metylamin dimetylamin trimetylamin tetrametylammonium jon primär sekundär!!!!!!!!!!!!! tertiär!!!!!!!!!!!kvartenär
Intermolekylära krafter
 Intermolekylära krafter Medicinsk Teknik KTH Biologisk kemi Vt 2012 Märit Karls Intermolekylära attraktioner Mål 5-6 i kap 5, 1 och 5! i kap 8, 1 i kap 9 Intermolekylära krafter Varför är is hårt? Varför
Intermolekylära krafter Medicinsk Teknik KTH Biologisk kemi Vt 2012 Märit Karls Intermolekylära attraktioner Mål 5-6 i kap 5, 1 och 5! i kap 8, 1 i kap 9 Intermolekylära krafter Varför är is hårt? Varför
Intermolekylära krafter
 Intermolekylära krafter Medicinsk Teknik KTH Biologisk kemi Vt 2011 Märit Karls Intramolekylära attraktioner Atomer hålls ihop av elektrostatiska krafter mellan protoner och.elektroner Joner hålls ihop
Intermolekylära krafter Medicinsk Teknik KTH Biologisk kemi Vt 2011 Märit Karls Intramolekylära attraktioner Atomer hålls ihop av elektrostatiska krafter mellan protoner och.elektroner Joner hålls ihop
Organiska ämnen (2) s
 Organiska ämnen (2) s126-154 Organiska stamträdet Ämnesklasser- reaktionstyper/reaktionsvägar) Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar
Organiska ämnen (2) s126-154 Organiska stamträdet Ämnesklasser- reaktionstyper/reaktionsvägar) Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar
Föreläsning 13. Aromater I Kapitel 13 F13. 1) Introduktion 2) Bensens struktur och egenskaper 3) Aromaticitet 4) Aromatiska föreningar
 Föreläsning 13 Aromater I Kapitel 13 1) Introduktion 2) Bensens struktur och egenskaper 3) Aromaticitet 4) Aromatiska föreningar 1. Introduktion π-system ger stabilisering allyliska radikaler och karbokatjoner
Föreläsning 13 Aromater I Kapitel 13 1) Introduktion 2) Bensens struktur och egenskaper 3) Aromaticitet 4) Aromatiska föreningar 1. Introduktion π-system ger stabilisering allyliska radikaler och karbokatjoner
Enzymer Farmaceutisk biokemi. Enzymet pepsin klyver proteiner i magsäcken till mindre peptider
 Enzymer Farmaceutisk biokemi Enzymet pepsin klyver proteiner i magsäcken till mindre peptider Enzymet CYP11A1, i t ex binjurar, testiklar och äggstockar, omvandlar kolesterol till könshormoner 1 Enzymet
Enzymer Farmaceutisk biokemi Enzymet pepsin klyver proteiner i magsäcken till mindre peptider Enzymet CYP11A1, i t ex binjurar, testiklar och äggstockar, omvandlar kolesterol till könshormoner 1 Enzymet
Avsnitt 12.1 Reaktionshastigheter Kemisk kinetik Kapitel 12 Kapitel 12 Avsnitt 12.1 Innehåll Reaktionshastigheter Reaktionshastighet = Rate
 Avsnitt 2. Kapitel 2 Kemisk kinetik Kemisk kinetik Området inom kemi som berör reaktionshastigheter Copyright Cengage Learning. All rights reserved 2 Kapitel 2 Innehåll 2. 2.2 Hastighetsuttryck: en introduktion
Avsnitt 2. Kapitel 2 Kemisk kinetik Kemisk kinetik Området inom kemi som berör reaktionshastigheter Copyright Cengage Learning. All rights reserved 2 Kapitel 2 Innehåll 2. 2.2 Hastighetsuttryck: en introduktion
!!!!! Undvikande!och!aggressivt!beteende! mot!främmande!människor!hos!hundar! i!finland!! Sofi!Sandbacka! 2014!!!!!!!!!!!
 Undvikandeochaggressivtbeteende motfrämmandemänniskorhoshundar ifinland SofiSandbacka 2014 Licentiatavhandlingiämnetveterinärmedicin Helsingforsuniversitet Veterinärmedicinskafakulteten Avdelningförkliniskproduktionsdjursmedicin
Undvikandeochaggressivtbeteende motfrämmandemänniskorhoshundar ifinland SofiSandbacka 2014 Licentiatavhandlingiämnetveterinärmedicin Helsingforsuniversitet Veterinärmedicinskafakulteten Avdelningförkliniskproduktionsdjursmedicin
Hastighet HOCH 2. *Enzymer är Katalysatorer. *Påverkar inte jämvikten
 Enzymer, Katalys och Kinetik MNXA10/12 Hans-Erik Åkerlund Hastighet Reglerbarhet *Enzymer är Katalysatorer Påskyndar reaktioner utan att själv förbrukas. Kan ingå i delreaktioner men återbildas alltid
Enzymer, Katalys och Kinetik MNXA10/12 Hans-Erik Åkerlund Hastighet Reglerbarhet *Enzymer är Katalysatorer Påskyndar reaktioner utan att själv förbrukas. Kan ingå i delreaktioner men återbildas alltid
Kapitel 12. Kemisk kinetik
 Kapitel 12 Kemisk kinetik Avsnitt 12.1 Reaktionshastigheter Kemisk kinetik Området inom kemi som berör reaktionshastigheter Copyright Cengage Learning. All rights reserved 2 Avsnitt 12.1 Reaktionshastigheter
Kapitel 12 Kemisk kinetik Avsnitt 12.1 Reaktionshastigheter Kemisk kinetik Området inom kemi som berör reaktionshastigheter Copyright Cengage Learning. All rights reserved 2 Avsnitt 12.1 Reaktionshastigheter
Organiska ämnen (2) s
 Organiska ämnen (2) s126-154 Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar lätt med andra ämnen. (p g a den elektronegativa halogenatomen) används
Organiska ämnen (2) s126-154 Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar lätt med andra ämnen. (p g a den elektronegativa halogenatomen) används
Kemiska reaktioner och reaktionshastigheter. Niklas Dahrén
 Kemiska reaktioner och reaktionshastigheter Niklas Dahrén Kemiska reaktioner När två partiklar (atomer, molekyler, joner etc.) kolliderar med varandra kan ibland en kemisk reaktion ske. De kolliderande
Kemiska reaktioner och reaktionshastigheter Niklas Dahrén Kemiska reaktioner När två partiklar (atomer, molekyler, joner etc.) kolliderar med varandra kan ibland en kemisk reaktion ske. De kolliderande
Inga hjälpmedel är tillåtna. 100 poäng
 rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2017 Tid: 9:00-13:00 Hjälpmedel: Inga
rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2017 Tid: 9:00-13:00 Hjälpmedel: Inga
Tentamen i organisk kemi, KOKA05 Tisdagen den 26 augusti 2010,
 Tentamen i organisk kemi, KKA05 Tisdagen den 26 augusti 2010, 8.00-13.00. Molekylmodeller och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer på varje
Tentamen i organisk kemi, KKA05 Tisdagen den 26 augusti 2010, 8.00-13.00. Molekylmodeller och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer på varje
7,5 högskolepoäng. Organisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik.
 rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2018 Tid: 9:00-13:00 Hjälpmedel: Inga
rganisk kemi Provmoment: Tentamen Ladokkod: A100TG Tentamen ges för: Kemiingenjör, tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 12 Januari, 2018 Tid: 9:00-13:00 Hjälpmedel: Inga
Kap 2 McMurry Viktiga Begrepp
 Kap 2 McMurry Viktiga Begrepp Funktionella grupper Alkaner Isomerer Nomenklatur Konformerer Sågbocks- och Newmanprojektioner Cykloalkaner Cis- och trans- Axiell och ekvatoriell Funktionella grupper En
Kap 2 McMurry Viktiga Begrepp Funktionella grupper Alkaner Isomerer Nomenklatur Konformerer Sågbocks- och Newmanprojektioner Cykloalkaner Cis- och trans- Axiell och ekvatoriell Funktionella grupper En
Skrivning i Oorganisk och organisk kemi för Bt3 och K2, KOK080
 Kemi- och bioteknik, CT 12 mars, 2011 1(16) Skrivning i organisk och organisk kemi för Bt3 och K2, KK080 Tid: Lördagen den 19 mars 2011, kl 14-18. Plats: V Lärare: Nina Kann, tel: 0705 162172 eller anknytning
Kemi- och bioteknik, CT 12 mars, 2011 1(16) Skrivning i organisk och organisk kemi för Bt3 och K2, KK080 Tid: Lördagen den 19 mars 2011, kl 14-18. Plats: V Lärare: Nina Kann, tel: 0705 162172 eller anknytning
Inga hjälpmedel är tillåtna. För att få godkänd kurs måste man få minst 40 poäng på examen.
 Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Bt11-Bt2 7,5 högskolepoäng NAMN Personnummer Tentamensdatum: 28 augusti 2012 Tid: 09.00 13.00 Hjälpmedel: Inga hjälpmedel är tillåtna Totalt
Organisk kemi Provmoment: Ladokkod: Tentamen ges för: TK061B Bt11-Bt2 7,5 högskolepoäng NAMN Personnummer Tentamensdatum: 28 augusti 2012 Tid: 09.00 13.00 Hjälpmedel: Inga hjälpmedel är tillåtna Totalt
Tentamen i Organisk kemi- grundkurs 7.5 hp (KEMA01),
 Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA0), 3-03-8 ) Molekylmodeller och är tillåtna hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
Tentamen i rganisk kemi- grundkurs 7.5 hp (KEMA0), 3-03-8 ) Molekylmodeller och är tillåtna hjälmedel. ) Besvara varje fråga på separat ark. Korta och koncisa svar uppskattas! 3) Skriv namn och och personnummer
Tentamen i Organisk kemi AK 2/6 2005,
 Tentamen i rganisk kemi AK 2/6 2005, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: 3:a minst 40 poäng 4:a minst 55 poäng 5:a minst 75 poäng Skriv
Tentamen i rganisk kemi AK 2/6 2005, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: 3:a minst 40 poäng 4:a minst 55 poäng 5:a minst 75 poäng Skriv
Proteiner. Biomolekyler kap 7
 Proteiner Biomolekyler kap 7 Generna (arvsanlagen) (och miljön) bestämmer hur en organism skall se ut och fungera. Hur? En gen är en ritning för hur ett protein skall se ut. Proteiner får saker att hända
Proteiner Biomolekyler kap 7 Generna (arvsanlagen) (och miljön) bestämmer hur en organism skall se ut och fungera. Hur? En gen är en ritning för hur ett protein skall se ut. Proteiner får saker att hända
Tentamensuppgifter moment 2, organisk kemi.
 UMEÅ UIVERSITET TETAME Kemiska Institutionen Tentamensdatum 2012-01-19 BE, KP Studiekurs: Kemi för miljö- och hälsoskyddsområdet, 15 hp. Kurskod: KE004 Tentamen: Moment 2, organisk kemi (sid 1-3) och Moment
UMEÅ UIVERSITET TETAME Kemiska Institutionen Tentamensdatum 2012-01-19 BE, KP Studiekurs: Kemi för miljö- och hälsoskyddsområdet, 15 hp. Kurskod: KE004 Tentamen: Moment 2, organisk kemi (sid 1-3) och Moment
Alla papper, även kladdpapper lämnas tillbaka.
 Maxpoäng 66 g 13 vg 28 varav 4 p av uppg. 18,19,20,21 mvg 40 varav 9 p av uppg. 18,19,20,21 Alla papper, även kladdpapper lämnas tillbaka. 1 (2p) En oladdad atom innehåller 121 neutroner och 80 elektroner.
Maxpoäng 66 g 13 vg 28 varav 4 p av uppg. 18,19,20,21 mvg 40 varav 9 p av uppg. 18,19,20,21 Alla papper, även kladdpapper lämnas tillbaka. 1 (2p) En oladdad atom innehåller 121 neutroner och 80 elektroner.
Föreläsning 7. Alkoholer, aminer och alkylhalogenider Kapitel 8. 1) Introduktion 2) Alkoholer 3) Aminer 4) Alkylhalogenider
 Föreläsning 7 Alkoholer, aminer och alkylhalogenider Kapitel 8 1) Introduktion 2) Alkoholer 3) Aminer 4) Alkylhalogenider 1. Introduktion Varför blir man berusad av alkohol? nervsignalen överförs via elektriska
Föreläsning 7 Alkoholer, aminer och alkylhalogenider Kapitel 8 1) Introduktion 2) Alkoholer 3) Aminer 4) Alkylhalogenider 1. Introduktion Varför blir man berusad av alkohol? nervsignalen överförs via elektriska
TENTAMEN I ALLMÄN OCH ORGANISK KEMI
 KAROLINSKA INSTITUTET Biomedicinutbildningen TENTAMEN I ALLMÄN OCH ORGANISK KEMI FREDAGEN DEN 13 JANUARI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för
KAROLINSKA INSTITUTET Biomedicinutbildningen TENTAMEN I ALLMÄN OCH ORGANISK KEMI FREDAGEN DEN 13 JANUARI 2006, 08.30-11.00 och 12.00-14.30. Tentamen är uppdelad i två pass med en uppsättning frågor för
Kapitel 2. Kovalent bindning
 Kapitel 2. Kovalent bindning 2.1 Instuderingsfrågor 2.1.1 Rangordna kväve, fluor, syre, kol och väte efter stigande elektronegativitet. 2.1.2 Vad menas med induktiv effekt? 2.1.3 Vad menas med dipolmoment?
Kapitel 2. Kovalent bindning 2.1 Instuderingsfrågor 2.1.1 Rangordna kväve, fluor, syre, kol och väte efter stigande elektronegativitet. 2.1.2 Vad menas med induktiv effekt? 2.1.3 Vad menas med dipolmoment?
Tentamen i Organisk kemi (KEGA01/KEGAH0/KEGAO0/KEGAOO/KEGAAK) (KEGL01/BIGLN3) 20 januari 2016, kl
 Institutionen för ingenjörs- och kemivetenskaper Karlstads universitet Tentamen i Organisk kemi (KEGA01/KEGAH0/KEGAO0/KEGAOO/KEGAAK) (KEGL01/BIGLN3) 20 januari 2016, kl 08.15 13.15 Betygsgränser: respektive:
Institutionen för ingenjörs- och kemivetenskaper Karlstads universitet Tentamen i Organisk kemi (KEGA01/KEGAH0/KEGAO0/KEGAOO/KEGAAK) (KEGL01/BIGLN3) 20 januari 2016, kl 08.15 13.15 Betygsgränser: respektive:
BASÅRET KEMI B BIOKEMI VT 2012. PROTEINER OCH ENZYMER 174-190 (sid. 140-156)
 BASÅRET KEMI B BIOKEMI PROTEINER OCH ENZYMER 174-190 (sid. 140-156) Hur lätt blir det fel i strukturen? ganska stora skillnader i sekvens - ganska lika strukturer proteinerna är bara identiska i 27 av
BASÅRET KEMI B BIOKEMI PROTEINER OCH ENZYMER 174-190 (sid. 140-156) Hur lätt blir det fel i strukturen? ganska stora skillnader i sekvens - ganska lika strukturer proteinerna är bara identiska i 27 av
Totalt 10 uppgifter, vardera värd 10p (totalt 100p). För godkänt fordras minst 50p, för 4:a minst 66p och för 5:a minst 83p.
 Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 28 augusti 2007, kl. 08.00-13.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och M-skift är bifogade
Tentamen i rganisk Kemi 2 (3B1760) Tisdagen den 28 augusti 2007, kl. 08.00-13.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och M-skift är bifogade
Kinetik. Föreläsning 4
 Kinetik Föreläsning 4 Fotokemi Med fotoreaktioner avses reaktioner som initieras av ljus. Exempel: Cl 2 + h ν Cl 2 * 2Cl Ljus = små odelbara energipaket med frekvens ν (Hz = s -1 ) є = h ν h = Plancks
Kinetik Föreläsning 4 Fotokemi Med fotoreaktioner avses reaktioner som initieras av ljus. Exempel: Cl 2 + h ν Cl 2 * 2Cl Ljus = små odelbara energipaket med frekvens ν (Hz = s -1 ) є = h ν h = Plancks
Valenselektroner = elektronerna i yttersta skalet visas nedan för några element ur grupperna
 Kapitel 9 är hittar du svar och lösningar till de övningsuppgifter som hänvisas till i inledningen. I vissa fall har lärobokens avsnitt Svar och anvisningar bedömts vara tillräckligt fylliga varför enbart
Kapitel 9 är hittar du svar och lösningar till de övningsuppgifter som hänvisas till i inledningen. I vissa fall har lärobokens avsnitt Svar och anvisningar bedömts vara tillräckligt fylliga varför enbart
Svar: Tentamen i Organisk kemi 2, TFKE06, ,
 Svar: Tentamen i rganisk kemi 2, TFKE06, 2008-10-21, 1 a) Vilka av dessa heterocykliska föreningar är aromatiska? (2 p) S N N romatisk nti aromatisk nti aromatisk romatisk ückels regel: 4n + 2 elektroner
Svar: Tentamen i rganisk kemi 2, TFKE06, 2008-10-21, 1 a) Vilka av dessa heterocykliska föreningar är aromatiska? (2 p) S N N romatisk nti aromatisk nti aromatisk romatisk ückels regel: 4n + 2 elektroner
dess energi ökar (S blir mer instabilt) TS sker tidigare i reaktionen strukturen på TS blir mer lik S (2p).
 Dugga 1 TFE44 2012 1. Vad innebär the Hammond postulate - om det finns ett instabilt intermediat under reaktionen, kommer transition state att likna strukturen av intermediatet (1p). Vad menas med the
Dugga 1 TFE44 2012 1. Vad innebär the Hammond postulate - om det finns ett instabilt intermediat under reaktionen, kommer transition state att likna strukturen av intermediatet (1p). Vad menas med the
Efterarbete: LÖSNINGSFÖRSLAG TILL UPPGIFTER - O +
 Linköping 10-03-15 IFM/Kemi Linköpings universitet TFKE51/GAN-SS Efterarbete: LÖSNINGSFÖRSLAG TILL UPPGIFTER Kap. 1-4 1. N - N + - + N - + N 2. Den första resonansstrukturen är stabilast. Kom ihåg: Ju
Linköping 10-03-15 IFM/Kemi Linköpings universitet TFKE51/GAN-SS Efterarbete: LÖSNINGSFÖRSLAG TILL UPPGIFTER Kap. 1-4 1. N - N + - + N - + N 2. Den första resonansstrukturen är stabilast. Kom ihåg: Ju
Föreläsning 15. Aromater III - andra reaktioner Kapitel 15
 Föreläsning 15 Aromater III - andra reaktioner Kapitel 15 1) Introduktion 2) Sammanfattning av EAS 3) Aromatiska alkholer - fenoler 4) Aromatiska aminer 5) Aromatiska halider 6) Andra reaktioner 7) Praktiska
Föreläsning 15 Aromater III - andra reaktioner Kapitel 15 1) Introduktion 2) Sammanfattning av EAS 3) Aromatiska alkholer - fenoler 4) Aromatiska aminer 5) Aromatiska halider 6) Andra reaktioner 7) Praktiska
Radikalcyklisering vid syntes av polycykliska indoler och pyrroler
 adikalcyklisering vid syntes av polycykliska indoler och pyrroler Anneka Tuomola Pro gradu elsingfors Universitet Kemiska institutionen Laboratoriet för svenskspråkig undervisning April 2008 Innehållsförteckning
adikalcyklisering vid syntes av polycykliska indoler och pyrroler Anneka Tuomola Pro gradu elsingfors Universitet Kemiska institutionen Laboratoriet för svenskspråkig undervisning April 2008 Innehållsförteckning
4. Kemisk jämvikt när motsatta reaktioner balanserar varandra
 4. Kemisk jämvikt när motsatta reaktioner balanserar varandra 4.1. Skriv fullständiga formler för följande reaktioner som kan gå i båda riktningarna (alla ämnen är i gasform): a) Kolmonoxid + kvävedioxid
4. Kemisk jämvikt när motsatta reaktioner balanserar varandra 4.1. Skriv fullständiga formler för följande reaktioner som kan gå i båda riktningarna (alla ämnen är i gasform): a) Kolmonoxid + kvävedioxid
Lösningsförslag: Tentamen i Organisk kemi 2, TFKE06,
 Lösningsförslag: Tentamen i rganisk kemi 2, TFKE06, 2009-10-23 1.a) Vilken förening i följande par har surast väte? Ge kort förklaring till svaret. (2 p/delsvar) a) F 2 l 2 2 3 c) d) a) Fluoriden mer elektronegativ
Lösningsförslag: Tentamen i rganisk kemi 2, TFKE06, 2009-10-23 1.a) Vilken förening i följande par har surast väte? Ge kort förklaring till svaret. (2 p/delsvar) a) F 2 l 2 2 3 c) d) a) Fluoriden mer elektronegativ
KEM A02 Allmän- och oorganisk kemi. KINETIK 2(2) A: Kap
 KEM A02 Allmän- och oorganisk kemi KINETIK 2(2) A: Kap 14.6 14.16 14.6 Andra ordningens kinetik Typiskt för bimolekylära reaktioner EXEMPEL: 2 HI H 2 + I 2 v = k [HI] 2 Typiskt för 2:a ordningens reaktion:
KEM A02 Allmän- och oorganisk kemi KINETIK 2(2) A: Kap 14.6 14.16 14.6 Andra ordningens kinetik Typiskt för bimolekylära reaktioner EXEMPEL: 2 HI H 2 + I 2 v = k [HI] 2 Typiskt för 2:a ordningens reaktion:
Föreläsning 12. Alkener III Kapitel 12 F12
 Föreläsning 12 Alkener III Kapitel 12 1) Introduktion 2) Allyliska system 3) Fleromättade kolväten 4) Färg och seende 5) Reaktioner 6) Sammanfattning och framåtblick 1. Introduktion Varför ser man bättre
Föreläsning 12 Alkener III Kapitel 12 1) Introduktion 2) Allyliska system 3) Fleromättade kolväten 4) Färg och seende 5) Reaktioner 6) Sammanfattning och framåtblick 1. Introduktion Varför ser man bättre
Aromatiska föreningar
 Aromatiska föreningar och aromaticitet tiitt Dan Johnels Kemiska Institutionen Aromatiska föreningar och aromaticitet Vi har lärt oss att konjugation i linjära system alltid leder till stabilisering Om
Aromatiska föreningar och aromaticitet tiitt Dan Johnels Kemiska Institutionen Aromatiska föreningar och aromaticitet Vi har lärt oss att konjugation i linjära system alltid leder till stabilisering Om
Inga hjälpmedel är tillåtna. 100 poäng
 rganisk kemi Provmoment: Ladokkod: Tentamen ges för: Tentamen A100TG Tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 15 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel är tillåtna
rganisk kemi Provmoment: Ladokkod: Tentamen ges för: Tentamen A100TG Tillämpad bioteknik 7,5 högskolepoäng TentamensKod: Tentamensdatum: 15 Januari, 2016 Tid: 9:00-13:00 jälpmedel: Inga hjälpmedel är tillåtna
Ange längst upp på omslaget ett referensnummer (6 tecken, t.ex. bilnummer) om du vill kunna se resultatet på kurshemsidan när rättningen är klar.
 Tentamen i organisk kemi, KK05 nsdagen den 25 maj 2011, 8.00-13.00. nge längst upp på omslaget ett referensnummer (6 tecken, t.ex. bilnummer) om du vill kunna se resultatet på kurshemsidan när rättningen
Tentamen i organisk kemi, KK05 nsdagen den 25 maj 2011, 8.00-13.00. nge längst upp på omslaget ett referensnummer (6 tecken, t.ex. bilnummer) om du vill kunna se resultatet på kurshemsidan när rättningen
Tentamen i Organisk kemi 16/ ,
 Tentamen i rganisk kemi 16/12 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p 5 75-90p 1) Besvara
Tentamen i rganisk kemi 16/12 2013, 8.00-13.00. Tentamen består av 9 frågor. Varje fråga ger maximalt 10p. Följande betygsgränser gäller: N-fak LT (T) G 40-59p 3 40-54p VG 60-90p 4 55-74p 5 75-90p 1) Besvara
4. Organiska föreningars struktur
 4. Organiska föreningars struktur Organisk kemi Alla föreningar i den levande naturen är uppbyggda av kol (C). Många innehåller dessutom väte (H), syre (O), kväve (N), fosfor (P) och svavel (S). Den levande
4. Organiska föreningars struktur Organisk kemi Alla föreningar i den levande naturen är uppbyggda av kol (C). Många innehåller dessutom väte (H), syre (O), kväve (N), fosfor (P) och svavel (S). Den levande
Organiska föreningar del 6: Rita och namnge etrar, aldehyder, ketoner, tioler och disulfider. Niklas Dahrén
 Organiska föreningar del 6: Rita och namnge etrar, aldehyder, ketoner, tioler och disulfider Niklas Dahrén Etrar Etrar har en etergrupp (eterbindning): R-grupperna är två identiska eller två olika kolvätegrupper/kolvätekedjor
Organiska föreningar del 6: Rita och namnge etrar, aldehyder, ketoner, tioler och disulfider Niklas Dahrén Etrar Etrar har en etergrupp (eterbindning): R-grupperna är två identiska eller två olika kolvätegrupper/kolvätekedjor
Övningsuppgifter. till Ellervik, Sterner; Organisk Kemi. Studentlitteratur, 2004
 RGANISK KEMI Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Karolina Aplander, Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Jakob Nilsson,
RGANISK KEMI Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Karolina Aplander, Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Jakob Nilsson,
Inhibitorer Kylvattenkonferens Solna 3/5 2017
 Inhibitorer Kylvattenkonferens Solna 3/5 2017 Niklas Dahlberg 1 Varför behövs vattenbehandling? Fokus på problemen: MIKROBIO KORROSION Vad orsakar scaling? Faktorer som påverkar bildandet av scaling: Suspenderande
Inhibitorer Kylvattenkonferens Solna 3/5 2017 Niklas Dahlberg 1 Varför behövs vattenbehandling? Fokus på problemen: MIKROBIO KORROSION Vad orsakar scaling? Faktorer som påverkar bildandet av scaling: Suspenderande
Metabolism och energi. Hur utvinner cellen energi från sin omgivning? Hur syntetiserar cellen de byggstenar som bygger upp dess makromolekyler?
 Metabolism och energi Hur utvinner cellen energi från sin omgivning? Hur syntetiserar cellen de byggstenar som bygger upp dess makromolekyler? Intermediär metabolism Escherichia coli som exempel Fler än
Metabolism och energi Hur utvinner cellen energi från sin omgivning? Hur syntetiserar cellen de byggstenar som bygger upp dess makromolekyler? Intermediär metabolism Escherichia coli som exempel Fler än
Organisk kemi AK KOK Ulf Ellervik
 rganisk kemi AK KK012 2013-01-29 Ulf Ellervik Föreläsning 3 Kolvätens egenskaper Kapitel 4 1) Introduktion 2) Konformationsanalys 3) Sura kolväten 4) Kolvätens reaktioner 1. Introduktion Vad händer egentligen
rganisk kemi AK KK012 2013-01-29 Ulf Ellervik Föreläsning 3 Kolvätens egenskaper Kapitel 4 1) Introduktion 2) Konformationsanalys 3) Sura kolväten 4) Kolvätens reaktioner 1. Introduktion Vad händer egentligen
Konc. i början 0.1M 0 0. Ändring -x +x +x. Konc. i jämvikt 0,10-x +x +x
 Lösning till tentamen 2013-02-28 för Grundläggande kemi 10 hp Sid 1(5) 1. CH 3 COO - (aq) + H 2 O (l) CH 3 COOH ( (aq) + OH - (aq) Konc. i början 0.1M 0 0 Ändring -x +x +x Konc. i jämvikt 0,10-x +x +x
Lösning till tentamen 2013-02-28 för Grundläggande kemi 10 hp Sid 1(5) 1. CH 3 COO - (aq) + H 2 O (l) CH 3 COOH ( (aq) + OH - (aq) Konc. i början 0.1M 0 0 Ändring -x +x +x Konc. i jämvikt 0,10-x +x +x
Övningsuppgifter. till Ellervik, Sterner; Organisk Kemi. Studentlitteratur, 2004
 Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Karolina Larsson, Jakob Nilsson, Ulf Nilsson,
Övningsuppgifter till Ellervik, Sterner; rganisk Kemi Studentlitteratur, 2004 Magnus Berglund, Johan Billing, Ulf Ellervik, Mårten Jacobsson, Richard Johnsson, Karolina Larsson, Jakob Nilsson, Ulf Nilsson,
Organiska ämnen (2) s
 Organiska ämnen (2) s126-154 Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar lätt med andra ämnen. (p g a den elektronegativa halogenatomen) används
Organiska ämnen (2) s126-154 Haloalkaner kolförening med en halogen ( F, Cl, Br, I ) bundna till kolatomer är reaktiva dvs de reagerar lätt med andra ämnen. (p g a den elektronegativa halogenatomen) används
AOT/AOP Avancerade OxidationsProcesser
 AOT/AOP Avancerade OxidationsProcesser Klas Hedman, Sweco Environment 1 H 2 HO 2 O/O 2 /O 3 /UV 3 H 2 O 2 /UV Fenton OH O 3 /UV Superkritisk vattenoxidation Fotokatalytisk oxidation H 2 O 2 /O 3 /UV 1987
AOT/AOP Avancerade OxidationsProcesser Klas Hedman, Sweco Environment 1 H 2 HO 2 O/O 2 /O 3 /UV 3 H 2 O 2 /UV Fenton OH O 3 /UV Superkritisk vattenoxidation Fotokatalytisk oxidation H 2 O 2 /O 3 /UV 1987
Tentamen i organisk kemi, KOKA05, 5 hp, Måndagen den 1 juni 2009, 14.00-19.00.
 Tentamen i organisk kemi, KKA05, 5 hp, Måndagen den 1 juni 2009, 14.00-19.00. Molekylmodeller och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer
Tentamen i organisk kemi, KKA05, 5 hp, Måndagen den 1 juni 2009, 14.00-19.00. Molekylmodeller och miniräknare får medtagas. Var vänlig besvara endast en uppgift per papper. Skriv namn och personnummer
Totalt 10 uppgifter, vardera värd 10p (totalt 100p). För godkänt fordras minst 50p, för 4:a minst 66p och för 5:a minst 83p.
 Tentamen i rganisk Kemi 2 (3B1760) nsdagen den 23 maj 2007, kl. 08.00-13.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och M-skift är bifogade
Tentamen i rganisk Kemi 2 (3B1760) nsdagen den 23 maj 2007, kl. 08.00-13.00 Tillåtet hjälpmedel: molekylmodeller Periodiskt system och tabeller med bindingsstyrkor, pk a -värden och M-skift är bifogade
