Lösning. ph = -lg 3,99*10-3 = 2,4
|
|
|
- Roger Blomqvist
- för 9 år sedan
- Visningar:
Transkript
1 till tentamen för Grundläggande kemi 10 hp Sid 1(8) 1. a) Beräkna ph i en 0.20 M lösning av vitamin C (askorbinsyra, pka = 4.10). b) Man vill göra en buffertlösning med ph = 3,3. Följande kemikalier finns tillgängliga: Ammoniumjodid, ammoniak, kaliumfluorid, kaliumvätekarbonat, natriumklorid, natriumbromid, saltsyra, fluorvätesyra och vätebromid (aq). Vilka kemikalier bör användas och vilka ungefärliga proportioner (inga beräkningar behövs) vad avser substansmängd skall tas av dessa? Det förutsätts att vatten finns tillgängligt vid eventuellt behov. a) AscOH (aq) + H 2 O (l) à AscO - ( (aq) + H3O + (aq) Konc, i början 0,20M 0 0 Ändring -x +x +x Konc, i jämvikt 0,20-x +x +x [AscO - ] * [H 3 O + ] K K a = x 2 /(0,2-x) a = [AscOH] AscOH är en svag syra, dvs, x<< 0,2 K a = x 2 /(0,2) och x = (K a *0,2) 0,5 Med K a = 7,94*10-5 får man då: x = (7,94*10-5 *0,2) 0,5 = 3,99*10-3 Test: 3,99*10-3 är verkligen << 0,2, approximationen var ok, ph = -lg 3,99*10-3 = 2,4 b) Ett syra-baspar med pka värdet nära 3,3 bör användas Enda möjligheten är HF/F - systemet med pka = 3,17 där buffertkapaciteten har ett maximum och [HF] = [F - ]. För att komma till ph = 3,3 behöver man mer HF än F - (KF), enligt [F - ] 0 ph = pk a + lg [HF]0 2. a) Reaktionen H 2 (g) + Br 2 (g) 2 HBr (g) har jämviktskonstanten K 1 = 4,0 x Den omvända reaktionen 2 HBr (g) H 2 (g) + Br 2 (g) har jämviktskonstanten K 2, som är okänd. i) Ställ upp massverkans lag för K 1 och K 2. ii) Vad är det matematiska sambandet mellan K 1 och K 2? iii) Beräkna K 2 b) Vi återgår till reaktionen H 2 (g) + Br 2 (g) 2 HBr (g) med H r 0 = -72 kj/mol och jämviktskonstanten K 1 = 4,0 x 10-2 vid 25 o C. Som ni vet är jämviktskonstanter temperaturberoende. Vid temperaturen T x är jämviktstrycken; p(h 2 ) = 1,10 bar, p(br 2 ) = 1,40 bar, p(hbr) = 0,12 bar.
2 i) Bestäm först K x vid den nya temperaturen T x. ii) Beräkna sedan temperaturen T x. Sid 2(8) a) K 1 = (p HBr ) 2 (p H2 ) * (p Br2 ) (p H2 ) * (p Br2 ) K 2 = (p HBr ) 2 K 2 = 1/ K 1 K 2 = 25 b) K 1 = 4.0 * 10-2 vid T 1 = 298 K i) (p HBr ) 2 K x = = 9.35*10-3 (p H2 ) * (p Br2 ) ii) K ln x 1 1 = R T 1 K 1 H 0 r Med R = J/K*mol 9.35*10-3 ln = -72*103 J/mol 1 4.0* J/K*mol 298 K = K * (3.356 * /T x ); T x = 314 K T x 1 T x 3. För en galvanisk cell vid 25 o C gäller följande cellschema: Fe (s) Fe 2+ (aq, 1,0M) H + (aq, ph=2,5) H 2 (g, 1,0 bar) Pt (s) a) Ange anod- och katodreaktionerna och cellreaktionen. Beräkna E 0 i volt för cellen. b) Beräkna därefter cellens spänning (cellpotentialen). a) Anod: Fe (s) à Fe 2+ (aq) + 2 e- Katod: 2 H + (aq) + 2 e- à H2 (g) Totalt: 2 H + (aq) + Fe (s) à H2 (g) + Fe 2+ (aq) E 0 cell = E 0 katod - E 0 anod = 0 V - (-0.44 V) = 0.44 V (Tabell 21) b) Nernst ekvation: E cell = E 0 RT cell - ln Q nf
3 Q = [Fe 2+ ]/[H + ] 2 = 1/[H + ] 2 [H + ] = = 3.16 * 10-3 M Q = 1 * 10 5 E cell = 0.44 V = 0.29 V Sid 3(8) 4. a) Vilken av figurerna beskriver reaktionshastighetens beroende av temperaturen? b) Vilket av påståendena är rätt? Aktiveringsenergin kan beskrivas som; A. kinetisk energi B. energin hos det aktiverade komplexet C. energiskillnaden mellan produkter och reaktanter D. energiskillnaden mellan det aktiverade komplexet och reaktanterna c) CH 3 COCH 3 (aq) + Br 2 (aq) CH 3 COCH 2 Br (aq) + Br (aq) + H + (aq) Man undersökte den syrakatalyserade reaktionen genom att mäta initialhastigheten för olika koncentrationer, se tabellen med experimentella värden nedan. Bestäm reaktionsordningen med avseende på reaktanterna och H + och ange uttrycket för R, den totala reaktionshastigheten. Man kan anse att raktionsordningarna är heltal. Initialkoncentration / mol dm 3 Initialhastighet Experiment [CH 3 COCH 3 (aq)] 0 [Br 2 (aq)] 0 [H + (aq)] 0 R 0 / 10 6 mol dm 3 s 1 1 0,30 0,05 0,05 5,60 2 0,30 0,10 0,05 5,60 3 0,30 0,05 0,10 11,1 4 0,40 0,05 0,20 30,5 5 0,40 0,05 0,05 7,55 a) Figur D. Reaktionshastigheten ökar med temperaturen. b) D. Se aktiveringsenergikurvan i figur B ovan. Det aktiverade komplexet finns i kurvans maximum. c) Reaktionshastigheten kan skrivas R= k[ch 3 COCH 3 ] m [Br 2 ] n [H + ] p
4 Sid 4(8) Inspektera data och undersök hur initialhastigheten varierar då koncentrationen hos var och en av reaktanterna ändras. För att bestämma exponenterna jämförs experiment där koncentrationen för det aktuella ämnet ändras medan övriga ämnens koncentrationer är konstanta. Reaktionsordning m.a.p. Br 2 : Jämför försök 1 och 2, [Br 2 ] fördubblas men R ändras inte, n=0. Reaktionen är av nollte ordningen m.a.p. Br 2. Reaktionsordning m.a.p. H + : Jämför försök 1 och 3. Då [H + ] fördubblas ökar R till det dubbla, p=1. Reaktionen är av första ordningen m.a.p. H +. Reaktionsordning m.a.p. CH 3 COCH 3 : Jämför försök 1 och 5. Då [CH 3 COCH 3 ] ökar tre gånger ökar R tre ganger, m=1. Reaktionen är av första ordningen m.a.p. CH 3 COCH 3. Totala reaktionshastigheten R= k[ch 3 COCH 3 ] [H + ] 5. a) Betrakta en elektron i en 5d-orbital. -- Ange kvanttalet n och l för denna elektron. -- Ange alla möjliga värden på kvanttalet m l för denna elektron. -- Ange alla möjliga värden på kvanttalet m s för denna elektron. -- Hur många 5d-orbitaler finns det? Ange hur detta antal är relaterat till något eller några av kvanttalen. b) Atomernas storlek ges av kovalenta atomradier medan jonernas storlek ges av jonradier. Förklara varför storleken på den neutrala natriumatomen 11 Na (r=1,54å) är storre an storleken på motsvarande positiva jon 11 Na + (r=1,02å). Förklara hur du resonerar. a) En elektron i en 5d-orbital 5d n=5 och l=2 n=5 för det står siffran 5 framför d, l=2 för en d-orbital har l=2 (medan en s-orbital har l=0, en p- orbital har l=1,...etc...) Definitionen -l m l +l ger här när l=2 att: -2 m l +2 m l =-2,-1,0,1,2. - för elektronen kan m s bara vara m s = -½, +½. - det finns fem stycken 5d-orbitaler. Detta eftersom antalet orbitaler i ett underskal är lika med antalet värden på m l, vilket är fem stycken här: m l =-2,-1,0,1,2. Antalet värden på m l är givet av 2l+1. b) Den neutrala natriumatomen 11 Na har elva elektroner som rör sig runt en kärna med elva protoner. Den positiva jonen 11 Na + har bara tio elektroner som rör sig runt en kärna med elva protoner. Kärnan med sina 11 protoner har lättare att attrahera 10 elektroner än 11 elektroner. Så Coulombkraften blir starkare mellan kärnan och 10 elektroner än mellan kärnan och 11 elektroner. De 10 elektronerna är tätare bundna till kärnan i 11 Na + än de 11 elektronerna är bundna till kärnan i 11 Na. Detta gör att 11 Na + är mindre (r=1,02å) än 11 Na (r=1,54å). 6. a) Beräkna H och S vid 25 ºC och trycket 1 bar för nedanstående reaktion. Ca 3 (PO 4 ) 2 (s) > 3 Ca 2+ (aq) + 2 PO 4 3- (aq) b) Beräkna jämviktskonstanten för reaktionen (löslighetsprodukten) vid 5 C. Jämför ditt värde med värdet i SI-Data vid 25 C. Ökar eller minskar lösligheten med temperaturen?
5 Sid 5(8) a) Ca 3 (PO 4 ) 2 (s) > 3 Ca 2+ (aq) + 2 PO 4 3- (aq) Värden ur SI-Data tabell 5. ΔHº =3ΔHº f Ca 2+ (aq) + 2ΔHº f PO 4 3- (aq) - ΔHº f Ca 3 (PO 4 ) 2 (s) = =3 (-543) + 2 (-1277) - (-4121) = -62 kj mol -1 ΔSº =2 Sº HBr(g) - Sº H 2 (g) - Sº Br 2 (l) = = 3 (-56) + 2 (-220) = -844 J mol -1 K -1 b) Antag att ΔHº och ΔSº för reaktionen inte beror på temperaturen. ΔGº = ΔHº - T ΔSº = ,2 (-844) = 1, J mol -1 ΔGº = - RT lnk K = e - ( ΔGº/RT) = 3, SI-Data ger vid 25 C K sp = 1, => lösligheten minskar när T minskar. c) ΔGº = ΔHº - T ΔSº = ,2 115 = -1, J mol -1 ΔG = ΔGº < 0 visar att reaktionen är spontan 7. a) Bindningsavståndet mellan kväveatomen och syreatomen i NO 3 molekylen är 1,24 Å vilket är längre än en standard N=O bindning (1,14 Å) och kortare än en standard N O bindning (1,36 Å). Förklara varför genom att bestämma Lewisstrukturen for NO Beräkna antalet valenselektroner, antalet delade elektroner och antalet odelade elektroner. -- Rita Lewisstrukturen. -- Beräkna den formella laddningen för varje atom i molekylen. -- Ange resonansstrukturer i molekylen om det finns fler än en entydig struktur. -- Kommentera ditt resultat och relatera det till bindningslängden for NO i molekylen jamfört med bindningslängderna för N=O och N O. b) Vinkeln H C H i metan (CH 4 ) är 109,5 medan vinklarna H C H i eten (H 2 C=CH 2 ) är ca Skillnaden beror på olika typ av hybridisering för kolatomen i dessa två molekyler. -- Bestäm vilken typ av hybridisering kolatomerna har i metan och i eten. Förklara och kommentera ditt svar. -- Vilken av dessa två molekyler är plan? Motivera. -- Vad heter geometrin för den andra molekylen? 7a)- NO-bindningen i NO 3 : Antalet valenselektroner V = 5+18=23 (5 för N, 3x6=18 för de 3 syreatomerna). Antalet elektroner för att uppfylla oktettregeln är totalt O = 4 x 8 = 32 elektroner för de 4 atomerna i molekylen. Antalet delade elektroner är B = O V = = 9 delade elektroner, dvs 4,5 bindningar. Antalet odelade elektroner är L = V B = 23 9 =14 odelade elektroner, dvs 7 fria elektronpar. -- Rita Lewisstrukturen
6 Sid 6(8) -- Formella laddningen F A för atom A i molekylen ges av F A =V A -[L A +½B A ]. (Formeln finns i Atkins&Jones, 5 th, sida 70). N : F N = 5 - [0 + ½9] = +½ O= : F O= = 6 - [6 + ½4] = 0 O : F O = 6 - [6 + ½2] = -1 O : F O = 6 - [4 + ½3] = +½ -- det finns 6 resonansstrukturer för molekylen: -- Om bara en av de 6 strukturerna är rätt så skulle NO 3 ha en kort N=O bindning, en lång N O bindning, och en tredje NO-bindning med bindningslängden intermediat mellan N=O och N O. I verkligheten är alla tre NO bindningarna i molekylen identiska och lika långa och detta därför att det finns fler än en resonansstruktur för NO 3 och den verkliga molekylen är en blandning av dessa 6 resonansstrukturer. b) hybridisering av kolatomen i metan och eten: -- (*) i metan bidrar kolatomen till fyra CH bindningar av sigma-typ. Man behöver ha fyra orbitaler på kolatomen, därför betraktar man en sp 3 -hybridisering för kolatomen: i en sp 3 -hybridisering kombinerar man 2s-orbitalen med de tre 2p-orbitaler i kol för att få fyra nya atomorbitaler som kallas för hybrid atomorbitaler eftersom de är en blandning av rena atomorbitaler. (**) i eten bidrar varje kolatom till tre sigma bindningar. Man behöver ha tre orbitaler på kolatomen, därför betraktar man en sp 2 -hybridisering för kolatomen: i en sp 2 -hybridisering kombinerar man 2s-orbitalen med de två 2p-orbitaler i kol för att få tre nya hybrid sp 2 -atomorbitaler, den tredje 2p-orbitalen på kol förblir en ren atomorbital. -- En sp 2 -hybridisering ger en plan geometri med en vinkel på 120 mellan två sp 2 - hybridorbitaler.
7 Alltså eten (H 2 C=CH 2 ), där kolatomerna har sp 2 -hybridisering, är en plan molekyl. Atomorbitalen som förblir en ren 2p-orbital är vinkelrätt mot planen och bidrar till en pibindning mellan de två kolatomerna i eten. -- Den andra molekylen i uppgiften är metan (CH 4 ) där kolatomen har sp 3 -hybridisering. En sp 3 -hybridisering ger en tetraedrisk geometri, med en vinkel på 109,5 mellan två sp 3 -hybridorbitaler. Alltså metan är tetraedrisk. Sid 7(8) 8. Ange med motivering om H, S och G är större än noll, mindre än noll eller lika med noll för processerna i a) och b). Beräkning behöver ej utföras. a) 2 C 8 H 18 (l) + 25 O 2 (g) > 16 CO 2 (g) + 18 H 2 O(l), fullständig förbränning av oktan. b ) En våt badhandduk som torkar i solen på en badstrand i Thailand, (vattnet = systemet). c) Beräkna med data i tabell 5 i SI Chemical Data, hur stor entalpi som krävs per kg vatten för processen i uppgift b). d) Gör en riskbedömning av aluminiumfosfid, AlP(s). Ange den kondenserade riskkoden och förklara betydelsen av denna betecknings olika delar (risk- och säkerhetsfraser skall inte anges). a) Värme avges i processen, H< 0. Δn gas = 16-25= -9mol < 0 ger S<0. G <0, förbränningsreaktioner är spontana. b) Värme tillförs i processen, H> 0. För processen (l) >(g) är Δn gas >0 vilket ger S> 0. Reaktion är spontan dvs G<0. c) I SI Data tabell 5 ges värden på ΔH sub och ΔH fus. Hess lag (se även formel (16) i formelsamlingen), ger ΔH vap = ΔH sub - ΔH fus = 50-6 = 44 kj mol -1. Entalpiändringen= tillförda entalpin= (m/m)44= (1000/18,0) 44 kj =2,44 MJ d) Den kondenserade riskkoden för aluminiumfosfid, AlP(s) är 4,3+6,9.07 i SI Chemical Data 6:e upplagan. ändrad riskkod jämfört med föregående upplaga av SI-Chemical Data 4.3 fast ämne som är farligt då det är vått + = mycket, 6 = giftigt ämne 9 miljöfarligt ämne 07 är en kondenserad riskfrasreferens som kan expanderas till risk- och säkerhetsfraser på sidorna huvudrisk placeras först, sekundär risk, placeras efter huvudrisken
Konc. i början 0.1M 0 0. Ändring -x +x +x. Konc. i jämvikt 0,10-x +x +x
 Lösning till tentamen 2013-02-28 för Grundläggande kemi 10 hp Sid 1(5) 1. CH 3 COO - (aq) + H 2 O (l) CH 3 COOH ( (aq) + OH - (aq) Konc. i början 0.1M 0 0 Ändring -x +x +x Konc. i jämvikt 0,10-x +x +x
Lösning till tentamen 2013-02-28 för Grundläggande kemi 10 hp Sid 1(5) 1. CH 3 COO - (aq) + H 2 O (l) CH 3 COOH ( (aq) + OH - (aq) Konc. i början 0.1M 0 0 Ändring -x +x +x Konc. i jämvikt 0,10-x +x +x
Allmän kemi. Läromålen. Molekylers geometri. Viktigt i kap 10. 10.1 VSEPR-modellen. 10.1 Molekylers geometri
 Läromålen Allmän kemi Kap 10 Kemisk bindning 2 Del 1 Molekylers geometri Studenten skall efter att ha genomfört delkurs 1 kunna: n redogöra för atomers och molekylers uppbyggnad och geometri på basal nivå
Läromålen Allmän kemi Kap 10 Kemisk bindning 2 Del 1 Molekylers geometri Studenten skall efter att ha genomfört delkurs 1 kunna: n redogöra för atomers och molekylers uppbyggnad och geometri på basal nivå
Kap. 3. Kemisk bindning: kovalenta bindningar
 Kap. 3. Kemisk bindning: kovalenta bindningar 3.1 Ex: H + H H 2 Kovalent kemisk bindning Kovalent bindning: - Elektron(moln) delas av kärnorna - Systemet av elektroner och kärnor söker lägsta energi -
Kap. 3. Kemisk bindning: kovalenta bindningar 3.1 Ex: H + H H 2 Kovalent kemisk bindning Kovalent bindning: - Elektron(moln) delas av kärnorna - Systemet av elektroner och kärnor söker lägsta energi -
Kemisk bindning II, A&J kap. 3
 Kemisk bindning II, A&J kap. 3 Varför är vattenmolekylen böjd medan koldioxid är rak? Kan en stabil e 2 molekyl bildas? - Lewisstrukturer Beskriver valenselektronerna i en molekyl (Förra föreläsningen!)
Kemisk bindning II, A&J kap. 3 Varför är vattenmolekylen böjd medan koldioxid är rak? Kan en stabil e 2 molekyl bildas? - Lewisstrukturer Beskriver valenselektronerna i en molekyl (Förra föreläsningen!)
Skriv reaktionsformler som beskriver vad som bör hända för följande blandningar: lösning blandas med 50 ml 0,05 H 3 PO 4 lösning.
 Lösning till tentamen 95 för Grundläggande kemi hp Sid (5). a) Perklorsyra är en stark syra varför pk a värde saknas i SI Chem Data. Behövs inte heller för phberäkning eftersom HClO 4 H O ClO 4 H 3 O går
Lösning till tentamen 95 för Grundläggande kemi hp Sid (5). a) Perklorsyra är en stark syra varför pk a värde saknas i SI Chem Data. Behövs inte heller för phberäkning eftersom HClO 4 H O ClO 4 H 3 O går
Kap 6: Termokemi. Energi:
 Kap 6: Termokemi Energi: Definition: Kapacitet att utföra arbete eller producera värme Termodynamikens första huvudsats: Energi är oförstörbar kan omvandlas från en form till en annan men kan ej förstöras.
Kap 6: Termokemi Energi: Definition: Kapacitet att utföra arbete eller producera värme Termodynamikens första huvudsats: Energi är oförstörbar kan omvandlas från en form till en annan men kan ej förstöras.
Syra-basjämvikter. (Kap. 16.1-5)
 Syra-basjämvikter. (Kap. 16.1-5) Endast vattenlösningar i denna kurs. Definitioner (16.1) Syra (enl. Brönsted & Lowry): Protongivare. HA(aq) + H 2 O(l) H 3 O + (aq) + A (aq) (Protolysreaktion) H 3 O +
Syra-basjämvikter. (Kap. 16.1-5) Endast vattenlösningar i denna kurs. Definitioner (16.1) Syra (enl. Brönsted & Lowry): Protongivare. HA(aq) + H 2 O(l) H 3 O + (aq) + A (aq) (Protolysreaktion) H 3 O +
Grundläggande kemi I 10 hp
 Grundläggande kemi I 10 hp Sid 1(5) Uppsala universitet Tentamenssdatum Kemi grundutbildning 2014-01-08 Provansvarig: Jan Davidsson Tentamen 2014-01-08 kl 14.00-19.00 TILLÅTNA HJÄLPMEDEL Miniräknare, SI
Grundläggande kemi I 10 hp Sid 1(5) Uppsala universitet Tentamenssdatum Kemi grundutbildning 2014-01-08 Provansvarig: Jan Davidsson Tentamen 2014-01-08 kl 14.00-19.00 TILLÅTNA HJÄLPMEDEL Miniräknare, SI
Tentamen i Allmän kemi NKEA02, 9KE211, 9KE351. 2010-09-20, kl. 14 00-19 00
 IFM/Kemi Tentamen i Allmän kemi NKEA02, 9KE211, 9KE351 2010-09-20, kl. 14 00-19 00 Ansvariga lärare: Helena Herbertsson 285605, 070-5669944 Lars Ojamäe 281380 50% rätt ger säkert godkänt! Hjälpmedel: Miniräknare
IFM/Kemi Tentamen i Allmän kemi NKEA02, 9KE211, 9KE351 2010-09-20, kl. 14 00-19 00 Ansvariga lärare: Helena Herbertsson 285605, 070-5669944 Lars Ojamäe 281380 50% rätt ger säkert godkänt! Hjälpmedel: Miniräknare
Lösning till dugga för Grundläggande kemi Duggauppgifter enligt lottning; nr X, Y och Z.
 till dugga för Grundläggande kemi 2013-11-29 Duggauppgifter enligt lottning; nr X, Y och Z. 1. a) Ange kvalitativt buffertkapacitetens storlek (stor eller liten, med motivering, dock inga beräkningar)
till dugga för Grundläggande kemi 2013-11-29 Duggauppgifter enligt lottning; nr X, Y och Z. 1. a) Ange kvalitativt buffertkapacitetens storlek (stor eller liten, med motivering, dock inga beräkningar)
David Wessman, Lund, 30 oktober 2014 Statistisk Termodynamik - Kapitel 5. Sammanfattning av Gunnar Ohléns bok Statistisk Termodynamik.
 Sammanfattning av Gunnar Ohléns bok Statistisk Termodynamik. 1 Jämviktsvillkor Om vi har ett stort system som består av ett litet system i kontakt med en värmereservoar. Storheter för det lilla systemet
Sammanfattning av Gunnar Ohléns bok Statistisk Termodynamik. 1 Jämviktsvillkor Om vi har ett stort system som består av ett litet system i kontakt med en värmereservoar. Storheter för det lilla systemet
Högskoletekniker i energi- och processteknik
 Processkemi Provmoment: Tentamen Ladokkod: TH171A Tentamen ges för: Högskoletekniker i energi- och processteknik 7,5 högskolepoäng Namn: Personnummer: Tentamensdatum: 2015-03-18 Tid: 9:00-13:00 Hjälpmedel:
Processkemi Provmoment: Tentamen Ladokkod: TH171A Tentamen ges för: Högskoletekniker i energi- och processteknik 7,5 högskolepoäng Namn: Personnummer: Tentamensdatum: 2015-03-18 Tid: 9:00-13:00 Hjälpmedel:
Kemisk bindning I, Chemical bonds A&J kap. 2
 Kemisk bindning I, Chemical bonds A&J kap. 2 Dagens Olika bindningstyper - Jonbindning - Kovalent bindning - Polär kovalent bindning - Metallbindning Elektronegativitet - Jonbindning eller kovalent bindning?
Kemisk bindning I, Chemical bonds A&J kap. 2 Dagens Olika bindningstyper - Jonbindning - Kovalent bindning - Polär kovalent bindning - Metallbindning Elektronegativitet - Jonbindning eller kovalent bindning?
Introduktion till kemisk bindning. Niklas Dahrén
 Introduktion till kemisk bindning Niklas Dahrén Kemiska bindningar delas in i två huvudtyper Intramolekylära bindningar: De bindningar som finns mellan atomerna i en molekyl, mellan jonerna i e5 salt eller
Introduktion till kemisk bindning Niklas Dahrén Kemiska bindningar delas in i två huvudtyper Intramolekylära bindningar: De bindningar som finns mellan atomerna i en molekyl, mellan jonerna i e5 salt eller
Lathund, procent med bråk, åk 8
 Lathund, procent med bråk, åk 8 Procent betyder hundradel, men man kan också säga en av hundra. Ni ska kunna omvandla mellan bråkform, decimalform och procentform. Nedan kan ni se några omvandlingar. Bråkform
Lathund, procent med bråk, åk 8 Procent betyder hundradel, men man kan också säga en av hundra. Ni ska kunna omvandla mellan bråkform, decimalform och procentform. Nedan kan ni se några omvandlingar. Bråkform
1. a) Förklara, genom användning av något lämpligt kemiskt argument, varför H 2 SeO 4 är en starkare syra än H 2 SeO 3.
 Lösning till tentamen 2008 12 15 för Grundläggande kemi 10 hp Sid 1(5) 1. a) Förklara, genom användning av något lämpligt kemiskt argument, varför H 2 SeO 4 är en starkare syra än H 2 SeO 3. b) Beräkna
Lösning till tentamen 2008 12 15 för Grundläggande kemi 10 hp Sid 1(5) 1. a) Förklara, genom användning av något lämpligt kemiskt argument, varför H 2 SeO 4 är en starkare syra än H 2 SeO 3. b) Beräkna
Beräkna substansmängd, molmassa och massa. Niklas Dahrén
 Beräkna substansmängd, molmassa och massa Niklas Dahrén Uppgifter som jag går igenom i den här filmen: 1. Bestäm molmassan för glukos (C 6 H 12 O 6 ). 2. Hur många mol glukos (C 6 H 12 O 6 ) finns i den
Beräkna substansmängd, molmassa och massa Niklas Dahrén Uppgifter som jag går igenom i den här filmen: 1. Bestäm molmassan för glukos (C 6 H 12 O 6 ). 2. Hur många mol glukos (C 6 H 12 O 6 ) finns i den
4-6 Trianglar Namn:..
 4-6 Trianglar Namn:.. Inledning Hittills har du arbetat med parallellogrammer. En sådan har fyra hörn och motstående sidor är parallella. Vad händer om vi har en geometrisk figur som bara har tre hörn?
4-6 Trianglar Namn:.. Inledning Hittills har du arbetat med parallellogrammer. En sådan har fyra hörn och motstående sidor är parallella. Vad händer om vi har en geometrisk figur som bara har tre hörn?
Övningshäfte i matematik för. Kemistuderande BL 05
 Övningshäfte i matematik för Kemistuderande BL 05 Detta häfte innehåller några grundläggande övningar i de delar av matematiken som man har användning för i de tidiga kemistudierna. Nivån är gymnasiematematik,
Övningshäfte i matematik för Kemistuderande BL 05 Detta häfte innehåller några grundläggande övningar i de delar av matematiken som man har användning för i de tidiga kemistudierna. Nivån är gymnasiematematik,
Föreläsning 5. Molekylers rymdgeometri, Dipolmoment, VSEPR-teori och hybridisering
 Föreläsning 5 Molekylers rymdgeometri, Dipolmoment, VSEPR-teori och hybridisering Fleratomiga molekylers geometri. (Kap. 8.1-4) Molekyler eller joner av typ XY n, där X = centralatom, Y = ligand Alla Y
Föreläsning 5 Molekylers rymdgeometri, Dipolmoment, VSEPR-teori och hybridisering Fleratomiga molekylers geometri. (Kap. 8.1-4) Molekyler eller joner av typ XY n, där X = centralatom, Y = ligand Alla Y
Atomen och periodiska systemet
 Atomen och periodiska systemet Ringa in rätt svar 1. Exempel på elementarpartiklar är: joner protoner molekyler atomer elektroner 2. Atomen i sin helhet är: elektriskt neutral positivt laddad negativt
Atomen och periodiska systemet Ringa in rätt svar 1. Exempel på elementarpartiklar är: joner protoner molekyler atomer elektroner 2. Atomen i sin helhet är: elektriskt neutral positivt laddad negativt
Hjälpmedel: räknare, formelsamling, periodiska system. Spänningsserien: K Ca Na Mg Al Zn Cr Fe Ni Sn Pb H Cu Hg Ag Pt Au. Kemi A
 Uppsala Universitet Fysiska Institutionen Tekniskt- naturvetenskapligt basår Raúl Miranda 2007 Namn: Stark Karl Grupp: Den bästa.. Datum: Tid: 08.00 12.00 jälpmedel: räknare, formelsamling, periodiska
Uppsala Universitet Fysiska Institutionen Tekniskt- naturvetenskapligt basår Raúl Miranda 2007 Namn: Stark Karl Grupp: Den bästa.. Datum: Tid: 08.00 12.00 jälpmedel: räknare, formelsamling, periodiska
4-3 Vinklar Namn: Inledning. Vad är en vinkel?
 4-3 Vinklar Namn: Inledning I det här kapitlet skall du lära dig allt om vinklar: spetsiga, trubbiga och räta vinklar. Och inte minst hur man mäter vinklar. Att mäta vinklar och sträckor är grundläggande
4-3 Vinklar Namn: Inledning I det här kapitlet skall du lära dig allt om vinklar: spetsiga, trubbiga och räta vinklar. Och inte minst hur man mäter vinklar. Att mäta vinklar och sträckor är grundläggande
Kapitel 6. f(x) = sin x. Figur 6.1: Funktionen sin x. 1 Oinas-Kukkonen m.fl. Kurs 6 kapitel 1
 Kapitel 6 Gränsvärde 6. Definition av gränsvärde När vi undersöker gränsvärdet av en funktion undersöker vi vad som händer med funktionsvärdet då variabeln, x, går mot ett visst värde. Frågeställningen
Kapitel 6 Gränsvärde 6. Definition av gränsvärde När vi undersöker gränsvärdet av en funktion undersöker vi vad som händer med funktionsvärdet då variabeln, x, går mot ett visst värde. Frågeställningen
Tentamen i Fysik A, Tekniskt-Naturvetenskapligt basår
 Tentamen i Fysik A, Tekniskt-Naturvetenskapligt basår Datum: 05-01-20 Skrivtid: 16.00-22.00 Hjälpmedel: Räknare, formelsamling Lärare: A. Gustafsson, M. Hamrin, L. Lundmark och L-E. Svensson Namn: Grupp:
Tentamen i Fysik A, Tekniskt-Naturvetenskapligt basår Datum: 05-01-20 Skrivtid: 16.00-22.00 Hjälpmedel: Räknare, formelsamling Lärare: A. Gustafsson, M. Hamrin, L. Lundmark och L-E. Svensson Namn: Grupp:
REPETITIONSKURS I KEMI LÖSNINGAR TILL ÖVNINGSUPPGIFTER
 KEMI REPETITIONSKURS I LÖSNINGAR TILL ÖVNINGSUPPGIFTER Magnus Ehinger Fullständiga lösningar till beräkningsuppgifterna. Kemins grunder.10 Vi antar att vi har 10 000 Li-atomer. Av dessa är då 74 st 6 Li
KEMI REPETITIONSKURS I LÖSNINGAR TILL ÖVNINGSUPPGIFTER Magnus Ehinger Fullständiga lösningar till beräkningsuppgifterna. Kemins grunder.10 Vi antar att vi har 10 000 Li-atomer. Av dessa är då 74 st 6 Li
konstanterna a och b så att ekvationssystemet x 2y = 1 2x + ay = b 2 a b
 Tentamen i Inledande matematik för V och AT, (TMV25), 20-0-26. Till denna uppgift skulle endast lämnas svar, men här ges kortfattade lösningar. a) Bestäm { konstanterna a och b så att ekvationssystemet
Tentamen i Inledande matematik för V och AT, (TMV25), 20-0-26. Till denna uppgift skulle endast lämnas svar, men här ges kortfattade lösningar. a) Bestäm { konstanterna a och b så att ekvationssystemet
Kovalent och polär kovalent bindning. Niklas Dahrén
 Kovalent och polär kovalent bindning Niklas Dahrén Indelning av kemiska bindningar Intramolekylära bindningar Kovalent bindning Polär kovalent bindning Jonbindning Kemisk bindning Dipol- dipolbindning
Kovalent och polär kovalent bindning Niklas Dahrén Indelning av kemiska bindningar Intramolekylära bindningar Kovalent bindning Polär kovalent bindning Jonbindning Kemisk bindning Dipol- dipolbindning
Lösning till Tentamen i Kemi (TFKE09), allmän och oorganisk del (NOP) 051017.
 Lösning till Tentamen i Kemi (TFKE09), allmän och oorganisk del (NP) 051017. 1. a) Mg(l 3 ) 2 (N 4 ) 3 b) Atimon(III)nitrid Kaliumjodat c) +IV I +II 0 Mn 2 (s) + 4 + (aq) + 2 l (aq) Mn 2+ (aq) + 2 2 (l)
Lösning till Tentamen i Kemi (TFKE09), allmän och oorganisk del (NP) 051017. 1. a) Mg(l 3 ) 2 (N 4 ) 3 b) Atimon(III)nitrid Kaliumjodat c) +IV I +II 0 Mn 2 (s) + 4 + (aq) + 2 l (aq) Mn 2+ (aq) + 2 2 (l)
Observera att alla funktioner kan ritas, men endast linjära funktioner blir räta linjer.
 1 Matematik som verktyg Antag att vi har en funktion som är en rät linje, y = 1 3x. Eftersom relationen mellan x och y är linjär räcker det med att vi hittar två punkter (två talpar) på linjen för att
1 Matematik som verktyg Antag att vi har en funktion som är en rät linje, y = 1 3x. Eftersom relationen mellan x och y är linjär räcker det med att vi hittar två punkter (två talpar) på linjen för att
ATT KUNNA TILL. MA1050 Matte Grund. 2011-06-14 Vuxenutbildningen Dennis Jonsson
 ATT KUNNA TILL MA1050 Matte Grund 2011-06-14 Vuxenutbildningen Dennis Jonsson Sida 2 av 5 Att kunna till prov G1 Kunna ställa upp och beräkna additions-, subtraktions-, multiplikations- och divisuionsuppgifter
ATT KUNNA TILL MA1050 Matte Grund 2011-06-14 Vuxenutbildningen Dennis Jonsson Sida 2 av 5 Att kunna till prov G1 Kunna ställa upp och beräkna additions-, subtraktions-, multiplikations- och divisuionsuppgifter
Övningshäfte Algebra, ekvationssystem och geometri
 Stockholms Tekniska Gmnasium --9 Övningshäfte Algebra, ekvationssstem och geometri Nivå: rätt svårt Fråga : f är ett polnom. Beräkna värdet av f, f och fπ Fråga : Ingångslönen på företaget Börjes Gurkinläggning
Stockholms Tekniska Gmnasium --9 Övningshäfte Algebra, ekvationssstem och geometri Nivå: rätt svårt Fråga : f är ett polnom. Beräkna värdet av f, f och fπ Fråga : Ingångslönen på företaget Börjes Gurkinläggning
SF1620 Matematik och modeller
 KTH Teknikvetenskap, Institutionen för matematik 1 SF160 Matematik och modeller 007-09-10 Andra veckan Trigonometri De trigonometriska funktionerna och enhetscirkeln Redan vid förra veckans avsnitt var
KTH Teknikvetenskap, Institutionen för matematik 1 SF160 Matematik och modeller 007-09-10 Andra veckan Trigonometri De trigonometriska funktionerna och enhetscirkeln Redan vid förra veckans avsnitt var
Bered en buffertlösning. Niklas Dahrén
 Bered en buffertlösning Niklas Dahrén Grundprincipen vid beredning av en buffertlösning ü När vi bereder en buffertlösning blandar vi en svag syra med dess korresponderande bas (den bas som syran också
Bered en buffertlösning Niklas Dahrén Grundprincipen vid beredning av en buffertlösning ü När vi bereder en buffertlösning blandar vi en svag syra med dess korresponderande bas (den bas som syran också
Kap. 8. Bindning: Generella begrepp
 Kap. 8. Bindning: Generella begrepp 8.1 Kemiska bindningar: olika typer Bindningslängd: avståndet mellan atomer vid energiminimum Bindningsenergi: Energivinsten vid minimum jämfört med fria atomerna, energin
Kap. 8. Bindning: Generella begrepp 8.1 Kemiska bindningar: olika typer Bindningslängd: avståndet mellan atomer vid energiminimum Bindningsenergi: Energivinsten vid minimum jämfört med fria atomerna, energin
DEMONSTRATIONER MAGNETISM II. Helmholtzspolen Elektronstråle i magnetfält Bestämning av e/m
 FyL VT6 DEMONSTRATIONER MAGNETISM II Helmholtzspolen Elektronstråle i magnetfält Bestämning av e/m Uppdaterad den 19 januari 6 Introduktion FyL VT6 I litteraturen och framför allt på webben kan du enkelt
FyL VT6 DEMONSTRATIONER MAGNETISM II Helmholtzspolen Elektronstråle i magnetfält Bestämning av e/m Uppdaterad den 19 januari 6 Introduktion FyL VT6 I litteraturen och framför allt på webben kan du enkelt
3.1 Linjens ekvation med riktningskoefficient. y = kx + l.
 Kapitel Analytisk geometri Målet med detta kapitel är att göra läsaren bekant med ekvationerna för linjen, cirkeln samt ellipsen..1 Linjens ekvation med riktningskoefficient Vi utgår från ekvationen 1
Kapitel Analytisk geometri Målet med detta kapitel är att göra läsaren bekant med ekvationerna för linjen, cirkeln samt ellipsen..1 Linjens ekvation med riktningskoefficient Vi utgår från ekvationen 1
KEMI 5. KURSBEDÖMNING: Kursprov: 8 uppgifter varav eleven löser max. 7 Tre av åtta uppgifter är från SE max. poäng: 42 gräns för godkänd: 12
 KEMI 5 Saana Ruotsala saana.ruotsala@mattliden.fi Kursbok Kaila, Meriläinen et al.: Kemi 5 Reaktioner och jämvikt All kursinfo (t. ex. lektionsanteckningar, eventuella övningsprov...) finns på Matteus.
KEMI 5 Saana Ruotsala saana.ruotsala@mattliden.fi Kursbok Kaila, Meriläinen et al.: Kemi 5 Reaktioner och jämvikt All kursinfo (t. ex. lektionsanteckningar, eventuella övningsprov...) finns på Matteus.
Biologisk katalysator
 Enzymer biologiska katalysatorer Enzymer är biologiska katalysatorer som sänker aktiverings-energin! Biochemistry Kapitel 8 samt delar av kapitel 9 och 10 Biologisk katalysator Enzymer sänker aktiveringsenergin!
Enzymer biologiska katalysatorer Enzymer är biologiska katalysatorer som sänker aktiverings-energin! Biochemistry Kapitel 8 samt delar av kapitel 9 och 10 Biologisk katalysator Enzymer sänker aktiveringsenergin!
Klorerade alifater. Ämnesgrupper Kemiska och fysikaliska egenskaper Nedbrytning. På säker grund för hållbar utveckling
 Klorerade alifater Ämnesgrupper Kemiska och fysikaliska egenskaper Nedbrytning På säker grund för hållbar utveckling Tre grupper Klorerade etener 2 kol och en dubbelbindning PCE TCE DCE VC Starka kovalenta
Klorerade alifater Ämnesgrupper Kemiska och fysikaliska egenskaper Nedbrytning På säker grund för hållbar utveckling Tre grupper Klorerade etener 2 kol och en dubbelbindning PCE TCE DCE VC Starka kovalenta
8.1 Se lärobokens svar och anvisningar. 8.2 Se lärobokens svar och anvisningar. 8.3 a) Skrivsättet innebär följande strukturformel
 Kapitel 8 är hittar du svar och lösningar till de övningsuppgifter som hänvisas till i inledningen. I vissa fall har lärobokens avsnitt Svar och anvisningar bedömts vara tillräckligt fylliga varför enbart
Kapitel 8 är hittar du svar och lösningar till de övningsuppgifter som hänvisas till i inledningen. I vissa fall har lärobokens avsnitt Svar och anvisningar bedömts vara tillräckligt fylliga varför enbart
m/s3,61 m/s, 5,0 s och 1,5 m/s 2 får vi längden av backen, 3,611,5 5,011,1 m/s11,1 3,6 km/h40,0 km/h
 Lina Rogström linro@ifm.liu.se Lösningar till Exempeltentamen, HT014, Fysik 1 för Basåret, BFL101 Del A A1. (p) En cyklist passerar ett backkrön. På backkrönet har han hastigheten 13 km/h och han accelererar
Lina Rogström linro@ifm.liu.se Lösningar till Exempeltentamen, HT014, Fysik 1 för Basåret, BFL101 Del A A1. (p) En cyklist passerar ett backkrön. På backkrönet har han hastigheten 13 km/h och han accelererar
Tentamen i KEMI del A för basåret GU (NBAK10) 2007-02-15 kl. 08.30-13.30. Institutionen för kemi, Göteborgs universitet
 Tentamen i KEMI del A för basåret GU (NBAK10) 2007-02-15 kl. 08.30-13.30. Institutionen för kemi, Göteborgs universitet VERSIN MED KRTA SVAR Hjälpmedel: Räknare Ansvarig lärare: Leif Holmlid 772 2832 Övriga
Tentamen i KEMI del A för basåret GU (NBAK10) 2007-02-15 kl. 08.30-13.30. Institutionen för kemi, Göteborgs universitet VERSIN MED KRTA SVAR Hjälpmedel: Räknare Ansvarig lärare: Leif Holmlid 772 2832 Övriga
KEMA00. Magnus Ullner. Föreläsningsanteckningar och säkerhetskompendium kan laddas ner från
 KEMA00 Magnus Ullner Föreläsningsanteckningar och säkerhetskompendium kan laddas ner från http://www.kemi.lu.se/utbildning/grund/kema00/dold Användarnamn: Kema00 Lösenord: DeltaH0 Repetition F2 Vågfunktion
KEMA00 Magnus Ullner Föreläsningsanteckningar och säkerhetskompendium kan laddas ner från http://www.kemi.lu.se/utbildning/grund/kema00/dold Användarnamn: Kema00 Lösenord: DeltaH0 Repetition F2 Vågfunktion
Kemiska bindningar. Medicinsk Teknik KTH Biologisk kemi Vt 2012. Märit Karls
 Kemiska bindningar Medicinsk Teknik KTH Biologisk kemi Vt 2012 Märit Karls Vad kan ni redan? Vad händer när man strör koksalt i hett vatten? A) saltet smälter B) saltet löser sig C) bägge alt är rätt,
Kemiska bindningar Medicinsk Teknik KTH Biologisk kemi Vt 2012 Märit Karls Vad kan ni redan? Vad händer när man strör koksalt i hett vatten? A) saltet smälter B) saltet löser sig C) bägge alt är rätt,
Kapitel Kapitel 12. Repetition inför delförhör 2. Kemisk kinetik. 2BrNO 2NO + Br 2
 Kapitel 1-18 Repetition inför delförhör Kapitel 1 Innehåll Kapitel 1 Kemisk kinetik Redoxjämvikter Kapitel 1 Definition Kapitel 1 Området inom kemi som berör reaktionshastigheter Kemisk kinetik Kapitel
Kapitel 1-18 Repetition inför delförhör Kapitel 1 Innehåll Kapitel 1 Kemisk kinetik Redoxjämvikter Kapitel 1 Definition Kapitel 1 Området inom kemi som berör reaktionshastigheter Kemisk kinetik Kapitel
Tentamen i Allmän kemi 7,5 hp 5 november 2014 ( poäng)
 1 (6) Tentamen i Allmän kemi 7,5 hp 5 november 2014 (50 + 40 poäng) Tentamen består av två delar, räkne- respektive teoridel: Del 1: Teoridel. Max poäng: 50 p För godkänt: 28 p Del 2: Räknedel. Max poäng:
1 (6) Tentamen i Allmän kemi 7,5 hp 5 november 2014 (50 + 40 poäng) Tentamen består av två delar, räkne- respektive teoridel: Del 1: Teoridel. Max poäng: 50 p För godkänt: 28 p Del 2: Räknedel. Max poäng:
Facit åk 6 Prima Formula
 Facit åk 6 Prima Formula Kapitel 3 Algebra och samband Sidan 95 1 a 12 cm (3 4 cm) b Han vet inte att uttrycket 3s betyder 3 s eller s + s + s 2 a 5x b 6y c 12z 3 a 30 cm (5 6 cm) b 30 cm (6 5 cm) Sidan
Facit åk 6 Prima Formula Kapitel 3 Algebra och samband Sidan 95 1 a 12 cm (3 4 cm) b Han vet inte att uttrycket 3s betyder 3 s eller s + s + s 2 a 5x b 6y c 12z 3 a 30 cm (5 6 cm) b 30 cm (6 5 cm) Sidan
Kapitel Repetition inför delförhör 2
 Kapitel 12-18 Repetition inför delförhör 2 Kapitel 1 Innehåll Kapitel 12 Kapitel 13 Kapitel 14 Kapitel 15 Kapitel 16 Kapitel 17 Kapitel 18 Kemisk kinetik Kemisk jämvikt Syror och baser Syra-basjämvikter
Kapitel 12-18 Repetition inför delförhör 2 Kapitel 1 Innehåll Kapitel 12 Kapitel 13 Kapitel 14 Kapitel 15 Kapitel 16 Kapitel 17 Kapitel 18 Kemisk kinetik Kemisk jämvikt Syror och baser Syra-basjämvikter
Tentamen. Makroekonomi NA0133. Juni 2016 Skrivtid 3 timmar.
 Jag har svarat på följande fyra frågor: 1 2 3 4 5 6 Min kod: Institutionen för ekonomi Rob Hart Tentamen Makroekonomi NA0133 Juni 2016 Skrivtid 3 timmar. Regler Svara på 4 frågor. (Vid svar på fler än
Jag har svarat på följande fyra frågor: 1 2 3 4 5 6 Min kod: Institutionen för ekonomi Rob Hart Tentamen Makroekonomi NA0133 Juni 2016 Skrivtid 3 timmar. Regler Svara på 4 frågor. (Vid svar på fler än
Pesach Laksman är lärarutbildare i matematik och matematikdidaktik vid Malmö högskola.
 111a Geometri med snöre Pesach Laksman är lärarutbildare i matematik och matematikdidaktik vid Malmö högskola. Areabegreppet När elever får frågan vad area betyder ges mestadels svar som antyder hur man
111a Geometri med snöre Pesach Laksman är lärarutbildare i matematik och matematikdidaktik vid Malmö högskola. Areabegreppet När elever får frågan vad area betyder ges mestadels svar som antyder hur man
Facit med lösningsförslag kommer att anslås på vår hemsida www.ebersteinska.norrkoping.se. Du kan dessutom få dem via e-post, se nedan.
 Detta häfte innehåller uppgifter från fyra olika områden inom matematiken. Meningen är att de ska tjäna som en självtest inför gymnasiet. Klarar du dessa uppgifter så är du väl förberedd inför gymnasiestudier
Detta häfte innehåller uppgifter från fyra olika områden inom matematiken. Meningen är att de ska tjäna som en självtest inför gymnasiet. Klarar du dessa uppgifter så är du väl förberedd inför gymnasiestudier
Modul 6: Integraler och tillämpningar
 Institutionen för Matematik SF65 Envariabelanalys Läsåret 5/6 Modul 6: Integraler och tillämpningar Denna modul omfattar kapitel 6. och 6.5 samt kapitel 7 i kursboken Calculus av Adams och Essex och undervisas
Institutionen för Matematik SF65 Envariabelanalys Läsåret 5/6 Modul 6: Integraler och tillämpningar Denna modul omfattar kapitel 6. och 6.5 samt kapitel 7 i kursboken Calculus av Adams och Essex och undervisas
Institutionen för matematik Envariabelanalys 1. Jan Gelfgren Datum: Fredag 9/12, 2011 Tid: 9-15 Hjälpmedel: Inga (ej miniräknare)
 Umeå universitet Dugga i matematik Institutionen för matematik Envariabelanalys 1 och matematisk statistik IE, ÖI, Stat. och Frist. Jan Gelfgren Datum: Fredag 9/12, 2011 Tid: 9-15 Hjälpmedel: Inga (ej
Umeå universitet Dugga i matematik Institutionen för matematik Envariabelanalys 1 och matematisk statistik IE, ÖI, Stat. och Frist. Jan Gelfgren Datum: Fredag 9/12, 2011 Tid: 9-15 Hjälpmedel: Inga (ej
1 Navier-Stokes ekvationer
 Föreläsning 5. 1 Navier-Stokes ekvationer I förra föreläsningen härledde vi rörelsemängdsekvationen Du j Dt = 1 τ ij + g j. (1) ρ x i Vi konstaterade också att spänningstensorn för en inviskös fluid kan
Föreläsning 5. 1 Navier-Stokes ekvationer I förra föreläsningen härledde vi rörelsemängdsekvationen Du j Dt = 1 τ ij + g j. (1) ρ x i Vi konstaterade också att spänningstensorn för en inviskös fluid kan
Tentamen i matematisk statistik (9MA241/9MA341/LIMAB6, STN2) 2012-01-09 kl 08-13
 LINKÖPINGS UNIVERSITET MAI Johan Thim Tentamen i matematisk statistik (9MA241/9MA341/LIMAB6, STN2) 212-1-9 kl 8-13 Hjälpmedel är: miniräknare med tömda minnen och formelbladet bifogat. Varje uppgift är
LINKÖPINGS UNIVERSITET MAI Johan Thim Tentamen i matematisk statistik (9MA241/9MA341/LIMAB6, STN2) 212-1-9 kl 8-13 Hjälpmedel är: miniräknare med tömda minnen och formelbladet bifogat. Varje uppgift är
Ekvationssystem, Matriser och Eliminationsmetoden
 Matematiska institutionen Göteborgs universitet och Chalmers tekniska högskola Version 359 Ekvationssystem, Matriser och Eliminationsmetoden - En inledning Ekvationssystem - matrisformulering Vi såg att
Matematiska institutionen Göteborgs universitet och Chalmers tekniska högskola Version 359 Ekvationssystem, Matriser och Eliminationsmetoden - En inledning Ekvationssystem - matrisformulering Vi såg att
Kemi. Fysik, läran om krafterna, energi, väderfenomen, hur alstras elektrisk ström mm.
 Kemi Inom no ämnena ingår tre ämnen, kemi, fysik och biologi. Kemin, läran om ämnena, vad de innehåller, hur de tillverkas mm. Fysik, läran om krafterna, energi, väderfenomen, hur alstras elektrisk ström
Kemi Inom no ämnena ingår tre ämnen, kemi, fysik och biologi. Kemin, läran om ämnena, vad de innehåller, hur de tillverkas mm. Fysik, läran om krafterna, energi, väderfenomen, hur alstras elektrisk ström
Börje Truedsson. Lösningar till Blandade uppgifter kap 1-2. Enheter / Prefix
 Lösningar till Blandade uppgifter kap 1-2 Enheter / Prefix G1. Vi jämför sträckornas längder genom att uttrycka dem i samma multipelenhet (nm). a) 13 nm b) 1600 pm = 1,6 nm c) 4 µm = 4000 nm d) 0,0003
Lösningar till Blandade uppgifter kap 1-2 Enheter / Prefix G1. Vi jämför sträckornas längder genom att uttrycka dem i samma multipelenhet (nm). a) 13 nm b) 1600 pm = 1,6 nm c) 4 µm = 4000 nm d) 0,0003
3. Värmeutvidgning (s. 49 57)
 3. Värmeutvidgning (s. 49 57) Om du vill öppna ett burklock som har fastnat kan du värma det under varmt vatten en stund och sedan lossnar det enklare. Detta beror på att värmen får locket att utvidga
3. Värmeutvidgning (s. 49 57) Om du vill öppna ett burklock som har fastnat kan du värma det under varmt vatten en stund och sedan lossnar det enklare. Detta beror på att värmen får locket att utvidga
SEPARABLA DIFFERENTIALEKVATIONER
 SEPARABLA DIFFERENTIALEKVATIONER En differentialekvation (DE) av första ordningen sägs vara separabel om den kan skrivas på formen P ( y) Q( ) () Den allmänna lösningen till () erhålles genom att integrera
SEPARABLA DIFFERENTIALEKVATIONER En differentialekvation (DE) av första ordningen sägs vara separabel om den kan skrivas på formen P ( y) Q( ) () Den allmänna lösningen till () erhålles genom att integrera
Föreläsning 5: Rekursion
 Föreläsning 5: Rekursion Vi har tidigare sett att man kan dela upp problem i mindre bitar med hjälp av underprogram, vilket är ett utmärkt sätt att lösa problem. Detta är ganska lätt att rita upp för sig
Föreläsning 5: Rekursion Vi har tidigare sett att man kan dela upp problem i mindre bitar med hjälp av underprogram, vilket är ett utmärkt sätt att lösa problem. Detta är ganska lätt att rita upp för sig
SKOGLIGA TILLÄMPNINGAR
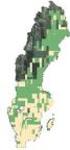 STUDIEAVSNITT 3 SKOGLIGA TILLÄMPNINGAR I detta avsnitt ska vi titta på några av de skogliga tillämpningar på geometri som finns. SKOGSKARTAN EN MODELL AV VERKLIGHETEN Arbetar man i skogen klarar man sig
STUDIEAVSNITT 3 SKOGLIGA TILLÄMPNINGAR I detta avsnitt ska vi titta på några av de skogliga tillämpningar på geometri som finns. SKOGSKARTAN EN MODELL AV VERKLIGHETEN Arbetar man i skogen klarar man sig
Får nyanlända samma chans i den svenska skolan?
 Får nyanlända samma chans i den svenska skolan? Sammanställning oktober 2015 De nyanlända eleverna (varit här högst fyra år) klarar den svenska skolan sämre än andra elever. Ett tydligt tecken är att för
Får nyanlända samma chans i den svenska skolan? Sammanställning oktober 2015 De nyanlända eleverna (varit här högst fyra år) klarar den svenska skolan sämre än andra elever. Ett tydligt tecken är att för
Snabbslumpade uppgifter från flera moment.
 Snabbslumpade uppgifter från flera moment. Uppgift nr Ställ upp och dividera utan hjälp av miniräknare talet 48 med 2 Uppgift nr 2 Skriv talet 3 8 00 med hjälp av decimalkomma. Uppgift nr 3 Uppgift nr
Snabbslumpade uppgifter från flera moment. Uppgift nr Ställ upp och dividera utan hjälp av miniräknare talet 48 med 2 Uppgift nr 2 Skriv talet 3 8 00 med hjälp av decimalkomma. Uppgift nr 3 Uppgift nr
aa + bb cc + dd gäller Q = a c d
 Jämviktslära begrepp och samband För en jämviktsreaktion vid ett visst tryck och temperatur så blir riktningen för processen, (dvs. höger eller vänster i reaktionsformeln), framåt, åt höger, om den ger
Jämviktslära begrepp och samband För en jämviktsreaktion vid ett visst tryck och temperatur så blir riktningen för processen, (dvs. höger eller vänster i reaktionsformeln), framåt, åt höger, om den ger
Tentamen i Kemi med Biokemi för K1 och Bt1 (KOO041) måndag 060306 08.30-13.30 (5 timmar)
 Kemi med biokemi KOO041 2006 03 06 1(4) CHALMERS TEKNISKA HÖGSKOLA SEKTIONEN FÖR KEMI- OCH BIOTEKNIK Tentamen i Kemi med Biokemi för K1 och Bt1 (KOO041) måndag 060306 08.30-13.30 (5 timmar) Examinator:
Kemi med biokemi KOO041 2006 03 06 1(4) CHALMERS TEKNISKA HÖGSKOLA SEKTIONEN FÖR KEMI- OCH BIOTEKNIK Tentamen i Kemi med Biokemi för K1 och Bt1 (KOO041) måndag 060306 08.30-13.30 (5 timmar) Examinator:
Kriterium Kvalitet 1 Kvalitet 2 Kvalitet 3 Kvalitet 4 Använda, Utveckla och uttrycka
 Matematik Enheter - Tid Utveckla och Känner till några enheter och enstaka mätinstrument. Utför enkla mätningar. Avläser analoga och digitala tider.använder både muntliga och skriftliga metoder samt tekniska
Matematik Enheter - Tid Utveckla och Känner till några enheter och enstaka mätinstrument. Utför enkla mätningar. Avläser analoga och digitala tider.använder både muntliga och skriftliga metoder samt tekniska
Tentamen i allmän och biofysikalisk kemi
 UPPSALA UNIVERSITET Institutionen for farmaci Tentamen i allmän och biofysikalisk kemi BionnedicUnprograrnnnet Datum: 2011-10-28 Slaivningstid: 8.00-14.00 Ansvarig lärare: Anders Ericsson, O 18-4 714126
UPPSALA UNIVERSITET Institutionen for farmaci Tentamen i allmän och biofysikalisk kemi BionnedicUnprograrnnnet Datum: 2011-10-28 Slaivningstid: 8.00-14.00 Ansvarig lärare: Anders Ericsson, O 18-4 714126
Tentamen i Syra/bas och Energi, 6hp
 Namn: Kod: Tentamen i Syra/bas och Energi, 6hp (1BA001) Programmet för Biomedicinska analytiker 2009-02-18 Tid:kl 09.00-13.00 Ulla Andersson Christina Lind Sarolta Pap Veronika Tillander ADRESS BESÖKSADRESS
Namn: Kod: Tentamen i Syra/bas och Energi, 6hp (1BA001) Programmet för Biomedicinska analytiker 2009-02-18 Tid:kl 09.00-13.00 Ulla Andersson Christina Lind Sarolta Pap Veronika Tillander ADRESS BESÖKSADRESS
Repetition F3. Lunds universitet / Naturvetenskapliga fakulteten / Kemiska institutionen / KEMA00
 Repetition F3 Oktettregeln Jonbindning och kovalent bindning Lewisstrukturer Elektronegativitet och polariserbarhet bindningskaraktär polära bindningar Bindningsstyrka F4 Molekylstrukturer Enkla molekyler
Repetition F3 Oktettregeln Jonbindning och kovalent bindning Lewisstrukturer Elektronegativitet och polariserbarhet bindningskaraktär polära bindningar Bindningsstyrka F4 Molekylstrukturer Enkla molekyler
Tentamen i Linjär algebra (TATA31/TEN1) 2013 08 24, 14 19.
 LINKÖPINGS UNIVERSITET Matematiska Institutionen Ulf Janfalk Kurskod: TATA Provkod: TEN Tentamen i Linjär algebra (TATA/TEN 8, 9. Inga hjälpmedel. Ej räknedosa. För godkänt räcker 9 poäng och minst uppgifter
LINKÖPINGS UNIVERSITET Matematiska Institutionen Ulf Janfalk Kurskod: TATA Provkod: TEN Tentamen i Linjär algebra (TATA/TEN 8, 9. Inga hjälpmedel. Ej räknedosa. För godkänt räcker 9 poäng och minst uppgifter
LPP laboration. Förmågor: Centralt innehåll: Kunskapskrav:
 LPP laboration Syfte: Eleverna ska få möjlighet att undersöka vardagliga naturvetenskapliga händelser och skapa förståelse kring varför dessa händelser äger rum. Eleverna ska göra det med hjälp av naturvetenskapliga
LPP laboration Syfte: Eleverna ska få möjlighet att undersöka vardagliga naturvetenskapliga händelser och skapa förståelse kring varför dessa händelser äger rum. Eleverna ska göra det med hjälp av naturvetenskapliga
Index vid lastbilstransporter
 index vid lastbilstransporter Matematiken Snabbhjälpen för att räkna rätt Index vid lastbilstransporter Innehåll A. Tre steg för att räkna rätt Sidan 1 B. Förändring enligt index 2 C. Andelskorrigering
index vid lastbilstransporter Matematiken Snabbhjälpen för att räkna rätt Index vid lastbilstransporter Innehåll A. Tre steg för att räkna rätt Sidan 1 B. Förändring enligt index 2 C. Andelskorrigering
Enkätresultat för elever i år 2 i Nösnäsgymnasiet 2 i Stenungsund våren 2014
 Enkätresultat för elever i år 2 i Nösnäsgymnasiet 2 i Stenungsund våren 2014 Antal elever: 47 Antal svarande: 40 Svarsfrekvens: 85% Klasser: 12BAa, 12BAb, 12LL Skolenkäten Skolenkäten går ut en gång per
Enkätresultat för elever i år 2 i Nösnäsgymnasiet 2 i Stenungsund våren 2014 Antal elever: 47 Antal svarande: 40 Svarsfrekvens: 85% Klasser: 12BAa, 12BAb, 12LL Skolenkäten Skolenkäten går ut en gång per
Väga paket och jämföra priser
 strävorna 2AC 3AC Väga paket och jämföra priser begrepp rutinuppgifter tal geometri Avsikt och matematikinnehåll Den huvudsakliga avsikten med denna aktivitet är att ge elever möjlighet att utveckla grundläggande
strävorna 2AC 3AC Väga paket och jämföra priser begrepp rutinuppgifter tal geometri Avsikt och matematikinnehåll Den huvudsakliga avsikten med denna aktivitet är att ge elever möjlighet att utveckla grundläggande
a n = A2 n + B4 n. { 2 = A + B 6 = 2A + 4B, S(5, 2) = S(4, 1) + 2S(4, 2) = 1 + 2(S(3, 1) + 2S(3, 2)) = 3 + 4(S(2, 1) + 2S(2, 2)) = 7 + 8 = 15.
 1 Matematiska Institutionen KTH Lösningar till tentamensskrivning på kursen Diskret Matematik, moment A, för D och F, SF161 och SF160, den juni 008 kl 08.00-1.00. DEL I 1. (p) Lös rekursionsekvationen
1 Matematiska Institutionen KTH Lösningar till tentamensskrivning på kursen Diskret Matematik, moment A, för D och F, SF161 och SF160, den juni 008 kl 08.00-1.00. DEL I 1. (p) Lös rekursionsekvationen
Kemisk reaktionskinetik. (Kap ej i kurs.)
 Kemisk reaktionskinetik. (Kap. 14.1-4. 14.5-6 ej i kurs.) Reaktionshastighet kemisk jämvikt. Reaktionshastighet avgör tiden att komma till jämvikt. Ett system i jämvikt reagerar inte. Jämviktsläge avgörs
Kemisk reaktionskinetik. (Kap. 14.1-4. 14.5-6 ej i kurs.) Reaktionshastighet kemisk jämvikt. Reaktionshastighet avgör tiden att komma till jämvikt. Ett system i jämvikt reagerar inte. Jämviktsläge avgörs
NATIONELLT KURSPROV I MATEMATIK KURS B HÖSTEN 1998. Tidsbunden del
 Nationellt kursprov i Matematik kurs B ht 1998 sida 1 (av 7) Skolverket hänvisar generellt beträffande provmaterial till bestämmelsen om sekretess i 4 kap. 3 sekretesslagen. För detta material gäller sekretessen
Nationellt kursprov i Matematik kurs B ht 1998 sida 1 (av 7) Skolverket hänvisar generellt beträffande provmaterial till bestämmelsen om sekretess i 4 kap. 3 sekretesslagen. För detta material gäller sekretessen
Mätning av effekter. Vad är elektrisk effekt? Vad är aktiv-, skenbar- reaktiv- medel- och direkteffekt samt effektfaktor?
 Mätning av effekter Vad är elektrisk effekt? Vad är aktiv-, skenbar- reaktiv- medel- och direkteffekt samt effektfaktor? Denna studie ger vägledning om de grundläggande parametrarna för 3-fas effektmätning.
Mätning av effekter Vad är elektrisk effekt? Vad är aktiv-, skenbar- reaktiv- medel- och direkteffekt samt effektfaktor? Denna studie ger vägledning om de grundläggande parametrarna för 3-fas effektmätning.
912 Läsförståelse och matematik behöver man lära sig läsa matematik?
 912 Läsförståelse och matematik behöver man lära sig läsa matematik? Med utgångspunkt från min egen forskning kring läsförståelse av matematiska texter kommer jag att diskutera olika aspekter av läsning
912 Läsförståelse och matematik behöver man lära sig läsa matematik? Med utgångspunkt från min egen forskning kring läsförståelse av matematiska texter kommer jag att diskutera olika aspekter av läsning
Laborativ matematik som bedömningsform. Per Berggren och Maria Lindroth 2016-01-28
 Laborativ matematik som bedömningsform Per Berggren och Maria Lindroth 2016-01-28 Kul matematik utan lärobok Vilka förmågor tränas Problemlösning (Förstå frågan i en textuppgift, Använda olika strategier
Laborativ matematik som bedömningsform Per Berggren och Maria Lindroth 2016-01-28 Kul matematik utan lärobok Vilka förmågor tränas Problemlösning (Förstå frågan i en textuppgift, Använda olika strategier
Diskussionsfrågor till version 1 och 2
 Diskussionsfrågor till version 1 och 2 Version 1 Tillgång till internet i hemmet A. Vilken åldersgrupp har haft den största ökningen av tillgång till internet under perioden? B. Kan man med hjälp av de
Diskussionsfrågor till version 1 och 2 Version 1 Tillgång till internet i hemmet A. Vilken åldersgrupp har haft den största ökningen av tillgång till internet under perioden? B. Kan man med hjälp av de
Sammanfattning på lättläst svenska
 Sammanfattning på lättläst svenska Utredningen skulle utreda och lämna förslag i vissa frågor som handlar om svenskt medborgarskap. Svenskt medborgarskap i dag Vissa personer blir svenska medborgare när
Sammanfattning på lättläst svenska Utredningen skulle utreda och lämna förslag i vissa frågor som handlar om svenskt medborgarskap. Svenskt medborgarskap i dag Vissa personer blir svenska medborgare när
Svenska Du kan med flyt läsa texter som handlar om saker du känner till. Du använder metoder som fungerar. Du kan förstå vad du läser.
 Svenska Du kan med flyt läsa texter som handlar om saker du känner till. Du använder metoder som fungerar. Du kan förstå vad du läser. Du berättar på ett enkelt sätt om det du tycker är viktigt i texten.
Svenska Du kan med flyt läsa texter som handlar om saker du känner till. Du använder metoder som fungerar. Du kan förstå vad du läser. Du berättar på ett enkelt sätt om det du tycker är viktigt i texten.
Algebra, polynom & andragradsekvationer en pampig rubrik på ett annars relativt obetydligt dokument
 Algebra, polynom & andragradsekvationer en pampig rubrik på ett annars relativt obetydligt dokument Distributiva lagen a(b + c) = ab + ac 3(x + 4) = 3 x + 3 4 = 3x + 12 3(2x + 4) = 3 2x + 3 4 = 6x + 12
Algebra, polynom & andragradsekvationer en pampig rubrik på ett annars relativt obetydligt dokument Distributiva lagen a(b + c) = ab + ac 3(x + 4) = 3 x + 3 4 = 3x + 12 3(2x + 4) = 3 2x + 3 4 = 6x + 12
Linjära system av differentialekvationer
 CTH/GU LABORATION MVE0-0/03 Matematiska vetenskaper Linjära system av differentialekvationer Inledning Vi har i envariabelanalysen sett på allmäna system av differentialekvationer med begynnelsevillkor
CTH/GU LABORATION MVE0-0/03 Matematiska vetenskaper Linjära system av differentialekvationer Inledning Vi har i envariabelanalysen sett på allmäna system av differentialekvationer med begynnelsevillkor
Två konstiga klockor
 strävorna C Två konstiga klockor resonemang geometri Avsikt och matematikinnehåll Det som kan göra det svårt för barn att avläsa en analog klocka är att förstå att den består av två skalor som är beroende
strävorna C Två konstiga klockor resonemang geometri Avsikt och matematikinnehåll Det som kan göra det svårt för barn att avläsa en analog klocka är att förstå att den består av två skalor som är beroende
Träning i bevisföring
 KTHs Matematiska Cirkel Träning i bevisföring Andreas Enblom Institutionen för matematik, 2005 Finansierat av Marianne och Marcus Wallenbergs Stiftelse 1 Mängdlära Här kommer fyra tips på hur man visar
KTHs Matematiska Cirkel Träning i bevisföring Andreas Enblom Institutionen för matematik, 2005 Finansierat av Marianne och Marcus Wallenbergs Stiftelse 1 Mängdlära Här kommer fyra tips på hur man visar
Arbeta bäst där du är Dialect Unified Mi
 Arbeta bäst där du är Dialect Unified Mi [Skriv sammanfattningen av dokumentet här. Det är vanligtvis en kort sammanfattning av innehållet i dokumentet. Skriv sammanfattningen av dokumentet här. Det är
Arbeta bäst där du är Dialect Unified Mi [Skriv sammanfattningen av dokumentet här. Det är vanligtvis en kort sammanfattning av innehållet i dokumentet. Skriv sammanfattningen av dokumentet här. Det är
1. Frekvensfunktionen nedan är given. (3p)
 TENTAMEN I MATEMATIK MED MATEMATISK STATISTIK HF14 TEN 11 kl 1.15-.15 Hjälpmedel: Formler och tabeller i statistik, räknedosa Fullständiga lösningar erfordras till samtliga uppgifter. Lösningarna skall
TENTAMEN I MATEMATIK MED MATEMATISK STATISTIK HF14 TEN 11 kl 1.15-.15 Hjälpmedel: Formler och tabeller i statistik, räknedosa Fullständiga lösningar erfordras till samtliga uppgifter. Lösningarna skall
Tentamen i Modern fysik, TFYA11, TENA
 IFM - Institutionen för Fysik, Kemi och Biologi Linköpings universitet Tentamen i Modern fysik, TFYA11, TENA Tisdagen den 23/8 2011 kl. 14.00-18.00 i TER2 Tentamen består av 4 sidor (inklusive denna sida)
IFM - Institutionen för Fysik, Kemi och Biologi Linköpings universitet Tentamen i Modern fysik, TFYA11, TENA Tisdagen den 23/8 2011 kl. 14.00-18.00 i TER2 Tentamen består av 4 sidor (inklusive denna sida)
Enkätresultat för elever i år 2 i Mega Musik gymnasium hösten 2014. Antal elever: 47 Antal svarande: 46 Svarsfrekvens: 98% Klasser: MM13
 Enkätresultat för elever i år 2 i Mega Musik gymnasium hösten 2014 Antal elever: 47 Antal svarande: 46 Svarsfrekvens: 98% Klasser: MM13 Skolenkäten Skolenkäten går ut en gång per termin till de skolor
Enkätresultat för elever i år 2 i Mega Musik gymnasium hösten 2014 Antal elever: 47 Antal svarande: 46 Svarsfrekvens: 98% Klasser: MM13 Skolenkäten Skolenkäten går ut en gång per termin till de skolor
Enkätresultat för elever i år 2 i Praktiska Skövde i Praktiska Sverige AB hösten 2014
 Enkätresultat för elever i år 2 i Praktiska Skövde i Praktiska Sverige AB hösten 2014 Antal elever: 18 Antal svarande: 13 Svarsfrekvens: 72% Klasser: År 2 Skolenkäten Skolenkäten går ut en gång per termin
Enkätresultat för elever i år 2 i Praktiska Skövde i Praktiska Sverige AB hösten 2014 Antal elever: 18 Antal svarande: 13 Svarsfrekvens: 72% Klasser: År 2 Skolenkäten Skolenkäten går ut en gång per termin
2005-01-31. Hävarmen. Peter Kock
 2005-01-31 Hävarmen Kurs: WT0010 Peter Kock Handledare: Jan Sandberg Sammanfattning Om man slår upp ordet hävarm i ett lexikon så kan man läsa att hävarm är avståndet mellan kraften och vridningspunkten.
2005-01-31 Hävarmen Kurs: WT0010 Peter Kock Handledare: Jan Sandberg Sammanfattning Om man slår upp ordet hävarm i ett lexikon så kan man läsa att hävarm är avståndet mellan kraften och vridningspunkten.
Elektronen och laddning
 Detta är en något omarbetad version av Studiehandledningen som användes i tryckta kursen på SSVN. Sidhänvisningar hänför sig till Quanta A 2000, ISBN 91-27-60500-0 Där det har varit möjligt har motsvarande
Detta är en något omarbetad version av Studiehandledningen som användes i tryckta kursen på SSVN. Sidhänvisningar hänför sig till Quanta A 2000, ISBN 91-27-60500-0 Där det har varit möjligt har motsvarande
Datorövning 2 Statistik med Excel (Office 2007, svenska)
 Datorövning 2 Statistik med Excel (Office 2007, svenska) Denna datorövning fokuserar på att upptäcka samband mellan två variabler. Det görs genom att rita spridningsdiagram och beräkna korrelationskoefficienter
Datorövning 2 Statistik med Excel (Office 2007, svenska) Denna datorövning fokuserar på att upptäcka samband mellan två variabler. Det görs genom att rita spridningsdiagram och beräkna korrelationskoefficienter
L(9/G)MA10 Kombinatorik och geometri Gruppövning 1
 L(9/G)MA10 Kombinatorik och geometri Gruppövning 1 Lisa och Pelle leker med svarta och vita byggklossar. Deras pedagogiska föräldrar vill att de lär sig matematik samtidigt som de håller på och leker.
L(9/G)MA10 Kombinatorik och geometri Gruppövning 1 Lisa och Pelle leker med svarta och vita byggklossar. Deras pedagogiska föräldrar vill att de lär sig matematik samtidigt som de håller på och leker.
Tentamen TAIU07 Matematiska beräkningar med MATLAB för MI
 TEKNISKA HÖGSKOLAN I LINKÖPING Matematiska institutionen Beräkningsmatematik/Fredrik Berntsson Tentamen TAIU07 Matematiska beräkningar med MATLAB för MI Tid: Provkod: TEN1 Hjälpmedel: Inga. Examinator:
TEKNISKA HÖGSKOLAN I LINKÖPING Matematiska institutionen Beräkningsmatematik/Fredrik Berntsson Tentamen TAIU07 Matematiska beräkningar med MATLAB för MI Tid: Provkod: TEN1 Hjälpmedel: Inga. Examinator:
Denna utrustning får endast demonstreras av personal.
 * Kort version Denna utrustning får endast demonstreras av personal. Känn på metallrören eller vattnet i spannarna Vad kan man använda en sån här apparat till? Kan den användas på mer än ett sätt? Ni har
* Kort version Denna utrustning får endast demonstreras av personal. Känn på metallrören eller vattnet i spannarna Vad kan man använda en sån här apparat till? Kan den användas på mer än ett sätt? Ni har
