KURSPROGRAM Inledande kemi (5)
|
|
|
- Bernt Arvidsson
- för 8 år sedan
- Visningar:
Transkript
1 KURSPROGRAM Inledande kemi (5) Föreläsningar Föreläsningar hålls av Johan Reimer Tid Plats Att läsa Innehåll Tisdag 20/1 KC:G Kap 2 Upprop/introduktion/repetition/nomenklatur Onsdag 21/1 KC:G Kap 3-5 Stökiometri/redoxreaktioner/Allmänna gaslagen Torsdag, 22/1 KC:G Kap 6 Termokemi, 1:a huvudsatsen, H, U, C P, Hess lag Fredag, 23/1 Fys:K404 Seminarium kap 2-5, 6 Tisdag, 27/1 KC:G Kap 8.1,2,3,6 Kap 9 Elektronkonfiguration, periodiska systemet Kemisk bindning, elektronegativitet, Onsdag, 28/1 Fredag, 30/1 Tisdag, 3/2 Torsdag, 5/2 Fredag, 6/2 Tisdag, 10/2 Onsdag, 11/2 Fredag, 13/2 Tisdag, 17/2 Onsdag, 18/2 Fredag, 20/2 Tisdag, 24/2 Onsdag, 25/2 Fredag, 27/2 Tisdag, 3/3 Onsdag, 4/3 Tisdag, 10/3 KC:G Kap Kap ,6 Lewisformler Molekylgeometrier, VSEPR, polaritet Intermolekylära krafter, fasomvandling, Clausius- Clapeyron Fys:K404 Seminarium kap 9, 10, 12 KC:G Kap ,5 Kap 15 Löslighet, Henrys lag, kemisk jämvikt, jämviktskonstanterna K C och K P, reaktionskvot (Q), homogena och heterogena jämvikter, Le Chateliers princip, jämviktsberäkningar se ovan KC:D Kap ,5 Kap 15 Fys:K404 Seminarium Kap 13, 15 KC:G Kap Syra/bas, starka/svaga syror, starka/svaga baser, ph-begreppet, ph-beräkningar, vattens autoprotolys (K a, K b, K W ), flerprotoniga syror, sura och basiska salter, KC:G Kap se ovan Fys:K404 Seminarium kap 16 KC:G Kap Buffertlösningar, titrering, löslighetsprodukt, gemensamma joneffekten KC:G Kap se ovan Fys:K404 Seminarium kap 17 KC:G Kap Andra o tredje huvudsatsen, S, G KC:G Kap se ovan Fys:K404 Seminarium kap 18 KC:G Kap 19 Galvaniska celler, Nernst ekvation KC:G Kap 19 Korrosion, elektrolys KC:G Genomgång x-tenta/ frågestund
2 KURSPROGRAM Inledande kemi (5) Övningar Uppgifter ur övningshäftet skall lösas vid övningstillfällena. Johan Reimer och Jan-Olle Malm är övningsledare Tid Plats Huvudsakligt innehåll Övningshäfte Torsdag, 22/1 Introduktion/repetition Kap 2-5 Måndag, 26/1 Termokemi Kap 6 kl Torsdag, 29/1 Kemisk bindning, Lewisformler, Kap 9, 10, 12 molekylgeometri, intermolekylära krafter Måndag, 2/2 kl, gr 1-2 KC:I Återlämning av inlämningsuppgift 1 Tisdag, 3/2 kl, gr 3-4 KC:H Torsdag 5/2 Jämviktslära Kap 13, 15 Torsdag 12/2 ph, Syra/bas Kap 16 Måndag, 16/2 kl, gr 1-2 Tisdag, 17/2 kl, gr 3-4 KC:I KC:H Återlämning av inlämningsuppgift 2 Torsdag 19/2 Buffertverkan, titreringar, K sp Kap 17 Torsdag 26/2 S, G Kap 18 Måndag, 2/3 kl, gr 1-2 Tisdag, 3/3 kl, gr 3-4 KC:I KC:H Återlämning av inlämningsuppgift 3 Torsdag 5/3 Elektrokemi Kap 19 Måndag, 9/3 Repetition kl
3 KURSPROGRAM Inledande kemi (5) Examination För godkänd kurs krävs godkända inlämningsuppgifter samt godkänd tentamen. Inlämningsuppgifter Under kursen ska tre inlämningsuppgifter lösas. Dessa delas ut och lämnas in under kursens gång på övningarna enligt schema nedan. Arbetet sker i fyramannagrupper. Varje grupp lämnar in en lösning per inlämningsuppgift. Lösningarna ska vara prydliga och klart motiverade. Om det behövs begär respektive övningsledare sedan ändringar och kompletteringar. Övningsledaren genomför även en muntlig genomgång och diskussion av inlämningsuppgifterna med varje grupp. Där måste varje gruppmedlem vara beredd att svara för samtliga lösningar. Samtliga gruppmedlemmar skall vara närvarande vid denna genomgång. Följande schema gäller för inlämningsuppgifterna: Lämnas ut Ska lämnas in Rättad/Återlämning Inlämningsuppgift 1 22/1 29/1 2-3/2 Inlämningsuppgift 2 5/2 12/ /2 Inlämningsuppgift 3 19/2 26/2 2-3/3 Tentamen Kursen tenteras måndagen den 16 mars kl i MA08 Vid ordinarie tentamenstillfälle kommer minst 25% av poängen på tentamen att hämtas från inlämningsuppgifter och övningsuppgifter. Omtentamen torsdagen den 7 maj kl 8-13 i MA10 A-C och måndagen den 24 augusti kl 8-13 i Sparta A-B. Tillåtna hjälpmedel vid tentamen är skrivmaterial, räknedosa och utdelad formelsamling Kontakt Johan Reimer johan.reimer@kemi.lu.se Jan-Olle Malm jan-olle.malm@chem.lu.se Kursens hemsida
4 KURSPROGRAM Inledande kemi (5) Inläsningsanvisningar till Chang Kap 2-5 Till största delen gymnasierepetition. Läses efter behov Kap 6 Första huvudsatsen samt betydelsen av de olika symbolerna. Beräkning av tryck-volym arbete för processer vid konstant tryck. Definition av entalpi (H). Kalorimetriska beräkningar (entalpier och värmekapaciteter). Användning av Hess lag (H är en tillståndsfunktion): Beräkning av bildningsentalpier ur förbränningsentalpier. Beräkning av reaktionsentalpier ur bildningsentalpier. Kap 8 Kännedom kring periodiska systemet. Förståelse för periodiska egenskaper hos elementen. Översiktlig kännedom om elementens kemiska egenskaper. Kap 9 Förstå och skriva Lewis formler. Elektronegativitet Förståelse för olika former av kemisk bindning. Kap 10 Molekylgeometri Förmåga att använda VSEPR modellen på enkla molekyler. Begreppet dipol Kap 12 Korta beskrivningar av olika typer av attraktionskrafter, deras energier och avståndsberoende. Vilka typer av växelverkan finns i olika system. Fasomvandlingar Egenskaper hos flytande ämnen, särskilt vatten. Kap.13 Förståelse av vilka faktorer som spelar roll beträffande lösligheten av olika ämnen. Henrys lag. Kap 15. Känna till följande begrepp: jämviktskonstanterna K C och K P, reaktionskvoten (Q), homogena och heterogena jämvikter, Le Chatelier's princip, jämviktsberäkningar och katalys. Ställa upp jämviktsuttryck och göra enklare beräkningar. Avgöra hur förändringar i koncentration, tryck, volym och temperatur påverkar jämviktsläget. Beräkna jämviktskonstanten med hjälp av tryck- och koncentrationsvärden. Beräkna jämviktstryck och jämviktskoncentrationer med hjälp av jämviktskonstanter. Kap 16. Starka syror och baser, svaga syror och baser, ph-skalan, ph-beräkningar för starka syror och baser, phberäkningar för svaga syror och baser, vattens autoprotolys - sambanden K W /K a /K b resp. pk W /pk a /pk b, flerprotoniga syror, syra/bas egenskaper hos salter. Beräkna ph i lösningar av starka och svaga syror och baser.
5 KURSPROGRAM Inledande kemi (5) Kap 17. Buffertlösningar och titreringar, neutraliseringsreaktioner, gemensamma joneffekten, buffertlösningar, Henderson Hasselbalch's ekvation, titrering, svårlösliga salter - löslighetsprodukten K sp. Beräkna ph för alla titrerpunkter och rita titrerkurvor för alla typer av syror och baser. Tillverka buffertlösningar med önskat ph. Beräkna ph i buffertlösningar. Utföra enkla beräkningar med K sp. Kap 18. Enkla resonemang kring entropiändringar för kemiska reaktioner. Beräkningar av ändringar i Gibbs fri energi. Slutsatser man kan dra mha tecknet på dessa. Sambandet mellan K och G. Kap 19. Elektrokemi, galvaniska celler, cellreaktioner och cellschema, cellpotential och fri energi, standardpotentialer, E -värden, Nernst ekvation, batterier, korrosion och elektrolys. Sambandet mellan E och G. Skriva halvcell- och cellreaktioner och cellschema. Beräkna E - och E- värden. Teckna de vanligaste halvcellreaktionerna vid korrosion. Du skall också ha kännedom om: De vanligaste batterierna och ackumulatorerna. Orsaker och förutsättningar för att korrosion skall ske.
KURSPROGRAM Inledande kemi (5)
 KURSPROGRAM Inledande kemi 2016 1(5) Föreläsningar Föreläsningar hålls av Johan Reimer Tid Plats Att läsa Innehåll Tisdag 19/1 Kap 2 Upprop/introduktion/repetition/nomenklatur Onsdag 20/1 15-17 Kap 3-5
KURSPROGRAM Inledande kemi 2016 1(5) Föreläsningar Föreläsningar hålls av Johan Reimer Tid Plats Att läsa Innehåll Tisdag 19/1 Kap 2 Upprop/introduktion/repetition/nomenklatur Onsdag 20/1 15-17 Kap 3-5
KURSPROGRAM 2013: GRUNDLÄGGANDE KEMI FÖR K och B (9 högskolepoäng)
 1 KURSPROGRAM 2013: GRUNDLÄGGANDE KEMI FÖR K och B (9 högskolepoäng) Grundläggande kemi läses av både Bioteknik- (B) och Kemiteknikprogrammet (K). Kursen börjar veckan innan första läsperioden med ett
1 KURSPROGRAM 2013: GRUNDLÄGGANDE KEMI FÖR K och B (9 högskolepoäng) Grundläggande kemi läses av både Bioteknik- (B) och Kemiteknikprogrammet (K). Kursen börjar veckan innan första läsperioden med ett
KURSPROGRAM 2012: GRUNDLÄGGANDE KEMI FÖR K och B (9 högskolepoäng)
 1 KURSPROGRAM 2012: GRUNDLÄGGANDE KEMI FÖR K och B (9 högskolepoäng) Grundläggande kemi läses av både Bioteknik- (B) och Kemiteknikprogrammet (K). Kursen börjar veckan innan första läsperioden med ett
1 KURSPROGRAM 2012: GRUNDLÄGGANDE KEMI FÖR K och B (9 högskolepoäng) Grundläggande kemi läses av både Bioteknik- (B) och Kemiteknikprogrammet (K). Kursen börjar veckan innan första läsperioden med ett
KURSPROGRAM 2010: GRUNDLÄGGANDE KEMI FÖR K och B (9 högskolepoäng)
 1 KEMICENTRUM 2010-08-26 (modifierat 100903) Polymer och materialkemi LTH KURSPROGRAM 2010: GRUNDLÄGGANDE KEMI FÖR K och B (9 högskolepoäng) 'Grundläggande kemi' läses av både Bioteknik- (B) och Kemiteknikprogrammet
1 KEMICENTRUM 2010-08-26 (modifierat 100903) Polymer och materialkemi LTH KURSPROGRAM 2010: GRUNDLÄGGANDE KEMI FÖR K och B (9 högskolepoäng) 'Grundläggande kemi' läses av både Bioteknik- (B) och Kemiteknikprogrammet
KURSPROGRAM 2017: KOOA15 ALLMÄN KEMI FÖR K och B (7,5 högskolepoäng)
 KURSPROGRAM 0: KOOA ALLMÄN KEMI FÖR K och B (, högskolepoäng) Kursen är en direkt fortsättning på kursen Inledande kemi (KOOA0). Kursen Allmän kemi har ett större fokus på kemiska beräkningar och problemlösning
KURSPROGRAM 0: KOOA ALLMÄN KEMI FÖR K och B (, högskolepoäng) Kursen är en direkt fortsättning på kursen Inledande kemi (KOOA0). Kursen Allmän kemi har ett större fokus på kemiska beräkningar och problemlösning
Schema och lite information för kzu200, moment-1 (jämvikt, 7.5hp) version:160815
 Schema och lite information för kzu200, moment-1 (jämvikt, 7.5hp) version:160815 Lärobok: Burrows, A., Holman, J., Parsons, A., Pilling, G. & Price, G. Chemistry 3 introducing inorganic, organic and physical
Schema och lite information för kzu200, moment-1 (jämvikt, 7.5hp) version:160815 Lärobok: Burrows, A., Holman, J., Parsons, A., Pilling, G. & Price, G. Chemistry 3 introducing inorganic, organic and physical
Kapitel Repetition inför delförhör 2
 Kapitel 12-18 Repetition inför delförhör 2 Kapitel 1 Innehåll Kapitel 12 Kapitel 13 Kapitel 14 Kapitel 15 Kapitel 16 Kapitel 17 Kapitel 18 Kemisk kinetik Kemisk jämvikt Syror och baser Syra-basjämvikter
Kapitel 12-18 Repetition inför delförhör 2 Kapitel 1 Innehåll Kapitel 12 Kapitel 13 Kapitel 14 Kapitel 15 Kapitel 16 Kapitel 17 Kapitel 18 Kemisk kinetik Kemisk jämvikt Syror och baser Syra-basjämvikter
Schema för grundläggande kemi, moment-i (jämvikt, 7.5hp) HT-2013
 Schema för grundläggande kemi, moment-i (jämvikt, 7.5hp) HT-2013 Lärare epost telefon Ulrich Häussermann (F) Ulrich.Haussermann@mmk.su.se 162390 Dag Noreus (R,F) Dag.Noreus@mmk.su.se 161253 Farid Akhtar
Schema för grundläggande kemi, moment-i (jämvikt, 7.5hp) HT-2013 Lärare epost telefon Ulrich Häussermann (F) Ulrich.Haussermann@mmk.su.se 162390 Dag Noreus (R,F) Dag.Noreus@mmk.su.se 161253 Farid Akhtar
Kapitel Kapitel 12. Repetition inför delförhör 2. Kemisk kinetik. 2BrNO 2NO + Br 2
 Kapitel 1-18 Repetition inför delförhör Kapitel 1 Innehåll Kapitel 1 Kemisk kinetik Redoxjämvikter Kapitel 1 Definition Kapitel 1 Området inom kemi som berör reaktionshastigheter Kemisk kinetik Kapitel
Kapitel 1-18 Repetition inför delförhör Kapitel 1 Innehåll Kapitel 1 Kemisk kinetik Redoxjämvikter Kapitel 1 Definition Kapitel 1 Området inom kemi som berör reaktionshastigheter Kemisk kinetik Kapitel
1. a) Förklara, genom användning av något lämpligt kemiskt argument, varför H 2 SeO 4 är en starkare syra än H 2 SeO 3.
 Lösning till tentamen 2008 12 15 för Grundläggande kemi 10 hp Sid 1(5) 1. a) Förklara, genom användning av något lämpligt kemiskt argument, varför H 2 SeO 4 är en starkare syra än H 2 SeO 3. b) Beräkna
Lösning till tentamen 2008 12 15 för Grundläggande kemi 10 hp Sid 1(5) 1. a) Förklara, genom användning av något lämpligt kemiskt argument, varför H 2 SeO 4 är en starkare syra än H 2 SeO 3. b) Beräkna
Schema Kemi för geovetare 15hp (KZ2003), VT 2013 Institutionen för Material och Miljökemi
 Schema Kemi för geovetare 15hp (KZ2003), VT 2013 Institutionen för Material och Miljökemi Kurslitteratur: S&S Zumdahl, Chemistry, 8th ed, 2010 Book of Data, Nuffield advanced science Lektionernas innehåll
Schema Kemi för geovetare 15hp (KZ2003), VT 2013 Institutionen för Material och Miljökemi Kurslitteratur: S&S Zumdahl, Chemistry, 8th ed, 2010 Book of Data, Nuffield advanced science Lektionernas innehåll
Schema Kemins grunder 15hp (KZ2007), VT2015 Institutionen för Material- och Miljökemi
 Schema Kemins grunder 15hp (KZ2007), VT2015 Institutionen för Material- och Miljökemi Kurslitteratur: S&S Zumdahl, Chemistry, 9 th ed, 2014 Book of Data, Nuffield advanced science Lektionernas innehåll
Schema Kemins grunder 15hp (KZ2007), VT2015 Institutionen för Material- och Miljökemi Kurslitteratur: S&S Zumdahl, Chemistry, 9 th ed, 2014 Book of Data, Nuffield advanced science Lektionernas innehåll
Tentamen i Kemisk Termodynamik 2011-01-19 kl 13-18
 Tentamen i Kemisk Termodynamik 2011-01-19 kl 13-18 Hjälpmedel: Räknedosa, BETA och Formelsamling för kurserna i kemi vid KTH. Endast en uppgift per blad! Skriv namn och personnummer på varje blad! Alla
Tentamen i Kemisk Termodynamik 2011-01-19 kl 13-18 Hjälpmedel: Räknedosa, BETA och Formelsamling för kurserna i kemi vid KTH. Endast en uppgift per blad! Skriv namn och personnummer på varje blad! Alla
KEMA02 Föreläsningsant. F2 February 18, 2011
 Syra/Bas-jämvikter - Svag syra HA vid ph>6 Uppskattning av ph för en mycket utspädd lösning av en svag syra med ph > 6 För svaga syror i sådan koncentration att syrans bidrag till ph är större än bidraget
Syra/Bas-jämvikter - Svag syra HA vid ph>6 Uppskattning av ph för en mycket utspädd lösning av en svag syra med ph > 6 För svaga syror i sådan koncentration att syrans bidrag till ph är större än bidraget
Tentamen i Allmän kemi 7,5 hp 5 november 2014 ( poäng)
 1 (6) Tentamen i Allmän kemi 7,5 hp 5 november 2014 (50 + 40 poäng) Tentamen består av två delar, räkne- respektive teoridel: Del 1: Teoridel. Max poäng: 50 p För godkänt: 28 p Del 2: Räknedel. Max poäng:
1 (6) Tentamen i Allmän kemi 7,5 hp 5 november 2014 (50 + 40 poäng) Tentamen består av två delar, räkne- respektive teoridel: Del 1: Teoridel. Max poäng: 50 p För godkänt: 28 p Del 2: Räknedel. Max poäng:
Schema för Grundläggande kemi 1, del 1 (jämvikt, 7.5hp) VT-2016, version:160118
 Schema för Grundläggande kemi 1, del 1 (jämvikt, 7.5hp) VT-2016, version:160118 Lärare epost telefon Dag Noréus (F) dag@mmk.su.se 161253 Anne Ertan (L) anne.ertan@mmk.su.se 162374 Yulia Trushkina (L) yulia.trushkina@mmk.su.se
Schema för Grundläggande kemi 1, del 1 (jämvikt, 7.5hp) VT-2016, version:160118 Lärare epost telefon Dag Noréus (F) dag@mmk.su.se 161253 Anne Ertan (L) anne.ertan@mmk.su.se 162374 Yulia Trushkina (L) yulia.trushkina@mmk.su.se
Kursprogram VT Konstruktionsteknik VBK013 (9hp)
 Bygg och Miljöteknologi Avdelningen för Konstruktionsteknik Kursprogram VT 2017 Konstruktionsteknik VBK013 (9hp) Avdelningen för Konstruktionsteknik ingår i institutionen för Bygg- och Miljöteknologi vid
Bygg och Miljöteknologi Avdelningen för Konstruktionsteknik Kursprogram VT 2017 Konstruktionsteknik VBK013 (9hp) Avdelningen för Konstruktionsteknik ingår i institutionen för Bygg- och Miljöteknologi vid
INSTITUTIONEN FÖR KEMI OCH MOLEKYLÄRBIOLOGI
 INSTITUTIONEN FÖR KEMI OCH MOLEKYLÄRBIOLOGI NBAK20 Basår: Kemi, 15 högskolepoäng Introduction to Natural Sciences: Chemistry, 15 higher education Fastställande Kursplanen är fastställd av Institutionen
INSTITUTIONEN FÖR KEMI OCH MOLEKYLÄRBIOLOGI NBAK20 Basår: Kemi, 15 högskolepoäng Introduction to Natural Sciences: Chemistry, 15 higher education Fastställande Kursplanen är fastställd av Institutionen
Kursprogram VT Konstruktionsteknik VBKF15 (9hp)
 Bygg och Miljöteknologi Avdelningen för Konstruktionsteknik Kursprogram VT 2018 Konstruktionsteknik VBKF15 (9hp) Avdelningen för Konstruktionsteknik ingår i institutionen för Bygg- och Miljöteknologi vid
Bygg och Miljöteknologi Avdelningen för Konstruktionsteknik Kursprogram VT 2018 Konstruktionsteknik VBKF15 (9hp) Avdelningen för Konstruktionsteknik ingår i institutionen för Bygg- och Miljöteknologi vid
Kapitel 15. Syra-basjämvikter
 Kapitel 15 Syra-basjämvikter Kapitel 15 Innehåll 15.1 Lösningar med gemensam jon 15.2 Bufferlösningar 15.3 Bufferkapacitet 15.4 Titrering och ph-kurvor 15.5 Copyright Cengage Learning. All rights reserved
Kapitel 15 Syra-basjämvikter Kapitel 15 Innehåll 15.1 Lösningar med gemensam jon 15.2 Bufferlösningar 15.3 Bufferkapacitet 15.4 Titrering och ph-kurvor 15.5 Copyright Cengage Learning. All rights reserved
Välkommen till kursen. Termodynamik HT- 15
 Välkommen till kursen Termodynamik HT- 15 Kurskod: KE1160 7,5hp LAB1 Laboration, 1.0, betygsskala: P, F TEN1 Tentamen, 5.0, betygsskala: A, B, C, D, E, Fx, F ÖVN1 - Obligatorisk närvaro, 1.5, betygsskala:
Välkommen till kursen Termodynamik HT- 15 Kurskod: KE1160 7,5hp LAB1 Laboration, 1.0, betygsskala: P, F TEN1 Tentamen, 5.0, betygsskala: A, B, C, D, E, Fx, F ÖVN1 - Obligatorisk närvaro, 1.5, betygsskala:
TENTAMEN I KEMI TFKE16 (4 p)
 Linköpings Universitet IFM-Kemi. Kemi för Y, M. m. fl. (TFKE16) TENTMEN I KEMI TFKE16. 2007-10-16 Lokal: TER2. Skrivtid: 14.00 18.00 nsvariga lärare: Nils-la Persson, tel. 1387, alt 070-517 1088. Stefan
Linköpings Universitet IFM-Kemi. Kemi för Y, M. m. fl. (TFKE16) TENTMEN I KEMI TFKE16. 2007-10-16 Lokal: TER2. Skrivtid: 14.00 18.00 nsvariga lärare: Nils-la Persson, tel. 1387, alt 070-517 1088. Stefan
INSTITUTIONEN FÖR KEMI OCH MOLEKYLÄRBIOLOGI
 INSTITUTIONEN FÖR KEMI OCH MOLEKYLÄRBIOLOGI NBAK00 Naturvetenskapligt basår, Kemi, 15 högskolepoäng Introduction to Natural Sciences: Chemistry, 15 Fastställande Kursplanen är fastställd av Institutionen
INSTITUTIONEN FÖR KEMI OCH MOLEKYLÄRBIOLOGI NBAK00 Naturvetenskapligt basår, Kemi, 15 högskolepoäng Introduction to Natural Sciences: Chemistry, 15 Fastställande Kursplanen är fastställd av Institutionen
Kursprogram VT Konstruktionsteknik VBK013 (9hp)
 Bygg och Miljöteknologi Avdelningen för Konstruktionsteknik Kursprogram VT 2015 Konstruktionsteknik VBK013 (9hp) Avdelningen för Konstruktionsteknik ingår i institutionen för Bygg- och Miljöteknologi vid
Bygg och Miljöteknologi Avdelningen för Konstruktionsteknik Kursprogram VT 2015 Konstruktionsteknik VBK013 (9hp) Avdelningen för Konstruktionsteknik ingår i institutionen för Bygg- och Miljöteknologi vid
aa + bb cc + dd gäller Q = a c d
 Jämviktslära begrepp och samband För en jämviktsreaktion vid ett visst tryck och temperatur så blir riktningen för processen, (dvs. höger eller vänster i reaktionsformeln), framåt, åt höger, om den ger
Jämviktslära begrepp och samband För en jämviktsreaktion vid ett visst tryck och temperatur så blir riktningen för processen, (dvs. höger eller vänster i reaktionsformeln), framåt, åt höger, om den ger
Kapitel 18. Elektrokemi. oxidation-reduktion (redox): innebär överföring av elektroner från ett reduktionsmedel till ett oxidationsmedel.
 Kapitel 18 Innehåll Kapitel 18 Elektrokemi 18.1 Balansera Redoxreaktionslikheter 18.2 Galvaniska celler 18.3 Standardreduktionspotentialer 18.4 Cellpotentialer, Elektriskt arbete och Fri energi 18.5 Cellpotentialens
Kapitel 18 Innehåll Kapitel 18 Elektrokemi 18.1 Balansera Redoxreaktionslikheter 18.2 Galvaniska celler 18.3 Standardreduktionspotentialer 18.4 Cellpotentialer, Elektriskt arbete och Fri energi 18.5 Cellpotentialens
Kapitel 18. Elektrokemi
 Kapitel 18 Elektrokemi Kapitel 18 Innehåll 18.1 Balansera Redoxreaktionslikheter 18.2 Galvaniska celler 18.3 Standardreduktionspotentialer 18.4 Cellpotentialer, Elektriskt arbete och Fri energi 18.5 Cellpotentialens
Kapitel 18 Elektrokemi Kapitel 18 Innehåll 18.1 Balansera Redoxreaktionslikheter 18.2 Galvaniska celler 18.3 Standardreduktionspotentialer 18.4 Cellpotentialer, Elektriskt arbete och Fri energi 18.5 Cellpotentialens
Kursprogram. Byggnadsmekanik VSMA05 HT 2016
 Byggnadsmekanik VSMA05 HT 2016 Kursprogram Allmänt Kursen Byggnadsmekanik omfattar 8 hp och ges under läsperiod 2. Kursen syftar till att ge en introduktion till byggnadsmekanik tillämpad på konstruktionstyper
Byggnadsmekanik VSMA05 HT 2016 Kursprogram Allmänt Kursen Byggnadsmekanik omfattar 8 hp och ges under läsperiod 2. Kursen syftar till att ge en introduktion till byggnadsmekanik tillämpad på konstruktionstyper
Välkommen till kursen. Termodynamik HT- 16
 Välkommen till kursen Termodynamik HT- 16 Kurskod: KE1160 7,5hp LAB1 Laboration, 1.0, betygsskala: P, F TEN1 Tentamen, 5.0, betygsskala: A, B, C, D, E, Fx, F ÖVN1 - Obligatorisk närvaro, 1.5, betygsskala:
Välkommen till kursen Termodynamik HT- 16 Kurskod: KE1160 7,5hp LAB1 Laboration, 1.0, betygsskala: P, F TEN1 Tentamen, 5.0, betygsskala: A, B, C, D, E, Fx, F ÖVN1 - Obligatorisk närvaro, 1.5, betygsskala:
JÄMVIKT i LÖSNING A: Kap 12 Föreläsning 3(3)
 KEM A02 Allmän- och oorganisk kemi JÄMVIKT i LÖSNING A: Kap 12 Föreläsning 3(3) mer löslighetsprodukt! Repetition Henderson-Hasselbach ekvationen för beräkning av ph i buffert - OK att använda - viktigast
KEM A02 Allmän- och oorganisk kemi JÄMVIKT i LÖSNING A: Kap 12 Föreläsning 3(3) mer löslighetsprodukt! Repetition Henderson-Hasselbach ekvationen för beräkning av ph i buffert - OK att använda - viktigast
JÄMVIKT i LÖSNING A: Kap 12 Föreläsning 2(2)
 KEM A02 Allmän- och oorganisk kemi JÄMVIKT i LÖSNING A: Kap 12 Föreläsning 2(2) mer löslighetsprodukt! 12.9 The common ion effect utsaltning[utfällning] genom tillsats av samma jonslag BAKGRUND Många metalljoner
KEM A02 Allmän- och oorganisk kemi JÄMVIKT i LÖSNING A: Kap 12 Föreläsning 2(2) mer löslighetsprodukt! 12.9 The common ion effect utsaltning[utfällning] genom tillsats av samma jonslag BAKGRUND Många metalljoner
Preliminärt detaljschema för kursen Kemi 15 Hp, Miljö och Hälsoskydd, Ht 2015, version
 Preliminärt detaljschema för kursen Kemi 15 Hp, Miljö och Hälsoskydd, Ht 2015, version 20150602 Ni förväntas komma väl förberedda till SG, vilket innebär att ni bör ha läst igenom texten i boken i förväg
Preliminärt detaljschema för kursen Kemi 15 Hp, Miljö och Hälsoskydd, Ht 2015, version 20150602 Ni förväntas komma väl förberedda till SG, vilket innebär att ni bör ha läst igenom texten i boken i förväg
Arbetshäfte kemi 9. Namn: Det här arbetshäftet innehåller dina anteckningar från genomgångarna i kemi. KEMI 9
 Arbetshäfte kemi 9 Namn: Det här arbetshäftet innehåller dina anteckningar från genomgångarna i kemi.!1 Repetition Grundämne eller kemisk förening 1. Rita och beskriv skillnaden mellan ett grundämne och
Arbetshäfte kemi 9 Namn: Det här arbetshäftet innehåller dina anteckningar från genomgångarna i kemi.!1 Repetition Grundämne eller kemisk förening 1. Rita och beskriv skillnaden mellan ett grundämne och
Tentamen i Kemisk Termodynamik kl 14-19
 Tentamen i Kemisk Termodynamik 2009-12-16 kl 14-19 Hjälpmedel: Räknedosa, BETA och Formelsamling för kurserna i kemi vid KTH. Endast en uppgift per blad! Skriv namn och personnummer på varje blad! Alla
Tentamen i Kemisk Termodynamik 2009-12-16 kl 14-19 Hjälpmedel: Räknedosa, BETA och Formelsamling för kurserna i kemi vid KTH. Endast en uppgift per blad! Skriv namn och personnummer på varje blad! Alla
Tentamen i Kemisk Termodynamik kl 14-19
 Tentamen i Kemisk Termodynamik 2011-06-09 kl 14-19 Hjälpmedel: Räknedosa, BETA och Formelsamling för kurserna i kemi vid KTH. Endast en uppgift per blad! Skriv namn och personnummer på varje blad! Alla
Tentamen i Kemisk Termodynamik 2011-06-09 kl 14-19 Hjälpmedel: Räknedosa, BETA och Formelsamling för kurserna i kemi vid KTH. Endast en uppgift per blad! Skriv namn och personnummer på varje blad! Alla
På samma sätt ges ph för en lösning av en svag bas och dess salt av:
 Kemiska beräkningar HT 2008 - Laboration 2 Syrabastitrering Syftet med den här laborationen är att ge laboranten insikt i användandet av phmeter vid ph-titreringar, samt förstå hur titrerkurvor för starka,
Kemiska beräkningar HT 2008 - Laboration 2 Syrabastitrering Syftet med den här laborationen är att ge laboranten insikt i användandet av phmeter vid ph-titreringar, samt förstå hur titrerkurvor för starka,
KOKA20 Läsanvisningar till läroboken, 6. upplagan, 2013
 KOKA20 Läsanvisningar till läroboken, 6. upplagan, 2013 Kapitel F A-C, E F kursivt (från fysik och gymnasium förväntas ni kunna: SI-enheter, energi, atomteori, molbegreppet, formelräkningar, omsättningar)
KOKA20 Läsanvisningar till läroboken, 6. upplagan, 2013 Kapitel F A-C, E F kursivt (från fysik och gymnasium förväntas ni kunna: SI-enheter, energi, atomteori, molbegreppet, formelräkningar, omsättningar)
Kemisk jämvikt. Kap 3
 Kemisk jämvikt Kap 3 En reaktionsformel säger vilka ämnen som reagerar vilka som bildas samt förhållandena mellan ämnena En reaktionsformel säger inte hur mycket som reagerar/bildas Ingen reaktion ger
Kemisk jämvikt Kap 3 En reaktionsformel säger vilka ämnen som reagerar vilka som bildas samt förhållandena mellan ämnena En reaktionsformel säger inte hur mycket som reagerar/bildas Ingen reaktion ger
Kursprogram. Byggnadsmekanik VSMA05 HT 2018
 Byggnadsmekanik VMA05 HT 2018 Kursprogram Allmänt Kursen Byggnadsmekanik omfattar 8 hp och ges under läsperiod 2. Kursen syftar till att ge en introduktion till byggnadsmekanik tillämpad på konstruktionstyper
Byggnadsmekanik VMA05 HT 2018 Kursprogram Allmänt Kursen Byggnadsmekanik omfattar 8 hp och ges under läsperiod 2. Kursen syftar till att ge en introduktion till byggnadsmekanik tillämpad på konstruktionstyper
Spelschema för årets fotbollsmästerskap! island tyskland Söndag 14/7 Växjö Arena, Växjö. Söndag 14/7 Kalmar Arena, Kalmar
 ! Onsdagen 10/7 Onsdagen 10/7 Torsdag 11/7 Torsdag 11/7, Fredag 12/7 Fredag 12/7 Lördag 13/7 Lördag 13/7 Söndag 14/7 Söndag 14/7 Måndag 15/7 Måndag 15/7 Tisdag 16/7 Tisdag 16/7 Onsdag 17/7 Onsdag 17/7
! Onsdagen 10/7 Onsdagen 10/7 Torsdag 11/7 Torsdag 11/7, Fredag 12/7 Fredag 12/7 Lördag 13/7 Lördag 13/7 Söndag 14/7 Söndag 14/7 Måndag 15/7 Måndag 15/7 Tisdag 16/7 Tisdag 16/7 Onsdag 17/7 Onsdag 17/7
Föreläsning 2.3. Fysikaliska reaktioner. Kemi och biokemi för K, Kf och Bt S = k lnw
 Kemi och biokemi för K, Kf och Bt 2012 N molekyler V Repetition Fö2.2 Entropi är ett mått på sannolikhet W i = 1 N S = k lnw Föreläsning 2.3 Fysikaliska reaktioner 2V DS = S f S i = Nkln2 Björn Åkerman
Kemi och biokemi för K, Kf och Bt 2012 N molekyler V Repetition Fö2.2 Entropi är ett mått på sannolikhet W i = 1 N S = k lnw Föreläsning 2.3 Fysikaliska reaktioner 2V DS = S f S i = Nkln2 Björn Åkerman
Grundläggningsteknik VGTF01
 Grundläggningsteknik VGTF01 Kursprogram 2016 Allmänt Efter avslutad kurs ska du kunna genomföra och förstå vetenskapligt baserad geoteknisk dimensionering. För att kunna detta ska du Praktiskt använda
Grundläggningsteknik VGTF01 Kursprogram 2016 Allmänt Efter avslutad kurs ska du kunna genomföra och förstå vetenskapligt baserad geoteknisk dimensionering. För att kunna detta ska du Praktiskt använda
Hur förändras den ideala gasens inre energi? Beräkna också q. (3p)
 entamen i kemisk termodynamik den 4 juni 2013 kl. 14.00 till 19.00 Hjälpmedel: Räknedosa, BEA och Formelsamling för kurserna i kemi vid KH. Endast en uppgift per blad! Skriv namn och personnummer på varje
entamen i kemisk termodynamik den 4 juni 2013 kl. 14.00 till 19.00 Hjälpmedel: Räknedosa, BEA och Formelsamling för kurserna i kemi vid KH. Endast en uppgift per blad! Skriv namn och personnummer på varje
Grundläggningsteknik VGTN01
 Grundläggningsteknik VGTN01 Kursprogram 2018 Allmänt Efter avslutad kurs ska du kunna genomföra och förstå vetenskapligt baserad geoteknisk dimensionering. För att kunna detta ska du Praktiskt använda
Grundläggningsteknik VGTN01 Kursprogram 2018 Allmänt Efter avslutad kurs ska du kunna genomföra och förstå vetenskapligt baserad geoteknisk dimensionering. För att kunna detta ska du Praktiskt använda
För godkänt resultat krävs 20 p och för väl godkänt krävs 30 p. Max poäng är 40 p
 Tentamen i kemi för Basåret, OKEOOl :2 den 20 april 2012 Skrivtid: 8.00-1300 Plats. 8132 Hjälpmedel: Räknare och tabell För godkänt resultat krävs 20 p och för väl godkänt krävs 30 p. Max poäng är 40 p
Tentamen i kemi för Basåret, OKEOOl :2 den 20 april 2012 Skrivtid: 8.00-1300 Plats. 8132 Hjälpmedel: Räknare och tabell För godkänt resultat krävs 20 p och för väl godkänt krävs 30 p. Max poäng är 40 p
Hållfasthetslära Z2, MME175 lp 3, 2005
 Hållfasthetslära Z2, MME175 lp 3, 2005 Examinator: Magnus Ekh (mekh@am.chalmers.se), tele: 7723479 Kurspoäng: 3 Kurslitteratur: "Grundläggande hållfasthetslära", Hans Lundh, KTH, Stockholm. "Exempelsamling
Hållfasthetslära Z2, MME175 lp 3, 2005 Examinator: Magnus Ekh (mekh@am.chalmers.se), tele: 7723479 Kurspoäng: 3 Kurslitteratur: "Grundläggande hållfasthetslära", Hans Lundh, KTH, Stockholm. "Exempelsamling
Tentamen i Kemi för miljö- och hälsoskyddsområdet: Allmän kemi och jämviktslära
 Umeå Universitet Kodnummer... Allmän kemi för miljö- och hälsoskyddsområdet Lärare: Olle Nygren och Roger Lindahl Tentamen i Kemi för miljö- och hälsoskyddsområdet: Allmän kemi och jämviktslära 29 november
Umeå Universitet Kodnummer... Allmän kemi för miljö- och hälsoskyddsområdet Lärare: Olle Nygren och Roger Lindahl Tentamen i Kemi för miljö- och hälsoskyddsområdet: Allmän kemi och jämviktslära 29 november
Grundläggningsteknik VGTN01
 Grundläggningsteknik VGTN01 Kursprogram 2019 Allmänt Efter avslutad kurs ska du kunna genomföra och förstå vetenskapligt baserad geoteknisk dimensionering. För att kunna detta ska du Praktiskt använda
Grundläggningsteknik VGTN01 Kursprogram 2019 Allmänt Efter avslutad kurs ska du kunna genomföra och förstå vetenskapligt baserad geoteknisk dimensionering. För att kunna detta ska du Praktiskt använda
Rättningstiden är i normalfall tre veckor, annars är det detta datum som gäller: Efter överenskommelse med studenterna är rättningstiden fem veckor.
 Kemi Bas A Provmoment: Tentamen Ladokkod: TX011X Tentamen ges för: Tbas, TNBas 7,5 högskolepoäng Namn: Personnummer: Tentamensdatum: 2012-10-22 Tid: 9:00-13:00 Hjälpmedel: papper, penna, radergummi kalkylator
Kemi Bas A Provmoment: Tentamen Ladokkod: TX011X Tentamen ges för: Tbas, TNBas 7,5 högskolepoäng Namn: Personnummer: Tentamensdatum: 2012-10-22 Tid: 9:00-13:00 Hjälpmedel: papper, penna, radergummi kalkylator
SYROR OCH BASER Atkins & Jones kap
 KEM A02 Allmän- och oorganisk kemi F3 SYROR OCH BASER Atkins & Jones kap 11.11-11.18 KEMA02 MJ 2012-11-13 1 ÖVERSIKT - Syror och baser grundläggande egenskaper - Svaga syror och baser - ph i lösningar
KEM A02 Allmän- och oorganisk kemi F3 SYROR OCH BASER Atkins & Jones kap 11.11-11.18 KEMA02 MJ 2012-11-13 1 ÖVERSIKT - Syror och baser grundläggande egenskaper - Svaga syror och baser - ph i lösningar
Skriv reaktionsformler som beskriver vad som bör hända för följande blandningar: lösning blandas med 50 ml 0,05 H 3 PO 4 lösning.
 Lösning till tentamen 95 för Grundläggande kemi hp Sid (5). a) Perklorsyra är en stark syra varför pk a värde saknas i SI Chem Data. Behövs inte heller för phberäkning eftersom HClO 4 H O ClO 4 H 3 O går
Lösning till tentamen 95 för Grundläggande kemi hp Sid (5). a) Perklorsyra är en stark syra varför pk a värde saknas i SI Chem Data. Behövs inte heller för phberäkning eftersom HClO 4 H O ClO 4 H 3 O går
HUSBYGGNADSTEKNIK ht Kursprogram
 LTH Ingenjörshögskolan i Helsingborg BYGGTEKNIK MED ARKITEKTUR HUSBYGGNADSTEKNIK ht2 2012 Kursprogram Lund 2012-08 Petter Wallentén ALLMÄNT Kursen ges under ht 2 för IBYA1. Kursomfattningen omfattar 6
LTH Ingenjörshögskolan i Helsingborg BYGGTEKNIK MED ARKITEKTUR HUSBYGGNADSTEKNIK ht2 2012 Kursprogram Lund 2012-08 Petter Wallentén ALLMÄNT Kursen ges under ht 2 för IBYA1. Kursomfattningen omfattar 6
Onsdag 5/9. 08:15 Matematik baskurs I. Lektion. N Hörsal N360 Introduktion. Algeriska uttryck och funktioner Gem Teknisk nat fakulteten 10:00
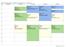 50501ht1, 5BX000,, 56503ht1, 5KX000,, +1 Kurstillfälle (3) v 36 Måndag 3/ Tisdag 4/ 0:30 Registrering, information Introduktionsföreläsning 0:30 Onsdag 5/ Introduktion. Algeriska uttryck och funktioner
50501ht1, 5BX000,, 56503ht1, 5KX000,, +1 Kurstillfälle (3) v 36 Måndag 3/ Tisdag 4/ 0:30 Registrering, information Introduktionsföreläsning 0:30 Onsdag 5/ Introduktion. Algeriska uttryck och funktioner
Kemisk jämvikt. Kap 3
 Kemisk jämvikt Kap 3 En reaktionsformel säger vilka ämnen som reagerar vilka som bildas samt förhållandena mellan ämnena En reaktionsformel säger inte hur mycket som reagerar/bildas Ingen reaktion ger
Kemisk jämvikt Kap 3 En reaktionsformel säger vilka ämnen som reagerar vilka som bildas samt förhållandena mellan ämnena En reaktionsformel säger inte hur mycket som reagerar/bildas Ingen reaktion ger
Kursprogram. Byggnadsmekanik VSMA05 HT 2017
 Byggnadsmekanik VMA05 HT 2017 Kursprogram Allmänt Kursen Byggnadsmekanik omfattar 8 hp och ges under läsperiod 2. Kursen syftar till att ge en introduktion till byggnadsmekanik tillämpad på konstruktionstyper
Byggnadsmekanik VMA05 HT 2017 Kursprogram Allmänt Kursen Byggnadsmekanik omfattar 8 hp och ges under läsperiod 2. Kursen syftar till att ge en introduktion till byggnadsmekanik tillämpad på konstruktionstyper
Lösningsförslag. Tentamen i KE1160 Termodynamik den 13 januari 2015 kl Ulf Gedde - Magnus Bergström - Per Alvfors
 Tentamen i KE1160 Termodynamik den 13 januari 2015 kl 08.00 14.00 Lösningsförslag Ulf Gedde - Magnus Bergström - Per Alvfors 1. (a) Joule- expansion ( fri expansion ) innebär att gas som är innesluten
Tentamen i KE1160 Termodynamik den 13 januari 2015 kl 08.00 14.00 Lösningsförslag Ulf Gedde - Magnus Bergström - Per Alvfors 1. (a) Joule- expansion ( fri expansion ) innebär att gas som är innesluten
Sura och basiska ämnen Syror och baser. Kap 5:1-5:3, (kap 9)
 Sura och basiska ämnen Syror och baser Kap 5:1-5:3, (kap 9) Syror / sura lösningar En sur lösning - har överskott på vätejoner, H + (protoner) En syra: - smakar surt - färgar BTB gult - reagerar med oädla
Sura och basiska ämnen Syror och baser Kap 5:1-5:3, (kap 9) Syror / sura lösningar En sur lösning - har överskott på vätejoner, H + (protoner) En syra: - smakar surt - färgar BTB gult - reagerar med oädla
Välkomna till kursen i elektroniska material! Martin Leijnse
 Välkomna till kursen i elektroniska material! Martin Leijnse Information Innehåll: fasta tillståndets fysik med fokus på halvledarfysik. Dioder, solceller, transistorer... Lärare: Martin Leijnse (föreläsare,
Välkomna till kursen i elektroniska material! Martin Leijnse Information Innehåll: fasta tillståndets fysik med fokus på halvledarfysik. Dioder, solceller, transistorer... Lärare: Martin Leijnse (föreläsare,
Välkomna till kursen i elektroniska material!
 Välkomna till kursen i elektroniska material! Information Innehåll: fasta tillståndets fysik med fokus på halvledarfysik. Dioder, solceller, transistorer... Lärare: Martin Leijnse (föreläsare, kursansvarig)
Välkomna till kursen i elektroniska material! Information Innehåll: fasta tillståndets fysik med fokus på halvledarfysik. Dioder, solceller, transistorer... Lärare: Martin Leijnse (föreläsare, kursansvarig)
Lösning till dugga för Grundläggande kemi Duggauppgifter enligt lottning; nr X, Y och Z.
 till dugga för Grundläggande kemi 2013-11-29 Duggauppgifter enligt lottning; nr X, Y och Z. 1. a) Ange kvalitativt buffertkapacitetens storlek (stor eller liten, med motivering, dock inga beräkningar)
till dugga för Grundläggande kemi 2013-11-29 Duggauppgifter enligt lottning; nr X, Y och Z. 1. a) Ange kvalitativt buffertkapacitetens storlek (stor eller liten, med motivering, dock inga beräkningar)
Teknisk modellering: Bärverksanalys VSMF05
 Teknisk modellering: Bärverksanalys VSMF05 Kursprogram 2015 Inledning Kursens syfte är att ge kunskaper om att välja fysikaliskt riktiga modeller samt att använda dessa för att lösa ingenjörsproblem.
Teknisk modellering: Bärverksanalys VSMF05 Kursprogram 2015 Inledning Kursens syfte är att ge kunskaper om att välja fysikaliskt riktiga modeller samt att använda dessa för att lösa ingenjörsproblem.
Lösningar till tentamen i Kemisk termodynamik
 Lösningar till tentamen i Kemisk termodynamik 203-0-9. Sambandet mellan tryck och temperatur för jämvikt mellan fast och gasformig HCN är givet enligt: ln(p/kpa) = 9, 489 4252, 4 medan kokpunktskurvan
Lösningar till tentamen i Kemisk termodynamik 203-0-9. Sambandet mellan tryck och temperatur för jämvikt mellan fast och gasformig HCN är givet enligt: ln(p/kpa) = 9, 489 4252, 4 medan kokpunktskurvan
VSMA05 Byggnadsmekanik - Kursprogram HT 2019
 VSMA05 Byggnadsmekanik - Kursprogram HT 2019 Allmänt Kursen Byggnadsmekanik omfattar 8 hp och ges under läsperiod 2. Kursen syftar till att ge en introduktion till byggnadsmekanik tillämpad på konstruktionstyper
VSMA05 Byggnadsmekanik - Kursprogram HT 2019 Allmänt Kursen Byggnadsmekanik omfattar 8 hp och ges under läsperiod 2. Kursen syftar till att ge en introduktion till byggnadsmekanik tillämpad på konstruktionstyper
Byggnadsmekanik, LTH MATERIAL, FORM OCH KRAFT
 Byggnadsmekanik, LTH MATERIAL, FORM OCH KRAFT KURSPROGRAM 2008 Material, form och kraft (VSM131, 9hp) Mål Målet med kursen är en fördjupad formförståelse; en förståelse om samspelet mellan material, form
Byggnadsmekanik, LTH MATERIAL, FORM OCH KRAFT KURSPROGRAM 2008 Material, form och kraft (VSM131, 9hp) Mål Målet med kursen är en fördjupad formförståelse; en förståelse om samspelet mellan material, form
KURSPROGRAM HT-10 MATEMATISK STATISTIK AK FÖR CDI, FMS 012
 LUNDS TEKNISKA HÖGSKOLA MATEMATIKCENTRUM MATEMATISK STATISTIK KURSPROGRAM HT-10 MATEMATISK STATISTIK AK FÖR CDI, FMS 012 Hemsida Kursens hemsida finns på http://www.maths.lth.se/matstat/kurser/fms012/
LUNDS TEKNISKA HÖGSKOLA MATEMATIKCENTRUM MATEMATISK STATISTIK KURSPROGRAM HT-10 MATEMATISK STATISTIK AK FÖR CDI, FMS 012 Hemsida Kursens hemsida finns på http://www.maths.lth.se/matstat/kurser/fms012/
Terminsplanering, för Biomedicinsk analytikerprogrammet 2013
 Umeå universitet, 901 87 Umeå Biomedicinsk laboratorievetenskap 2013-06-16 Terminsplanering Terminsansvarig: Viking Wikström Viking.wikstrom@climi.umu.se Terminsplanering, för Biomedicinsk analytikerprogrammet
Umeå universitet, 901 87 Umeå Biomedicinsk laboratorievetenskap 2013-06-16 Terminsplanering Terminsansvarig: Viking Wikström Viking.wikstrom@climi.umu.se Terminsplanering, för Biomedicinsk analytikerprogrammet
KEMA02 Oorganisk kemi grundkurs F3
 KEMA02 Oorganisk kemi grundkurs F3 Syror och baser Atkins & Jones kap 11.111.16 Översikt Syror och baser grundläggande egenskaper och begrepp Autoprotolys och ph Svaga syror och baser ph i lösningar av
KEMA02 Oorganisk kemi grundkurs F3 Syror och baser Atkins & Jones kap 11.111.16 Översikt Syror och baser grundläggande egenskaper och begrepp Autoprotolys och ph Svaga syror och baser ph i lösningar av
Tentamen i Termodynamik för K och B kl 8-13
 Tentamen i Termodynamik för K och B 081025 kl 8-13 Tillåtna hjälpmedel: Miniräknare (med tillhörande handbok), utdelat formelblad med tabellsamling. Slutsatser skall motiveras och beräkningar redovisas.
Tentamen i Termodynamik för K och B 081025 kl 8-13 Tillåtna hjälpmedel: Miniräknare (med tillhörande handbok), utdelat formelblad med tabellsamling. Slutsatser skall motiveras och beräkningar redovisas.
KOKA01 Läsanvisningar till läroboken, 6. upplagan, 2013
 KOKA01 Läsanvisningar till läroboken, 6. upplagan, 2013 Kapitel F A-C, E F kursivt (från fysik och gymnasium förväntas ni kunna: SI-enheter, energi, atomteori, molbegreppet, formelräkningar, omsättningar)
KOKA01 Läsanvisningar till läroboken, 6. upplagan, 2013 Kapitel F A-C, E F kursivt (från fysik och gymnasium förväntas ni kunna: SI-enheter, energi, atomteori, molbegreppet, formelräkningar, omsättningar)
Allmän Kemi 2 (NKEA04 m.fl.)
 Allmän Kemi (NKEA4 m.fl.) --4 Uppgift a) K c [NO] 4 [H O] 6 /([NH ] 4 [O ] 5 ) eller K p P(NO) 4 P(H O) 6 /(P(NH ) 4 P(O ) 5 ) Om kärlets volym minskar ökar trycket och då förskjuts jämvikten åt den sida
Allmän Kemi (NKEA4 m.fl.) --4 Uppgift a) K c [NO] 4 [H O] 6 /([NH ] 4 [O ] 5 ) eller K p P(NO) 4 P(H O) 6 /(P(NH ) 4 P(O ) 5 ) Om kärlets volym minskar ökar trycket och då förskjuts jämvikten åt den sida
Grundläggningsteknik VGTF01
 Grundläggningsteknik VGTF01 Kursprogram 2015 Allmänt Efter avslutad kurs ska du kunna genomföra och förstå vetenskapligt baserad geoteknisk dimensionering. För att kunna detta ska du Praktiskt använda
Grundläggningsteknik VGTF01 Kursprogram 2015 Allmänt Efter avslutad kurs ska du kunna genomföra och förstå vetenskapligt baserad geoteknisk dimensionering. För att kunna detta ska du Praktiskt använda
Prov i kemi kurs A. Atomens byggnad och periodiska systemet 2(7) Namn:... Hjälpmedel: räknedosa + tabellsamling
 Prov i kemi kurs A Namn:... Hjälpmedel: räknedosa + tabellsamling Lösningar och svar skall ges på särskilt inskrivningspapper för de uppgifter som är skrivna med kursiv stil. I övriga fall ges svaret och
Prov i kemi kurs A Namn:... Hjälpmedel: räknedosa + tabellsamling Lösningar och svar skall ges på särskilt inskrivningspapper för de uppgifter som är skrivna med kursiv stil. I övriga fall ges svaret och
KEMA02 Oorganisk kemi grundkurs F4
 KEMA02 Oorganisk kemi grundkurs F4 Jämvikt i lösning Atkins & Jones kap 11.17 11.19 & 12.1 12.7 Översikt kap 11.17 11.19 & 12.1 12.7 Fördelningsdiagram ph i utspädda lösningar Blandade lösningar och buffertar
KEMA02 Oorganisk kemi grundkurs F4 Jämvikt i lösning Atkins & Jones kap 11.17 11.19 & 12.1 12.7 Översikt kap 11.17 11.19 & 12.1 12.7 Fördelningsdiagram ph i utspädda lösningar Blandade lösningar och buffertar
Konc. i början 0.1M 0 0. Ändring -x +x +x. Konc. i jämvikt 0,10-x +x +x
 Lösning till tentamen 2013-02-28 för Grundläggande kemi 10 hp Sid 1(5) 1. CH 3 COO - (aq) + H 2 O (l) CH 3 COOH ( (aq) + OH - (aq) Konc. i början 0.1M 0 0 Ändring -x +x +x Konc. i jämvikt 0,10-x +x +x
Lösning till tentamen 2013-02-28 för Grundläggande kemi 10 hp Sid 1(5) 1. CH 3 COO - (aq) + H 2 O (l) CH 3 COOH ( (aq) + OH - (aq) Konc. i början 0.1M 0 0 Ändring -x +x +x Konc. i jämvikt 0,10-x +x +x
Allmän kemi. Programkurs 6.0 hp General Chemistry 8BKG13 Gäller från: 2018 HT. Fastställd av. Fastställandedatum
 DNR LIU-2017-02621 1(5) Allmän kemi Programkurs 6.0 hp General Chemistry 8BKG13 Gäller från: 2018 HT Fastställd av Utbildningsnämnden för grund- och avancerad nivå vid Medicinska fakulteten Fastställandedatum
DNR LIU-2017-02621 1(5) Allmän kemi Programkurs 6.0 hp General Chemistry 8BKG13 Gäller från: 2018 HT Fastställd av Utbildningsnämnden för grund- och avancerad nivå vid Medicinska fakulteten Fastställandedatum
KURSPROGRAM HT-18 MATEMATISK STATISTIK FÖR B, K, N, BME OCH KEMISTER, FMSF70 & MASB02
 LUNDS TEKNISKA HÖGSKOLA MATEMATIKCENTRUM MATEMATISK STATISTIK KURSPROGRAM HT-18 MATEMATISK STATISTIK FÖR B, K, N, BME OCH KEMISTER, FMSF70 & MASB02 Allmänt Kursen ger 7.5hp och omfattar 26 timmar föreläsning,
LUNDS TEKNISKA HÖGSKOLA MATEMATIKCENTRUM MATEMATISK STATISTIK KURSPROGRAM HT-18 MATEMATISK STATISTIK FÖR B, K, N, BME OCH KEMISTER, FMSF70 & MASB02 Allmänt Kursen ger 7.5hp och omfattar 26 timmar föreläsning,
Statistik och testmetodik
 Psykologiska institutionen Anvisningar och schema till delkursen Statistik och testmetodik 7,5 högskolepoäng 17 januari-9 mars 2011 Momentansvarig: Emma Bäck Schema Datum Tid Grupp Lokal Lärare Innehåll
Psykologiska institutionen Anvisningar och schema till delkursen Statistik och testmetodik 7,5 högskolepoäng 17 januari-9 mars 2011 Momentansvarig: Emma Bäck Schema Datum Tid Grupp Lokal Lärare Innehåll
Kemisk jämvikt. Kap 3
 Kemisk jämvikt Kap 3 Vilken info ger en reaktionsformel? En reaktionsformel säger - vilka ämnen som reagerar, - vilka som bildas - samt förhållandena mellan ämnena som reagerar/bildas En reaktionsformel
Kemisk jämvikt Kap 3 Vilken info ger en reaktionsformel? En reaktionsformel säger - vilka ämnen som reagerar, - vilka som bildas - samt förhållandena mellan ämnena som reagerar/bildas En reaktionsformel
Kap 8 Redox-reaktioner. Reduktion/Oxidation (elektrokemi)
 Kap 8 Redox-reaktioner Reduktion/Oxidation (elektrokemi) Zinkbleck (zinkplåt) i en kopparsulfatlösning Zn (s) + CuSO 4 (aq) Zn (s) + Cu 2+ (aq) + SO 4 2+ (aq) Vad händer? Magnesium brinner i luft Vad
Kap 8 Redox-reaktioner Reduktion/Oxidation (elektrokemi) Zinkbleck (zinkplåt) i en kopparsulfatlösning Zn (s) + CuSO 4 (aq) Zn (s) + Cu 2+ (aq) + SO 4 2+ (aq) Vad händer? Magnesium brinner i luft Vad
Linjär algebra och geometri 1
 UPPSALA UNIVERSITET MATEMATISKA INSTITUTIONEN Ryszard Rubinsztein Oswald Fogelklou Linjär algebra och geometri 1 för K1, W1, KandKe1 Höstterminen 2008 Kurslitteratur H.Anton, C.Rorres, Elementary Linear
UPPSALA UNIVERSITET MATEMATISKA INSTITUTIONEN Ryszard Rubinsztein Oswald Fogelklou Linjär algebra och geometri 1 för K1, W1, KandKe1 Höstterminen 2008 Kurslitteratur H.Anton, C.Rorres, Elementary Linear
Respektive skriftlig tentamen ges vid tre tillfällen, när kursmomentet slutar, cirka en månad därefter samt i nästföljande augusti.
 Bengt Ingvarsson Kursansvarig nuvarande kurs LFB367 LFB368 Campusträffar och tentamenstider HT 16: 29 augusti 13 januari 2017 VT 17: 16 januari 2 juni HT 17: 28 augusti 12 januari 2018 VT 18: 15 januari
Bengt Ingvarsson Kursansvarig nuvarande kurs LFB367 LFB368 Campusträffar och tentamenstider HT 16: 29 augusti 13 januari 2017 VT 17: 16 januari 2 juni HT 17: 28 augusti 12 januari 2018 VT 18: 15 januari
Grundläggningsteknik VGTF01
 Grundläggningsteknik VGTF01 Kursprogram 2014 Allmänt Efter avslutad kurs ska du kunna genomföra och förstå vetenskapligt baserad geoteknisk dimensionering. För att kunna detta ska du Praktiskt använda
Grundläggningsteknik VGTF01 Kursprogram 2014 Allmänt Efter avslutad kurs ska du kunna genomföra och förstå vetenskapligt baserad geoteknisk dimensionering. För att kunna detta ska du Praktiskt använda
PRÖVNINGSANVISNINGAR
 PRÖVNINGSANVISNINGAR Prövning i Matematik D Kurskod Ma 104 Gymnasiepoäng 100 Läromedel Prov Muntligt prov Inlämningsuppgift Kontakt med examinator Övrigt Valfri aktuell lärobok för kurs Matematik D t.ex.
PRÖVNINGSANVISNINGAR Prövning i Matematik D Kurskod Ma 104 Gymnasiepoäng 100 Läromedel Prov Muntligt prov Inlämningsuppgift Kontakt med examinator Övrigt Valfri aktuell lärobok för kurs Matematik D t.ex.
KEMISK TERMODYNAMIK. Lab 1, Datorlaboration APRIL 10, 2016
 KEMISK TERMODYNAMIK Lab 1, Datorlaboration APRIL 10, 2016 ALEXANDER TIVED 9405108813 Q2 ALEXANDER.TIVED@GMAIL.COM WILLIAM SJÖSTRÖM Q2 DKW.SJOSTROM@GMAIL.COM Innehållsförteckning Inledning... 2 Teori, bakgrund
KEMISK TERMODYNAMIK Lab 1, Datorlaboration APRIL 10, 2016 ALEXANDER TIVED 9405108813 Q2 ALEXANDER.TIVED@GMAIL.COM WILLIAM SJÖSTRÖM Q2 DKW.SJOSTROM@GMAIL.COM Innehållsförteckning Inledning... 2 Teori, bakgrund
FMS032: MATEMATISK STATISTIK AK FÖR V OCH L KURSPROGRAM HT 2015
 Lunds tekniska högskola Matematikcentrum Matematisk statistik FMS032: MATEMATISK STATISTIK AK FÖR V OCH L KURSPROGRAM HT 2015 HEMSIDA Kursens hemsida finns på http://www.maths.lth.se/matstat/kurser/fms032/
Lunds tekniska högskola Matematikcentrum Matematisk statistik FMS032: MATEMATISK STATISTIK AK FÖR V OCH L KURSPROGRAM HT 2015 HEMSIDA Kursens hemsida finns på http://www.maths.lth.se/matstat/kurser/fms032/
Teknisk modellering: Bärverksanalys VSMF05
 Teknisk modellering: Bärverksanalys VSMF05 Kursprogram 2017 Inledning Kursens syfte är att ge kunskaper om att välja fysikaliskt riktiga modeller samt att använda dessa för att lösa ingenjörsproblem.
Teknisk modellering: Bärverksanalys VSMF05 Kursprogram 2017 Inledning Kursens syfte är att ge kunskaper om att välja fysikaliskt riktiga modeller samt att använda dessa för att lösa ingenjörsproblem.
Kursplan. Kemi med didaktisk inriktning 2. Lärarutbildningsnämnden Kemi
 Dnr: KEGL02/20161 Lärarutbildningsnämnden Kemi Kursplan Kemi med didaktisk inriktning 2 Kurskod: KEGL02 Kursens benämning: Kemi med didaktisk inriktning 2 Chemistry and Chemistry Education 2 Högskolepoäng:
Dnr: KEGL02/20161 Lärarutbildningsnämnden Kemi Kursplan Kemi med didaktisk inriktning 2 Kurskod: KEGL02 Kursens benämning: Kemi med didaktisk inriktning 2 Chemistry and Chemistry Education 2 Högskolepoäng:
LTH Ingenjörshögskolan i Helsingborg BYGGTEKNIK MED ARKITEKTUR KURSPROGRAM IBYA2 VBF605 BYGGNADSFYSIK LP2 HT 2012
 LTH Ingenjörshögskolan i Helsingborg BYGGTEKNIK MED ARKITEKTUR KURSPROGRAM IBYA2 VBF605 BYGGNADSFYSIK LP2 HT 2012 Lund 2012 ALLMÄNT Kursen ges under läsperiod 2 för IBYA 2. Kursen omfattar 6 högskolepoäng
LTH Ingenjörshögskolan i Helsingborg BYGGTEKNIK MED ARKITEKTUR KURSPROGRAM IBYA2 VBF605 BYGGNADSFYSIK LP2 HT 2012 Lund 2012 ALLMÄNT Kursen ges under läsperiod 2 för IBYA 2. Kursen omfattar 6 högskolepoäng
Kemi 1 för basår. Programkurs 8 hp Chemistry 1 for Foundation Year BKL101 Gäller från: 2018 VT. Fastställd av. Fastställandedatum.
 1(9) Kemi 1 för basår Programkurs 8 hp Chemistry 1 for Foundation Year BKL101 Gäller från: 2018 VT Fastställd av Övrigt Fastställandedatum LINKÖPINGS UNIVERSITET 2(9) Huvudområde Övriga ämnen Utbildningsnivå
1(9) Kemi 1 för basår Programkurs 8 hp Chemistry 1 for Foundation Year BKL101 Gäller från: 2018 VT Fastställd av Övrigt Fastställandedatum LINKÖPINGS UNIVERSITET 2(9) Huvudområde Övriga ämnen Utbildningsnivå
Repetition F7. Lunds universitet / Naturvetenskapliga fakulteten / Kemiska institutionen / KEMA00
 Repetition F7 Intermolekylär växelverkan kortväga repulsion elektrostatisk växelverkan (attraktion och repulsion): jon-jon (långväga), jon-dipol, dipol-dipol medelvärdad attraktion (van der Waals): roterande
Repetition F7 Intermolekylär växelverkan kortväga repulsion elektrostatisk växelverkan (attraktion och repulsion): jon-jon (långväga), jon-dipol, dipol-dipol medelvärdad attraktion (van der Waals): roterande
Föreläsningarnas innehåll och motsvarande avsnitt i läroboken.
 Inledande kemi (18,5 hp) KZ2004 Kursen Inledande kemi består av två moment 1) Kemisk jämvikt 10 hp (teori 6,5 hp och laborationer 3,5 hp) och 2) Molekylstruktur 8,5 hp (teori 5 hp och laborationer 3,5
Inledande kemi (18,5 hp) KZ2004 Kursen Inledande kemi består av två moment 1) Kemisk jämvikt 10 hp (teori 6,5 hp och laborationer 3,5 hp) och 2) Molekylstruktur 8,5 hp (teori 5 hp och laborationer 3,5
Rättningstiden är i normalfall 15 arbetsdagar, annars är det detta datum som gäller:
 Kemi Bas 1 Provmoment: Ladokkod: Tentamen ges för: TentamensKod: Tentamen 40S01A KBAST och KBASX 7,5 högskolepoäng Tentamensdatum: 2016-10-27 Tid: 09:00-13:00 Hjälpmedel: papper, penna, radergummi, kalkylator
Kemi Bas 1 Provmoment: Ladokkod: Tentamen ges för: TentamensKod: Tentamen 40S01A KBAST och KBASX 7,5 högskolepoäng Tentamensdatum: 2016-10-27 Tid: 09:00-13:00 Hjälpmedel: papper, penna, radergummi, kalkylator
Kapitel 14. Syror och baser
 Kapitel 14 Syror och baser Kapitel 14 Innehåll 14.1 Syror och baser 14.2 Syrastyrka 14.3 ph-skalan 14.4 Beräkna ph för en stark syra 14.5 Beräkna ph för en svag syra 14.6 Baser 14.7 Flerprotoniga syror
Kapitel 14 Syror och baser Kapitel 14 Innehåll 14.1 Syror och baser 14.2 Syrastyrka 14.3 ph-skalan 14.4 Beräkna ph för en stark syra 14.5 Beräkna ph för en svag syra 14.6 Baser 14.7 Flerprotoniga syror
Institutionen för material- och miljökemi (MMK)
 2016/08/05 Institutionen för material- och miljökemi (MMK) Preliminärt schema HT2016 för kurser: Inledande kemi (18,5 hp; IK) Kemisk dataanalys (4 hp; KDA) Forskning, kommunikation och vetenskaplighet
2016/08/05 Institutionen för material- och miljökemi (MMK) Preliminärt schema HT2016 för kurser: Inledande kemi (18,5 hp; IK) Kemisk dataanalys (4 hp; KDA) Forskning, kommunikation och vetenskaplighet
Allmän kemi. Läromålen. Viktigt i kap 17. Kap 17 Termodynamik. Studenten skall efter att ha genomfört delkurs 1 kunna:
 Allmän kemi Kap 17 Termodynamik Läromålen Studenten skall efter att ha genomfört delkurs 1 kunna: n - använda de termodynamiska begreppen entalpi, entropi och Gibbs fria energi samt redogöra för energiomvandlingar
Allmän kemi Kap 17 Termodynamik Läromålen Studenten skall efter att ha genomfört delkurs 1 kunna: n - använda de termodynamiska begreppen entalpi, entropi och Gibbs fria energi samt redogöra för energiomvandlingar
5.10 Kemi. Mål för undervisningen
 5.10 Kemi Undervisningen i kemi ska hjälpa de studerande att utveckla ett naturvetenskapligt tänkande och en modern världsbild som en del av en mångsidig allmänbildning. Undervisningen ska ge de studerande
5.10 Kemi Undervisningen i kemi ska hjälpa de studerande att utveckla ett naturvetenskapligt tänkande och en modern världsbild som en del av en mångsidig allmänbildning. Undervisningen ska ge de studerande
utvecklar förståelse av sambandet mellan struktur, egenskaper och funktion hos kemiska ämnen samt varför kemiska reaktioner sker,
 Kemi Ämnets syfte Utbildningen i ämnet kemi syftar till fördjupad förståelse av kemiska processer och kunskap om kemins skiftande tillämpningar och betydelse inom vardagsliv, industri, medicin och livsmiljö.
Kemi Ämnets syfte Utbildningen i ämnet kemi syftar till fördjupad förståelse av kemiska processer och kunskap om kemins skiftande tillämpningar och betydelse inom vardagsliv, industri, medicin och livsmiljö.
Kursplan. Kemi med didaktisk inriktning 1. Lärarutbildningsnämnden Kemi
 Dnr: KEGL01/20162 Lärarutbildningsnämnden Kemi Kursplan Kemi med didaktisk inriktning 1 Kurskod: KEGL01 Kursens benämning: Kemi med didaktisk inriktning 1 Chemistry and Chemistry Education 1 Högskolepoäng:
Dnr: KEGL01/20162 Lärarutbildningsnämnden Kemi Kursplan Kemi med didaktisk inriktning 1 Kurskod: KEGL01 Kursens benämning: Kemi med didaktisk inriktning 1 Chemistry and Chemistry Education 1 Högskolepoäng:
KEMA02 Oorganisk kemi grundkurs F9
 KEMA02 Organisk kemi grundkurs F9 Elektrkemi Redxreaktiner ch Galvaniska er 1 Atkins & Jnes kap 13.1 13.5 Översikt kapitel 13.1 13.5 Redxreaktiner Halvreaktiner Balansering av redxreaktiner Galvaniska
KEMA02 Organisk kemi grundkurs F9 Elektrkemi Redxreaktiner ch Galvaniska er 1 Atkins & Jnes kap 13.1 13.5 Översikt kapitel 13.1 13.5 Redxreaktiner Halvreaktiner Balansering av redxreaktiner Galvaniska
GRUNDARBETEN I KEMI I
 GRUNDARBETEN I KEMI I ARBETSBESKRIVNING NAMN: INLÄMNAD: GODKÄND: 2 3 ARBETE I. GASBRÄNNARE OCH LÅGREAKTIONER Resultat Undersökt förening Lågans färg Uppgifter 1. Förklara kort varför lågorna har olika
GRUNDARBETEN I KEMI I ARBETSBESKRIVNING NAMN: INLÄMNAD: GODKÄND: 2 3 ARBETE I. GASBRÄNNARE OCH LÅGREAKTIONER Resultat Undersökt förening Lågans färg Uppgifter 1. Förklara kort varför lågorna har olika
