Joner, syror och baser
|
|
|
- Elisabeth Berglund
- för 9 år sedan
- Visningar:
Transkript
1 Joner, syror och baser
2 REPETITION ATOMER OCH MOLEKYLER Atomer är byggstenar Flera atomer som sitter ihop kallas en molekyl Exempel på atomer: O = syre, N = kväve Exempel på molekyler: O2 = syremolekyl, N2 = kvävemolekyl, CO2 = koldioxidmolekyl, H2O = vattenmolekyl Molekyler kan bestå av flera hundra atomer
3 FASER (g) = gas (l) = liquid = flytande (s) = solid = fast (aq) = aqueous = löst i vatten
4 ATOMENS BYGGNAD I en atom är det lika många protoner som elektroner alltså tar laddningarna ut varandra.! Kärna Positiva Protoner Neutrala Neutroner! Runt om Negativa Elektroner
5 ATOMENS UPPBYGGNAD Atomkärnan: Är gjord av protoner (p + ) och neutroner (n) Antalet protoner bestämmer vilket ämne det är!! 1 proton = väte, 2 protoner = helium, 3 protoner = litium. Antalet protoner står i periodiska systemet!! Elektronerna åker runt kärnan i olika skal Atomer har lika många p som e - Periodiska systemet- världens största fusklapp, antal protoner och antal valenselektroner
6 ELEKTRON-SKAL Bilden visar en atom där det röda i mitten är atomens kärna Elektronerna finns i olika skal, de kallas K, L och M skal I det innersta K-skalet får det plats 2 e - I nästa skal - L-skalet, får det plats 8 e - I nästa skal, M-skalet får det plats 18 e - Atomer gillar att det yttersta skalet är fullt Elektronerna i det yttersta skalet kallas valenselektroner
7 VARFÖR BLIR EN DEL ATOMER JONER??? För att förklara det måste vi först förstå hur atomer är uppbyggda Atomen är inte den minsta partikel som finns - atomer är uppbyggda av ännu mindre partiklar Dessa partiklar kallas protoner (förkortas p + ), neutroner (n) och elektroner (e - ). (I kemin bryr vi oss inte om neutronerna - de har att göra med om ämnen är radioaktiva eller inte) Protoner har laddning + (plus ett), därför skriver man p + Elektroner har laddning - (minus ett), därför skriver man e - Neutroner har ingen laddning alls - de är oladdade
8 VAD ÄR EN JON? En jon är en laddad atom eller molekyl Exempel på atomer: Na = natrium, Cl = klor Exempel på jon: Na + = natriumjon, Cl - = kloridjon Exempel på molekyl: NH3 = ammoniakmolekyl Exempel på sammansatta joner: NH4 + = ammoniumjon, OH - = hydroxidjon
9 Joner Ämnen kan vara uppbyggda av atomer. Men det finns även en annan sorts byggsten - joner. Skillnaden är att en atom har lika många elektroner och protoner, men en jon har olika många.! Ibland kan en atom lämna ifrån sig eller ta upp en elektron. Då får atomen olika många elektroner och protoner och blir en jon.! En atom som lämnar ifrån sig elektroner blir en positiv jon. För att få namnet på en positiv jon lägger man till -jon till grundämnets namn. Väteatomer bildar positiva joner som heter vätejoner.! När en atom tar upp elektroner får den fler minusladdningar än plusladdningar. Den blir en negativ jon. För att få namnet på en negativ jon skjuter man till ändelsen -id före -jon t ex kloridjon.!
10 Positiva joner bildas när elektroner avges en Hur bildas joner? Om man låter metallen natrium reagera med icke-metallen klor, bil das ett vitt ämne som smakar salt. Energi frigörs som värme och ljus. Det vita ämnet är koksalt kemisk förening av positiva natriurn joner och negativa kloridjoner (se s 78). Vad är det som händer? När atomerna kolliderar, flyttar elektroner över från natriurnatomer till kloratomer. Elektriskt laddade joner bildas. Jonernas laddningar gör att de binds hårt till varandra i saltkristaller. Uppgift J 4 5 Positiva joner bildas när elektroner avges Alla metaller har få valenselektroner. Natriumatomen har bara en. Om den blir av med den yttersta elektronen till en annan atom, har den åtta elektroner i skalet inunder, dvs ädelgasstruktur. Eftersom en så dan struktur är stabil, avger natrium och andra metaller gärna sina va lenselektroner till andra ämnen. Då bildas positiva joner. Sd bildas joner med en plusladdning Natrium tillhör grupp 1 i det periodiska systemet. Natrium är en metall, vars atomer har en elekt ron i yttersta skalet. Om natriumatomen gör sig av med sin valens elektron, får den ett fullt ytterskal. Men när en elektron har försvunnit från atomen är den inte längre elektriskt neutral. Den har fler protoner än elektroner. Eftersom en elektron försvann är överskottet en plusladdning. Det har uppstått en laddad partikel, en jon. 1 det här fallet ärjonen en positiv natriurnjon med en plusladdning. Den skrivs så här: Na. På samma sätt kan en litiumatorn omvandlas till en litiumjon, Li. Sd bildas joner med flera plusladdningar Grundämnena i grupp 2 har två valenselektro ner. De uppnår ädelgasstruktur genom att avge dessa. Det bildas joner med laddningen 2+. På motsvarande sätt bildar metallerna i grupp 3 joner med laddningen 3+ genom att avge sina tre elektroner. Aluminium hör till grupp 3. När aluminiumatomen omvandlas till aluminium jon avges alla detre elektronerna i det yttersta skalet. Aluminiumjonen får j onladdningen 3+. Även andra metaller har få valenselektroner. De bildar därför positiva joner. O :11+, 12+ O 1 avges avges avges Natriumatom, Na atomnummer 11 elektroner 11 protoner 11 + laddning Natriumjon, Na elektroner 1 protoner 11 laddning 1 + Magnesiumatom, Mg atomnummer 12 elektroner 12 protoner 12 + laddning 2 Magnesiumjon, Mg elektroner 1 protoner 12 + laddning 2 +
11 Negativa joner bildas när elektroner tas upp 1 egativa joner bildas när elektroner tas upp rundämnefla till höger i det periodiska systemet (icke-metallerna) ar många elektroner i sitt yttersta skal. Genom att ta upp elektroner an de få detta fyllt. Med åtta elektroner i yttersta skalet har även des a ämnen nått ädelgasstruktur. Icke-metallerna får då ett överskott av.lektroner och bildar negativa joner. Så bildas joner med en minusladdning Icke-metallerfla i grupp 17 i det periodiska sys temet har sju elektroner i sitt yttersta skal. Ge nom att fånga in en elektron, kan dessa ämnen få ett fullt elektronskal. Det bildas joner med laddningen 1. Fluoratom, F 1 tas upp atomnummer 9 elektroner 9 protoner 9 + laddning Fluoridjon, F eektroner 1 protoner 9 + laddning 1 Så bildas joner med två minusladdningar Icke-metallerna i grupp 16 har sex valenselekt roner. För att få ädelgasstruktur behöver ato merna ta upp två elektroner. Det bildas då joner med laddningen 2. Syreatom, atomnummer 8 elektroner 8 OG tas upp protoner 8 + laddning Oxidjon, &ektroner 1 protoner 8 + laddning 2 Oxidation och reduktion Vi har tidigare nämnt att metaller oxideras elektrongivare och en elektronmottagare. xiär de reagerar med syre. Ordet oxidation Man kallar ett sådant par för ett redoxpai; och används mer allmänt för att beskriva att den kemiska reaktionen mellan dem kallas elektroner avges. Motsatsen, att elektroner en redoxreaktion. tas upp, kallas reduktion. Hur kan atomerna i exemplen ovan kombine För att joner ska bildas så som beskrivits ras till olika redoxpar? Hur många atomer av var här ovan, måste det ske både en oxidation je sort behövs för att alla ska få ädelgasstruktur? och en reduktion. Det måste finnas både en 14
12 Vilken laddning har följande ämnen som joner samt var heter dem? Beryllium! Klor! Syre
13 Sammansatta joner - molekyler med laddning Det är inte bara enstaka atomer som kan lämna bort eller ta upp elektroner. Det kan också bildas joner genom att en hel molekyl tar upp eller lämnar bort elektroner och blir elektriskt laddad. Den sortens joner kallas för sammansatta joner.! En av de enklaste sammansatta jonerna är hydroxidjonen, OH-. Den består av en syreatom och en väteatom som har tagit upp en extra elektron tillsammans.! I en molekyl är det lika många elektroner som protoner, den är oladdad. Men i en sammansatt jon är protonerna och elektronerna olika många, och den har därför laddning.
14 Hur bildas jonföreningar? Om Här Nu Oj, Vänta Du, har vad jag jag nu! jag trist bara du börjar fullt! livet kunde känna är bli Jippi mig av!!! med lite attraherad en elektron av dig Det Om Vänta Nu Tack! och har tycker jag nu! jag jag bara av jag fullt kunde dig med! Jippi få en!!! elektron Natriumflourid Na + - F
15 Hur bildas jonföreningar? När natrium reagerar med klor, flyttar elektroner från natrium- till klor atornerna, så att båda atomslagen omvandlas till joner: Natriumatomen avger sin enda valenselektron till kloratomen. Tv joner med stabil ädelgasstruktur bildas. + o o o o o o / e\ Q Q Q 17+ natriumatom kloratom natriumjon kloridjon Natrium och klor passar ihop och reagerar gärna med varandra. Natrium oxideras, dvs avger en elektron, och klor reduceras, dvs tar upp en elektron. Jonerna som bildas ordnar sig till saltkristaller. Efter den kemiska reaktionen är tillståndet mycket mer stabilt än det var före reaktionen. Produkten, jonföreningen natriumkiorid, inne håller mindre energi än natrium och klor. En del av den kemiska energin omvandlas vid reaktionen till värme och ljus (jfr s 117). Både natrium och klorgas är ämnen som man inte gärna handskas med utan skyddsutrustning. Men om en elektron i varje natriumatom flyttar över till varsin kloratorn förenas de alltså till helt ofarligt salt! Vid reaktionen ovan går det åt lika många natriumatomer som kloratomer. Vad händer om klor i stället reagerar med magnesium, som har två valenselektroner? Jo, då behövs det dubbelt så många kloratomer som magnesiumatomer för att det ska gå jämnt ut. Salter hålls samman av jonbindning Alla kemiska föreningar som består av joner kallas saker. De bildar kris taller, som håller ihop genom att joner med olika laddningar dras till varandra. Plusjoner dras alltså till minusjoner. Bindningen mellan jo nerna kallas jonbindning. Den är mycket stark, och salter har därför ofta mycket hög smältpunkt. En saltkristall innehåller lika många positiva som negativa jon Iaddningar. 1 koksalt (natriumkiorid) vägs en plusladdning hos natri umjonen, Na, upp av en minusladdning hos kloridjonen, Cl. När en koksaltkristall byggs upp, kommer det därför att finnas lika många na triumjoner som kloridjoner. Saltets formel, NaC1, visar bara just det ta. Saltet magnesiumklorid byggs upp av dubbelt så många kloridjoner som magnesiumjoner och skrivs MgC1 Formeln för ett salt anger inte en avgränsad atomgrupp på samma sätt som formeln för en molekylförening. Att saltkristallen är uppbyggd av enskilda, elektriskt laddade joner framgår inte av formeln. Den an ger bara proportionerna mellan de atomsiag som ingår Modell av en koksaltkristall. Lägg märke till hur tält packade jonerna ligger i kristallen. Vad håller samman koksaltkristallen? 15
16 Salter När vi pratar om salt tänker vi oftast på koksalt som vi har till maten. Men det finns många andra salter t ex gips, salmiak, marmor.! Alla salter är fasta kristaller vid rumstemperatur. De kan ha olika färger beroende på vilka mineraler som finns i saltet. Artists palette i Death valley 2PLUOJ)j!pWfl!,N =1 4QuP5uuJJaduJni 1)j =1 IlesNoN = V w;jnsieddo = :iabisj P)fflO ebuew eq uej iajeg
17 När syra och bas möts bildas salt Ett salt kan bildas genom att man blandar en syra och en bas t ex om man blandar saltsyra (HCl) och natriumhydroxid (NaOH).! Då slår de farliga väte- och hydroxidjonerna sig samman till ofarliga vattenmolekyler och lösningen blir neutral. Man säger att syran och basen har neutraliserat varandra. Reaktionen kallas för neutralisation.! Kvar i lösningen finns det natrium- och kloridjoner som slås ihop. När vattnet avdunstar blidas kristaller av natriumklorid (koksalt)!
18 Koksalt från saltvatten och gruvor Man kan även utvinna koksalt ur havsvatten som får avdunsta. Man utnyttjar även naturliga saltsjöar (Döda Havet, 33 %).! Det finns även bergssalt - avlagringar av koksalt nere i marken som kan utvinnas genom gruvbrytning eller att man borrar en brunn och pumpar ner vatten, som löser upp saltet och tar med det upp till markytan.! Filmer om salt:
19 Syror Väteatom, en vätejon bildas när väteatomen blir av med sin elektron. Det som är kvar är atomens kärna, en positivt laddad proton. Syror är sura, men vad är motsatsen? Sött? Nej inte när det kommer till kemi då pratar vi om surt och basiskt istället. Men syror är sura, de har ett lägre ph än 7.! Ju fler vätejoner H+, desto surare lösning och lägre ph.! Hur sur en lösning är beror på dels koncentrationen hur mycket syra den innehåller dels hur stark syran är.! Syror är frätande och desto mer koncentrerad en syra är desto mer fräter den.
20 Baser Hydroxidjon, det är en sammansatt jon där atomerna i! molekylen delar på elektronerna. En hydroxidjon! kan uppkomma genom att en syreatom och en! väteatom tillsammans tagit upp en extra elektron. Baser har ett högre ph än 7.! Baser innehåller många hydroxidjoner OH.! Baser kan man känna igen genom att fingrarna känns hala om man gnider en bas mellan dem. T ex tvål och diskmedel. Annars är det ganska svårt att känna igen en bas, de smakar inte, syror kan man relatera till de smakar surt.! Baser är liksom syror frätande. H H H H HH H H
21 ph Indikator - ett ämne som ändrar färg efter surhetsgraden, antalet vätejoner.! Syror och baser har olika ph. Syror har ett ph under 7. Baser ett ph över 7. ph 7 är neutralt, varken surt eller basiskt. Genom att bland syror och baser kan man göra det sura mer basiskt och det basiska mer surt. Genom att blanda syror och baser kan man neutralisera dem.! Olika typer av ph-indikatorer;! Naturliga indikatorer- rödbetor, rödkål, blåbär och mest känd lackmus (en lav). Lackmus är violett när den visar neutral lösning, röd vid sur och blå vid basisk lösning.! ph-papper -universalindikator blandning av flera indikatorer! BTB (bromtymolblått) & Fenolftalein (visar endast på basisk lösning) - konstgjorda indikatorer
22 Syror, vad används de till, hur verkar de?!! Arbeta med din parkompis med att ta reda på information om nedanstående syror. Myrsyra! Ättiksyra! Oxalsyra! Citronsyra! Salicylsyra! Askorbinsyra! Mjölksyra! Efter arbetet med syrorna arbeta vidare med följande frågor:! - Vad är en syra?!! - Nämn en svag syra.!! - Förklara så bra ni kan vad som har! gjort att bägarna ändrat färg?! Vad har hänt? Börja med den! vänstra bägaren.!! - Vad står bokstäverna i SIV-regeln för?!! - Vad menas med SIV-regeln?!! -Vad är den kemiska beteckningen för saltsyra, salpetersyra, svavelsyra samt kolsyra?!! -Repetera alla farosymboler.!
23 Syror avger vätejoner Saltsyra HCl: Magens bakteriefälla, starkt frätande och har en stickande lukt. Vår magsaft innehåller saltsyra, den dödar bakterier och bryter ner vår mat. Används till: framställning av plaster och färgämnen.! Svavelsyra H 2 SO 4 : Tjockflytande och starkt frätande, luktfri. Svavelsyra används bland annat i konstgödsel, sprängämnen och bilbatterier. I bilbatterier är den koncentrerad så var försiktiga!! Salpetersyra HNO 3 : Starkt frätande med stickande lukt. Den gulfärgar hud och naglar. Den är starkt frätande och fräter på alla metaller utom guld och platina. Används till konstgödsel och sprängämnen.! Kolsyra H 2 CO 3 : Är en svag syra som bildar koldioxid då den löser sig i vatten. Används till läsk.
24 Syror-önskade och oönskade resultat! Används i skönhetsindustrin för att göra huden slätare ta bort rynkor, acneärr mm. Vissa syror likt glycolsyra verkar på djupet, mjölksyra tar bort döda hudceller och ger huden fukt. Vill man ge huden en liten snabbkick prova t ex att lägga en papayamask. Ta fruktköttet och lägg på huden, stramar upp och löser upp pormaskar. Det är syrorna i frukten som hjälper till med detta.! Tyvärr har syror under de senaste åren börjat användas som vapen mot kvinnor. Blir en man på något sätt missnöjd, svartsjuk, avundsjuk med sin fru eller flickvän, dotter, svärdotter, mamma, kastar han själv eller någon anlitad person syra i ansiktet för att förstöra kvinnans framtid. Hon är märkt förevigt. I fattigare länder finns inte den teknik och resurser som rikare länder har, många får ingen hjälp alls.!
25 Baser- plockar upp vätejoner Natriumhydroxid NaOH (Stark bas) Vitt fast ämne som lätt löser sig i vatten och bildar joner. Används till tillverkning av pappersmassa, tvål mm. I handeln säljs natriumhydroxid under namnet kaustik soda. Kaustik soda är mycket frätande och hälls i avlopp om det är stopp. Den förvandlar fettet i propparna till tvål. Fettet har fungerat som klister i propparna. Det kallas natronlut när NaOH löst sig i vatten.! Kaliumhydroxid KOH (stark bas): Vitt fast ämne som lätt löser sig i vatten. Är den löst i vatten kallas den ibland för kalilut. Används vid framställning av såpa.
26 forts baser Kalciumhydroxid Ca(OH)2 (Stark bas): Är ett vitt svårlösligt ämne. Kalciumhydroxid löst i vatten kallas kalkvatten. Kalciumhydroxid(även kallad släckt kalk) används bla vid tillverkning av socker. Det ingår också i murbruk. I murbruksblandningen tar kalciumhydroxiden upp koldioxid från luften, CO 2, och förvandlas till krita vilket gör att bruket hårdnar.! Natriumkarbonat Na2 CO 3 (mellanstark bas) Kallas också soda. Löser sig lätt i vatten. Natriumkarbonat har inga egna OH - (hydroxidjoner) så den rycker åt sig H + (vätejoner) från vattnet så att den kan bilda OH - joner. Soda används till olika typer av tvätt, eftersom den löser upp smuts och tar bort hårda kalksalter i vatten och gör det mjukt. Den används främst inom glastillverkning där den blandas med sand och utsätts för hög värme.!
27 forts baser Ammoniak NH3 (mellanstark bas): Är en färglös gas med stickande lukt. Löser sig lätt i vatten. Den används för tillverkning av handelsgödsel och salpetersyra. Ni som har bakat med hjorthornssalt någon gång har känt den speciella lukten av ammoniak. Har man känt den en gång känner man igen den för resten av livet. Mums, drömkakor!
28 Frågor att arbeta med kring baser Vad finns det för baser som du kan träffa på till vardags eller i hemmet?! Ibland säger man att hydroxidjonen (OH- ) är en trasig vattenmolekyl, vad tror du att man menar med det?! Vad är skillnaden mellan en svag respektive stark bas?! Lutfisk äter vi i jultider men hur tillverkas den?! Vad menas med hårt respektive mjukt vatten? Hur ser vattnet ut på Värmdö är det hårt eller mjukt? Är det någon skillnad beroende på var man bor?
29 Vad betyder formlerna?! 3 H! O2! 2 H2 O! CO2! Hur skriver man 3 kväveatomer och två kolmonoxidmolekyler?
30 Reaktionsformler För att beskriva en kemisk reaktion kan vi skriva en reaktionsformel. Först skriver vi vad det finns för ämnen från början. Sedan ritar vi en pil som visar att det blir en kemisk reaktion. Efter pilen skriver vi formlerna för de ämnen som bildas vid reaktionen.! H2 + O 2 H 2 O! När man skrivit en reaktionsformel ska man alltid kontrollera att det finns lika många atomer före som efter pilen. Inga atomer kan försvinna och inga kan nybildas. Formeln måste balanseras.! 2 H2 + O 2 2 H 2 O
31 Exempel reaktionsformler - hur ska vi balansera dem? C + O2 CO 2! N2 + H 2 NH 3! S + O2 SO 2! Na + Cl 2 NaCl! Cu2 O + O 2 CuO
32 Formelfrossa Sätt ut rätt siffror. 1. Cu +.I 2 CuI 2. Zn +. Cl 2. ZnCl 2 3. Al +. S.Al 2 S 3 4. Fe +. Cl 2. Fe Cl 3 5. Ca +. S +.. O 2 CaSO 4 6. K +.N 2 +. O 2.. KNO H 2 +. Cl 2... HCl 8. C +.H 2.C 2 H 6 9. O 2 +.H 2.H 2 O 1. C +.H 2.C 2 H C +.H 2 +. O 2.C 2 H 5 OH Fantasin tog slut - nu tar jag X & Q 12.. X 2 +.Q XQ 13. X +. Q 4 XQ 14. X 2 +.Q 2. XQ X +. Q 3... X 2 Q 3 Göran Stenman, Ursviksskolan 6-9, Ursviken
33 Utmaningar... C6 H 12 O 6 CH 4 + CO 2! CO2 + C 2 H 6 O C 6 H 12 O 6
34 SURT REGN Allt regn är surt, eftersom luftens koldioxid (CO2) löser sig i vatten och då bildas kolsyra (H2CO3) CO2(g) + H2O(l) ---> H2CO3(aq) Gaser som svaveloxider (SOx) och kväveoxider (NOx) gör att regnet blir ännu surare. Detta kallas surt regn. Surt regn kan göra att träd dör.
Joner, syror och baser
 Joner, syror och baser REPETITION ATOMER OCH MOLEKYLER Atomer är byggstenar Flera atomer som sitter ihop kallas en molekyl Exempel på atomer: O = syre, N = kväve Exempel på molekyler: O2 = syremolekyl,
Joner, syror och baser REPETITION ATOMER OCH MOLEKYLER Atomer är byggstenar Flera atomer som sitter ihop kallas en molekyl Exempel på atomer: O = syre, N = kväve Exempel på molekyler: O2 = syremolekyl,
Joner, syror och baser
 Joner, syror och baser Vad kan vi hitta för information i det periodiska systemet? REPETITION Atomer och molekyler Atomer är byggstenar Flera atomer som sitter ihop kallas en molekyl Exempel på atomer:
Joner, syror och baser Vad kan vi hitta för information i det periodiska systemet? REPETITION Atomer och molekyler Atomer är byggstenar Flera atomer som sitter ihop kallas en molekyl Exempel på atomer:
Joner Syror och baser 2 Salter. Kemi direkt sid. 162-175
 Joner Syror och baser 2 Salter Kemi direkt sid. 162-175 Efter att du läst sidorna ska du kunna: Joner Förklara skillnaden mellan en atom och en jon. Beskriva hur en jon bildas och ge exempel på vanliga
Joner Syror och baser 2 Salter Kemi direkt sid. 162-175 Efter att du läst sidorna ska du kunna: Joner Förklara skillnaden mellan en atom och en jon. Beskriva hur en jon bildas och ge exempel på vanliga
Göran Stenman. Syror och Baser. Göran Stenman, Ursviksskolan 6-9, Ursviken
 Göran Stenman Syror och Baser Göran Stenman, Ursviksskolan 6-9, Ursviken www.lektion.se Syror och baser är frätande, det viktigaste att komma ihåg då vi laborerar är.. Skyddsglasögon Göran Göran Stenman
Göran Stenman Syror och Baser Göran Stenman, Ursviksskolan 6-9, Ursviken www.lektion.se Syror och baser är frätande, det viktigaste att komma ihåg då vi laborerar är.. Skyddsglasögon Göran Göran Stenman
Syror, baser och jonföreningar
 Syror, baser och jonföreningar Joner är laddade byggstenar I en atom är antalet elektroner det samma som antalet protoner i kärnan. En jon är en atom som lämnat ifrån sig eller tagit upp en eller flera
Syror, baser och jonföreningar Joner är laddade byggstenar I en atom är antalet elektroner det samma som antalet protoner i kärnan. En jon är en atom som lämnat ifrån sig eller tagit upp en eller flera
Lösningar kan vara sura, neutrala eller basiska Gemensamt för sura och basiska ämnen är att de är frätande.
 Syror och baser Lösningar Lösningar kan vara sura, neutrala eller basiska Gemensamt för sura och basiska ämnen är att de är frätande. Om man blandar en syra och en bas kan man få det att bli neutralt.
Syror och baser Lösningar Lösningar kan vara sura, neutrala eller basiska Gemensamt för sura och basiska ämnen är att de är frätande. Om man blandar en syra och en bas kan man få det att bli neutralt.
Här växer människor och kunskap
 Syror och baser 2 - Elektron, -1 - Protoner, +1 Natrium (Na) Valenselektron 1 st Elektronskal 3st 3 Natrium Neon 11 10 Alla ämnen vill ha fullt ytterskal. Så Na försöker efterlikna Ne. 4 Denna elektron
Syror och baser 2 - Elektron, -1 - Protoner, +1 Natrium (Na) Valenselektron 1 st Elektronskal 3st 3 Natrium Neon 11 10 Alla ämnen vill ha fullt ytterskal. Så Na försöker efterlikna Ne. 4 Denna elektron
Kemi. Fysik, läran om krafterna, energi, väderfenomen, hur alstras elektrisk ström mm.
 Kemi Inom no ämnena ingår tre ämnen, kemi, fysik och biologi. Kemin, läran om ämnena, vad de innehåller, hur de tillverkas mm. Fysik, läran om krafterna, energi, väderfenomen, hur alstras elektrisk ström
Kemi Inom no ämnena ingår tre ämnen, kemi, fysik och biologi. Kemin, läran om ämnena, vad de innehåller, hur de tillverkas mm. Fysik, läran om krafterna, energi, väderfenomen, hur alstras elektrisk ström
Syror och baser. Syror kan ge otäcka frätskador och kan även lösa upp metaller. Därför har flaskor med syra ofta varningssymbolen "varning frätande".
 Syror och baser En syra är ämne som lämnar eller kan lämna ifrån sig en vätejon (H + ). Detta gör att det finns fria vätejoner i lösningen. Lösningen blir därmed sur. En stark syra lämnar alltid ifrån
Syror och baser En syra är ämne som lämnar eller kan lämna ifrån sig en vätejon (H + ). Detta gör att det finns fria vätejoner i lösningen. Lösningen blir därmed sur. En stark syra lämnar alltid ifrån
Periodiska systemet. Atomens delar och kemiska bindningar
 Periodiska systemet Atomens delar och kemiska bindningar Atomens delar I mitten av atomen finns atomkärnan där protonerna finns. Protoner är positivt laddade partiklar Det är antalet protoner som avgör
Periodiska systemet Atomens delar och kemiska bindningar Atomens delar I mitten av atomen finns atomkärnan där protonerna finns. Protoner är positivt laddade partiklar Det är antalet protoner som avgör
Atomen och periodiska systemet
 Atomen och periodiska systemet Ringa in rätt svar 1. Exempel på elementarpartiklar är: joner protoner molekyler atomer elektroner 2. Atomen i sin helhet är: elektriskt neutral positivt laddad negativt
Atomen och periodiska systemet Ringa in rätt svar 1. Exempel på elementarpartiklar är: joner protoner molekyler atomer elektroner 2. Atomen i sin helhet är: elektriskt neutral positivt laddad negativt
Jonföreningar och jonbindningar del 1. Niklas Dahrén
 Jonföreningar och jonbindningar del 1 Niklas Dahrén Innehåll Del 1: o Hur jonföreningar bildas/framställs. o Hur jonföreningar är uppbyggda (kristallstruktur). o Jonbindning. o Hur atomernas radie påverkas
Jonföreningar och jonbindningar del 1 Niklas Dahrén Innehåll Del 1: o Hur jonföreningar bildas/framställs. o Hur jonföreningar är uppbyggda (kristallstruktur). o Jonbindning. o Hur atomernas radie påverkas
Periodiska systemet. Namn:
 Periodiska systemet Namn: Planering Vecka Aktivitet Viktigt 4 Repetition kemiska begrepp 5 Repetition kemiska begrepp + Periodiska systemet 6 Periodiska systemet + balansering av formler 7 Repetition +
Periodiska systemet Namn: Planering Vecka Aktivitet Viktigt 4 Repetition kemiska begrepp 5 Repetition kemiska begrepp + Periodiska systemet 6 Periodiska systemet + balansering av formler 7 Repetition +
ATOMENS BYGGNAD. En atom består av : Kärna ( hela massan finns i kärnan) Positiva Protoner Neutrala Neutroner. Runt om Negativa Elektroner
 periodiska systemet ATOMENS BYGGNAD En atom består av : Kärna ( hela massan finns i kärnan) Positiva Protoner Neutrala Neutroner Runt om Negativa Elektroner En Elektron har en negativt laddning. Och elektronerna
periodiska systemet ATOMENS BYGGNAD En atom består av : Kärna ( hela massan finns i kärnan) Positiva Protoner Neutrala Neutroner Runt om Negativa Elektroner En Elektron har en negativt laddning. Och elektronerna
Syror är en grupp av ämnen med en gemensam egenskap de är sura.
 FACIT TILL TESTA DIG SJÄLV TESTA DIG SJÄLV 4.1 syra Syror är en grupp av ämnen med en gemensam egenskap de är sura. bas Baser är ämnen som kan ta bort det sura från syror. neutral lösning En neutral lösning
FACIT TILL TESTA DIG SJÄLV TESTA DIG SJÄLV 4.1 syra Syror är en grupp av ämnen med en gemensam egenskap de är sura. bas Baser är ämnen som kan ta bort det sura från syror. neutral lösning En neutral lösning
Syror, baser och ph-värde. Niklas Dahrén
 Syror, baser och ph-värde Niklas Dahrén Syror är protongivare Syror kännetecknas av följande: 1. De har förmåga att avge vätejoner, H + (protoner), vilket leder till en ph-sänkning. 2. De ger upphov till
Syror, baser och ph-värde Niklas Dahrén Syror är protongivare Syror kännetecknas av följande: 1. De har förmåga att avge vätejoner, H + (protoner), vilket leder till en ph-sänkning. 2. De ger upphov till
Labbrapport 1 Kemilaboration ämnens uppbyggnad, egenskaper och reaktioner. Naturkunskap B Hösten 2007 Av Tommy Jansson
 Labbrapport 1 Kemilaboration ämnens uppbyggnad, egenskaper och reaktioner. Naturkunskap B Hösten 2007 Av Tommy Jansson Försök 1: Beskriv ämnet magnesium: Magnesium är ett grundämne (nummer 12 i det periodiska
Labbrapport 1 Kemilaboration ämnens uppbyggnad, egenskaper och reaktioner. Naturkunskap B Hösten 2007 Av Tommy Jansson Försök 1: Beskriv ämnet magnesium: Magnesium är ett grundämne (nummer 12 i det periodiska
KEMI 2H 2 + O 2. Fakta och övningar om atomens byggnad, periodiska systemet och formelskrivning
 KEMI Ämnen och reaktioner 1+ 1+ 9+ Be 2+ O 2 2 2 + O 2 2 2 O Fakta och övningar om atomens byggnad, periodiska systemet och formelskrivning Bertram Stenlund Fridell This w ork is licensed under the Creative
KEMI Ämnen och reaktioner 1+ 1+ 9+ Be 2+ O 2 2 2 + O 2 2 2 O Fakta och övningar om atomens byggnad, periodiska systemet och formelskrivning Bertram Stenlund Fridell This w ork is licensed under the Creative
Kemi. Fysik, läran om krafterna, energi, väderfenomen, hur alstras elektrisk ström mm.
 Kemi Inom no ämnena ingår tre ämnen, kemi, fysik och biologi. Kemin, läran om ämnena, vad de innehåller, hur de tillverkas mm. Fysik, läran om krafterna, energi, väderfenomen, hur alstras elektrisk ström
Kemi Inom no ämnena ingår tre ämnen, kemi, fysik och biologi. Kemin, läran om ämnena, vad de innehåller, hur de tillverkas mm. Fysik, läran om krafterna, energi, väderfenomen, hur alstras elektrisk ström
Indikator BTB. lösning
 Sura, neutrala och basiska Lösningar Sura ar smakar surt vilket du själv har märkt då du ätit syrliga karameller eller smakat på saften från en citron. Motsatsen till sura ar är basiska ar. Man skulle
Sura, neutrala och basiska Lösningar Sura ar smakar surt vilket du själv har märkt då du ätit syrliga karameller eller smakat på saften från en citron. Motsatsen till sura ar är basiska ar. Man skulle
Protonen upptäcktes 1918 och neutronen 1932. 2. Atommodellen
 1. Atomens historia Det har alltid funnits olika teorier om vad allting består av. Under antiken utvecklades läran om de 4 elementen som blev den teorin som användes mest ända fram till modern tid. Teorin
1. Atomens historia Det har alltid funnits olika teorier om vad allting består av. Under antiken utvecklades läran om de 4 elementen som blev den teorin som användes mest ända fram till modern tid. Teorin
Oxidationstal. Niklas Dahrén
 Oxidationstal Niklas Dahrén Innehåll Förklaring över vad oxidationstal är. Regler för att bestämma oxidationstal. Vad innebär oxidation och reduktion? Oxidation: Ett ämne (atom eller jon) får ett elektronunderskott
Oxidationstal Niklas Dahrén Innehåll Förklaring över vad oxidationstal är. Regler för att bestämma oxidationstal. Vad innebär oxidation och reduktion? Oxidation: Ett ämne (atom eller jon) får ett elektronunderskott
atomkärna Atomkärna är en del av en atom, som finns mitt inne i atomen. Det är i atomkärnan som protonerna finns.
 Facit till Kap 13 Grundboken s. 341-355 och Lightboken s. 213 222 (svart bok) även facit finalen. Testa Dig Själv 13.1TESTA DIG SJÄLV 13.1 GRUNDBOK proton Protoner är en av de partiklar som atomer är uppbyggda
Facit till Kap 13 Grundboken s. 341-355 och Lightboken s. 213 222 (svart bok) även facit finalen. Testa Dig Själv 13.1TESTA DIG SJÄLV 13.1 GRUNDBOK proton Protoner är en av de partiklar som atomer är uppbyggda
I vår natur finns det mängder av ämnen. Det finns några ämnen som vi kallar grundämnen. Grundämnen är uppbyggda av likadana atomer.
 TEORI Kemi I vår natur finns det mängder av ämnen. Det finns några ämnen som vi kallar grundämnen. Grundämnen är uppbyggda av likadana atomer. Länge trodde man att atomer var de minsta byggstenarna. Idag
TEORI Kemi I vår natur finns det mängder av ämnen. Det finns några ämnen som vi kallar grundämnen. Grundämnen är uppbyggda av likadana atomer. Länge trodde man att atomer var de minsta byggstenarna. Idag
Jonföreningar och jonbindningar del 2. Niklas Dahrén
 Jonföreningar och jonbindningar del 2 Niklas Dahrén Del 1: Innehåll o Introduktion till jonföreningar och jonbindningar. o Jämförelse mellan jonföreningar och molekylföreningar. o Hur jonföreningar är
Jonföreningar och jonbindningar del 2 Niklas Dahrén Del 1: Innehåll o Introduktion till jonföreningar och jonbindningar. o Jämförelse mellan jonföreningar och molekylföreningar. o Hur jonföreningar är
Jonföreningar och jonbindningar del 1. Niklas Dahrén
 Jonföreningar och jonbindningar del 1 Niklas Dahrén Del 1: Innehåll o Introduktion till jonföreningar och jonbindningar. o Jämförelse mellan jonföreningar och molekylföreningar. o Hur jonföreningar är
Jonföreningar och jonbindningar del 1 Niklas Dahrén Del 1: Innehåll o Introduktion till jonföreningar och jonbindningar. o Jämförelse mellan jonföreningar och molekylföreningar. o Hur jonföreningar är
Syror och baser. H 2 O + HCl H 3 O + + Cl H + Vatten är en amfolyt + OH NH 3 + H 2 O NH 4. Kemiföreläsning 3 2009-10-27
 Begrepp Syror och baser Kemiföreläsning 9--7 Några vanliga syror HCl (aq) saltsyra HNO salpetersyra H SO svavelsyra H CO kolsyra H PO fosforsyra HAc ättiksyra (egentligen CH COOH, Ac är en förkortning
Begrepp Syror och baser Kemiföreläsning 9--7 Några vanliga syror HCl (aq) saltsyra HNO salpetersyra H SO svavelsyra H CO kolsyra H PO fosforsyra HAc ättiksyra (egentligen CH COOH, Ac är en förkortning
Det mesta är blandningar
 Det mesta är blandningar Allt det vi ser runt omkring oss består av olika ämnen ex vatten, socker, salt, syre och guld. Det är sällan man träffar på rena ämnen. Det allra mesta är olika sorters blandningar
Det mesta är blandningar Allt det vi ser runt omkring oss består av olika ämnen ex vatten, socker, salt, syre och guld. Det är sällan man träffar på rena ämnen. Det allra mesta är olika sorters blandningar
Grundläggande Kemi 1
 Grundläggande Kemi 1 Det mesta är blandningar Allt det vi ser runt omkring oss består av olika ämnen ex vatten, socker, salt, syre och guld. Det är sällan man träffar på rena ämnen. Det allra mesta är
Grundläggande Kemi 1 Det mesta är blandningar Allt det vi ser runt omkring oss består av olika ämnen ex vatten, socker, salt, syre och guld. Det är sällan man träffar på rena ämnen. Det allra mesta är
VAD ÄR KEMI? Vetenskapen om olika ämnens: Egenskaper Uppbyggnad Reaktioner med varandra KEMINS GRUNDER
 VAD ÄR KEMI? Vetenskapen om olika ämnens: Egenskaper Uppbyggnad Reaktioner med varandra ANVÄNDNINGSOMRÅDEN Bakning Läkemedel Rengöring Plast GoreTex o.s.v. i all oändlighet ÄMNENS EGENSKAPER Utseende Hårdhet
VAD ÄR KEMI? Vetenskapen om olika ämnens: Egenskaper Uppbyggnad Reaktioner med varandra ANVÄNDNINGSOMRÅDEN Bakning Läkemedel Rengöring Plast GoreTex o.s.v. i all oändlighet ÄMNENS EGENSKAPER Utseende Hårdhet
PERIODISKA SYSTEMET. Atomkemi
 PERIODISKA SYSTEMET Atomkemi Atomhistorik 400 f.kr nämner den grekiske filosofen Demokritos att materiens minsta delar är odelbara atomer. 300 f.kr så strider Aristoteles mot Demokritos och säger att materia
PERIODISKA SYSTEMET Atomkemi Atomhistorik 400 f.kr nämner den grekiske filosofen Demokritos att materiens minsta delar är odelbara atomer. 300 f.kr så strider Aristoteles mot Demokritos och säger att materia
VAD ÄR KEMI? Vetenskapen om olika ämnens: Egenskaper Uppbyggnad Reaktioner med varandra KEMINS GRUNDER
 VAD ÄR KEMI? Vetenskapen om olika ämnens: Egenskaper Uppbyggnad Reaktioner med varandra ANVÄNDNINGSOMRÅDEN Bakning Läkemedel Rengöring Plast GoreTex o.s.v. i all oändlighet ÄMNENS EGENSKAPER Utseende Hårdhet
VAD ÄR KEMI? Vetenskapen om olika ämnens: Egenskaper Uppbyggnad Reaktioner med varandra ANVÄNDNINGSOMRÅDEN Bakning Läkemedel Rengöring Plast GoreTex o.s.v. i all oändlighet ÄMNENS EGENSKAPER Utseende Hårdhet
Kovalenta bindningar, elektronegativitet och elektronformler. Niklas Dahrén
 Kovalenta bindningar, elektronegativitet och elektronformler Niklas Dahrén Innehåll ü Opolära kovalenta bindningar ü Polära kovalenta bindningar ü Elektronegativitet ü Paulingskalan ü Elektronformler ü
Kovalenta bindningar, elektronegativitet och elektronformler Niklas Dahrén Innehåll ü Opolära kovalenta bindningar ü Polära kovalenta bindningar ü Elektronegativitet ü Paulingskalan ü Elektronformler ü
Jonföreningar och jonbindningar del 2. Niklas Dahrén
 Jonföreningar och jonbindningar del 2 Niklas Dahrén Innehåll Del 1: o Hur jonföreningar bildas/framställs. o Hur jonföreningar är uppbyggda (kristallstruktur). o Jonbindning. o Hur atomernas radie påverkas
Jonföreningar och jonbindningar del 2 Niklas Dahrén Innehåll Del 1: o Hur jonföreningar bildas/framställs. o Hur jonföreningar är uppbyggda (kristallstruktur). o Jonbindning. o Hur atomernas radie påverkas
JONER. Joner är partiklar med elektrisk laddning. Både ensamma atomer och molekyler kan bilda joner.
 JONER Joner är partiklar med elektrisk laddning. Både ensamma atomer och molekyler kan bilda joner. Från era studier i atomens uppbyggnad vet ni att atomen består av i huvudsak tre partiklar. Protonen,
JONER Joner är partiklar med elektrisk laddning. Både ensamma atomer och molekyler kan bilda joner. Från era studier i atomens uppbyggnad vet ni att atomen består av i huvudsak tre partiklar. Protonen,
Materien. Vad är materia? Atomer. Grundämnen. Molekyler
 Materien Vad är materia? Allt som går att ta på och väger någonting är materia. Detta gäller även gaser som t.ex. luft. Om du sticker ut handen genom bilrutan känner du tydligt att det finns något där
Materien Vad är materia? Allt som går att ta på och väger någonting är materia. Detta gäller även gaser som t.ex. luft. Om du sticker ut handen genom bilrutan känner du tydligt att det finns något där
Jonbindning och metallbindning. Niklas Dahrén
 Jonbindning och metallbindning Niklas Dahrén Jonbindning Jonbindning uppstår mellan metaller och ickemetaller Natrium har en valenselektron och klor har 7 valenselektroner. Cl är bra på a< a
Jonbindning och metallbindning Niklas Dahrén Jonbindning Jonbindning uppstår mellan metaller och ickemetaller Natrium har en valenselektron och klor har 7 valenselektroner. Cl är bra på a< a
Repetitionsuppgifter. gymnasiekemi
 Repetitionsuppgifter i gymnasiekemi Att börja med: A 2, 5, 7 B 2, 4, 5, 14, 15, 16, 19 C 2, 7, 8 D 1,2, 3 Om det är för lätt: B 9, 10, 12, 13, 21 C 3, 6 D 4, 5 Boel Lindegård 2006 Reviderad 2012 A. Atomernas
Repetitionsuppgifter i gymnasiekemi Att börja med: A 2, 5, 7 B 2, 4, 5, 14, 15, 16, 19 C 2, 7, 8 D 1,2, 3 Om det är för lätt: B 9, 10, 12, 13, 21 C 3, 6 D 4, 5 Boel Lindegård 2006 Reviderad 2012 A. Atomernas
Syror och baser. Arbetshäfte. Namn: Klass: 9A
 Arbetshäfte Namn: Klass: 9A 1 Syftet med undervisningen är att du ska träna din förmåga att: använda kunskaper i kemi för att granska information, kommunicera och ta ställning i frågor som rör energi,
Arbetshäfte Namn: Klass: 9A 1 Syftet med undervisningen är att du ska träna din förmåga att: använda kunskaper i kemi för att granska information, kommunicera och ta ställning i frågor som rör energi,
TESTA DIG SJÄLV 13.1 GRUNDBOK FÖRKLARA BEGREPPEN proton Protoner är en av de partiklar som atomer är uppbyggda av. Protonerna finns i atomkärnan, i
 TESTA DIG SJÄLV 13.1 GRUNDBOK proton Protoner är en av de partiklar som atomer är uppbyggda av. Protonerna finns i atomkärnan, i mitten av atomerna. Det är antalet protoner som bestämmer vilket atomslag
TESTA DIG SJÄLV 13.1 GRUNDBOK proton Protoner är en av de partiklar som atomer är uppbyggda av. Protonerna finns i atomkärnan, i mitten av atomerna. Det är antalet protoner som bestämmer vilket atomslag
Molekyler och molekylmodeller. En modell av strukturen hos is, fruset vatten
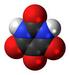 Molekyler och molekylmodeller En modell av strukturen hos is, fruset vatten Sammanställt av Franciska Sundholm 2007 Molekyler och molekylmodeller En gren av kemin beskriver strukturen hos olika föreningar
Molekyler och molekylmodeller En modell av strukturen hos is, fruset vatten Sammanställt av Franciska Sundholm 2007 Molekyler och molekylmodeller En gren av kemin beskriver strukturen hos olika föreningar
Den elektrokemiska spänningsserien. Niklas Dahrén
 Den elektrokemiska spänningsserien Niklas Dahrén Metaller som reduktionsmedel Metaller fungerar ofta som reduktionsmedel: Metaller fungerar ofta som reduktionsmedel eftersom de avger sina valenselektroner
Den elektrokemiska spänningsserien Niklas Dahrén Metaller som reduktionsmedel Metaller fungerar ofta som reduktionsmedel: Metaller fungerar ofta som reduktionsmedel eftersom de avger sina valenselektroner
Den elektrokemiska spänningsserien. Niklas Dahrén
 Den elektrokemiska spänningsserien Niklas Dahrén Metaller som reduktionsmedel ü Metaller avger gärna sina valenselektroner till andra ämnen p.g.a. låg elektronegativitet och eftersom de metalljoner som
Den elektrokemiska spänningsserien Niklas Dahrén Metaller som reduktionsmedel ü Metaller avger gärna sina valenselektroner till andra ämnen p.g.a. låg elektronegativitet och eftersom de metalljoner som
Rättningstiden är i normalfall 15 arbetsdagar, annars är det detta datum som gäller:
 Kemi Bas 1 Provmoment: Ladokkod: Tentamen ges för: TentamensKod: Tentamen 40S01A KBAST och KBASX 7,5 högskolepoäng Tentamensdatum: 2016-10-27 Tid: 09:00-13:00 Hjälpmedel: papper, penna, radergummi, kalkylator
Kemi Bas 1 Provmoment: Ladokkod: Tentamen ges för: TentamensKod: Tentamen 40S01A KBAST och KBASX 7,5 högskolepoäng Tentamensdatum: 2016-10-27 Tid: 09:00-13:00 Hjälpmedel: papper, penna, radergummi, kalkylator
Smälter Förångas FAST FLYTANDE GAS Stelnar Kondensera
 Olika ämnen har olika egenskaper, vissa är salta andra är söta och det finns många egenskaper som gör att vi kan särskilja på olika ämnen. T.ex. färg, densitet, lukt etc. Allt är uppbyggt av atomer beroende
Olika ämnen har olika egenskaper, vissa är salta andra är söta och det finns många egenskaper som gör att vi kan särskilja på olika ämnen. T.ex. färg, densitet, lukt etc. Allt är uppbyggt av atomer beroende
Materien. Vad är materia? Atomer. Grundämnen. Molekyler
 Materien Vad är materia? Allt som går att ta på och väger någonting är materia. Detta gäller även gaser som t.ex. luft. Om du sticker ut handen genom bilrutan känner du tydligt att det finns något där
Materien Vad är materia? Allt som går att ta på och väger någonting är materia. Detta gäller även gaser som t.ex. luft. Om du sticker ut handen genom bilrutan känner du tydligt att det finns något där
Här kan du svara t.ex. När våra förfäder blev sjuka försökte de att få fram botemedel. Det betyder att de har sysslat med kemi.
 - 1 - Kemin, läran om ämnena, vad de innehåller, hur de tillverkas mm. Dessa frågor och svar ger dig grundläggande kunskaper i kemi för grundskolan. Det innebär att du får de viktiga orden/begreppen med
- 1 - Kemin, läran om ämnena, vad de innehåller, hur de tillverkas mm. Dessa frågor och svar ger dig grundläggande kunskaper i kemi för grundskolan. Det innebär att du får de viktiga orden/begreppen med
FACIT TILL FINALEN GRUNDBOK
 FACIT TILL FINALEN GRUNDBOK Kommentar: Ett sätt att avgöra om ett påstående bygger på naturvetenskap är att tänka efter om påståendet i första hand säger vad någon enskild person tycker. I så fall bygger
FACIT TILL FINALEN GRUNDBOK Kommentar: Ett sätt att avgöra om ett påstående bygger på naturvetenskap är att tänka efter om påståendet i första hand säger vad någon enskild person tycker. I så fall bygger
Några vanliga syror och baser
 Några vanliga syror och baser Index Namn Sida Syra Bas Ammoniak 2 x Kalciumhydroxid 3 x Kolsyra 4 x Natriumhydroxid 5 x Några vanliga syror 6 x Salpetersyra 7 x Saltsyra 8 x Svavelsyra 9 x Repetitionsfrågor
Några vanliga syror och baser Index Namn Sida Syra Bas Ammoniak 2 x Kalciumhydroxid 3 x Kolsyra 4 x Natriumhydroxid 5 x Några vanliga syror 6 x Salpetersyra 7 x Saltsyra 8 x Svavelsyra 9 x Repetitionsfrågor
Blommensbergsskola/kemiht13/HSA Minivariant 1
 Blommensbergsskola/kemiht13/HSA Minivariant 1 Kemin, läran om ämnena, vad de innehåller, hur de tillverkas mm. Dessa frågor och svar ger dig grundläggande kunskaper i kemi för grundskolan. Det innebär
Blommensbergsskola/kemiht13/HSA Minivariant 1 Kemin, läran om ämnena, vad de innehåller, hur de tillverkas mm. Dessa frågor och svar ger dig grundläggande kunskaper i kemi för grundskolan. Det innebär
Bild 1: Schematisk bild av en lipid, där bollen är vattenlöslig och svansen är fettlöslig.
 Olika ämnen har olika egenskaper, vissa är salta andra är söta och det finns många egenskaper som gör att vi kan särskilja på olika ämnen. T.ex. färg, densitet, lukt etc. Allt är uppbyggt av atomer beroende
Olika ämnen har olika egenskaper, vissa är salta andra är söta och det finns många egenskaper som gör att vi kan särskilja på olika ämnen. T.ex. färg, densitet, lukt etc. Allt är uppbyggt av atomer beroende
4 Beräkna massprocenthalten koppar i kopparsulfat femhydrat Hur många gram natriumklorid måste man väga upp för att det ska bli 2 mol?
 Stökiometri VI 1 Hur många atomer finns det i en molekyl H 2SO 4? 1 2 Skriv kemiska formeln för jonföreningar: 2 a) Kalciumoxid b) Kaliumjodid c) Strontiumhydroxid d) Aluminiumsulfit 3 Ange eller beräkna:
Stökiometri VI 1 Hur många atomer finns det i en molekyl H 2SO 4? 1 2 Skriv kemiska formeln för jonföreningar: 2 a) Kalciumoxid b) Kaliumjodid c) Strontiumhydroxid d) Aluminiumsulfit 3 Ange eller beräkna:
Analysera gifter, droger och andra ämnen med enkla metoder. Niklas Dahrén
 Analysera gifter, droger och andra ämnen med enkla metoder Niklas Dahrén De flesta ämnen inkl. gifter och droger är antingen molekyl- eller jonföreningar 1. Molekylföreningar: o Molekylföreningar är ämnen
Analysera gifter, droger och andra ämnen med enkla metoder Niklas Dahrén De flesta ämnen inkl. gifter och droger är antingen molekyl- eller jonföreningar 1. Molekylföreningar: o Molekylföreningar är ämnen
Atomen - Periodiska systemet. Kap 3 Att ordna materian
 Atomen - Periodiska systemet Kap 3 Att ordna materian Av vad består materian? 400fKr (före år noll) Empedokles: fyra element, jord, eld, luft, vatten Demokritos: små odelbara partiklar! -------------------------
Atomen - Periodiska systemet Kap 3 Att ordna materian Av vad består materian? 400fKr (före år noll) Empedokles: fyra element, jord, eld, luft, vatten Demokritos: små odelbara partiklar! -------------------------
ENKEL Kemi 2. Atomer och molekyler. Art nr 515. Atomer. Grundämnen. Atomens historia
 ENKEL Kemi 2 Atomer och molekyler atomkärna elektron Atomer Allting runt omkring oss är uppbyggt av atomer. En atom är otroligt liten. Den går inte att se för blotta ögat. Ett sandkorn rymmer ungefär hundra
ENKEL Kemi 2 Atomer och molekyler atomkärna elektron Atomer Allting runt omkring oss är uppbyggt av atomer. En atom är otroligt liten. Den går inte att se för blotta ögat. Ett sandkorn rymmer ungefär hundra
Rättningstiden är i normalfall tre veckor, annars är det detta datum som gäller: Efter överenskommelse med studenterna är rättningstiden fem veckor.
 Kemi Bas A Provmoment: Tentamen Ladokkod: TX011X Tentamen ges för: Tbas, TNBas 7,5 högskolepoäng Namn: Personnummer: Tentamensdatum: 2012-10-22 Tid: 9:00-13:00 Hjälpmedel: papper, penna, radergummi kalkylator
Kemi Bas A Provmoment: Tentamen Ladokkod: TX011X Tentamen ges för: Tbas, TNBas 7,5 högskolepoäng Namn: Personnummer: Tentamensdatum: 2012-10-22 Tid: 9:00-13:00 Hjälpmedel: papper, penna, radergummi kalkylator
Prov i kemi kurs A. Atomens byggnad och periodiska systemet 2(7) Namn:... Hjälpmedel: räknedosa + tabellsamling
 Prov i kemi kurs A Namn:... Hjälpmedel: räknedosa + tabellsamling Lösningar och svar skall ges på särskilt inskrivningspapper för de uppgifter som är skrivna med kursiv stil. I övriga fall ges svaret och
Prov i kemi kurs A Namn:... Hjälpmedel: räknedosa + tabellsamling Lösningar och svar skall ges på särskilt inskrivningspapper för de uppgifter som är skrivna med kursiv stil. I övriga fall ges svaret och
Kemiskafferiet modul 3 kemiteori. Atomer och joner
 Atomer och joner Kan man se atomer? Idag har man instrument som gör att man faktiskt kan "se atomer" i ett elektronmikroskop. Med speciella metoder kan man se vilket mönster atomerna bildar i en kristall
Atomer och joner Kan man se atomer? Idag har man instrument som gör att man faktiskt kan "se atomer" i ett elektronmikroskop. Med speciella metoder kan man se vilket mönster atomerna bildar i en kristall
KEMI 1 MÄNNISKANS KEMI OCH KEMIN I LIVSMILJÖ
 KEMI 1 MÄNNISKANS KEMI OCH KEMIN I LIVSMILJÖ Vad är KEMI? Ordet kemi kommer från grekiskans chemeia =blandning Allt som finns omkring oss och som påverkar oss handlar om KEMI. Vad du tycker DU att kemi
KEMI 1 MÄNNISKANS KEMI OCH KEMIN I LIVSMILJÖ Vad är KEMI? Ordet kemi kommer från grekiskans chemeia =blandning Allt som finns omkring oss och som påverkar oss handlar om KEMI. Vad du tycker DU att kemi
De delar i läroplanerna som dessa arbetsuppgifter berör finns redovisade på den sista sidan i detta häfte. PERIODISKA SYSTEMET
 Ar be tsu pp gi fte r ARBETSUPPGIFTER Uppgifterna är kopplade till följande film ur serien Area Kemins grunder: 9. Syror Uppgifterna är av olika svårighetsgrad A-C, och du måste använda dig av läroboken
Ar be tsu pp gi fte r ARBETSUPPGIFTER Uppgifterna är kopplade till följande film ur serien Area Kemins grunder: 9. Syror Uppgifterna är av olika svårighetsgrad A-C, och du måste använda dig av läroboken
Repetitionskompendium Grundläggande kemi Årskurs 7 2016
 Repetitionskompendium Grundläggande kemi Årskurs 7 2016 Innehållsförteckning 1 Atomer naturens egna byggstenar... 3 2 Molekyler är grupper av atomer... 4 3 Grundämnen och kemiska föreningar... 5 4 Kemiska
Repetitionskompendium Grundläggande kemi Årskurs 7 2016 Innehållsförteckning 1 Atomer naturens egna byggstenar... 3 2 Molekyler är grupper av atomer... 4 3 Grundämnen och kemiska föreningar... 5 4 Kemiska
Sura och basiska ämnen Syror och baser. Kap 5:1-5:3, (kap 9)
 Sura och basiska ämnen Syror och baser Kap 5:1-5:3, (kap 9) Syror / sura lösningar En sur lösning - har överskott på vätejoner, H + (protoner) En syra: - smakar surt - färgar BTB gult - reagerar med oädla
Sura och basiska ämnen Syror och baser Kap 5:1-5:3, (kap 9) Syror / sura lösningar En sur lösning - har överskott på vätejoner, H + (protoner) En syra: - smakar surt - färgar BTB gult - reagerar med oädla
Marie Curie, kärnfysiker, 1867 1934. Atomfysik. Heliumatom. Partikelacceleratorn i Cern, Schweiz.
 Marie Curie, kärnfysiker, 1867 1934. Atomfysik Heliumatom Partikelacceleratorn i Cern, Schweiz. Atom (grek. odelbar) Ordet atom användes för att beskriva materians minsta beståndsdel. Nu vet vi att atomen
Marie Curie, kärnfysiker, 1867 1934. Atomfysik Heliumatom Partikelacceleratorn i Cern, Schweiz. Atom (grek. odelbar) Ordet atom användes för att beskriva materians minsta beståndsdel. Nu vet vi att atomen
Introduktion till det periodiska systemet. Niklas Dahrén
 Introduktion till det periodiska systemet Niklas Dahrén Det periodiska systemet Vad är det periodiska systemet?: Det periodiska systemet är en tabell där alla kända grundämnen och atomslag ingår. Hur är
Introduktion till det periodiska systemet Niklas Dahrén Det periodiska systemet Vad är det periodiska systemet?: Det periodiska systemet är en tabell där alla kända grundämnen och atomslag ingår. Hur är
Materia Sammanfattning. Materia
 Materia Sammanfattning Material = vad föremålet (materiel) är gjort av. Materia finns överallt (består av atomer). OBS! Materia Något som tar plats. Kan mäta hur mycket plats den tar eller väga. Materia
Materia Sammanfattning Material = vad föremålet (materiel) är gjort av. Materia finns överallt (består av atomer). OBS! Materia Något som tar plats. Kan mäta hur mycket plats den tar eller väga. Materia
Syror, baser och ph-värde. Niklas Dahrén
 Syror, baser och ph-värde Niklas Dahrén Syror är protongivare Syror kännetecknas av följande: 1. De har förmåga att avge vätejoner, H + (protoner), vilket leder till en ph-sänkning. 2. De ger upphov till
Syror, baser och ph-värde Niklas Dahrén Syror är protongivare Syror kännetecknas av följande: 1. De har förmåga att avge vätejoner, H + (protoner), vilket leder till en ph-sänkning. 2. De ger upphov till
Kovalenta och polära kovalenta bindningar. Niklas Dahrén
 Kovalenta och polära kovalenta bindningar Niklas Dahrén Indelning av kemiska bindningar Jonbindning Bindningar mellan jonerna i en jonförening (salt) Kemiska bindningar Metallbindning Kovalenta bindningar
Kovalenta och polära kovalenta bindningar Niklas Dahrén Indelning av kemiska bindningar Jonbindning Bindningar mellan jonerna i en jonförening (salt) Kemiska bindningar Metallbindning Kovalenta bindningar
Prov Ke1 Atomer och periodiska systemet NA1+TE1/ /PLE
 Prov Ke1 Atomer och periodiska systemet NA1+TE1/2017-10-12/PLE Hjalmar Namn: Fel svar på ervalsfrågorna ger poängavdrag! Del I: svara i provet 1. Ange masstal, atomnummer och antalet elektroner, protoner
Prov Ke1 Atomer och periodiska systemet NA1+TE1/2017-10-12/PLE Hjalmar Namn: Fel svar på ervalsfrågorna ger poängavdrag! Del I: svara i provet 1. Ange masstal, atomnummer och antalet elektroner, protoner
Kemisk bindning. Mål med avsnittet. Jonbindning
 Kemisk bindning Det är få grundämnen som förekommer i ren form i naturen De flesta söker en kompis med kompletterande egenskaper Detta kan ske på några olika sätt, både inom molekylen och mellan molekylen
Kemisk bindning Det är få grundämnen som förekommer i ren form i naturen De flesta söker en kompis med kompletterande egenskaper Detta kan ske på några olika sätt, både inom molekylen och mellan molekylen
Terminsplanering i Kemi för 7P4 HT 2012
 Terminsplanering i Kemi för 7P4 HT 2012 Vecka Tema Dag Planering Atomer och kemiska V35 reaktioner V36 V37 V38 Atomer och kemiska reaktioner Luft Luft V40 V41 V42 Vatten Vissa förändringar kan förekomma
Terminsplanering i Kemi för 7P4 HT 2012 Vecka Tema Dag Planering Atomer och kemiska V35 reaktioner V36 V37 V38 Atomer och kemiska reaktioner Luft Luft V40 V41 V42 Vatten Vissa förändringar kan förekomma
Identifiera okända ämnen med enkla metoder. Niklas Dahrén
 Identifiera okända ämnen med enkla metoder Niklas Dahrén Det finns två huvudgrupper av ämnen 1. Jonföreningar (salter): En jonförening är uppbyggd av posi5va och nega5va joner som binder 5ll varandra e:ersom
Identifiera okända ämnen med enkla metoder Niklas Dahrén Det finns två huvudgrupper av ämnen 1. Jonföreningar (salter): En jonförening är uppbyggd av posi5va och nega5va joner som binder 5ll varandra e:ersom
FACIT TILL TESTA DIG SJÄLV GRUNDBOK
 FACIT TILL TESTA DIG SJÄLV GRUNDBOK TESTA DIG SJÄLV 3.1 GRUNDBOK saltvatten Saltvatten är det vatten på jorden som innehåller så mycket salt att det inte går att använda som dricksvatten. Vattnet i haven
FACIT TILL TESTA DIG SJÄLV GRUNDBOK TESTA DIG SJÄLV 3.1 GRUNDBOK saltvatten Saltvatten är det vatten på jorden som innehåller så mycket salt att det inte går att använda som dricksvatten. Vattnet i haven
1. Ett grundämne har atomnummer 82. En av dess isotoper har masstalet 206.
 1. Ett grundämne har atomnummer 82. En av dess isotoper har masstalet 206. a) Antalet protoner är., antalet neutroner är. och antalet elektroner. hos atomer av isotopen. b) Vilken partikel bildas om en
1. Ett grundämne har atomnummer 82. En av dess isotoper har masstalet 206. a) Antalet protoner är., antalet neutroner är. och antalet elektroner. hos atomer av isotopen. b) Vilken partikel bildas om en
Historia De tidigaste kända idéerna om något som liknar dagens atomer utvecklades av Demokritos i Grekland runt 450 f.kr. År 1803 använde John Dalton
 Atomen En atom, från grekiskans ἄτομος, átomos, vilket betyder "odelbar", är den minsta enheten av ett grundämne som definierar dess kemiska egenskaper. Historia De tidigaste kända idéerna om något som
Atomen En atom, från grekiskans ἄτομος, átomos, vilket betyder "odelbar", är den minsta enheten av ett grundämne som definierar dess kemiska egenskaper. Historia De tidigaste kända idéerna om något som
JONER. Joner är partiklar med elektrisk laddning. Både ensamma atomer och molekyler kan bilda joner.
 JONER Joner är partiklar med elektrisk laddning. Både ensamma atomer och molekyler kan bilda joner. Från era studier i atomens uppbyggnad vet ni att atomen består av i huvudsak tre partiklar. Protonen,
JONER Joner är partiklar med elektrisk laddning. Både ensamma atomer och molekyler kan bilda joner. Från era studier i atomens uppbyggnad vet ni att atomen består av i huvudsak tre partiklar. Protonen,
Introduktion till kemisk bindning. Niklas Dahrén
 Introduktion till kemisk bindning Niklas Dahrén Indelning av kemiska bindningar Jonbindning Bindningar mellan jonerna i en jonförening (salt) Kemiska bindningar Metallbindning Kovalenta bindningar Bindningar
Introduktion till kemisk bindning Niklas Dahrén Indelning av kemiska bindningar Jonbindning Bindningar mellan jonerna i en jonförening (salt) Kemiska bindningar Metallbindning Kovalenta bindningar Bindningar
Tentamen i Allmän kemi NKEA02, 9KE211, 9KE351. 2010-09-20, kl. 14 00-19 00
 IFM/Kemi Tentamen i Allmän kemi NKEA02, 9KE211, 9KE351 2010-09-20, kl. 14 00-19 00 Ansvariga lärare: Helena Herbertsson 285605, 070-5669944 Lars Ojamäe 281380 50% rätt ger säkert godkänt! Hjälpmedel: Miniräknare
IFM/Kemi Tentamen i Allmän kemi NKEA02, 9KE211, 9KE351 2010-09-20, kl. 14 00-19 00 Ansvariga lärare: Helena Herbertsson 285605, 070-5669944 Lars Ojamäe 281380 50% rätt ger säkert godkänt! Hjälpmedel: Miniräknare
Olika kovalenta bindningar. Niklas Dahrén
 Olika kovalenta bindningar Niklas Dahrén Indelning av kemiska bindningar Jonbindning Bindningar mellan jonerna i en jonförening (salt) Kemiska bindningar Metallbindning Kovalenta bindningar (intramolekylära)
Olika kovalenta bindningar Niklas Dahrén Indelning av kemiska bindningar Jonbindning Bindningar mellan jonerna i en jonförening (salt) Kemiska bindningar Metallbindning Kovalenta bindningar (intramolekylära)
Hemlaboration 4 A (Norrköping)
 Hemlaboration 4 A (Norrköping) Grundläggande om syror och baser Materiel: Det materiel som du behöver till denna hemlaboration finns i laborationslådan. Där hittar du 12-brunnars plattan, kassettfodralet
Hemlaboration 4 A (Norrköping) Grundläggande om syror och baser Materiel: Det materiel som du behöver till denna hemlaboration finns i laborationslådan. Där hittar du 12-brunnars plattan, kassettfodralet
Oxidation, reduktion och redoxreaktioner. Niklas Dahrén
 Oxidation, reduktion och redoxreaktioner Niklas Dahrén Vad innebär oxidation och reduktion? Oxida'on: Ämnet får e* elektronundersko* genom a* elektroner avges helt eller delvis (oxida8onstalet ökar). Reduk'on:
Oxidation, reduktion och redoxreaktioner Niklas Dahrén Vad innebär oxidation och reduktion? Oxida'on: Ämnet får e* elektronundersko* genom a* elektroner avges helt eller delvis (oxida8onstalet ökar). Reduk'on:
KEMI 1 MÄNNISKANS KEMI OCH KEMIN I LIVSMILJÖ
 KEMI 1 MÄNNISKANS KEMI OCH KEMIN I LIVSMILJÖ FYSIK BIOLOGI KEMI MEDICIN TEKNIK Laborationer Ett praktiskt och konkret experiment Analys av t ex en reaktion Bevisar en teori eller lägger grunden för en
KEMI 1 MÄNNISKANS KEMI OCH KEMIN I LIVSMILJÖ FYSIK BIOLOGI KEMI MEDICIN TEKNIK Laborationer Ett praktiskt och konkret experiment Analys av t ex en reaktion Bevisar en teori eller lägger grunden för en
Atomer, joner och kemiska reaktioner
 Andreas Sandqvist 2015-11-24 Atomer, joner och kemiska reaktioner Namn: Uppgifter Lös uppgifterna med hjälp av läroboken, filmgenomgångarna, ett periodiskt system och internet. Arbeta tillsammans i era
Andreas Sandqvist 2015-11-24 Atomer, joner och kemiska reaktioner Namn: Uppgifter Lös uppgifterna med hjälp av läroboken, filmgenomgångarna, ett periodiskt system och internet. Arbeta tillsammans i era
Begrepp vem hör ihop med vem?
 Syftet med arbetet är att du ska utveckla din förmåga att använda kemins begrepp, modeller och teorier för att beskriva och förklara kemiska samband i samhället, naturen och inuti människan. Målet är att
Syftet med arbetet är att du ska utveckla din förmåga att använda kemins begrepp, modeller och teorier för att beskriva och förklara kemiska samband i samhället, naturen och inuti människan. Målet är att
KEMINS ÄMNESSPECIFIKA BEGREPP
 KEMINS ÄMNESSPECIFIKA BEGREPP A Absoluta nollpunkten: Temperaturen 0 K eller -273,15 o C. Kallare än så kan det inte bli. Alkalimetaller: Metallerna i grupp 1 i det periodiska systemet. Har en valenselektron
KEMINS ÄMNESSPECIFIKA BEGREPP A Absoluta nollpunkten: Temperaturen 0 K eller -273,15 o C. Kallare än så kan det inte bli. Alkalimetaller: Metallerna i grupp 1 i det periodiska systemet. Har en valenselektron
Materia och aggregationsformer. Niklas Dahrén
 Materia och aggregationsformer Niklas Dahrén Vad är materia? Materia är egentligen allting som vi ser omkring oss! Allt som är uppbyggt av atomer kallas för materia. Materia kännetecknas av att det har
Materia och aggregationsformer Niklas Dahrén Vad är materia? Materia är egentligen allting som vi ser omkring oss! Allt som är uppbyggt av atomer kallas för materia. Materia kännetecknas av att det har
Studenter i lärarprogrammet LAG F-3 T6. Periodiska systemet, tabell över joner och skrivverktyg. 55 p. Väl godkänd: 41 p
 Kemi 11F360 Provmoment: Ladokkod: Tentamen ges för: Kemi 2,5 hp Studenter i lärarprogrammet LAG F3 T6 22,5 högskolepoäng TentamensKod: Tentamensdatum: 180406 Tid: 09.00 13.00 Hjälpmedel: Periodiska systemet,
Kemi 11F360 Provmoment: Ladokkod: Tentamen ges för: Kemi 2,5 hp Studenter i lärarprogrammet LAG F3 T6 22,5 högskolepoäng TentamensKod: Tentamensdatum: 180406 Tid: 09.00 13.00 Hjälpmedel: Periodiska systemet,
Viktigt! Glöm inte att skriva Tentamenskod på alla blad du lämnar in.
 Kemi Bas 1 Provmoment: Ladokkod: Tentamen ges för: TentamensKod: Tentamen 40S01A KBAST och KBASX 7,5 högskolepoäng Tentamensdatum: 2015-10-30 Tid: 09:00-13:00 Hjälpmedel: papper, penna, radergummi, kalkylator
Kemi Bas 1 Provmoment: Ladokkod: Tentamen ges för: TentamensKod: Tentamen 40S01A KBAST och KBASX 7,5 högskolepoäng Tentamensdatum: 2015-10-30 Tid: 09:00-13:00 Hjälpmedel: papper, penna, radergummi, kalkylator
Föreläsningsplan 2010. Del 1 Allmän kemi
 IFM-Kemi 9NV221, 9NV321, LINVA6 101018 Kemi för NV-lärare Föreläsningsplan 2010 Del 1 Allmän kemi Föreläsn.1 + 2 Kap. 12. Atomer och atommodeller. Föreläsn. 3 Kap. 14 Kemi: Grundämnen och föreningar. Föreläsn.
IFM-Kemi 9NV221, 9NV321, LINVA6 101018 Kemi för NV-lärare Föreläsningsplan 2010 Del 1 Allmän kemi Föreläsn.1 + 2 Kap. 12. Atomer och atommodeller. Föreläsn. 3 Kap. 14 Kemi: Grundämnen och föreningar. Föreläsn.
Hjälpmedel: räknare, formelsamling, periodiska system. Spänningsserien: K Ca Na Mg Al Zn Cr Fe Ni Sn Pb H Cu Hg Ag Pt Au. Kemi A
 Uppsala Universitet Fysiska Institutionen Tekniskt- naturvetenskapligt basår Raúl Miranda 2007 Namn: Stark Karl Grupp: Den bästa.. Datum: Tid: 08.00 12.00 jälpmedel: räknare, formelsamling, periodiska
Uppsala Universitet Fysiska Institutionen Tekniskt- naturvetenskapligt basår Raúl Miranda 2007 Namn: Stark Karl Grupp: Den bästa.. Datum: Tid: 08.00 12.00 jälpmedel: räknare, formelsamling, periodiska
De delar i läroplanerna som dessa arbetsuppgifter berör finns redovisade på den sista sidan i detta häfte. PERIODISKA SYSTEMET
 ARBETSUPPGIFTER Uppgifterna är kopplade till följande film i serien Area 41 Kemins grunder: 7. Jonföreningar Uppgifterna är av olika svårighetsgrad A-C, och du måste använda dig av läroboken och periodiska
ARBETSUPPGIFTER Uppgifterna är kopplade till följande film i serien Area 41 Kemins grunder: 7. Jonföreningar Uppgifterna är av olika svårighetsgrad A-C, och du måste använda dig av läroboken och periodiska
Om syror baser och ph
 Om syror baser och ph Att syra och mumifiera är praktisk antik kunskap Syror och baser har man känt till mycket länge. Ättikan var den första syran man kunde framställa (ur vin). Ättiksyrabakterien är
Om syror baser och ph Att syra och mumifiera är praktisk antik kunskap Syror och baser har man känt till mycket länge. Ättikan var den första syran man kunde framställa (ur vin). Ättiksyrabakterien är
Mål och betygskriterier för kemi
 Mål och betygskriterier för kemi För att bli GODKÄND på samtliga kurser skall du: Kunna skyddsföreskrifter inom NO-institutionen, samt veta var skydds- och nödutrustning finns Kunna handha den laboratorieutrustning
Mål och betygskriterier för kemi För att bli GODKÄND på samtliga kurser skall du: Kunna skyddsföreskrifter inom NO-institutionen, samt veta var skydds- och nödutrustning finns Kunna handha den laboratorieutrustning
ATOMER OCH ATOMMODELLEN. Lärare: Jimmy Pettersson
 ATOMER OCH ATOMMODELLEN Lärare: Jimmy Pettersson Grundämnen Atomer och Grundämnen All materia byggs upp av mycket små byggstenar som kallas atomer. Varje typ av atom är byggstenar för varje kemiskt ämne.
ATOMER OCH ATOMMODELLEN Lärare: Jimmy Pettersson Grundämnen Atomer och Grundämnen All materia byggs upp av mycket små byggstenar som kallas atomer. Varje typ av atom är byggstenar för varje kemiskt ämne.
Periodiska systemet Betygskriterier - Periodiska systemet För att få godkänt ska du... För att få väl godkänt ska du också kunna...
 Periodiska systemet Betygskriterier - Periodiska systemet För att få godkänt ska du... Veta vad atomer är för något, rita upp en modell av en atom. Veta skillnaden mellan en atom och en jon. Känna till
Periodiska systemet Betygskriterier - Periodiska systemet För att få godkänt ska du... Veta vad atomer är för något, rita upp en modell av en atom. Veta skillnaden mellan en atom och en jon. Känna till
Kemins grunder. En sammanfattning enligt planeringen men i den ordning vi gjort delarna
 Kemins grunder En sammanfattning enligt planeringen men i den ordning vi gjort delarna Konkreta mål Undervisning Bedömning Centralt innehåll Kunskapskrav Vi ska lära oss Genomgångar: Skriftligt prov Kemin
Kemins grunder En sammanfattning enligt planeringen men i den ordning vi gjort delarna Konkreta mål Undervisning Bedömning Centralt innehåll Kunskapskrav Vi ska lära oss Genomgångar: Skriftligt prov Kemin
Kapitel 4. Reaktioner i vattenlösningar
 Kapitel 4 Reaktioner i vattenlösningar Kapitel 4 Innehåll 4.1 Vatten, ett lösningsmedel 4.2 Starka och svaga elektrolyter 4.3 Lösningskoncentrationer 4.4 Olika slags kemiska reaktioner 4.5 Fällningsreaktioner
Kapitel 4 Reaktioner i vattenlösningar Kapitel 4 Innehåll 4.1 Vatten, ett lösningsmedel 4.2 Starka och svaga elektrolyter 4.3 Lösningskoncentrationer 4.4 Olika slags kemiska reaktioner 4.5 Fällningsreaktioner
Syror och baser 1. Indikatorer
 Syror och baser 1 NÄR DU HAR ARBETAT MED AVSNITTET SYROR OCH BASER 1 KAN DU ge exempel på några indikatorer och deras egenskaper redogöra för ph-skalan och ph-värdena för en syra, en bas och en neutral
Syror och baser 1 NÄR DU HAR ARBETAT MED AVSNITTET SYROR OCH BASER 1 KAN DU ge exempel på några indikatorer och deras egenskaper redogöra för ph-skalan och ph-värdena för en syra, en bas och en neutral
Kemiska beteckningar på de vanligaste atomslagen - känna till jonladdning på de vanligaste olika kemiska jonerna
 Elektrokemi Kemiska beteckningar på de vanligaste atomslagen - känna till jonladdning på de vanligaste olika kemiska jonerna Elektrokemiska spänningsserien: Alla metaller i det periodiska systemet finns
Elektrokemi Kemiska beteckningar på de vanligaste atomslagen - känna till jonladdning på de vanligaste olika kemiska jonerna Elektrokemiska spänningsserien: Alla metaller i det periodiska systemet finns
Repetition av hur en atom blir en jon.
 Repetition av hur en atom blir en jon. ex. 11 Na Det finns en elektron i det yttersta skalet. Natrium vill bli av med den för att få fullt i sitt yttersta skal. Natrium ger då bort den och natriumatomen
Repetition av hur en atom blir en jon. ex. 11 Na Det finns en elektron i det yttersta skalet. Natrium vill bli av med den för att få fullt i sitt yttersta skal. Natrium ger då bort den och natriumatomen
Intermolekylära krafter
 Intermolekylära krafter Medicinsk Teknik KTH Biologisk kemi Vt 2011 Märit Karls Intramolekylära attraktioner Atomer hålls ihop av elektrostatiska krafter mellan protoner och.elektroner Joner hålls ihop
Intermolekylära krafter Medicinsk Teknik KTH Biologisk kemi Vt 2011 Märit Karls Intramolekylära attraktioner Atomer hålls ihop av elektrostatiska krafter mellan protoner och.elektroner Joner hålls ihop
