Information till forskningsperson för studie HP-CD-CL-2002
|
|
|
- Viktor Ström
- för 7 år sedan
- Visningar:
Transkript
1 Information till forskningsperson för studie HP-CD-CL-2002 Studietitel En fas I-II, randomiserad, dubbelblind, placebokontrollerad, säkerhet- och tolerabilitetsstudie av intermittent bilateral intraputaminal Cerebral Dopamin Neurotrofisk Faktor (CDNF) infusioner som ges via ett administreringssystem till patienter med idiopatisk Parkinsons sjukdom (PS) av måttlig svårighetsgrad. Förfrågan om deltagande Du tillfrågas härmed om du vill delta i en forskningsstudie för att testa ett nytt sätt att behandla Parkinsons sjukdom. Studieläkemedlet heter CDNF och är en vätska som innehåller ett protein som tillförs hjärnan med hjälp av ett administreringssystem som består av mycket tunna slangar (katetrar)som leder vätskan till rätt område i hjärnan. Administreringssystemet som är under utveckling opereras in i din hjärna med hjälp av en operationsrobot och kirurgiska instrument. Operationsroboten finns tillgänglig på marknaden men för denna studie kommer en ny modul av mjukvaran att användas för att guida roboten och förbereda operationen. De kirurgiska instrument som används i denna studie har använts i andra studier innan men har inte tidigare använts i kliniska sammanhang. Deltagande i denna studie är helt frivilligt. Du kan avböja att vara med i studien eller när som helst avbryta ditt deltagande utan vidare förklaring. Du behöver inte delta i denna studie för att få traditionell behandling. Din studieläkare kommer att förklara vilka behandlingsalternativ som finns för din sjukdom. Vänligen ta dig tid att läsa igenom detta informationsblad. Om du har några frågor så fråga din studieläkare eller någon annan i studieteamet. Om du beslutar dig för att delta i studien kommer vi att be dig skriva under ett skriftligt samtyckesformulär och ge dig en kopia på informationen och samtyckesformuläret. Studien är granskad och godkänd av Läkemedelsverket, Regionala etikprövningsnämnden i Stockholm samt strålskyddskommittén. Studiens genomförande Denna studie kommer att genomföras på två sjukhus i Sverige och ett i Finland. Läkemedelsbolaget Herantis Pharma Plc som utvecklar studieläkemedlet är sponsor för studien i ett samarbete med företaget Renishaw Plc som utvecklat administreringssystemet och operationsroboten. Bakgrund och syfte med studien Syftet med studien är att undersöka säkerheten och tolerabiliteten av administreringssystemet samt behandling med CDNF. Syftet är även att utvärdera noggrannheten vid implanteringen av administreringssystemet. Studieläkemedlet Studieläkemedlet som kallas CDNF är ett protein som finns naturligt i kroppen. Detta protein tillhör en grupp som kallas neurotrofiska faktorer. I djurstudier har man sett att CDNF har kunnat förhindra död och nedbrytning av dopaminproducerande nervceller och att den kan stimulera tillväxten och funktionen av dessa celler. Detta skulle kunna leda till en förbättring av sjukdomstillståndet hos sjukdomar som orsakas av nedbrytning av nervceller som vid Parkinsons sjukdom. Eftersom CDNF är ett protein kan det inte tas som en tablett eller injiceras perifert eftersom kroppen då inte kan Sida 1 av 18
2 transportera det vidare in i hjärnan. I denna studie kommer CDNF att ges med hjälp av ett administreringssystem som implanteras i din hjärna. Administreringssystemet Administreringssystemet är ännu inte slutgiltigt godkänt för implantering och administrering av läkemedel in i hjärnan. Ett av syftena med den här studien är att undersöka säkerheten och funktionaliteten hos detta administreringssystem. Adminstreringssystemet består av tre delar: 1. Total fyra katetrar (1.7 mm i diameter; två på var sida) kommer att sättas in i de delar av hjärnan som kallas putamen (som står i förbindelse med den delen av hjärnan där nervceller bryts ned som mest i Parkinsons sjukdom). 2. En port (ungefär 5 mm i diameter och en höjd på 1 cm), som kan kopplas till 4 individuella slangar när studieläkemedlet/placebo ska doseras. Porten sätts fast i skallbenet under huden strax bakom örat. 3. Fyra filter kopplas mellan slangarna och porten. Filterna tar bort bakterier och luft som kan komma in i slangarna när man administrerar studieläkemedlet/placebo. 1.# 3.# 2.# Ovan visas en bild av de inplanterade mikrokateterna genom utskärningar i huden (1.) placeringen av porten på huvudet (2.) och även porten för administrering av studieläkemedlet/placebo med filter mellan slangarna och porten(3.). Den kirurgiska roboten och planeringsmjukvaran Den kirurgiska roboten finns tillgänglig på marknaden för användning i kliniskt arbete, men nya moduler för mjukvaran kommer att användas i studien för att guida roboten och planera operationen. Operationen för att sätta in administreringssystemet kommer att genomföras cirka åtta veckor före start av behandlingen med studieläkemedlet/placebo och kommer att genomföras av erfarna neurokirurger. Neurokirurgerna kommer även att ha hjälp av medarbetare från Renishaw Plc under operationen. Renishaw Plc är företaget som utvecklar administreringssystemet. Tidigare erfarenhet av CDNF, administreringssystemet och kirurgisk teknik CDNF har inte tidigare testats på människor. Adminstreringssystemet samt de kirurgiska instrument som kommer användas i denna studie har dock använts på över 40 patienter i tidigare studier men är Sida 2 av 18
3 inte godkända på marknaden för kliniskt bruk. Den kirurgiska roboten är godkänd på marknaden men en ny modul för mjukvaran som kommer att användas i denna studie har inte tidigare använts i kliniska sammanhang och är inte godkänd på marknaden för kliniskt bruk. För att kunna se att administreringssystemet fungerar som det ska kommer ett kontrastmedel vid namn Gadolinium (Magnevist ) att ges och en magnetröntgen av huvudet att göras. Gadolinium är godkänt att användas intravenöst. Administrering av Gadolinium direkt in i hjärnan är experimentellt men har använts i tidigare studier. Studiemetodik och procedur: Hur kommer studien att genomföras? Detta är en klinisk forskningsstudie där patienter med Parkinsons sjukdom som är mellan år tillfrågas om att delta,20 patienter kommer att opereras och 18 patienter kommer att behandlas med CDNF eller placebo. Patienter kommer att inkluderas från tre olika sjukhus; två i Sverige (Lund och Stockholm) samt ett i Finland (Helsingfors). Under studiens gång kommer CDNF att testas och jämföras med placebo (vätska som inte innehåller substansen CDNF men som i övrigt är identisk). Totalt planeras 6 doser av studieläkemedlet/placebo att ges under en period av 6 månader. Placebo förväntas inte ge någon effekt men kan hjälpa till att urskilja vilka effekter som kommer från administreringssystemet och vilka effekter som kommer från studieläkemedlet. De två första patienterna i studien kommer att få en extra dos av placebo innan det beslutas om vilken dosgrupp de kommer att tillhöra. Din studieläkare kommer att informera dig om du är en av dessa två patienter i studien och därför kommer att få denna extra placebodos. Två av tre patienter kommer att få CDNF och en av tre kommer att få placebo. Du lottas till behandlingen vid start av studien. Varken du eller studieläkaren kan påverka vilken behandlingsgrupp du placeras i eller vet vilken behandling du fått förrän studien är avslutad. Olika doser av studieläkemedlet kommer att ges i studien. Alla patienter som ska få studieläkemedel kommer att börja med att få en låg dos (120 µg).en oberoende grupp av experter kommer sedan att granska datan innan dosen ökas till medeldos (400 µg) för att säkerställa att inga säkerhetsrisker kan kopplas till studieläkemedlet. En granskning kommer även att göras för att bekräfta att det anses säkert att höja dosen till en högdos (1200 µg). Sida 3 av 18
4 Första 2 patienterna Placebo Placebo grupp 6 patienter Mellandos- grupp 3 patienter 3 patienter 1:a dosen 2:a dosen 3:e dosen 4:e dosen 5:e dosen 6:e dosen Placebo Placebo Placebo Placebo Placebo Placebo Låg dos (=120 μg) Låg dos (=120 μg) Låg dos (=120 μg) Låg dos (=120 μg) Låg dos (=120 μg) Mellandos Mellandosgrupp Mellandos (=400 μg) (=400 μg) Mellandos (=400 μg) (=400 μg) Mellandos (=400 μg) Behandlingsgrupp Mellandos Mellandos (=400 μg) Mellandos (=400 μg) Högdos- grupp 6 patienter Lågdos (=120 μg) Låg dos (=120 μg) (=400 μg) Mellandos Mellandos (=400 μg) Hög dos (=1200 μg) Hög dos (=1200 μg) Du måste uppfylla vissa krav för att få vara med i studien. Om du inte kan delta får du veta orsaken och fortsätter få sedvanlig vård. Studien varar i 10 månader och består av 18 besök (19 besök om du är en av de två första patienterna i studien eller om du skulle behöva ytterligare en placeboinfusion under studien), däribland besöket där vi undersöker om du uppfyller studiekraven, operationen för att operera in administreringssystemet i din hjärna, tre testinfusioner med MRI undersökningar, 2 PET undersökningar, behandlingsperioden samt uppföljningsbesöket. I samband med operationen kommer du att få stanna på sjukhuset i ungefär 4 dagar efter operationen. Efter den första och andra administreringen av studieläkemedlet/placebo kommer du att behöva stanna över natten på kliniken. Vid fyra tillfällen under studiens gång kommer du att läggas in på kliniken över natten och avstå från din Parkinsonmedicin upp till 24 timmar (beroende på vilken typ av medicin du tar) före undersökningarna (besök 2, 9, 14 och 19). Du kommer också att bli ombedd att avstå från att ta din Parkinsonmedicin före de två PET undersökningarna (besök 8 och 18). Din studieläkare kommer att diskutera detta med dig. Under studien kommer olika undersökningar, scanningar, tester och skattningar med skalor att utföras för att kartlägga din hälsa och dina symtom: Generella undersökningar Vid varje besök kommer du att tillfrågas om du har haft några hälsoproblem eller gjort några förändringar i din medicinering sedan det senaste besöket. Läkarundersökningar kommer att genomföras vid ett flertal tillfällen och din puls, blodtryck, temperatur och vikt kommer att mätas. EKG och blodprover tas rutinmässigt för att undersöka om du har fått någon reaktion av behandlingen. Vid första besöket kommer du att testas för HIV, hepatit B och hepatit C (om något av dessa tester är positiva kvävs att vi meddelar Folkhälsomyndigheten och smittskyddsläkaren i landstinget i enlighet med Smittskyddslagen). Om du är kvinna i fertil ålder kommer graviditetstest i form av urinprov att göras. Sida 4 av 18
5 Symtom och tecken på Parkinsons sjukdom För att se eventuella förändringar av dina symtom av Parkinsons sjukdom kommer de att graderas med hjälp av ett antal olika tester: Patientdagbok: Under studiens gång kommer du att bli ombedd att fylla i en patientdagbok genom att kryssa i ett av fyra alternativ för att dokumentera din rörlighet och tid i sömn. Du ska dokumentera din rörlighet varje vaken halvtimme under 24 timmar per dag, i tre hela dagar före åtta av studiebesöken (screening, alla sex doseringsbesöken och uppföljningsbesöket). Parkinsons KinetiGraf (PKG ): Under studiens gång kommer du att få bära en Parkinsons KinetiGraf (PKG ). PKG bärs på handleden, precis som en klocka och dokumenterar dina rörelser under flera dagar. PKG mätaren kommer att skickas hem till dig cirka 10 dagar före ditt nästkommande besök och du kommer att bära PKG mätaren dag och natt under sex sammanhängande dagar före varje doseringsbesök samt uppföljningsbesöket. Frågeformulär och skalor: Graden på dina symtom kommer att graderas med hjälp av ett antal frågeformulär. Du kommer att få besvara frågor om din livskvalitet, ditt humör, minne, impulskontroll och mentala hälsa. Graden av din sjukdom kommer att mätas med hjälp av en skala. För att kunna utvärdera dina symtom utan påverkan av din Parkinsonsmedicin blir du ombedd att inte ta dina mediciner upp till 24 timmar innan vissa av testerna, tidsramen beror på vilken typ av medicin du tar(så kallat OFF ). Din studieläkare kommer att diskutera detta med dig. Svårighetsgraden på din sjukdom kommer därefter att utvärderas baserat på vissa skalor. Så snart testet är färdigt kommer du att få ta dina mediciner som vanligt. Andra undersökningar Portbedömning: Vid varje besök efter operationen, förutom vid PET besöken, kommer studiepersonalen att undersöka porten och huden som omger den. Om en hudreaktion har uppkommit vid porten kommer studiepersonalen att ta en bild på porten och den omgivande huden. Du kommer även att tillfrågas om du har följt instruktionerna för rengöring av porten och om silikonlocket har fallit av. Ryggmärgsvätska (CSF) från ryggmärgsvätskeprov: Ryggmärgsvätska är den vätska som omger din ryggrad och hjärna. CSF prov tas vid två tillfällen (besök 9 och 16) och testas för säkerhetsuppföljning, för att mäta CDNF nivån samt för att se hur din kropp reagerar på CDNF. Provet tas genom en nål in i ryggraden. Provtagningen görs under lokalbedövning men kan också göras när du är sövd om det inte är möjligt för dig att ligga eller sitta still under provtagningen. Du kommer att få ligga ner en kort stund efter provtagningen. Magnetisk resonanstomografi (MRI/magnetröntgen av huvudet): Om du inte gjort någon magnetröntgen inom 6 månader före studiestart kommer du ombes att genomgå en röntgen för att se att det inte finns något som kan förhindra att du deltar i studien. Du kommer sedan, under studiens gång, genomgå magnetröntgen före operationen och vid tre ytterligare tillfällen i samband med testinfusionerna, se nedan. Under undersökningen kommer du att få ligga på en brits som kommer att åka in i MRI maskinen där ett magnetiskt fält startas. Vid den magnetröntgenundersökning som görs före operationen kommer du att sövas. Under de övriga MRI undersökningarna kommer du att vara vaken, det är viktigt att du ligger still under tiden undersökningen pågår. Positronemissionstomografi (PET) PET är en bildteknik som genomförs med hjälp av en radioaktiv substans, en så kallad radioligand. Genom att injicera en väldigt liten mängd av denna radioligand i ett blodkärl i din arm når radioliganden din hjärna via blodbanan. PET kameran mäter sedan fördelningen av radioliganden i din hjärna. Mätningarna visas som bilder och genom att jämföra bilder innan och efter att du fått Sida 5 av 18
6 studieläkemedlet/placebo kan man beräkna mängden nervceller som producerar dopamin. I denna studie används radioliganden [ 18 F]FE-PE21. Under PET undersökningarna kommer du att ligga på en bänk med ditt huvud inne i PET maskinen. Du kommer att ha kontakt med studiepersonalen under hela undersökningen. Eftersom undersökningen kräver att du ligger helt stilla i samma position kommer det att tillverkas en hjälm för fixering av ditt huvud. Denna hjälm ser ut ungefär om en hockeyhjälm. Datortomografi (DT) DT är en röntgenteknik där flera små röntgenstrålar riktas genom din kropp från flera olika vinklar. Under undersökningen kommer du att ligga på en brits som åker in i röntgenmaskinen. Ett röntgenrör roterar runt din kropp och skickar röntgenstrålar i flera vinklar genom din kropp. Studiebesök Under studiens gång kommer du att besöka kliniken för totalt 18 besök (19 besök om du är en av de två första patienterna i studien eller om det vid den första testinfusionen vid besök 6 finns indikationer på att en av katetrarna är blockerade och du därmed behöver en extra placeboinfusion). De olika undersökningarna, testerna och utvärderingarna som kommer att göras beskrivs nedan i detalj. Vänligen läs igenom detta noggrant. Besök 1 och 2: Screening (ungefär 8 veckor innan operation) Syftet med besöket är att se om du uppfyller kraven för att få delta i studien. Först om du samtycker till att delta kommer du att få signera ett samtyckesformulär. Därefter kommer du att genomgå en hälsoundersökning och EKG, blodtryck, puls, kroppstemperatur, vikt och längd kommer att mätas. Du kommer att få besvara frågor om din livskvalité, ditt humör, minne, impulskontroll och mentala hälsa. En magnetröntgenundersökning kommer att göras på en separat dag om du inte har gjort en sådan undersökning inom 6 månader före besök 1. Om du är en kvinna i fertil ålder kommer du att få lämna ett graviditetstest i form av urinprov. Du kommer att få träning i hur du fyller i dagboken och få med dig dagboken hem för att fylla i under tre sammanhängande dagar före besök nummer två. Du kommer även att få med dig PKG mätaren hem som du bär sex dagar före besök nummer två. På besök två ska du komma dagen innan och stanna på kliniken eller patienthotellet över natten. Du ombeds att avstå från din anti- Parkinsonsmedicin enligt de instruktioner du får från din studieläkare. Följande dag kommer dina symtom för Parkinsons sjukdom att graderas med hjälp av skalor. När testet är färdigt kommer du att få ta Levodopa medicin och tester kommer att göras för att se hur väl du svarar på denna. Ditt blodtryck och puls kommer att mätas och du kommer tillfrågas om du har haft några besvär med hälsan sedan det senaste besöket. Besök 3: Planering av operationen Ungefär fyra veckor innan din planerade operation kommer du på ett besök till sjukhuset där operationen kommer att genomföras. Under besöket träffar du de neurokirurger som kommer att utföra operationen och även en narkosläkare. Den planerade operationen kommer att förklaras för dig. Du kommer även få lämna blod- och urinprov samt lämna ett graviditetstest i form av urinprov om du är kvinna i fertil ålder. Du kommer att tillfrågas om du haft några besvär med hälsan eller om du gjort några förändringar i din medicinering sedan senaste besöket. En magnetröntgenundersökning kommer att göras som kommer att användas för planering av operationen. Under undersökningen kommer du att vara sövd. Sida 6 av 18
7 Besök 4: Operation Under detta besök kommer du att läggas in på sjukhuset för att genomgå operationen för att implantera administreringssystemet för studieläkemedlet/placebo. Dagen före operationen kommer du att behöva lämna blod- och urinprov en vikt kommer också att tas. Om du är kvinna i fertil ålder kommer du att få lämna ett graviditetstest i form av urinprov. Du kommer att vara sövd under operationen. En metallram av aluminium kommer att fästas på ditt huvud för att kunna vägleda roboten under operationen. Kroppstemperatur, blodtryck och puls kommer att mätas vid flera tillfällen. En datortomografiundersökning kommer att utföras av ditt huvud efter att ramen satts fast och bilden kommer att användas för att göra den sista delen av målpunktsplaneringen införoperationen. Ytterligare en datortomografi kommer att göras efter att operationen är genomförd för att säkerställa att kateterna har placerats på rätt sätt i hjärnan. Läkaren som genomför operationen kan även besluta att genomföra ytterligare en datortomografiundersökning under operationen för att bekräfta att kateterna sitter rätt innan operationen avslutas. För att placera katetrarna borras fyra hål i skallbenet och katetrarna sätts på plats i hjärnan med hjälp av guiderör. Denna typ av operation är baserad på Djup Hjärnstimulering (DBS), som är en väletablerad operationsmetod som används för att behandla patienter med Parkinsons sjukdom. Katetrarna kopplas sedan till en port som sätts fast bakom ditt öra. Porten fästs i skallbenet med hjälp av benskruvar. Huden bakom örat samt benet där porten ska fästas kommer att försänkas i benet för att porten inte ska stå ut för mycket och minimera risken att området blir inflammerat. Du kommer att stanna på sjukhuset i ungefär 4 dagar efter operationen. Om datortomografiundersökningen efter operationen indikerar att katetrarna inte placerats korrekt eller om den första testinfusionen (se besök sex) indikerar att katetrarna är blockerade, kan en andra operation bli nödvändig innan man startar med infusion av studieläkemedlet/placebo. Besök 5: Uppföljning efter operationen Ungefär 2 veckor efter operationen kommer du tillbaka till kliniken för att kontrollera sårläkning och ta bort stygnen samt lämna blod- och urinprov. Din port och den omgivande huden kommer att undersökas. Om du är kvinna i fertil ålder får du lämna ett graviditetstest i form av urinprov. Du kommer att tillfrågas om du haft några besvär med hälsan eller om du gjort några förändringar i din medicinering sedan senaste besöket. Besök 6, 13 och 17: Testinfusioner Administreringssystemet kommer att funktionstestas tre gånger under studiens gång. Första testet kommer att göras före den första infusionen med studieläkemedlet/placebo, andra testet görs före den fjärde infusionen och sista testet görs efter att den sjätte dosen studieläkemedel/placebo har getts. Vid dessa tester kommer kontrastmedlet Gadolinium att ges genom administreringssystemet. Magnetröntgen kommer att göras innan och efter infusionen för att kontrollera att kontrastmedlet sprids så som det är tänkt i hjärnan och bekräfta att katetrarna inte är blockerade. Under besöken kommer ditt blodtryck och puls att mätas vid ett flertal tillfällen före, under och efter infusionen. Din port och den omgivande huden kommer att undersökas. Du kommer också att tillfrågas om du haft några besvär med hälsan eller om du gjort några förändringar i din medicinering sedan senaste besöket. Vid den första testinfusionen på besök sex kommer blod- och urinprov att tas. Studiepersonalen kommer att kontakta dig via telefon 1-2 veckor efter testinfusionen för att fråga om du haft några besvär med din hälsa. Sida 7 av 18
8 Besök 7: Infusion med placebo Om du är en av de två första patienterna i studien, eller om det vid första testinfusionen, på besök 6, indikerats att en kateter är blockerad, kommer du att få en infusion med placebo före det bestäms vilken behandlingsgrupp du kommer att tillhöra. Under detta besök kommer du att få lämna blodoch urinprov. Ditt blodtryck och puls kommer att mätas vid ett flertal tillfällen. Din port och den omgivande huden kommer att undersökas. Du kommer att tillfrågas om du haft några besvär med hälsan eller om du gjort några förändringar i din medicinering sedan senaste besöket. Studiepersonalen kommer att kontakta dig via telefon 1-2 veckor efter infusionen för att fråga om du haft några besvär med din hälsa. Din studieläkare kommer att informera dig om du kommer att genomföra detta besök. Besök 8 och 18 PET undersökning En PET undersökning kommer att genomföras före första dosen och efter sista dosen av studieläkemedlet/placebo. Under PET undersökningarna kommer ditt huvud placeras i en hjälm specialgjord för dig. Under båda PET undersökningarna kommer du att ombes att avstå från din anti- Parkinsonmedicin under minst 10 timmar beroende på vilken typ av medicin du tar. Din studieläkare kommer att diskutera detta med dig. Förutom PET undersökningen kommer ditt blodtryck och puls mätas. Du kommer att tillfrågas om du haft några besvär med hälsan eller om du gjort några förändringar i din medicinering sedan senaste besöket. En PET undersökning tar ungefär en timme. En PET undersökning kan bli försenad eller inställd på grund av tillverkningen av radioliganden eller andra tekniska problem. Schemat kommer då att anpassas från fall till fall efter att detta har diskuterats med dig. Om du behöver ta någon typ av anti-parkisonmedicin under besöket kommer detta att dokumenteras. I Sverige kommer PET undersökningarna att göras på PET centret på Karolinska sjukhuset i Solna (Stockholm). Beroende på var du bor kan du behöva åka till Stockholm dagen före undersökningen och bo på hotell över natten. Besök 9: Utgångsvärde och randomisering En vecka innan start av behandlingen i studien kommer du att besöka kliniken och graden av dina sjukdomssymtom mätas med olika skattningsskalor och frågeformulär. Du kommer att bli ombedd att inta en fettsnål frukost och lunch under detta besök. En hälsoundersökning kommer att göras och blod- och urinprov tas. Det kommer även att tas ryggmärgsvätskeprov och EKG. Din port och den omgivande huden kommer att undersökas. Du kommer att tillfrågas om du haft några besvär med hälsan eller om du gjort några förändringar i din medicinering sedan senaste besöket. Om du är kvinna i fertil ålder kommer du att få lämna ett graviditetstest i form av urinprov. Efter att alla bedömningar har genomförts kommer du att få bo över natten på kliniken eller patienthotellet. För att kunna utvärdera dina symtom utan påverkan av din Parkinsonsmedicin blir du ombedd att inte ta dina mediciner innan testet (så kallat OFF ). Dagen efter kommer din studieläkare att bedöma dina Parkinsonssymtom. Så snart bedömningen är gjord får du ta din anti-parkinsonmedicin igen. När alla bedömningar är gjorda kommer din studieläkare att besluta om du uppfyller kraven och om det är säkert för dig att delta i studien. Innan du lämnar kliniken kommer du att få med dig en dagbok hem för att fylla i tre dagar innan första doseringsbesöket. Du kommer även att få en PKG mätare som du ska bära sex dagar innan det första doseringsbesöket. Besök 10 och 11: Första doseringsbesöket Resultaten från PKG mätaren kommer att samlas in vid dessa besök. Du kommer även att få lämna blod- och urinprov och om du är kvinna i fertil ålder får du lämna ett graviditetstest i form av Sida 8 av 18
9 urinprov. Du kommer att få lämna in dagboken som du fyllt i under tre dagar före besöket och du kommer att få en ny dagbok hem att fylla i tre dagar innan kommande doseringsbesök. Din port och den omgivande huden kommer att undersökas. Du kommer också att tillfrågas om du har haft några besvär med hälsan eller om du har gjort några förändringar i din medicinering sedan senaste besöket. Vid besök 11 kommer din mentala hälsa att utvärderas med hjälp av en skala. En dos av studieläkemedlet eller placebo kommer att ges. Ditt blodtryck och puls kommer att mätas vid flera tillfällen både innan, under och efter dosering. Som en säkerhetsåtgärd kommer du att få stanna på kliniken 24 timmar efter att studieläkemedlet/placebo getts vid båda dessa besök.. Studiepersonalen kommer att kontakta dig via telefon 1-2 veckor efter besöket för att fråga om du haft några besvär med din hälsa eller om du gjort några förändringar i din medicinering sedan senaste besöket. PKG mätaren kommer att skickas hem till dig cirka 10 dagar innan nästa studiebesök och du kommer att bära den i sex dagar innan ditt kommande besök. Besök 12 och 14-16: Doseringsbesök (studieläkemedel/placebo): Du kommer till kliniken var fjärde vecka för att få behandling med studieläkemedlet eller placebo. PKG mätaren kommer att skickas hem till dig cirka 10 dagar innan respektive besök och du kommer att bära den i sex dagar innan varje doseringsbesök. Resultaten från PKG mätaren kommer att samlas in vid dessa besök. Du ska ta med dig dagboken som du fyllt i under tre dagar före varje besök och du kommer att få med dig en ny dagbok hem för att fylla i tre dagar innan nästkommande doseringsbesök. Under besöket kommer ditt blodtryck och din puls att mätas vid flera tillfällen både innan, under och efter dosering. Du kommer att få lämna blod- och urinprov. Din port och den omgivande huden kommer att undersökas och du kommer att tillfrågas om du haft några besvär med hälsan samt om du har gjort några förändringar i din medicinering sedan senaste besöket. Om du är kvinna i fertil ålder kommer du att få lämna ett graviditetstest i form av urinprov. Vid besök 12 och 16 kommer du att bli ombedd att inta en fettsnål frukost och lunch. Vid besök 14 blir du ombedd att komma till kliniken dagen före doseringen. Efter att ovan utvärderingar, skalor och frågeformulär (om din livskvalité, humör, minne, impulskontroll och mentala hälsa) har gjorts och ett EKG har utförts kommer du att få stanna över natten på kliniken eller på patienthotellet och under denna tid vara utan din Parkinsonsmedicin. Dagen efter kommer din studieläkare att bedöma dina Parkinson symtom. För att kunna utvärdera dina symtom utan påverkan av din Parkinsonsmedicin blir du ombedd att inte ta dina mediciner innan testet (så kallat OFF ). Så snart bedömningen är gjord får du ta din medicin igen. Vid besök 16 kommer det att tas ryggmärgsvätska genom ryggmärgvätskesprov. Efter att dessa utvärderingar genomförts kommer studieläkemedlet eller placebo att ges. Besök 19: Uppföljningsbesök Cirka 10 dagar innan besök 19 kommer PKG mätaren att skickas hem till dig och du kommer att bära den i sex dagar innan detta besök. Resultaten från PKG mätaren kommer att samlas in vid besöket. Du kommer till kliniken cirka fyra veckor efter ditt sista doseringsbesök. Under första dagen på detta besök kommer du att få lämna blod- och urinprov, genomgå ett EKG samt besvara ett antal skalor och frågeformulär (om din livskvalité, humör, minne, impulskontroll och mentala hälsa). Om du är kvinna i fertil ålder kommer du att få lämna ett graviditetstest i form av ett urinprov. Du kommer även att få lämna tillbaka den dagbok som du har fyllt i under tre dagar innan besöket. Du kommer att tillfrågas om du haft några besvär med hälsan och om du gjort några förändringar i din medicinering sedan senaste besöket. Efter att ovan utvärderingar har gjorts kommer du att få stanna över natten på kliniken eller på patienthotellet. För att kunna utvärdera dina symtom utan påverkan av din Parkinsonsmedicin blir du ombedd att inte ta dina mediciner (så kallat OFF ). Dagen efter kommer din studieläkare att göra en hälsoundersökning samt bedöma dina Parkinsonsymtom med hjälp av funktionstest. Din port och den omgivande huden kommer att undersökas. Sida 9 av 18
10 Restriktioner under studiens gång Eftersom det inte finns någon information om hur porten reagerar om du badar bastu rekommenderar vi att du inte bastar under studiens gång tills porten har tagits bort. Du kan simma i sjöar, åar eller havet eller bada som du vanligtvis gör såvida huden runt porten inte blir infekterad. Bada i pool eller dyka rekommenderas inte. Du rekommenderas att alltid ha silikonlocket på porten och rengöra det regelbundet. Du kommer att få instruktioner på hur du ska rengöra porten. Du bör inte köra bil eller använda maskiner förrän efter 24 timmar efter att doseringen av studieläkemedlet/placebo och Gadolinium är gjord. Under studien kan du fortsätta med din medicinering av din anti-parkinsonsmedicin. Det finns dock några mediciner som du inte ska ta eller kan behöva avslutas under tiden du är med i denna studie. Diskutera med din studieläkare innan du tar några mediciner inkluderat örtmediciner och vitaminer. Vid besök 9, 12 och 16 kommer speciella blodprover att tas inför dessa kommer du bli ombedd att inta en fettsnål frukost och lunch. Frivilligt deltagande Ditt deltagande i denna studie är helt frivilligt. Om du beslutar dig för att delta kan du när som helst under studiens gång välja att avsluta studien utan någon ytterligare förklaring. Om du väljer att inte delta eller att avsluta studien i förtid kommer detta inte att påverka din nuvarande eller framtida vård. Om du väljer att gå ur studien kommer du bli ombedd av säkerhetsskäl att genomgå ett uppföljningsbesök som innebär en läkarundersökning samt provtagning. Ditt deltagande i studien kan avbrytas när som helst av den ansvarige studieläkaren eller sponsor på grund av något av följande skäl: Administreringssystemet kunde inte implanteras på korrekt sätt eller att katetrarna inte fungerar för att ge studieläkemedlet/placebo Ditt fortsatta deltagande i studien anses vara skadligt för dig Det anses inte vara det bästa för dig att fortsätta i studien Sponsorn stoppar studien på grund av säkerhets- eller vetenskapliga skäl Om ditt deltagande i studien avslutas efter att porten och administreringssystemet implanterats kommer du att kontaktas var tredje månad. Du kommer då att tillfrågas om du har haft några besvär med din hälsa. Du kommer också att uppmanas att ta kontakt med studiepersonalen om du upplever några besvär med administreringssystemet, porten eller om du blir inlagd på sjukhus. Du kommer att följas upp av din läkare var 3:e månad efter behandlingens sluttill det att det implanterade systemet och porten har tagits bort eller om du samtycker till att delta i en uppföljningsstudie. Vad händer om det kommer fram ny relevant information under studiens gång? Din ansvariga studieläkare och sponsorn är tvungna att berätta för dig om det kommer fram ny information under studiens gång som kan påverka ditt beslut att fortsätta delta. Din studieläkare kommer då att diskutera detta med dig och kan möjligen besluta att det är bäst för dig att avbryta ditt deltagande i studien. Om det är nödvändigt kan hela studien avbrytas. Vad händer efter studiens slut? Du och din studieläkare kommer att diskutera vad som är bäst behandling för dig i god tid innan studien är slut. Du kommer att informeras om vilka möjligheter som finns för den bästa och mest effektiva behandlingen för din Parkinsons sjukdom. Sida 10 av 18
11 Det implanterade systemet, förutom den port som sitter under huden kommer att sitta kvar i din hjärna efter studiens slut, såvida det inte finns medicinska skäl eller om du ber om att det ska tas bort. Det implanterade systemet hindrar inte eventuella framtida operationer för behandling av Parkinsons sjukdom, till exempel Djup hjärnstimulering, (DBS) efter studiens slut. Sponsorn planerar att utföra ytterligare studier efter att denna studie är slutförd. I den första förlängningsstudien planeras att ytterligare sex doser av studieläkemedlet ska ges till personer som genomfört behandlingen med antingen studieläkemedlet eller placebo. Förlängningsstudien planeras att följas av en studie som innebär långtidsuppföljning av inkluderade patienter. Dessa studier är just nu i planeringsstadiet och behöver få godkännande av både Läkemedelsverket och Etikprövningsnämnd innan de kan starta. Ytterligare information kommer då att ges till dig och du kommer att få signera ett nytt informerat samtycke. Vad finns det för alternativ till studiebehandlingen? Din studieläkare kommer att diskutera tillgängliga behandlingsmetoder inklusive de fördelar och risker de innebär. Ditt deltagande i denna studie kommer inte att påverka din nuvarande behandling av Parkinsons sjukdom och du kommer att fortsätta med din nuvarande medicin. Dock är det inte tillåtet att du tar något annat studieläkemedel eller behandlas med någon medicinteknisk produkt (som inte är godkänd för medicinskt bruk) under denna studies gång. Det finns även mediciner som du inte får ta under studiens gång. Din studieläkare kommer att diskutera dessa mediciner med dig. Vad finns det för risker/obehag? Möjliga risker med operationen för implantatet Under operationen och under magnetröntgen innan operationen kommer du att vara nedsövd vilket är förenat med vissa risker. Operationen kan orsaka huvudvärk, vävnadsdöd, svullnad, blödning och/eller infektion av hjärnan, hårbottnen och huden och skallbenet runt porten. Om du skulle få en infektion kan du behöva behandlas med antibiotika. Blödning kan orsaka mer eller mindre allvarliga symtom såsom epileptiska anfall, förlamning, koncentrationssvårigheter, minnesförlust, talförlust eller förlust av annan hjärnfunktion. Det finns en risk för blåmärken på hjärnvävnaden under operationen vilket kan leda till stroke och/eller förlamning av en av dina kroppshalvor. Katetrarna kan bli placerade på ett annat ställe än vad som är planerat och på grund av detta kan studieläkemedlet/placebo hamna på fel ställe i hjärnan. Undersökningarna med CT röntgen i samband med operationen samt första infusionen med Gadolinium kommer att utföras för att bekräfta rätt position och funktion av katetrarna innan den första dosen med studieläkemedle ges. Om neurokirurgen inte anser att katetrarna sitter rätt kan en andra operation behövas för att placera katetrarna rätt. Neurokirurgerna som deltar i studien är speciellt utbildade och erfarna i att utföra operationer på hjärnan. Magnetröntgen- och DTundersökningarna kommer att hjälpa neurokirurgerna när de planerar operationen och speciella verktyg kommer att användas för att minska risken att man borrar igenom hjärnlager under skallbenet. Risken för blödning och skador på hjärnan som konsekvens av placeringen av katetrarna i hjärnan kan bäst jämföras med en operation för att placera elektroder för Djup hjärnstimulering, (DBS) hos patient med Parkinsons sjukdom. I en studie med 214 deltagare drabbades ungefär 1 av 100 patienter (1 %) av blödning i hjärnan efter att katetrarna satt på plats med hjälp av guidning från bilder. Inga av dessa fall resulterade i permanenta neurologiska symtom eller död som en orsak av blödningen. Om katetrarna inte kan opereras in i rätt läge, eller om du får blödningar i hjärnan efter operationen, kan det bedömas att inte vara möjligt att ge dig behandling med CDNF eller placebo. I dessa fall Sida 11 av 18
12 kommer porten att opereras bort. Läkaren bedömer då i samråd med dig om det är nödvändigt att också operera bort de inopererade katetrarna Möjliga risker med administreringssystemet Portens design är likvärdig den som används vid hörapparater (Baha) och kan orsaka inflammation och lokal hudirritation. Det finns även en risk att porten lossnar vilket kan öka risken för dessa biverkningar. Om porten lossnar kan den ibland fästas igen men i vissa fall kan den behöva tas bort. Blodflödet i huden över administreringssystemet kan minska vilket kan resultera i degenerering och irritation av huden. Din kropp kan även reagera på materialet i administreringssystemet. Det finns en risk för infektion i hjärnan, hårbotten och huden runt porten vid varje dostillfälle. Lokala infektioner kan behandlas med steroider och/eller antibiotika. Studieläkarna och annan studiepersonal kommer att tränas i hur de ska ge infusionen av studieläkemedlet/placebo och Gadolinium för att minska risken för infektioner. Om en av katetrarna är (delvis) blockerad kan det vara möjligt att ge studieläkemedlet/placebo genom den andra katetern, detta kommer dock att öka tiden för infusionen eftersom mängden läkemedel i en kateter kommer att öka. Om två katetrar i samma putamen är blockerade är inte dosering i denna putamen möjlig och den andra putamen kommer endast att doseras med hälften av den totala dosen. Det är viktigt att porten rengörs dagligen. Du kommer att få instruktioner om hur du ska göra detta. Möjliga risker och obehag med PET undersökningen Vid PET centrat i Solna, Sverige, har det utförts mer än 5000 PET undersökningar och erfarenhet visar att dessa tolereras väl. Under PET undersökningen kommer ditt huvud att placeras i en hjälm, vilket kan kännas obehagligt med tryck på huvudet. Detta kan avhjälpas med att minska trycket eller vaddera hjälmen. Under undersökningen, vilket tar ungefär en timme, kommer du att ligga på rygg på en brits vilket kan orsaka stelhet i ryggen och vara fysiskt obehagligt. Detta kan avhjälpas genom att ändra positionen på britsen. Radioliganden [ 18 F]FE-PE2I har tidigare administrerats till 15 patienter med Parkinsons sjukdom och 14 kontrollpatienter utan några säkerhetsproblem. Spårämnet avger en liten mängd strålning som motsvarar den genomsnittliga stråldos en person bosatt i Sverige erhåller från omgivningen under 2.5 år. Deltagande i studien medför exponering för joniserande strålning. Denna studie har godkänts av strålskyddskommittén vid Karolinska Universitetssjukhuset i Solna. Möjliga risker med CDNF CDNF är ett studieläkemedel som aldrig tidigare har getts till människa. Därför känner man inte till alla biverkningar. Om man dessutom tar mediciner i kombination med studieläkemedlet kan det uppstå biverkningar och risker som kan vara svåra att förutspå. Det är därför viktigt att du informerar din studieläkare och/eller din studiesjuksköterska om eventuella biverkningar du får under studien oavsett om du tror att de beror på studieläkemedlet eller inte. I djurstudier har man inte sett några biverkningar relaterade till CDNF. Behandling med andra neurotrofiska faktorer hos människor har orsakat en pirrande känsla som av nålar eller smärta, Lhermittes tecken (en elektrisk ilning längs ryggen och ut i armar och ben), aptitlöshet, viktminskning, illamående, kräkningar, låg nivå av natrium i blodet och magproblem (diarré, förstoppning). Under studiens gång kommer du att kontrolleras för eventuella biverkningar. Möjliga risker med Gadolinium som används för testinfusionerna och operationsförberedande magnetröntgen Under den planläggande magnetröntgen kommer Gadolinium att användas som kontrastmedel. Det kommer vid detta besök att injiceras i en ven (blodkärl) och dosen baseras på din kroppsvikt. Sida 12 av 18
13 Gadolinium är godkänt på marknaden för att användas på detta vis. Biverkningar kopplat till Gadolinium efter att det administrerats på detta sätt är: yrsel, huvudvärk, kräkningar, illamående, förändringar i smakupplevelse, känsla av att frysa eller vara varm och reaktioner vid injektionsstället. Hypersensivitet och allvarliga allergiska reaktioner kan inträffa i ovanliga fall. Man har noterat en ökad ansamling av Gadolinium i vävnader då man har gett upprepade höga doser av preparatet. Denna påverkan har framförallt noterats hos patienter med nedsatt njurfunktion. En liten mängd av Gadolinium kommer även att användas som kontrastmedel under testinfusionerna. Under dessa undersökningar kommer det att ges in i hjärnan via det inopererade administreringssystemet. Detta administreringssätt har tidigare testats på 15 vuxna och tre barn under experimentella förhållanden men har ännu inte blivit godkänt av myndigheter. Därför är inte alla biverkningar av Gadolinium som administreras på detta sättkända. Du kommer att få tre infusioner med Gadolinium under studien. Din studieläkare kan besluta om att ge ytterligare en infusion med Gadolinium om katetrarna behöver justeras. Du kommer att övervakas noggrant under två timmar efter varje Gadoliniuminfusion. Övriga risker/obehag I samband med undersökningar Blodprov: Kan vara obehagligt, smärtsamt och orsaka blåmärken, ge svullnad eller inflammation. Vi kommer under studiens gång att ta blodprover vid 14 tillfällen till en sammanlagd blodvolym av 350 ml under 10 månader. Detta kan jämföras med 450ml som ges vid en vanlig bloddonation. Ryggmärgsvätskeprov för ryggmärgsvätska: Den vanligaste biverkan är mild huvudvärk som kan hålla i sig i några timmar upp till ett par dagar. Huvudvärken kan i vissa fall vara mer allvarlig och man kan drabbas av yrsel, stel nacke eller öronsus. Provtagningen orsakar sällan stort obehag. Ryggmärgsvätska kommer att tas vid två besök (besök 9 och 16) och 10 ml kommer att tas vid varje tillfälle. Magnetröngen (MR): Du kommer att behöva ligga helt stilla i ungefär 40 minuter. Kameran är liten vilket kan uppfattas som obehagligt om du har anlag för klaustrofobi. Kameran är högljudd och du kan därför få bära hörselskydd. Magnetröntgen genomförs på fem besök (besök 1, 3, 6, 13 och 17). CT: Undersökningen innebär att du blir utsatt för en liten mängd strålning. Under operationen kan två, max tre röntgenundersökningar göras. Varje CT undersökning kommer att utsätta dig för strålning motsvarande 1 års bakgrundsstrålning under normala levnadsförhållanden. Uppehåll i din medicinering för Parkinsons sjukdom: Vid PET undersökningen (besök 8 och 18) samt vid besök 2, 9, 14 och 19 görs undersökningar (rörelsefunktion och L-dopa test) när du inte har tagit din normala medicindos på minst 10 timmar beroende på vilken typ av medicin du tar. Att vara utan din normala medicin (så kallat OFF ) kan förvärra dina symtom av Parkinsons sjukdom. Så snart undersökningarna har gjorts kommer du att få ta din vanliga medicindos, men det kan ta lite tid innan du känner dig stabil igen. Potentiell risk för kvinnor i fertil ålder: Kvinnliga deltagare: Risken för barn och mamma vid behandling av studieläkemedlet under graviditet är inte känd. Gravida kvinnor eller kvinnor som vill bli gravida kan därför inte delta i denna studie. Kvinnor i fertil ålder måste därför använda ett mycket effektivt preventivmedel för att förhindra graviditet under och även 30 dagar efter denna studies avslutande. Din studieläkare kommer att diskutera detta med dig. Om du blir gravid under eller efter behandling med studieläkemedlet måste du diskutera riskerna och vilka åtgärder som behöver vidtas, med din studieläkare. Det är inte känt om CDNF utsöndras i bröstmjölk därför kan man inte amma under studiens gång. Sida 13 av 18
14 Manliga deltagare: Om du är man och har en partner som kan bli gravid ska du använda kondom och inte donera spermier förrän tidigast 3 månader efter varje PET undersökning. Du behöver informera din studieläkare om din partner blir gravid under studiens gång. Om du har en kvinnlig partner behöver hon vara villig att använda ett mycket effektivt preventivmedel till och med 3 månader efter din sista PET undersökning.. Din studieläkare kommer att diskutera detta med dig. Vilka är de eventuella fördelarna? Syftet med denna studie är att utvärdera säkerheten och tolerabiliteten av studieläkemedlet och administreringssystemet. En möjligt positiv effekt av behandling hos Parkinsons sjukdom kommer att utvärderas men det är dock inte säkert att du kommer att ha någon fördel med att vara med i denna studie. Insamlad data kommer att ge mer kunskap om studieläkemedlet och administreringssystemet och kan komma att bidra till utvecklingen av ett nytt läkemedel för att behandla Parkinsons sjukdom. Data från denna studie kan komma att gagna patienter med Parkinsons sjukdom i framtiden. Hantering av blod- och ryggmärgsvätska Huvuddelen av proverna som tas under studiens gång är rutinprover. Dessa kommer att analyseras direkt när de tas på sjukhusets laboratorium och sedan destrueras. HIV, hepatit B och hepatit C sparas rutinmässigt på sjukhuset. Övriga prover tagna i studien kommer att sparas i en biobank med referensnummer 164 som TFS, Trial Form Support, ansvarar för. Blod och ryggmärgsvätska kommer att analyseras för att se om din kropp reagerar på studieläkemedlet och hur läkemedlet fördelar sig från hjärnan. Dessa prover kommer att skickas till laboratorier i Finland och Qatar, som har en annan dataskyddsnivå än inom EU/EES, för förvaring i väntan på analys i högst 5 år. Proverna kan komma att kasseras tidigare. Proverna kommer endast att användas på det sätt som beskrivs i denna patientinformation. Proverna märks med en unik kod för att undvika förväxling. De kan endast kopplas till dig genom en kodnyckel som endast studieläkaren och annan behörig studiepersonal har tillgång till. Du har rätt att begära att dina prover kasseras utan ytterligare förklaring. Lagen om biobanker i hälso- och sjukvården (2002:297) reglerar hur insamlade prover kan förvaras och användas och reglerar kvalitet och säkerhet för biobanker. Hantering av personuppgifter Under operationen kommer personal från Renishaw Plc att vara närvarande i operationssalen för att stötta neurokirurgerna. De kommer först när du är sövd så du kommer inte att träffa dem. Renishawanställda kommer också vara närvarande på kliniken för att stötta studiepersonalen vid infusionerna, de kan behöva se dina personuppgifter såsom ditt namn, men inga personuppgifter kommer att samlas in av dem. Du kommer att videofilmas när ett av utvärderingstesten genomförs för att bedöma ditt sjukdomstillstånd. Bandet kommer att användas i säkerhetskopieringssyfte och kommer inte att lämna kliniken om du inte får information och ger tillstånd för detta. Ett skriftligt godkännande från myndighet och/eller Etikprövningsnämnd kommer också att behövas innan vi kan be om din tillåtelse att skicka iväg bandet. Dina uppgifter, fotografier tagna om en hudreaktion har uppkommit vid porten och röntgenbilder som samlas in i studien behandlas anonymt och är endast försedda med en patientkod. Din studieläkare förvarar en kodlista som tillåter identifiering av dig personligen som endast studiepersonalen har tillgång till. Under studiens gång kommer vi att samla in uppgifter om födelsedatum, kön, etnisk tillhörighet, hälsodata (såsom nuvarande och tidigare sjukdomar) samt Sida 14 av 18
15 resultat av undersökningarna i studien inklusive bilder från magnetröntgen och PET. Insamlade uppgifter inklusive magnetröntgen, fotografier på eventuella hudreaktioner vid portenoch PET bilder kommer att överföras i kodad form, utan ditt namn eller personnummer, till sponsorn, Herantis Pharma Plc, för analys samt till sponsorns samarbetspartners såsom Renishaw Plc och TFS, Trial Form Support AB. Denna information är avidentifierad och kommer inte att raderas efter att du har avslutat ditt deltagande i studien. Insamlad data kommer att förvaras, behandlas och sammanställas manuellt och elektroniskt av TFS, Trial Form Support, Herantis Pharma Plc och Renishaw Plc. Syftet med behandling av personuppgifter är forskning och utveckling av studieläkemedlet och administreringssystemet såsom beskrivits i denna patientinformation. Syftet är också, som i fallet med Renishaw Plc, att få regulatoriskt godkännande för administreringssystmet. Resultat kan också komma att publiceras i medicinsk tidskrift och presenteras på neurologiska konferenser, möten och seminarier, dock utan att din identitet uppges. För angivna ändamål kan kodade uppgifter komma att överföras till andra företag som samarbetar med Herantis Pharma Plc och även till svenska och utländska myndigheter. Dessa överföringar kan ske till mottagaren såväl inom som utanför EU och även till länder som inte har samma höga skydd för behandling av personuppgifter som Sverige (t.ex USA). Alla uppgifter insamlade i studien används i enlighet med denna patientinformation och PUL (Personuppgiftslagen SFS 1998:204). En beskrivning av denna studie kommer att finnas på Denna sida kommer inte att innehålla information som kan identifiera dig. Som mest kommer sidan att innehålla en summering av resultaten som är skrivna på engelska. Du kan när som helst söka på denna sida och du kan även be om information från studiepersonalen och få tillgång till publicerad data. Om du bestämmer dig för att avbryta studien i förtid kommer uppgifter som samlats in innan du tog tillbaka ditt samtycke att fortsätta användas i utvärdering av studien och för ändamål som beskrivits ovan men inga nya uppgifter kommer att samlas in. Herantis Pharma Plc och Renishaw Plc är personuppgiftsansvariga för behandling av personuppgifter som överlämnats till dem. Du har rätt att en gång per år kostnadsfritt få veta vilka personuppgifter som har registrerats om dig, varifrån uppgifterna hämtats och vilka kategorier av mottagare de eventuellt har lämnats ut till. Du har rätt att begära att felaktiga uppgifter om dig rättas i enlighet med PUL (Personuppgiftslagen SFS 1998:204). Du kan vända dig till ansvarig studieläkare/studiesjuksköterska som hjälper dig att kontakta Herantis Pharma Plc. Tillgång till din medicinska journal För att kontrollera att studien har blivit rätt genomförd kan behöriga representanter från Herantis Pharma Plc och Renishaw Plc samt deras samarbetspartners TFS, Trial Form Support AB komma att läsa relevanta delar av din medicinska journal. Behörig representant från Läkemedelsverket (svensk kontrollmyndighet av läkemedel), etikprövningsnämnd eller utländsk läkemedelsmyndighet kan behöva tillgång till relevanta delar av din medicinska journal för att kontrollera att studien blivit rätt genomförd. Detta får ske efter godkännande av journalansvarig läkare och under förbehåll av sekretess. Positivt resultat för HIV, hepatit B eller C kommer att meddelas Folkhälsomyndigheten och smittskyddsläkaren i lanstinget i enlighet med Smittskyddslagen. Är jag försäkrad? Precis som i rutinsjukvård omfattas du av Patientförsäkringen. Herantis Pharma Plc och Renishaw Plc har även tecknat en försäkring som täcker medicinska kostnader för skada som anses orsakad av ditt Sida 15 av 18
Information till forskningsperson för studie HP-CD-CL-2003
 Studietitel Information till forskningsperson för studie HP-CD-CL-2003 En randomiserad, dubbelblind, multi-center förlängningsstudie med syfte att utvärdera säkerheten av studieläkemedlet CDNF, för patienter
Studietitel Information till forskningsperson för studie HP-CD-CL-2003 En randomiserad, dubbelblind, multi-center förlängningsstudie med syfte att utvärdera säkerheten av studieläkemedlet CDNF, för patienter
Patientinformation & Informerat samtycke PATIENTINFORMATION
 PATIENTINFORMATION Klinisk läkemedelsstudie ASA-CRCLM-2014 En multi-center, dubbel-blind, placebo-jämförande, randomiserad studie för att utvärdera säkerhet och effekt av acetylsalicylsyra eller placebo
PATIENTINFORMATION Klinisk läkemedelsstudie ASA-CRCLM-2014 En multi-center, dubbel-blind, placebo-jämförande, randomiserad studie för att utvärdera säkerhet och effekt av acetylsalicylsyra eller placebo
Information till forskningsperson
 Information till forskningsperson En dosundersökande studie i två delar utförd på friska forskningspersoner med syfte att utvärdera säkerhet, tolerabilitet och effekter med LMW-DS infusionslösning efter
Information till forskningsperson En dosundersökande studie i två delar utförd på friska forskningspersoner med syfte att utvärdera säkerhet, tolerabilitet och effekter med LMW-DS infusionslösning efter
Patientinformation och samtycke
 Sida 1 av 7 Patientinformation och samtycke Dubbelblind, placebokontrollerad fas 2 studie för att undersöka effekt, säkerhet och tolerabilitet hos studieläkemedlet Lymfactin (adenovirusmedierad lymfkärlstillvätfaktor
Sida 1 av 7 Patientinformation och samtycke Dubbelblind, placebokontrollerad fas 2 studie för att undersöka effekt, säkerhet och tolerabilitet hos studieläkemedlet Lymfactin (adenovirusmedierad lymfkärlstillvätfaktor
PATIENTINFORMATION. E-kod/Initialer:.
 PATIENTINFORMATION En placebo-kontrollerad, dubbel-blindad, randomiserad studie på patienter med typ 2-diabetes för att utvärdera om läkemedlen Epanova och dapagliflozin kan minska andelen fett i levern.
PATIENTINFORMATION En placebo-kontrollerad, dubbel-blindad, randomiserad studie på patienter med typ 2-diabetes för att utvärdera om läkemedlen Epanova och dapagliflozin kan minska andelen fett i levern.
Information till deltagare i forskningsstudien:
 Information till deltagare i forskningsstudien: En single-center studie för utvärdering av ViscoGels säkerhet samt dess säkerhet och effekt som adjuvans i Act-HIB vaccinet administrerat intramuskulärt
Information till deltagare i forskningsstudien: En single-center studie för utvärdering av ViscoGels säkerhet samt dess säkerhet och effekt som adjuvans i Act-HIB vaccinet administrerat intramuskulärt
Vill du vara med i forskningsstudien ALASCCA?
 Vill du vara med i forskningsstudien ALASCCA? Du tillfrågas härmed om du vill delta i forskningsstudien ALASCCA. Läs igenom denna information noggrant och i lugn och ro innan du bestämmer dig för om du
Vill du vara med i forskningsstudien ALASCCA? Du tillfrågas härmed om du vill delta i forskningsstudien ALASCCA. Läs igenom denna information noggrant och i lugn och ro innan du bestämmer dig för om du
Försökspersonsinformation och Samtycke
 Försökspersonsinformation och Samtycke Titel BUP1502: En öppen studie som har för avsikt att bekräfta att farmakokinetiken av plåster innehållandes buprenorfin är liknande hos äldre och yngre personer.
Försökspersonsinformation och Samtycke Titel BUP1502: En öppen studie som har för avsikt att bekräfta att farmakokinetiken av plåster innehållandes buprenorfin är liknande hos äldre och yngre personer.
Patientinformation. Denna studie har godkänts av en oberoende etikprövningsnämnd för att garantera din säkerhet och dina rättigheter.
 Patientinformation En dubbel-blind, randomiserad, placebo-kontrollerad, multicenter, klinisk fas IV-studie för att utvärdera prestanda, säkerhet och användbarhet av myrsyra på patienter med vårtor på händer,
Patientinformation En dubbel-blind, randomiserad, placebo-kontrollerad, multicenter, klinisk fas IV-studie för att utvärdera prestanda, säkerhet och användbarhet av myrsyra på patienter med vårtor på händer,
Patientinformationsblad för studien PPL07
 Prövningstitel: Studie för att utvärdera effekten av kontinuerlig infusion av tafoxiparin för behandling av långsamt eller avstannat värkarbete hos fullgångna förstföderskor. Du tillfrågas om att vara
Prövningstitel: Studie för att utvärdera effekten av kontinuerlig infusion av tafoxiparin för behandling av långsamt eller avstannat värkarbete hos fullgångna förstföderskor. Du tillfrågas om att vara
Bipacksedel: Information till patienten. Teceos 13 mg beredningssats för radioaktivt läkemedel. tetranatriumbutedronat
 Bipacksedel: Information till patienten Teceos 13 mg beredningssats för radioaktivt läkemedel tetranatriumbutedronat Läs noga igenom denna bipacksedel innan du ges detta läkemedel. Den innehåller information
Bipacksedel: Information till patienten Teceos 13 mg beredningssats för radioaktivt läkemedel tetranatriumbutedronat Läs noga igenom denna bipacksedel innan du ges detta läkemedel. Den innehåller information
PATIENTINFORMATION OCH SAMTYCKE TILL ATT DELTA I EN FORSKNINGSSTUDIE
 PATIENTINFORMATION OCH SAMTYCKE TILL ATT DELTA I EN FORSKNINGSSTUDIE Namn på forskningsstudien: Randomiserad, dubbelblind, placebokontrollerad, parallellgruppsstudie för att bedöma kardiovaskulära resultat
PATIENTINFORMATION OCH SAMTYCKE TILL ATT DELTA I EN FORSKNINGSSTUDIE Namn på forskningsstudien: Randomiserad, dubbelblind, placebokontrollerad, parallellgruppsstudie för att bedöma kardiovaskulära resultat
EPP06 Patientinformation, Version
 Enrolleringsnummer: Initialer: Information till försökspersonerna (Enkel/Multipel stigande dos) Säkerhet och tolerabilitet av lokalt applicerad EP0003 kräm 0.45 % hos friska frivilliga försökspersoner
Enrolleringsnummer: Initialer: Information till försökspersonerna (Enkel/Multipel stigande dos) Säkerhet och tolerabilitet av lokalt applicerad EP0003 kräm 0.45 % hos friska frivilliga försökspersoner
Patientinformation. Denna studie har godkänts av en oberoende etikprövningsnämnd för att garantera din säkerhet och dina rättigheter.
 Patientinformation En dubbel-blind, randomiserad, placebo-kontrollerad, multicenter, klinisk fas IV-studie för att utvärdera prestanda, säkerhet och användbarhet av myrsyra på patienter med vårtor på händer,
Patientinformation En dubbel-blind, randomiserad, placebo-kontrollerad, multicenter, klinisk fas IV-studie för att utvärdera prestanda, säkerhet och användbarhet av myrsyra på patienter med vårtor på händer,
Hydrocephalus och shunt
 Hydrocephalus och shunt Den här broschyren berättar om hydrocephalus (vattenskalle) och shunt. Den riktar sig i första hand till familjer och personal som kommer i kontakt med barn och ungdomar som har
Hydrocephalus och shunt Den här broschyren berättar om hydrocephalus (vattenskalle) och shunt. Den riktar sig i första hand till familjer och personal som kommer i kontakt med barn och ungdomar som har
Patientinformation. Bakgrund och studiemål
 Patientinformation I PsAer-IgY studien kommer vi att undersöka om långtidsanvändning av en ny medicin mot Pseudomonas-bakterien har möjlighet att förlänga tiden till återfall av Pseudomonasinfektion hos
Patientinformation I PsAer-IgY studien kommer vi att undersöka om långtidsanvändning av en ny medicin mot Pseudomonas-bakterien har möjlighet att förlänga tiden till återfall av Pseudomonasinfektion hos
Information till försökspersoner som deltar i en studie av ett nytt drickbart vaccin mot ETEC-diarré
 Information till försökspersoner som deltar i en studie av ett nytt drickbart vaccin mot ETEC-diarré Vill du vara med i en studie där vi prövar ett nytt drickbart vaccin mot diarré som orsakas av så kallade
Information till försökspersoner som deltar i en studie av ett nytt drickbart vaccin mot ETEC-diarré Vill du vara med i en studie där vi prövar ett nytt drickbart vaccin mot diarré som orsakas av så kallade
Patientinformation och informerat samtycke
 Patientinformation och informerat samtycke Patientinformation Du tillfrågas härmed om att delta i en studie vid ändtarmscancer. Studien testar om det finns fördel med att ge tilläggsbehandling med cytostatika
Patientinformation och informerat samtycke Patientinformation Du tillfrågas härmed om att delta i en studie vid ändtarmscancer. Studien testar om det finns fördel med att ge tilläggsbehandling med cytostatika
Forskningspersonsinformation till frisk frivillig kontroll
 BILAGA 4 Version 4.0 2018-06-13 1(5) Forskningspersonsinformation till frisk frivillig kontroll Bakgrund och syfte Inflammation har tilldragit sig ett växande intresse som tänkbar mekanism bakom depression,
BILAGA 4 Version 4.0 2018-06-13 1(5) Forskningspersonsinformation till frisk frivillig kontroll Bakgrund och syfte Inflammation har tilldragit sig ett växande intresse som tänkbar mekanism bakom depression,
En forskningsstudie om Kronisk Myeloisk Leukemi, KML
 En forskningsstudie om Kronisk Myeloisk Leukemi, KML FORSKNINGSPERSONINFORMATION Du tillfrågas härmed om du vill delta i studie angående Kronisk Myeloisk Leukemi, KML, och kan tänka dig att lämna extra
En forskningsstudie om Kronisk Myeloisk Leukemi, KML FORSKNINGSPERSONINFORMATION Du tillfrågas härmed om du vill delta i studie angående Kronisk Myeloisk Leukemi, KML, och kan tänka dig att lämna extra
Till dig som ska behandlas med TECENTRIQ q
 Till dig som ska behandlas med TECENTRIQ q qdetta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera nysäkerhetsinformation. Du kan hjälpa till genom
Till dig som ska behandlas med TECENTRIQ q qdetta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera nysäkerhetsinformation. Du kan hjälpa till genom
Patientinformation 1(5)
 1(5) Patientinformation Du tillfrågas härmed om att delta i en studie med läkemedlen Avastin (bevacizumab) Tarceva (erlotinib) och Xeloda (capecitabine) för patienter med spridd tjock- /ändtarmscancer.
1(5) Patientinformation Du tillfrågas härmed om att delta i en studie med läkemedlen Avastin (bevacizumab) Tarceva (erlotinib) och Xeloda (capecitabine) för patienter med spridd tjock- /ändtarmscancer.
Information om. Hulio. (adalimumab) För patienter med inflammatorisk tarmsjukdom
 Information om Hulio (adalimumab) För patienter med inflammatorisk tarmsjukdom Hulio Ett bra alternativ för behandling av din inflammatoriska tarmsjukdom Hulio är ett biologiskt läkemedel som kan hjälpa
Information om Hulio (adalimumab) För patienter med inflammatorisk tarmsjukdom Hulio Ett bra alternativ för behandling av din inflammatoriska tarmsjukdom Hulio är ett biologiskt läkemedel som kan hjälpa
Information till dig som får behandling med ZALTRAP (aflibercept)
 Information till dig som får behandling med ZALTRAP (aflibercept) 2 Om ZALTRAP I denna broschyr kan du läsa om vad behandling med ZALTRAP innebär, så du vet vad du kan förvänta dig av behandlingen. ZALTRAP
Information till dig som får behandling med ZALTRAP (aflibercept) 2 Om ZALTRAP I denna broschyr kan du läsa om vad behandling med ZALTRAP innebär, så du vet vad du kan förvänta dig av behandlingen. ZALTRAP
BIPACKSEDEL: INFORMATION TILL PATIENTEN. Fludeoxyglucose (18F) Akademiska sjukhuset 250 MBq/ml injektionsvätska, lösning fludeoxiglukos ( 18 F)
 BIPACKSEDEL: INFORMATION TILL PATIENTEN Fludeoxyglucose (18F) Akademiska sjukhuset 250 MBq/ml injektionsvätska, lösning fludeoxiglukos ( 18 F) Läs noga igenom denna bipacksedel innan du får detta läkemedel.
BIPACKSEDEL: INFORMATION TILL PATIENTEN Fludeoxyglucose (18F) Akademiska sjukhuset 250 MBq/ml injektionsvätska, lösning fludeoxiglukos ( 18 F) Läs noga igenom denna bipacksedel innan du får detta läkemedel.
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN
 BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Tetrofosmin ROTOP 0,23 mg beredningssats för radioaktivt läkemedel tetrofosmin i form av tetrofosmintetrafluoroborat Läs noga igenom denna bipacksedel innan du
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Tetrofosmin ROTOP 0,23 mg beredningssats för radioaktivt läkemedel tetrofosmin i form av tetrofosmintetrafluoroborat Läs noga igenom denna bipacksedel innan du
Till dig som fått VELCADE. Information till patienter och anhöriga
 Till dig som fått VELCADE Information till patienter och anhöriga Information om Velcade till patienter och anhöriga Din läkare har rekommenderat behandling med VELCADE (bortezomib). VELCADE är det första
Till dig som fått VELCADE Information till patienter och anhöriga Information om Velcade till patienter och anhöriga Din läkare har rekommenderat behandling med VELCADE (bortezomib). VELCADE är det första
Bipacksedel: Information till patienten. fludeoxiglukos ( 18 F)
 Bipacksedel: Information till patienten Fludeoxyglucose ( 18 F) SUS Lund, 400MBq- 90 GBq, injektionsvätska, lösning fludeoxiglukos ( 18 F) Läs noga igenom denna bipacksedel innan du får detta läkemedel.
Bipacksedel: Information till patienten Fludeoxyglucose ( 18 F) SUS Lund, 400MBq- 90 GBq, injektionsvätska, lösning fludeoxiglukos ( 18 F) Läs noga igenom denna bipacksedel innan du får detta läkemedel.
Central venkateter CVK
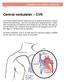 Central venkateter CVK Om du ska få läkemedel som dropp kommer du troligen att behöva en central infart till ditt blodomlopp. I den kan du få läkemedel, blodtransfusioner, vätska eller näringsdropp och
Central venkateter CVK Om du ska få läkemedel som dropp kommer du troligen att behöva en central infart till ditt blodomlopp. I den kan du få läkemedel, blodtransfusioner, vätska eller näringsdropp och
PARTNER-studien. Det är en europeisk studie som kommer att omfatta cirka 950 manliga homosexuella par.
 Deltagarinformation och informerat samtycke för den HIV-negativa partnern PARTNER-studien PARTNER-studien är en studie som riktar sig till par där: (i) den ena partnern är HIV-positiv och den andra är
Deltagarinformation och informerat samtycke för den HIV-negativa partnern PARTNER-studien PARTNER-studien är en studie som riktar sig till par där: (i) den ena partnern är HIV-positiv och den andra är
Den här broschyren har du fått via din behandlande läkare. Bra att veta om din intravenösa infusionsbehandling med ORENCIA (abatacept)
 Den här broschyren har du fått via din behandlande läkare. Bra att veta om din intravenösa infusionsbehandling med ORENCIA (abatacept) Innehållsförteckning Om ORENCIA 3 Din behandling 7 Användbara delar
Den här broschyren har du fått via din behandlande läkare. Bra att veta om din intravenösa infusionsbehandling med ORENCIA (abatacept) Innehållsförteckning Om ORENCIA 3 Din behandling 7 Användbara delar
BIPACKSEDEL. Klexane 150 mg/ml injektionsvätska, lösning, förfylld spruta Enoxaparin
 BIPACKSEDEL Klexane 150 mg/ml injektionsvätska, lösning, förfylld spruta Enoxaparin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. - Spara denna bipacksedel, du kan behöva läsa
BIPACKSEDEL Klexane 150 mg/ml injektionsvätska, lösning, förfylld spruta Enoxaparin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. - Spara denna bipacksedel, du kan behöva läsa
Förfrågan om att delta i forskningsprojekt STATICH: Blodproppsförebyggande läkemedelsbehandling efter hjärnblödning.
 Förfrågan om att delta i forskningsprojekt STATICH: Blodproppsförebyggande läkemedelsbehandling efter hjärnblödning. Bakgrund och syfte Efter hjärtinfarkt eller hjärninfarkt som beror på blodpropp i hjärtats
Förfrågan om att delta i forskningsprojekt STATICH: Blodproppsförebyggande läkemedelsbehandling efter hjärnblödning. Bakgrund och syfte Efter hjärtinfarkt eller hjärninfarkt som beror på blodpropp i hjärtats
Information till deltagare i studien Effekter av förhöjd dopaminergisk neurotransmission på resultaten av arbetsminnesträning bland friska äldre
 Information till deltagare i studien Effekter av förhöjd dopaminergisk neurotransmission på resultaten av arbetsminnesträning bland friska äldre Tillfrågande om deltagande Du har anmält intresse av att
Information till deltagare i studien Effekter av förhöjd dopaminergisk neurotransmission på resultaten av arbetsminnesträning bland friska äldre Tillfrågande om deltagande Du har anmält intresse av att
Information om forskningsstudien Born into Life (5-6 årsuppföljning av Life Gene Gravidstudien och Födelsekohorten)
 Sid: 1 / 5 Information om forskningsstudien Born into Life (5-6 årsuppföljning av Life Gene Gravidstudien och Födelsekohorten) Vad är Born into Life? I studien har vi följt dig och ditt barn med frågeformulär
Sid: 1 / 5 Information om forskningsstudien Born into Life (5-6 årsuppföljning av Life Gene Gravidstudien och Födelsekohorten) Vad är Born into Life? I studien har vi följt dig och ditt barn med frågeformulär
Studie: 1237.19 DYNAGITO EudraCT nr: 2014-002275-28 Patient nr.:
 Titel: En randomiserad, dubbelblind studie, med syfte att utvärdera effekten av 52 veckors behandling med inhalation Olodaterol + Tiotropium i fast doskombination en gång per dag, jämfört med behandling
Titel: En randomiserad, dubbelblind studie, med syfte att utvärdera effekten av 52 veckors behandling med inhalation Olodaterol + Tiotropium i fast doskombination en gång per dag, jämfört med behandling
Information till försökspersoner i studie med vaccin mot pandemi (H1N1) och säsongsinfluensa
 Deltagarnummer: Information till försökspersoner i studie med vaccin mot pandemi (H1N1) och säsongsinfluensa Du tillfrågas härmed om att delta i en vaccinstudie mot influensa orsakad av H1N1 (svininfluensa)
Deltagarnummer: Information till försökspersoner i studie med vaccin mot pandemi (H1N1) och säsongsinfluensa Du tillfrågas härmed om att delta i en vaccinstudie mot influensa orsakad av H1N1 (svininfluensa)
Din guide till YERVOY (ipilimumab)
 Detta utbildningsmaterial är obligatoriskt enligt ett villkor i godkännandet för försäljning av YERVOY TM för att ytterligare minimera särskilda risker. Din guide till YERVOY (ipilimumab) Patientbroschyr
Detta utbildningsmaterial är obligatoriskt enligt ett villkor i godkännandet för försäljning av YERVOY TM för att ytterligare minimera särskilda risker. Din guide till YERVOY (ipilimumab) Patientbroschyr
Forskningspersonsinformation
 Forskningspersonsinformation Jämförande studie mellan öppen kirurgi och robot-assisterad titthålskirurgi vid tidig livmoderhalscancer. Bakgrund och syfte Behandlingen av patienter med tidig livmoderhalscancer
Forskningspersonsinformation Jämförande studie mellan öppen kirurgi och robot-assisterad titthålskirurgi vid tidig livmoderhalscancer. Bakgrund och syfte Behandlingen av patienter med tidig livmoderhalscancer
Bipacksedel: Information till användaren. Fludeomap 250 MBq/ml injektionsvätska, lösning. fludeoxiglukos( 18 F)
 Bipacksedel: Information till användaren Fludeomap 250 MBq/ml injektionsvätska, lösning fludeoxiglukos( 18 F) Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller information
Bipacksedel: Information till användaren Fludeomap 250 MBq/ml injektionsvätska, lösning fludeoxiglukos( 18 F) Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller information
Syftet med det planerade försöket är att ta reda på hur kroppen påverkas vid belastning av en vikt, i det här fallet en viktväst.
 Forskningspersonsinformation och samtycke Du tillfrågas härmed att frivilligt delta i följande studie: Effekten av viktvästar på kroppsvikt hos överviktiga individer Syfte Syftet med det planerade försöket
Forskningspersonsinformation och samtycke Du tillfrågas härmed att frivilligt delta i följande studie: Effekten av viktvästar på kroppsvikt hos överviktiga individer Syfte Syftet med det planerade försöket
Simdax 2,5 mg/ml koncentrat till infusionsvätska, lösning Levosimendan. Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel.
 BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Simdax 2,5 mg/ml koncentrat till infusionsvätska, lösning Levosimendan Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Spara denna information,
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Simdax 2,5 mg/ml koncentrat till infusionsvätska, lösning Levosimendan Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Spara denna information,
Bipacksedel: Information till patienten. Ceretec 0,5 mg beredningssats för radioaktivt läkemedel exametazim
 Bipacksedel: Information till patienten Ceretec 0,5 mg beredningssats för radioaktivt läkemedel exametazim Läs noga igenom denna bipacksedel innan du ges detta läkemedel. Den innehåller information som
Bipacksedel: Information till patienten Ceretec 0,5 mg beredningssats för radioaktivt läkemedel exametazim Läs noga igenom denna bipacksedel innan du ges detta läkemedel. Den innehåller information som
Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Steripet 250 MBq/ml injektionsvätska, lösning fludeoxiglukos ( F) Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller information som
Bipacksedel: Information till användaren Steripet 250 MBq/ml injektionsvätska, lösning fludeoxiglukos ( F) Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller information som
Patientinformation. Till dig som behandlas med OPDIVO (nivolumab)
 Patientinformation Till dig som behandlas med OPDIVO (nivolumab) www.bms.se Inledning Före behandling med OPDIVO Det här är en broschyr avsedd som vägledning för dig som behandlas med OPDIVO. Här får du
Patientinformation Till dig som behandlas med OPDIVO (nivolumab) www.bms.se Inledning Före behandling med OPDIVO Det här är en broschyr avsedd som vägledning för dig som behandlas med OPDIVO. Här får du
Information om. Hulio. (adalimumab) För dig med psoriasis
 Information om Hulio (adalimumab) För dig med psoriasis Hulio Ett bra alternativ för behandling av din plackpsoriasis Hulio är ett biologiskt läkemedel som kan hjälpa till att minska symptomen vid psoriasis.
Information om Hulio (adalimumab) För dig med psoriasis Hulio Ett bra alternativ för behandling av din plackpsoriasis Hulio är ett biologiskt läkemedel som kan hjälpa till att minska symptomen vid psoriasis.
PATIENTINFORMATION Information om studie gällande interaktioner mellan hjärna och tarm efter
 PATIENTINFORMATION Information om studie gällande interaktioner mellan hjärna och tarm efter probiotiskt kosttillskott till personer med IBS, Irritable Bowel Syndrome. Förfrågan om deltagande i forskningsstudie
PATIENTINFORMATION Information om studie gällande interaktioner mellan hjärna och tarm efter probiotiskt kosttillskott till personer med IBS, Irritable Bowel Syndrome. Förfrågan om deltagande i forskningsstudie
En studie av ett nytt kikhostevaccin
 En studie av ett nytt kikhostevaccin Sveriges expertmyndighet för smittskydd (Smittskyddsinstitutet, SMI) har tillsammans med INSERM, French Health and Medical Research National Institute (som är sponsor
En studie av ett nytt kikhostevaccin Sveriges expertmyndighet för smittskydd (Smittskyddsinstitutet, SMI) har tillsammans med INSERM, French Health and Medical Research National Institute (som är sponsor
MabThera (rituximab) patientinformation
 MabThera (rituximab) patientinformation Du som lever med reumatoid artrit, RA, har antagligen redan genomgått en hel del olika behandlingsformer. Nu har din läkare ordinerat MabThera (rituximab) för din
MabThera (rituximab) patientinformation Du som lever med reumatoid artrit, RA, har antagligen redan genomgått en hel del olika behandlingsformer. Nu har din läkare ordinerat MabThera (rituximab) för din
Om din behandling med Xiapex
 PATIENTINFORMATION PATIENTINFORMATION Om din behandling med Xiapex Dupuytrens kontraktur Dupuytrens kontraktur är en bindvävssjukdom som ibland även kallas vikingasjukan eftersom den är vanligare i Skandi
PATIENTINFORMATION PATIENTINFORMATION Om din behandling med Xiapex Dupuytrens kontraktur Dupuytrens kontraktur är en bindvävssjukdom som ibland även kallas vikingasjukan eftersom den är vanligare i Skandi
PICC-line, perifert inlagd central venkateter
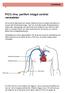 PICC-line, perifert inlagd central venkateter Om du ska få läkemedel som dropp i blodet kommer du troligen att behöva en central infart till ditt blodomlopp. I den kan du få läkemedel, blodtransfusioner,
PICC-line, perifert inlagd central venkateter Om du ska få läkemedel som dropp i blodet kommer du troligen att behöva en central infart till ditt blodomlopp. I den kan du få läkemedel, blodtransfusioner,
Förfrågan om att delta i ett forskningsprojekt
 Förfrågan om att delta i ett forskningsprojekt Ändtarmscancer: operation med stomi där anus lämnas kvar eller tas bort. (Hartmann eller Abdominoperineal excision med intersfinkterisk dissektion vid rektalcancer:
Förfrågan om att delta i ett forskningsprojekt Ändtarmscancer: operation med stomi där anus lämnas kvar eller tas bort. (Hartmann eller Abdominoperineal excision med intersfinkterisk dissektion vid rektalcancer:
Bipacksedeln: Information till användaren. Skinoren 20% kräm azelainsyra
 Bipacksedeln: Information till användaren Skinoren 20% kräm azelainsyra Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. - Spara
Bipacksedeln: Information till användaren Skinoren 20% kräm azelainsyra Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. - Spara
Röntgen och nuklearmedicin
 Röntgen och nuklearmedicin Vad är undersökningarna bra för och är de säkra? Strålning används på olika sätt för att ta bilder av kroppens inre. Bilderna behövs för att kunna hitta sjukdomar och som hjälp
Röntgen och nuklearmedicin Vad är undersökningarna bra för och är de säkra? Strålning används på olika sätt för att ta bilder av kroppens inre. Bilderna behövs för att kunna hitta sjukdomar och som hjälp
Celsite Implanterbara injektionsportar
 Celsite Implanterbara injektionsportar Patientinformation Patientinformation Patientens namn: Patientens adress: Telefonnummer: Sjukhus: Sjukhusadress: Telefonnummer: Läkare: Läkarens telefonnummer: Injektionsportens
Celsite Implanterbara injektionsportar Patientinformation Patientinformation Patientens namn: Patientens adress: Telefonnummer: Sjukhus: Sjukhusadress: Telefonnummer: Läkare: Läkarens telefonnummer: Injektionsportens
Patientinformation för Hälso- och livsstilsverktyg
 Patientinformation för Hälso- och livsstilsverktyg Vi skriver till Dig som vill förbättra Din hälsa, Dina levnadsvanor och Ditt mående. Du inbjuds härmed att delta i en forskningsstudie om ett Hälso- och
Patientinformation för Hälso- och livsstilsverktyg Vi skriver till Dig som vill förbättra Din hälsa, Dina levnadsvanor och Ditt mående. Du inbjuds härmed att delta i en forskningsstudie om ett Hälso- och
Röntgen och Nuklearmedicin ALERIS RÖNTGEN
 Röntgen och Nuklearmedicin ALERIS RÖNTGEN Vad är undersökningarna bra för och är de säkra? Strålning används på olika sätt för att ta bilder av kroppens inre. Bilderna behövs för att kunna hitta sjukdomar
Röntgen och Nuklearmedicin ALERIS RÖNTGEN Vad är undersökningarna bra för och är de säkra? Strålning används på olika sätt för att ta bilder av kroppens inre. Bilderna behövs för att kunna hitta sjukdomar
Patientinformation. Till dig som behandlas med OPDIVO (nivolumab) i kombination med YERVOY TM (ipilimumab) REGIMEN
 Patientinformation Till dig som behandlas med OPDIVO (nivolumab) i kombination med YERVOY TM (ipilimumab) WWW.BMS.SE REGIMEN Inledning Före behandling med OPDIVO i kombination med YERVOY TM Det här är
Patientinformation Till dig som behandlas med OPDIVO (nivolumab) i kombination med YERVOY TM (ipilimumab) WWW.BMS.SE REGIMEN Inledning Före behandling med OPDIVO i kombination med YERVOY TM Det här är
Detta informationsblad som du har fått av din läkare/sjuk sköterska innehåller information om Dacepton (apomorfin) Behandling med D-mine Pen
 Detta informationsblad som du har fått av din läkare/sjuk sköterska innehåller information om Dacepton (apomorfin) Behandling med D-mine Pen Vad är Dacepton? Dacepton är ett läkemedel som liknar dopamin
Detta informationsblad som du har fått av din läkare/sjuk sköterska innehåller information om Dacepton (apomorfin) Behandling med D-mine Pen Vad är Dacepton? Dacepton är ett läkemedel som liknar dopamin
Caprelsa. Vandetanib DOSERINGS- OCH ÖVERVAKNINGSGUIDE FÖR CAPRELSA (VANDETANIB) FÖR PATIENTER OCH VÅRDNADSHAVARE (PEDIATRISK ANVÄNDNING)
 Caprelsa Vandetanib Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de biverkningar
Caprelsa Vandetanib Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de biverkningar
Medtronic DBSvid. av epilepsi. mer. trygghet oberoende frihet. Shannan B. Får DBS-behandling sedan 2XXX. Shannan B.
 Medtronic DBSvid epilepsi mer trygghet oberoende frihet Shannan B. Får DBS-behandling sedan 2XXX Shannan B. får Medtronic DBSbehandling av epilepsi mer ut av livet Du behöver inte nöja dig med ett liv
Medtronic DBSvid epilepsi mer trygghet oberoende frihet Shannan B. Får DBS-behandling sedan 2XXX Shannan B. får Medtronic DBSbehandling av epilepsi mer ut av livet Du behöver inte nöja dig med ett liv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Skinoren 20% kräm azelainsyra Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. Spara
Bipacksedel: Information till användaren Skinoren 20% kräm azelainsyra Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. Spara
Bipacksedel: Information till patienten Octreoscan
 Bipacksedel: Information till patienten Octreoscan Beredningssats för radioaktiva läkemedel, 111 In-Pentetreotid 111 MBq/ml Läs noga igenom denna bipacksedel innan du ges detta läkemedel - Spara denna
Bipacksedel: Information till patienten Octreoscan Beredningssats för radioaktiva läkemedel, 111 In-Pentetreotid 111 MBq/ml Läs noga igenom denna bipacksedel innan du ges detta läkemedel - Spara denna
För patienter med reumatoid artrit. Information till dig som behandlas med RoACTEMRA
 För patienter med reumatoid artrit Information till dig som behandlas med RoACTEMRA RoACTEMRA - Behandling för patienter med RA (reumatoid artrit) Du har blivit ordinerad RoACTEMRA av din läkare. I denna
För patienter med reumatoid artrit Information till dig som behandlas med RoACTEMRA RoACTEMRA - Behandling för patienter med RA (reumatoid artrit) Du har blivit ordinerad RoACTEMRA av din läkare. I denna
PATIENTINFORMATION. Studietitel: En dosutvärdering av ALK träd AIT (Allergi Immunterapi Tablett)
 PATIENTINFORMATION Studietitel: En dosutvärdering av ALK träd AIT (Allergi Immunterapi Tablett) Bakgrund och syfte Du tillfrågas om att delta i denna forskningsstudie eftersom du har hösnuva och är allergisk
PATIENTINFORMATION Studietitel: En dosutvärdering av ALK träd AIT (Allergi Immunterapi Tablett) Bakgrund och syfte Du tillfrågas om att delta i denna forskningsstudie eftersom du har hösnuva och är allergisk
Gilenya (fingolimod) Information för dig som ska starta behandling med GILENYA. För fullständig GILENYA information se bipacksedeln eller
 Novartis Neuroscience Gilenya (fingolimod) Information för dig som ska starta behandling med För fullständig information se bipacksedeln eller www.fass.se - ditt nya läkemedel En kapsel en gång om dagen
Novartis Neuroscience Gilenya (fingolimod) Information för dig som ska starta behandling med För fullständig information se bipacksedeln eller www.fass.se - ditt nya läkemedel En kapsel en gång om dagen
En studie om barns hälsa i Västerbotten. Inbjudan till dig som blivande förälder
 En studie om barns hälsa i Västerbotten Inbjudan till dig som blivande förälder Fokus i studien Northpop är att undersöka risk- och friskfaktorer för vanligt förekommande sjukdomar hos barn. Alla blivande
En studie om barns hälsa i Västerbotten Inbjudan till dig som blivande förälder Fokus i studien Northpop är att undersöka risk- och friskfaktorer för vanligt förekommande sjukdomar hos barn. Alla blivande
Information till dig som blivit ordinerad
 PATIENTINFORMATION FRÅN SANOFI GENZYME Information till dig som blivit ordinerad AUBAGIO (teriflunomid) 1 Vad är multipel skleros? Denna information är avsedd för dig som har skovvis förlöpande multipel
PATIENTINFORMATION FRÅN SANOFI GENZYME Information till dig som blivit ordinerad AUBAGIO (teriflunomid) 1 Vad är multipel skleros? Denna information är avsedd för dig som har skovvis förlöpande multipel
Bipacksedel: Information till användaren. Typhim Vi 25 mikrogram/0,5 ml injektionsvätska, lösning i förfylld spruta
 Bipacksedel: Information till användaren Typhim Vi 25 mikrogram/0,5 ml injektionsvätska, lösning i förfylld spruta polysackaridvaccin mot tyfoidfeber Läs noga igenom denna bipacksedel innan du eller ditt
Bipacksedel: Information till användaren Typhim Vi 25 mikrogram/0,5 ml injektionsvätska, lösning i förfylld spruta polysackaridvaccin mot tyfoidfeber Läs noga igenom denna bipacksedel innan du eller ditt
Barium-id Giltigt t.o.m Version 4
 Innehållsansvarig: Daniel Hellner, Överläkare, Läkare Kardiologi (danhe) Granskad av: Erik Frick, Överläkare, Läkare Kardiologi (erifr) Godkänd av: Stellan Ahlström, Verksamhetschef, Ledningsgrupp M3 (steah)
Innehållsansvarig: Daniel Hellner, Överläkare, Läkare Kardiologi (danhe) Granskad av: Erik Frick, Överläkare, Läkare Kardiologi (erifr) Godkänd av: Stellan Ahlström, Verksamhetschef, Ledningsgrupp M3 (steah)
Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för dig.
 BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Selexid 200 mg och 400 mg filmdragerade tabletter Pivmecillinamhydroklorid Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Selexid 200 mg och 400 mg filmdragerade tabletter Pivmecillinamhydroklorid Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller
1. Vad Selexid är och vad det används för
 BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Selexid 200 mg och 400 mg filmdragerade tabletter Pivmecillinamhydroklorid Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Selexid 200 mg och 400 mg filmdragerade tabletter Pivmecillinamhydroklorid Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller
En studie om barns hälsa i Västerbotten. Inbjudan till dig som blivande förälder
 En studie om barns hälsa i Västerbotten Inbjudan till dig som blivande förälder Fokus i studien Northpop är att undersöka risk- och friskfaktorer för vanligt förekommande sjukdomar hos barn. Alla blivande
En studie om barns hälsa i Västerbotten Inbjudan till dig som blivande förälder Fokus i studien Northpop är att undersöka risk- och friskfaktorer för vanligt förekommande sjukdomar hos barn. Alla blivande
The Alzheimer s Association multi-center study on lumbar puncture feasibility
 The Alzheimer s Association multi-center study on lumbar puncture feasibility Bakgrund Biomarkörer i cerebrospinalvätska (CSF), tau och amyloid β (Aβ) har visat sig var lovande verktyg för diagnos av Alzheimers
The Alzheimer s Association multi-center study on lumbar puncture feasibility Bakgrund Biomarkörer i cerebrospinalvätska (CSF), tau och amyloid β (Aβ) har visat sig var lovande verktyg för diagnos av Alzheimers
Din guide till. Eylea används för att behandla synnedsättning till följd av diabetiska makulaödem (DME)
 Din guide till Eylea används för att behandla synnedsättning till följd av diabetiska makulaödem (DME) Välkommen till din Eylea-guide Häftet innehåller: Din läkare har skrivit ut Eylea eftersom du har
Din guide till Eylea används för att behandla synnedsättning till följd av diabetiska makulaödem (DME) Välkommen till din Eylea-guide Häftet innehåller: Din läkare har skrivit ut Eylea eftersom du har
Aktuell forskning och behandling av AAT-brist. Eeva Piitulainen Adj professor/överläkare Lung-och allergisektionen Skånes universitetssjukhus Malmö
 Aktuell forskning och behandling av AAT-brist Eeva Piitulainen Adj professor/överläkare Lung-och allergisektionen Skånes universitetssjukhus Malmö Agenda AAT-brist och risk för lungsjukdom Aktuell forskning
Aktuell forskning och behandling av AAT-brist Eeva Piitulainen Adj professor/överläkare Lung-och allergisektionen Skånes universitetssjukhus Malmö Agenda AAT-brist och risk för lungsjukdom Aktuell forskning
Bra att veta om din behandling med ORENCIA (abatacept) vid reumatoid artrit
 Bra att veta om din behandling med ORENCIA (abatacept) vid reumatoid artrit O R E N C I A a b ata c e p t 1 2 O R E N C I A a b ata c e p t Innehåll Om Orencia 5 Din behandlingsplan 6 Biverkningar 9 Vanliga
Bra att veta om din behandling med ORENCIA (abatacept) vid reumatoid artrit O R E N C I A a b ata c e p t 1 2 O R E N C I A a b ata c e p t Innehåll Om Orencia 5 Din behandlingsplan 6 Biverkningar 9 Vanliga
Bipacksedel: Information till patienten. Marcain spinal tung 5 mg/ml injektionsvätska, lösning. bupivakainhydroklorid
 Bipacksedel: Information till patienten Marcain spinal tung 5 mg/ml injektionsvätska, lösning bupivakainhydroklorid Läs noga igenom denna bipacksedel innan du ges detta läkemedel. Den innehåller information
Bipacksedel: Information till patienten Marcain spinal tung 5 mg/ml injektionsvätska, lösning bupivakainhydroklorid Läs noga igenom denna bipacksedel innan du ges detta läkemedel. Den innehåller information
Till dig som ordinerats
 Aug 2016 Till dig som ordinerats av din läkare Information till patienter Introduktion Din läkare har förskrivit JANUVIA (sitagliptin) för behandling av typ 2-diabetes. Denna broschyr är avsedd för att
Aug 2016 Till dig som ordinerats av din läkare Information till patienter Introduktion Din läkare har förskrivit JANUVIA (sitagliptin) för behandling av typ 2-diabetes. Denna broschyr är avsedd för att
Några minuter idag. Många liv i morgon.
 Några minuter idag. Många liv i morgon. Karma Kamera www.karmakamera.se Karolinska Institutet genomför under hösten 2013 forskningsstudien Karma Kamera i samarbete med Södersjukhuset. Vi ställer nu frågan
Några minuter idag. Många liv i morgon. Karma Kamera www.karmakamera.se Karolinska Institutet genomför under hösten 2013 forskningsstudien Karma Kamera i samarbete med Södersjukhuset. Vi ställer nu frågan
WARFARINBEHANDLING ENLIGT TRADITIONELL KINESISK MEDICIN
 Akupunkturakademin Vårtermin 2017 Grupp 26 WARFARINBEHANDLING ENLIGT TRADITIONELL KINESISK MEDICIN Examensarbete Hos Akupunkturakademin Lindborg & Torssell Författare: Minna Murto minna.m.murto@gmail.com
Akupunkturakademin Vårtermin 2017 Grupp 26 WARFARINBEHANDLING ENLIGT TRADITIONELL KINESISK MEDICIN Examensarbete Hos Akupunkturakademin Lindborg & Torssell Författare: Minna Murto minna.m.murto@gmail.com
Bipacksedel: Information till patienten. Nanocis 0,24 mg beredningssats för radioaktivt läkemedel rheniumsulfid
 Bipacksedel: Information till patienten Nanocis 0,24 mg beredningssats för radioaktivt läkemedel rheniumsulfid Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller information
Bipacksedel: Information till patienten Nanocis 0,24 mg beredningssats för radioaktivt läkemedel rheniumsulfid Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller information
TILL DIG SOM FÅTT LAMICTAL ORDINERAT PATIENTINFORMATION
 TILL DIG SOM FÅTT LAMICTAL ORDINERAT PATIENTINFORMATION TILL DIG SOM FÅTT LAMICTAL Du har fått en receptbelagd medicin som heter Lamictal utskrivet av din doktor. Lamictal är en förebyggande behandling
TILL DIG SOM FÅTT LAMICTAL ORDINERAT PATIENTINFORMATION TILL DIG SOM FÅTT LAMICTAL Du har fått en receptbelagd medicin som heter Lamictal utskrivet av din doktor. Lamictal är en förebyggande behandling
Sammanfattning av riskhanteringsplanen (RMP) för Portrazza (necitumumab)
 EMA/33513/2016 Sammanfattning av riskhanteringsplanen (RMP) för Portrazza (necitumumab) Detta är en sammanfattning av riskhanteringsplanen för Portrazza som beskriver åtgärder som ska vidtas för att säkerställa
EMA/33513/2016 Sammanfattning av riskhanteringsplanen (RMP) för Portrazza (necitumumab) Detta är en sammanfattning av riskhanteringsplanen för Portrazza som beskriver åtgärder som ska vidtas för att säkerställa
Bipacksedel: Information till patienten. Pulmocis 2 mg beredningssats för radioaktivt läkemedel. humant albumin som makroaggregat
 Bipacksedel: Information till patienten Pulmocis 2 mg beredningssats för radioaktivt läkemedel humant albumin som makroaggregat Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller
Bipacksedel: Information till patienten Pulmocis 2 mg beredningssats för radioaktivt läkemedel humant albumin som makroaggregat Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller
Vill du delta i en undersökning om matvanor?
 Till ungdomar i åk 2 på gymnasiet Vill du delta i en undersökning om matvanor? Bakgrund och syfte med Riksmaten ungdom Livsmedelsverket jobbar för säker mat och för bra matvanor. Livsmedelsverket behöver
Till ungdomar i åk 2 på gymnasiet Vill du delta i en undersökning om matvanor? Bakgrund och syfte med Riksmaten ungdom Livsmedelsverket jobbar för säker mat och för bra matvanor. Livsmedelsverket behöver
Vad handlade studien om? Varför behövdes studien? Vilka läkemedel studerades? BI
 Detta är en sammanfattning av en klinisk studie på patienter med idiopatisk lungfibros, en sällsynt lungsjukdom. Den är skriven för den vanliga läsaren och använder ett språk som är lätt att förstå. Den
Detta är en sammanfattning av en klinisk studie på patienter med idiopatisk lungfibros, en sällsynt lungsjukdom. Den är skriven för den vanliga läsaren och använder ett språk som är lätt att förstå. Den
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel.
 Läs mer om avregistrerade läkemedel Klexane, Klexane (med konserveringsmedel) 100 mg/ml injektionsvätska, lösning, förfylld spruta samt injektionsvätska, lösning Läs noga igenom denna bipacksedel innan
Läs mer om avregistrerade läkemedel Klexane, Klexane (med konserveringsmedel) 100 mg/ml injektionsvätska, lösning, förfylld spruta samt injektionsvätska, lösning Läs noga igenom denna bipacksedel innan
INFORMATION TILL STUDIEDELTAGARE
 INFORMATION TILL STUDIEDELTAGARE Information om studie gällande interaktioner mellan hjärna och tarm efter probiotiskt kosttillskott till friska personer Förfrågan om deltagande i forskningsstudie Du tillfrågas
INFORMATION TILL STUDIEDELTAGARE Information om studie gällande interaktioner mellan hjärna och tarm efter probiotiskt kosttillskott till friska personer Förfrågan om deltagande i forskningsstudie Du tillfrågas
En ny behandlingsform inom RA
 En ny behandlingsform inom RA Du som lever med reumatoid artrit har antagligen redan genomgått en hel del olika behandlingsformer. Nu har din läkare ordinerat MabThera (rituximab) för din RA. Din läkare
En ny behandlingsform inom RA Du som lever med reumatoid artrit har antagligen redan genomgått en hel del olika behandlingsformer. Nu har din läkare ordinerat MabThera (rituximab) för din RA. Din läkare
Förfrågan om att delta i ett forskningsprojekt
 1 Förfrågan om att delta i ett forskningsprojekt Ändtarmscancer: operation med stomi där anus lämnas kvar eller tas bort. (Hartmann eller Abdominoperineal excision med intersfinkterisk dissektion vid rektalcancer:
1 Förfrågan om att delta i ett forskningsprojekt Ändtarmscancer: operation med stomi där anus lämnas kvar eller tas bort. (Hartmann eller Abdominoperineal excision med intersfinkterisk dissektion vid rektalcancer:
Om din behandling med Xiapex
 p a t i e n t i n f o r m a t i o n P a t i e n t i n f o r m a t i o n Om din behandling med Xiapex Dupuytrens kontraktur Dupuytrens kontraktur är en bindvävssjukdom som ibland även kallas vikingasjukan
p a t i e n t i n f o r m a t i o n P a t i e n t i n f o r m a t i o n Om din behandling med Xiapex Dupuytrens kontraktur Dupuytrens kontraktur är en bindvävssjukdom som ibland även kallas vikingasjukan
Patientbroschyr. Jinarc (tolvaptan)
 Jinarc (tolvaptan) Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de biverkningar
Jinarc (tolvaptan) Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de biverkningar
Vad Pamifos är och vad det används för Vad du behöver veta innan du får Pamifos
 amifos Pamidronsyra Vad Pamifos är och vad det används för Pamifos är ett läkemedel som påverkar uppbyggnad och nedbrytning av ben. Läkemedlet tillhandahålls i form av en lösning som kan ges som långsam
amifos Pamidronsyra Vad Pamifos är och vad det används för Pamifos är ett läkemedel som påverkar uppbyggnad och nedbrytning av ben. Läkemedlet tillhandahålls i form av en lösning som kan ges som långsam
Till Dig Som har fått NexplaNoN förskrivet DeNNa patientinformation DelaS ut av berörd SjukvårDSperSoNal
 Till dig som har fått Nexplanon förskrivet Denna patientinformation delas ut av berörd sjukvårdspersonal Nexplanon skyddar dig från att bli gravid under tre år. Nexplanon är en liten hormonstav som placeras
Till dig som har fått Nexplanon förskrivet Denna patientinformation delas ut av berörd sjukvårdspersonal Nexplanon skyddar dig från att bli gravid under tre år. Nexplanon är en liten hormonstav som placeras
Accelererad eliminering av AUBAGIO. (teriflunomid)
 Accelererad eliminering av AUBAGIO (teriflunomid) Accelererad eliminering av AUBAGIO AUBAGIO är indicerat för behandling av vuxna patienter med skovvis förlöpande multipel skleros (MS). 1 Det finns en
Accelererad eliminering av AUBAGIO (teriflunomid) Accelererad eliminering av AUBAGIO AUBAGIO är indicerat för behandling av vuxna patienter med skovvis förlöpande multipel skleros (MS). 1 Det finns en
Bipacksedel: Information till användaren. Myoview 230 mikrogram, beredningssats för radioaktiva läkemedel tetrofosmin
 Bipacksedel: Information till användaren Myoview 230 mikrogram, beredningssats för radioaktiva läkemedel tetrofosmin Läs noga igenom denna bipacksedel innan du får Myoview. Den innehåller information som
Bipacksedel: Information till användaren Myoview 230 mikrogram, beredningssats för radioaktiva läkemedel tetrofosmin Läs noga igenom denna bipacksedel innan du får Myoview. Den innehåller information som
Ver. 2.0 ( )
 1/5 Information till deltagare i studien Effekten av fysisk och kognitiv träning på äldres kognitiva förmåga Studieansvarig: Martin Lövdén Tillfrågande om deltagande Du har anmält intresse för att delta
1/5 Information till deltagare i studien Effekten av fysisk och kognitiv träning på äldres kognitiva förmåga Studieansvarig: Martin Lövdén Tillfrågande om deltagande Du har anmält intresse för att delta
PATIENTINFORMATION. Din behandling med Avastin (bevacizumab)
 PATIENTINFORMATION Din behandling med Avastin (bevacizumab) 1 Din läkare planerar att du ska få behandling med läkemedlet Avastin (bevacizumab). Den här broschyren kommer att hjälpa dig förstå hur Avastin
PATIENTINFORMATION Din behandling med Avastin (bevacizumab) 1 Din läkare planerar att du ska få behandling med läkemedlet Avastin (bevacizumab). Den här broschyren kommer att hjälpa dig förstå hur Avastin
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN. Dequalinium Orifarm 10 mg vaginaltabletter dekvaliniumklorid
 BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Dequalinium Orifarm 10 mg vaginaltabletter dekvaliniumklorid Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Dequalinium Orifarm 10 mg vaginaltabletter dekvaliniumklorid Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
