Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler
|
|
|
- Gustav Lundqvist
- för 7 år sedan
- Visningar:
Transkript
1 12 October 2017 EMA/PRAC/662565/2017 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagna vid PRAC:s möte den september 2017 Ordalydelsen för produktinformationen i detta dokument är ett utdrag ur dokumentet med titeln PRAC:s rekommendationer om signaler, som innehåller hela texten till PRAC:s rekommendationer för uppdatering av produktinformation samt viss allmän vägledning om hantering av signaler. Dokumentet finns här (endast på engelska). Ny text som ska läggas till i produktinformationen är understruken. Befintlig text som ska strykas är genomstruken. 1. Acetazolamid Akut generaliserad exantematös pustulos (AGEP) (EPITT no 18892) Uppkomst av ett febrilt generaliserat erytem i samband med pustler vid behandlingsstart kan vara ett symtom på akut generaliserad exantematös pustulos (AGEP) (se avsnitt 4.8). Vid AGEP-diagnos ska acetazolamid sättas ut och all efterföljande administrering av acetazolamid är kontraindicerad. 30 Churchill Place Canary Wharf London E14 5EU United Kingdom Telephone +44 (0) Facsimile +44 (0) Send a question via our website An agency of the European Union European Medicines Agency, Reproduction is authorised provided the source is acknowledged.
2 2. Azitromycin; klaritromycin; erytromycin; roxitromycin Akut generaliserad exantematös pustulos (AGEP) (EPITT no 18891) Klaritromycin Vid allvarliga akuta överkänslighetsreaktioner, såsom anafylaxi, allvarliga hudbiverkningar (SCAR) (t.ex. akut generaliserad exantematös pustulos (AGEP), Stevens-Johnsons syndrom, toxisk epidermal nekrolys och läkemedelsutslag med eosinofili och systemiska symtom (DRESS)) ska behandling med klaritromycin omedelbart sättas ut och lämplig behandling ska inledas snarast. Erytromycin Liksom för andra makrolider har sällsynta allvarliga allergiska reaktioner, däribland akut generaliserad exantematös pustulos (AGEP), rapporterats. Om en allergisk reaktion inträffar ska läkemedlet sättas ut och lämplig behandling inledas. Läkare måste vara medvetna om att de allergiska symtomen kan återkomma när den symtomatiska behandlingen sätts ut. EMA/PRAC/662565/2017 Sida 2/7
3 Azitromycin Överkänslighet Liksom för erytromycin och andra makrolider har sällsynta allvarliga allergiska reaktioner rapporterats, däribland angioödem och anafylaxi (sällan med dödlig utgång), hudreaktioner såsom akut generaliserad exantematös pustulos (AGEP), Stevens-Johnsons syndrom (SJS), toxisk epidermal nekrolys (TEN) (sällan med dödlig utgång) och läkemedelsreaktion med eosinofili och systemiska symtom (DRESS). Några av dessa reaktioner med <produktnamn> resulterade i återkommande symtom och krävde en längre tids observation och behandling. Om en allergisk reaktion inträffar ska läkemedlet sättas ut och lämplig behandling inledas. Läkare måste vara medvetna om att de allergiska symtomen kan återkomma när den symtomatiska behandlingen sätts ut. Sällsynta: akut generaliserad exantematös pustulos (AGEP) Allvarliga hudbiverkningar Sällsynta: hudutslag som kännetecknas av snabb uppkomst av områden med röd hud med utspridda små pustler (små blåsor fyllda med vit/gul vätska). Roxitromycin Allvarliga bullösa reaktioner Fall av allvarliga bullösa hudreaktioner såsom Stevens-Johnsons syndrom, toxisk epidermal nekrolys och akut generaliserad exantematös pustulos (AGEP), har rapporterats med roxitromycin. Om symtom eller tecken på AGEP, Stevens-Johnsons syndrom eller toxisk epidermal nekrolys (t.ex. progressiva hudutslag ofta med blåsor eller slemhinnelesioner) uppträder ska behandlingen med roxitromycin sättas ut. 2. Vad du behöver veta innan du tar <produktnamn> EMA/PRAC/662565/2017 Sida 3/7
4 Om ett utbrett, allvarligt hudutslag uppträder, med symtom som blåsbildning eller fjällning av huden, samt tecken på influensa och feber (Stevens-Johnsons syndrom), allmän sjukdomskänsla, feber, frossa och muskelvärk (toxisk epidermal nekrolys), eller röda, fjälliga utslag med knölar under huden och blåsor (akut generaliserad exantematös pustulos) ska du omedelbart uppsöka läkare eftersom dessa hudreaktioner kan vara livshotande. Allvarliga hudbiverkningar 3. Kladribin Progressiv multifokal leukoencefalopati (PML) (EPITT no 18875) Berörda läkemedel: kladribin-innehållande produkter som godkänts för onkologiska indikationer. Progressiv multifokal leukoencefalopati (PML) Fall av PML, inklusive fall med dödlig utgång, har rapporterats med kladribin. PML rapporterades från 6 månader till flera år efter behandling med kladribin. Ett samband med långvarig lymfopeni har rapporterats i flera av dessa fall. Läkare bör överväga PML i differentialdiagnosen för patienter med nya eller förvärrade neurologiska, kognitiva eller beteendemässiga tecken eller symtom. I den föreslagna utvärderingen för PML ingår neurologikonsultation, magnetisk resonanstomografi av hjärnan samt analys av cerebrospinalvätskan för JC-virus (JCV) DNA genom polymeraskedjereaktion (PCR) eller en hjärnbiopsi med provtagning för JCV. Ett negativt JCV PCR utesluter inte PML. Ytterligare uppföljning och utvärdering kan vara motiverad om ingen alternativ diagnos kan ställas. Patienter med misstänkt PML ska inte få ytterligare behandling med kladribin. 2. Vad du behöver veta innan du <tar> <använder> <produktnamn> Varningar och försiktighet Tala med läkare <eller> <apotekspersonal> <eller sjuksköterska> innan du <tar> <använder> <produktnamn> Tala genast om för läkare eller sjuksköterska om du någon gång under eller efter behandlingen: upplever dimsyn, synförlust eller dubbelseende, talsvårigheter, svaghet i en arm eller ett ben, förändring i sättet att gå eller problem med balansen, ihållande domningar, nedsatt känsel eller förlorad känsel, minnesförlust eller förvirring. Alla dessa symtom kan tyda på en allvarlig och potentiellt dödlig hjärnsjukdom som kallas progressiv multifokal leukoencefalopati (PML). EMA/PRAC/662565/2017 Sida 4/7
5 Om du hade dessa symtom före behandlingen med kladribin, tala om för läkare om dessa symtom förändras på något sätt. 4. Desloratadin; loratadin Viktökning hos barn (EPITT no 18906) Loratadin Undersökningar Ingen känd frekvens: viktökning Har rapporterats: viktökning Desloratadin Undersökningar Ingen känd frekvens: viktökning Metabolism och nutrition Ingen känd frekvens: ökad aptit Har rapporterats: viktökning, ökad aptit 5. Doxycyklin Doxycyklin-inducerad Jarisch-Herxheimerreaktion (EPITT no 18937) EMA/PRAC/662565/2017 Sida 5/7
6 Vissa patienter med spiroketinfektioner kan få en Jarisch-Herxheimer-reaktion kort tid efter att doxycyklinbehandling inletts. Patienter ska informeras om att detta är en oftast självbegränsande följd av antibiotikabehandling vid spiroketinfektioner. Immunsystemet Ingen känd frekvens: Jarisch-Herxheimer-reaktion (se avsnitt 4.4) Kontakta din läkare snarast möjligt om något av följande symtom uppstår: - Jarisch-Herxheimer-reaktion som ger feber, frossa, huvudvärk, muskelsmärta och hudutslag. Dessa symptom är oftast självbegränsande. Detta inträffar kort tid efter påbörjad doxycyklinbehandling av infektioner orsakade av spiroketer såsom borreliainfektion. 6. Flukloxacillin High anion gap metabolic acidosis (HAGMA) (EPITT no 18844) Försiktighet rekommenderas när flukloxacillin administreras tillsammans med paracetamol på grund av den ökade risken för HAGMA (high anion gap metabolic acidosis). Till patienter med hög risk för HAGMA hör i synnerhet de med svårt nedsatt njurfunktion, sepsis eller malnutrition, särskilt vid användning av maximala dygnsdoser av paracetamol. Efter samtidig administering av flukloxacillin och paracetamol rekommenderas noggrann övervakning för att upptäcka uppkomsten av syra-basstörningar, d.v.s. HAGMA, inklusive sökning efter 5-oxoprolin i urinen. Om behandlingen med flukloxacillin fortsätter efter utsättning av paracetamol är det lämpligt att försäkra sig om att det inte finns några signaler på HAGMA, eftersom det finns en möjlighet att flukloxacillin upprätthåller den kliniska bilden av HAGMA (se avsnitt 4.5) Interaktioner med andra läkemedel och övriga interaktioner Försiktighet bör iakttas vid samtidig användning av flukloxacillin och paracetamol eftersom samtidigt intag har förknippats med HAGMA (high anion gap metabolic acidosis), särskilt hos patienter med riskfaktorer. (se avsnitt 4.4.) Metabolism och nutrition EMA/PRAC/662565/2017 Sida 6/7
7 Erfarenhet efter marknadsintroduktion: mycket sällsynta fall av HAGMA (high anion gap metabolic acidosis) vid samtidig användning av flukloxacillin och paracetamol, oftast i närvaro av riskfaktorer (se avsnitt 4.4.) 2. Vad du behöver veta innan du tar <produktnamn> Varningar och försiktighet Tala med läkare eller apotekspersonal innan du tar detta läkemedel: Om du tar eller kommer att ta paracetamol Vid samtidig användning av flukloxacillin och paracetamol finns det risk för blod- och vätskerubbningar (metabolisk acidos på grund av högt anjongap, s.k. HAGMA), vilket uppstår när surhetsgraden i blodplasma ökar, särskilt i vissa patientgrupper som har förhöjd risk, t.ex. patienter med svårt nedsatt njurfunktion, blodförgiftning eller undernäring och särskilt vid användning av maximala dygnsdoser av paracetamol. HAGMA är ett allvarlig tillstånd som kräver skyndsam behandling. [Följande läkemedelsbiverkning ska läggas till med frekvensen mycket sällsynta (kan förekomma hos upp till 1 av personer)] Mycket sällsynta fall av blod- och vätskerubbningar (metabolisk acidos på grund av högt anjongap), vilket uppstår när surhetsgraden i blodplasma ökar, vid samtidig användning av flukloxacillin och paracetamol, oftast hos patienter som har riskfaktorer (se avsnitt 2). EMA/PRAC/662565/2017 Sida 7/7
Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler
 25 January 2018 EMA/PRAC/35592/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagna vid PRAC:s möte den 8 11 januari
25 January 2018 EMA/PRAC/35592/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagna vid PRAC:s möte den 8 11 januari
Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler
 25 February 2016 EMA/PRAC/137774/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagna vid PRAC:s möte den 8 11
25 February 2016 EMA/PRAC/137774/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagna vid PRAC:s möte den 8 11
PRAC:s rekommendationer om signaler för uppdatering av produktinformationen
 22 januari 2015 EMA/PRAC/63320/2015 Kommittén för säkerhetsövervakning och riskbedömning av läkemedel PRAC:s rekommendationer om signaler för uppdatering av produktinformationen Antagna vid PRAC:s möte
22 januari 2015 EMA/PRAC/63320/2015 Kommittén för säkerhetsövervakning och riskbedömning av läkemedel PRAC:s rekommendationer om signaler för uppdatering av produktinformationen Antagna vid PRAC:s möte
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Flucloxacillin Sandoz 500 mg, 750 mg filmdragerade tabletter flukloxacillin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller
Bipacksedel: Information till användaren Flucloxacillin Sandoz 500 mg, 750 mg filmdragerade tabletter flukloxacillin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Flucloxacillin Sandoz 500 mg, 750 mg filmdragerade tabletter flukloxacillin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller
Bipacksedel: Information till användaren Flucloxacillin Sandoz 500 mg, 750 mg filmdragerade tabletter flukloxacillin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller
Bipacksedel: Information till användaren. Flucloxacillin Orion 750 mg filmdragerade tabletter. Flucloxacillin Orion 1 g filmdragerade tabletter
 Bipacksedel: Information till användaren Flucloxacillin Orion 500 mg filmdragerade tabletter Flucloxacillin Orion 750 mg filmdragerade tabletter Flucloxacillin Orion 1 g filmdragerade tabletter flukloxacillin
Bipacksedel: Information till användaren Flucloxacillin Orion 500 mg filmdragerade tabletter Flucloxacillin Orion 750 mg filmdragerade tabletter Flucloxacillin Orion 1 g filmdragerade tabletter flukloxacillin
Bilaga I. Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning
 Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning 1 Vetenskapliga slutsatser Med hänsyn till utredningsrapporten från kommittén för säkerhetsövervakning
Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning 1 Vetenskapliga slutsatser Med hänsyn till utredningsrapporten från kommittén för säkerhetsövervakning
EMA bekräftar rekommendationer för att minska risken för hjärninfektionen PML med Tysabri
 25/04/2016 EMA/266665/2016 EMA bekräftar rekommendationer för att minska risken för hjärninfektionen PML med Mer frekventa MRT-undersökningar bör övervägas för patienter med högre risk Den 25 februari
25/04/2016 EMA/266665/2016 EMA bekräftar rekommendationer för att minska risken för hjärninfektionen PML med Mer frekventa MRT-undersökningar bör övervägas för patienter med högre risk Den 25 februari
Bipacksedeln: Information till patienten. Azyter 15 mg/g, ögondroppar, lösning i endosbehållare. azitromycindihydrat
 Bipacksedeln: Information till patienten Azyter 15 mg/g, ögondroppar, lösning i endosbehållare azitromycindihydrat Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller
Bipacksedeln: Information till patienten Azyter 15 mg/g, ögondroppar, lösning i endosbehållare azitromycindihydrat Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller
Bipacksedel: Information till användaren. Heracillin 750 mg filmdragerade tabletter. Heracillin 1 g filmdragerade tabletter flukloxacillin
 Bipacksedel: Information till användaren Heracillin 125 mg filmdragerade tabletter Heracillin 500 mg filmdragerade tabletter Heracillin 750 mg filmdragerade tabletter Heracillin 1 g filmdragerade tabletter
Bipacksedel: Information till användaren Heracillin 125 mg filmdragerade tabletter Heracillin 500 mg filmdragerade tabletter Heracillin 750 mg filmdragerade tabletter Heracillin 1 g filmdragerade tabletter
Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler
 17 December 2015 EMA/PRAC/835768/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagen vid PRAC:s möte den 30 november
17 December 2015 EMA/PRAC/835768/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagen vid PRAC:s möte den 30 november
Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler
 4 January 2019 1 EMA/PRAC/855009/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagna vid PRAC:s möte den 26 29
4 January 2019 1 EMA/PRAC/855009/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagna vid PRAC:s möte den 26 29
VIKTIG SÄKERHETSINFORMATION FÖR PATIENTER SOM BEHANDLAS MED RIXATHON (RITUXIMAB)
 (RITUXIMAB) INFORMATIONSBROSCHYR FÖR PATIENTER VID ICKE-ONKOLOGISKA INDIKATIONER Detta läkemedel är föremål för utökad övervakning. rituksimabi Godkänd av Fimea, juli/2018 2 3 VAD DU BÖR VETA OM RIXATHON
(RITUXIMAB) INFORMATIONSBROSCHYR FÖR PATIENTER VID ICKE-ONKOLOGISKA INDIKATIONER Detta läkemedel är föremål för utökad övervakning. rituksimabi Godkänd av Fimea, juli/2018 2 3 VAD DU BÖR VETA OM RIXATHON
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Clindamycin Orifarm 300 mg hårda kapslar klindamycin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är
Bipacksedel: Information till användaren Clindamycin Orifarm 300 mg hårda kapslar klindamycin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är
Bipacksedel: Information till användaren. Clindamycin Orifarm 150 mg hårda kapslar. klindamycin
 Bipacksedel: Information till användaren Clindamycin Orifarm 150 mg hårda kapslar klindamycin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är
Bipacksedel: Information till användaren Clindamycin Orifarm 150 mg hårda kapslar klindamycin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är
Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännandena för försäljning
 Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännandena för försäljning 1 Vetenskapliga slutsatser Med hänsyn till PRAC:s utredningsprotokoll om den periodiska säkerhetsrapporten
Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännandena för försäljning 1 Vetenskapliga slutsatser Med hänsyn till PRAC:s utredningsprotokoll om den periodiska säkerhetsrapporten
Riskhanteringsplan för kladribin (MAVENCLAD), version 1.0 Godkänt av Fimea PATIENTGUIDE
 MAVENCLAD PATIENTGUIDE RISKHANTERINGS SKOLNINGSMATERIAL - FI/CLA/1117/0052 Viktig information för patienter som påbörjar behandling med MAVENCLAD Innehåll Introduktion till MAVENCLAD Hur ges behandling
MAVENCLAD PATIENTGUIDE RISKHANTERINGS SKOLNINGSMATERIAL - FI/CLA/1117/0052 Viktig information för patienter som påbörjar behandling med MAVENCLAD Innehåll Introduktion till MAVENCLAD Hur ges behandling
Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler
 20 July 2017 EMA/PRAC/467501/2017 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagna vid PRAC:s möte den 3 6 juli
20 July 2017 EMA/PRAC/467501/2017 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagna vid PRAC:s möte den 3 6 juli
BILAGA III RELEVANTA AVSNITT AV PRODUKTRESUMÉ OCH BIPACKSEDEL. Anm.: Dessa ändringar av produktresumén och bipacksedeln gäller vid
 BILAGA III RELEVANTA AVSNITT AV PRODUKTRESUMÉ OCH BIPACKSEDEL Anm.: Dessa ändringar av produktresumén och bipacksedeln gäller vid tidpunkten för kommissionens beslut. Efter kommissionens beslut kommer
BILAGA III RELEVANTA AVSNITT AV PRODUKTRESUMÉ OCH BIPACKSEDEL Anm.: Dessa ändringar av produktresumén och bipacksedeln gäller vid tidpunkten för kommissionens beslut. Efter kommissionens beslut kommer
Bipacksedel: Information till användaren. Metronidazol EQL Pharma 200 mg tablett Metronidazol EQL Pharma 400 mg tablett.
 Bipacksedel: Information till användaren Metronidazol EQL Pharma 200 mg tablett Metronidazol EQL Pharma 400 mg tablett metronidazol Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel.
Bipacksedel: Information till användaren Metronidazol EQL Pharma 200 mg tablett Metronidazol EQL Pharma 400 mg tablett metronidazol Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel.
Leflunomide STADA. Version, V1.0
 Leflunomide STADA Version, V1.0 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 Delområden av en offentlig sammanfattning Leflunomide STADA 10 mg filmdragerade tabletter Leflunomide STADA 20 mg filmdragerade
Leflunomide STADA Version, V1.0 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 Delområden av en offentlig sammanfattning Leflunomide STADA 10 mg filmdragerade tabletter Leflunomide STADA 20 mg filmdragerade
Denna manual innehåller information om webbrapportens dataelement, layout, tolkning och funktioner.
 Skydd för patienthälsa Denna manual innehåller information om webbrapportens dataelement, layout, tolkning och funktioner. 1. Dataelement... 2 2. Närmare uppgifter om dataelement... 4 3. Layout... 5 4.
Skydd för patienthälsa Denna manual innehåller information om webbrapportens dataelement, layout, tolkning och funktioner. 1. Dataelement... 2 2. Närmare uppgifter om dataelement... 4 3. Layout... 5 4.
Patientbroschyr. Vad du bör känna till om MabThera. Viktig säkerhetsinformation för patienter som får behandling med MabThera
 Patientbroschyr Vad du bör känna till om MabThera Viktig säkerhetsinformation för patienter som får behandling med MabThera Denna broschyr innehåller viktig säkerhetsinformation. Läs MabTheras produktresumé
Patientbroschyr Vad du bör känna till om MabThera Viktig säkerhetsinformation för patienter som får behandling med MabThera Denna broschyr innehåller viktig säkerhetsinformation. Läs MabTheras produktresumé
Bipacksedel: Information till användaren. Surlid 150 mg filmdragerade tabletter roxitromycin
 Bipacksedel: Information till användaren Surlid 150 mg filmdragerade tabletter roxitromycin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är
Bipacksedel: Information till användaren Surlid 150 mg filmdragerade tabletter roxitromycin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är
Naproxen Orion 25 mg/ml oral suspension , Version 1.2 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN
 Naproxen Orion 25 mg/ml oral suspension 26.10.2015, Version 1.2 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 VI.2.1 Delområden av en offentlig sammanfattning Information om sjukdomsförekomst Naproxen
Naproxen Orion 25 mg/ml oral suspension 26.10.2015, Version 1.2 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 VI.2.1 Delområden av en offentlig sammanfattning Information om sjukdomsförekomst Naproxen
ÄNDRINGAR SOM SKA INKLUDERAS I DE RELEVANTA AVSNITTEN I PRODUKTRESUMÉN FÖR NIMESULID-INNEHÅLLANDE LÄKEMEDEL (SYSTEMISKA FORMULERINGAR)
 BILAGA III 1 ÄNDRINGAR SOM SKA INKLUDERAS I DE RELEVANTA AVSNITTEN I PRODUKTRESUMÉN FÖR NIMESULID-INNEHÅLLANDE LÄKEMEDEL (SYSTEMISKA FORMULERINGAR) Tillägg är kursiverade och understrukna, raderingar är
BILAGA III 1 ÄNDRINGAR SOM SKA INKLUDERAS I DE RELEVANTA AVSNITTEN I PRODUKTRESUMÉN FÖR NIMESULID-INNEHÅLLANDE LÄKEMEDEL (SYSTEMISKA FORMULERINGAR) Tillägg är kursiverade och understrukna, raderingar är
Bipacksedel: Information till användaren. Rifadin 20 mg/ml, oral suspension. rifampicin
 Bipacksedel: Information till användaren Rifadin 20 mg/ml, oral suspension rifampicin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig
Bipacksedel: Information till användaren Rifadin 20 mg/ml, oral suspension rifampicin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig
Bisolvon. Bipacksedel: Information till användaren. 1,6 mg/ml oral lösning bromhexinhydroklorid
 Bipacksedel: Information till användaren Bisolvon 1,6 mg/ml oral lösning bromhexinhydroklorid Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är
Bipacksedel: Information till användaren Bisolvon 1,6 mg/ml oral lösning bromhexinhydroklorid Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är
1. Vad Nebcina är och vad det används för
 Bipacksedel: Information till användaren Nebcina Nebcina 10 mg/ml injektionsvätska, lösning. Nebcina 40 mg/ml injektionsvätska, lösning. Nebcina 80 mg/ml injektionsvätska, lösning. tobramycin Läs noga
Bipacksedel: Information till användaren Nebcina Nebcina 10 mg/ml injektionsvätska, lösning. Nebcina 40 mg/ml injektionsvätska, lösning. Nebcina 80 mg/ml injektionsvätska, lösning. tobramycin Läs noga
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Bisolvon 8 mg tabletter bromhexinhydroklorid Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig
Bipacksedel: Information till användaren Bisolvon 8 mg tabletter bromhexinhydroklorid Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig
FÖRSKRIVNINGSGUIDE MAVENCLAD. Riskhanteringsplan för kladribin (MAVENCLAD), version 1.0 Godkänt av Fimea
 MAVENCLAD FÖRSKRIVNINGSGUIDE RISKHANTERINGS SKOLNINGSMATERIAL - FI/CLA/1117/0051 Innehåll Introduktion till MAVENCLAD Behandlingsregimer Övervakning under behandling Antalet lymfocyter Allvarliga infektioner
MAVENCLAD FÖRSKRIVNINGSGUIDE RISKHANTERINGS SKOLNINGSMATERIAL - FI/CLA/1117/0051 Innehåll Introduktion till MAVENCLAD Behandlingsregimer Övervakning under behandling Antalet lymfocyter Allvarliga infektioner
Bipacksedel: Information till användaren. Pamol 500 mg filmdragerade tabletter. paracetamol
 Bipacksedel: Information till användaren Pamol 500 mg filmdragerade tabletter paracetamol Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig
Bipacksedel: Information till användaren Pamol 500 mg filmdragerade tabletter paracetamol Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig
Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Doxycyklin EQL Pharma 100 mg tabletter Doxycyklin Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig
Bipacksedel: Information till användaren Doxycyklin EQL Pharma 100 mg tabletter Doxycyklin Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig
Bilaga II. Vetenskapliga slutsatser och skäl till tillfälligt upphävande av godkännandena för försäljning
 Bilaga II Vetenskapliga slutsatser och skäl till tillfälligt upphävande av godkännandena för försäljning 11 Vetenskapliga slutsatser och skäl till tillfälligt upphävande av godkännandena för försäljning
Bilaga II Vetenskapliga slutsatser och skäl till tillfälligt upphävande av godkännandena för försäljning 11 Vetenskapliga slutsatser och skäl till tillfälligt upphävande av godkännandena för försäljning
Behandlingsdagbok: Registrera biverkningar under behandlingen. Denna broschyr har du fått av din behandlande läkare
 Denna broschyr har du fått av din behandlande läkare Behandlingsdagbok: Registrera biverkningar under behandlingen Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att
Denna broschyr har du fått av din behandlande läkare Behandlingsdagbok: Registrera biverkningar under behandlingen Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att
Bipacksedeln: Information till användaren. Pamol 500 mg filmdragerade tabletter. paracetamol
 Bipacksedeln: Information till användaren Pamol 500 mg filmdragerade tabletter paracetamol Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig
Bipacksedeln: Information till användaren Pamol 500 mg filmdragerade tabletter paracetamol Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig
6-12 år: 2,5-5 ml (2-4 mg) 3 gånger dagligen. 1-5 år: 2,5 ml (2 mg) 3 gånger dagligen.
 PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Bromhex 0,8 mg/ml oral lösning 2 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 ml oral lösning innehåller: Bromhexinhydroklorid 0,8 mg. Hjälpämnen med känd effekt: Sorbitol
PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Bromhex 0,8 mg/ml oral lösning 2 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 ml oral lösning innehåller: Bromhexinhydroklorid 0,8 mg. Hjälpämnen med känd effekt: Sorbitol
Bilaga I. Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning
 Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning 1 Vetenskapliga slutsatser Med hänsyn till PRAC:s utredningsprotokoll om de periodiska säkerhetsrapporterna
Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning 1 Vetenskapliga slutsatser Med hänsyn till PRAC:s utredningsprotokoll om de periodiska säkerhetsrapporterna
Metacam. meloxikam. Vad är Metacam? Vad används Metacam för? Sammanfattning av EPAR för allmänheten
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Sammanfattning av EPAR för allmänheten meloxikam Detta är en sammanfattning av det offentliga europeiska utredningsprotokollet (EPAR) för. Det förklarar hur kommittén
EMA/CVMP/259397/2006 EMEA/V/C/000033 Sammanfattning av EPAR för allmänheten meloxikam Detta är en sammanfattning av det offentliga europeiska utredningsprotokollet (EPAR) för. Det förklarar hur kommittén
Bipacksedel: Information till användaren. Terbinafin Orifarm 250 mg tabletter terbinafin
 Bipacksedel: Information till användaren Terbinafin Orifarm 250 mg tabletter terbinafin Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för
Bipacksedel: Information till användaren Terbinafin Orifarm 250 mg tabletter terbinafin Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för
ARAVA (leflunomid) Särskild säkerhetsinformation till förskrivare
 ARAVA (leflunomid) Särskild säkerhetsinformation till förskrivare Arava (leflunomid) är ett immunomodulerande antireumatiskt läkemedel (DMARD; disease-modifying antirheumatic drug) indicerat för behandling
ARAVA (leflunomid) Särskild säkerhetsinformation till förskrivare Arava (leflunomid) är ett immunomodulerande antireumatiskt läkemedel (DMARD; disease-modifying antirheumatic drug) indicerat för behandling
Bilaga I. Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning
 Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning 1 Vetenskapliga slutsatser Med hänsyn till PRAC:s utredningsprotokoll om de periodiska säkerhetsuppdateringarna
Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning 1 Vetenskapliga slutsatser Med hänsyn till PRAC:s utredningsprotokoll om de periodiska säkerhetsuppdateringarna
Gul till brun viskös lösning med apelsinsmak. Partiklar från växtmaterial kan förekomma.
 PRODUKTRESUMÉ 1. LÄKEMEDLETS NAMN Echinagard, oral lösning 2. KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 ml oral lösning innehåller 24,8 mg torkad pressaft från Echinacea purpurea (L.) Moench (röd solhatt)
PRODUKTRESUMÉ 1. LÄKEMEDLETS NAMN Echinagard, oral lösning 2. KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 ml oral lösning innehåller 24,8 mg torkad pressaft från Echinacea purpurea (L.) Moench (röd solhatt)
Delområden av en offentlig sammanfattning
 Daptomycin STADA 350 mg och 500 mg pulver till injektions /infusionsvätska, lösning 4.5.2017, version V1.3 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 Delområden av en offentlig sammanfattning
Daptomycin STADA 350 mg och 500 mg pulver till injektions /infusionsvätska, lösning 4.5.2017, version V1.3 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 Delområden av en offentlig sammanfattning
ADMINISTRERING OCH PRAKTISKA RÅD
 ADMINISTRERING OCH PRAKTISKA RÅD Innan behandlingsstart med Tysabri (natalizumab) För att kunna påbörja behandling med Tysabri måste det finnas en genomförd MRT-undersökning som är gjord inom de tre senaste
ADMINISTRERING OCH PRAKTISKA RÅD Innan behandlingsstart med Tysabri (natalizumab) För att kunna påbörja behandling med Tysabri måste det finnas en genomförd MRT-undersökning som är gjord inom de tre senaste
Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler
 1 October 2018 1 EMA/PRAC/621128/2018 Corr 2 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagna vid PRAC:s möte den
1 October 2018 1 EMA/PRAC/621128/2018 Corr 2 Pharmacovigilance Risk Assessment Committee (PRAC) Ny lydelse för produktinformation Utdrag ur PRAC:s rekommendationer om signaler Antagna vid PRAC:s möte den
PRODUKTRESUMÉ. Vid besvär från andningsvägarna rekommenderas medicinsk rådgivning om symtomen inte förbättras.
 PRODUKTRESUMÉ 1. LÄKEMEDLETS NAMN Bisolvon 8 mg tabletter 2. KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 tablett innehåller: bromhexinhydroklorid 8 mg Hjälpämnen: laktosmonohydrat 74 mg För fullständig
PRODUKTRESUMÉ 1. LÄKEMEDLETS NAMN Bisolvon 8 mg tabletter 2. KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 tablett innehåller: bromhexinhydroklorid 8 mg Hjälpämnen: laktosmonohydrat 74 mg För fullständig
Viktiga saker att komma ihåg för dig som har ordinerats och tar GILENYA
 Viktiga saker att komma ihåg för dig som har ordinerats och tar GILENYA Se bipacksedeln eller www.fass.se för fullständig GILENYA-information. (03/2016) Din läkare kommer att be dig att stanna kvar på
Viktiga saker att komma ihåg för dig som har ordinerats och tar GILENYA Se bipacksedeln eller www.fass.se för fullständig GILENYA-information. (03/2016) Din läkare kommer att be dig att stanna kvar på
KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
 PRODUKTRESUMÉ 1. LÄKEMEDLETS NAMN Echinagard, sugtabletter 2. KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 sugtablett innehåller 88,5 mg torkad pressaft från Echinacea purpurea (L.) Moench (röd solhatt)
PRODUKTRESUMÉ 1. LÄKEMEDLETS NAMN Echinagard, sugtabletter 2. KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 sugtablett innehåller 88,5 mg torkad pressaft från Echinacea purpurea (L.) Moench (röd solhatt)
Patientinformation och behandlingsdagbok
 Patientinformation och behandlingsdagbok Till dig som behandlas med (nivolumab) WWW.BMS.COM/SE Inledning Före behandling med OPDIVO Det här är en broschyr avsedd som vägledning för dig som behandlas med
Patientinformation och behandlingsdagbok Till dig som behandlas med (nivolumab) WWW.BMS.COM/SE Inledning Före behandling med OPDIVO Det här är en broschyr avsedd som vägledning för dig som behandlas med
Entyvio 300 mg pulver till koncentrat till infusionsvätska, lösning (vedolizumab)
 Entyvio 300 mg pulver till koncentrat till infusionsvätska, lösning (vedolizumab) OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN 27.6.2014, version 1.0 VI.2 Delområden av en offentlig sammanfattning
Entyvio 300 mg pulver till koncentrat till infusionsvätska, lösning (vedolizumab) OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN 27.6.2014, version 1.0 VI.2 Delområden av en offentlig sammanfattning
Information för sjukvårdspersonal FÖR MALARIA KEMOPROFYLAX LARIAM (MEFLOKIN)
 Information för sjukvårdspersonal LARIAM (MEFLOKIN) FÖR MALARIA KEMOPROFYLAX Denna broschyr avser att ge information gällande biverkningar - speciellt neuropsykiatriska biverkningar- vid kemoprofylaktisk
Information för sjukvårdspersonal LARIAM (MEFLOKIN) FÖR MALARIA KEMOPROFYLAX Denna broschyr avser att ge information gällande biverkningar - speciellt neuropsykiatriska biverkningar- vid kemoprofylaktisk
Vägledning om tolkning av spontana fallrapporter om misstänkta läkemedelsbiverkningar
 Den 30 januari 2017 Inspektioner, säkerhetsövervakning av humanläkemedel och kommittéer för säkerhetsövervakning EMA/749446/2016 Revision 1* Vägledning om tolkning av spontana fallrapporter om misstänkta
Den 30 januari 2017 Inspektioner, säkerhetsövervakning av humanläkemedel och kommittéer för säkerhetsövervakning EMA/749446/2016 Revision 1* Vägledning om tolkning av spontana fallrapporter om misstänkta
Bilaga I. Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning
 Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning 1 Vetenskapliga slutsatser Med hänsyn till utredningsrapporten från kommittén för säkerhetsövervakning
Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning 1 Vetenskapliga slutsatser Med hänsyn till utredningsrapporten från kommittén för säkerhetsövervakning
PRODUKTRESUMÉ. 1 LÄKEMEDLETS NAMN Bromhexin ABECE 1,6 mg/ml oral lösning
 PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Bromhexin ABECE 0,8 mg/ml oral lösning Bromhexin ABECE 1,6 mg/ml oral lösning 2 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING Bromhexin Abece 0,8 mg/ml oral lösning 1 ml innehåller:
PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Bromhexin ABECE 0,8 mg/ml oral lösning Bromhexin ABECE 1,6 mg/ml oral lösning 2 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING Bromhexin Abece 0,8 mg/ml oral lösning 1 ml innehåller:
MITOXANTRON. Patientkort. Viktig obligatorisk information om riskminimering Meda AB (A Mylan Company)
 MITOXANTRON Patientkort Viktig obligatorisk information om riskminimering 2018 Meda AB (A Mylan Company) NOVANTRONE (mitoxantron) För behandling av multipel skleros (MS) med mycket aktiva återfall förknippad
MITOXANTRON Patientkort Viktig obligatorisk information om riskminimering 2018 Meda AB (A Mylan Company) NOVANTRONE (mitoxantron) För behandling av multipel skleros (MS) med mycket aktiva återfall förknippad
KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
 PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Heracillin 50 mg/ml pulver till oral suspension 2 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 ml oral suspension innehåller flukloxacillinmagnesiumoktahydrat motsvarande
PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Heracillin 50 mg/ml pulver till oral suspension 2 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 ml oral suspension innehåller flukloxacillinmagnesiumoktahydrat motsvarande
Sammanfattning av Metacam och varför det är godkänt inom EU
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Sammanfattning av Metacam och varför det är godkänt inom EU Vad är Metacam och vad används det för? Metacam är ett antiinflammatoriskt läkemedel som ges till nötkreatur,
EMA/CVMP/259397/2006 EMEA/V/C/000033 Sammanfattning av Metacam och varför det är godkänt inom EU Vad är Metacam och vad används det för? Metacam är ett antiinflammatoriskt läkemedel som ges till nötkreatur,
PRODUKTRESUMÉ. Vid besvär från andningsvägarna rekommenderas medicinsk rådgivning om symtomen inte förbättras.
 PRODUKTRESUMÉ 1. LÄKEMEDLETS NAMN Bisolvon 1,6 mg/ml oral lösning 2. KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 ml innehåller: bromhexinhydroklorid 1,6 mg Hjälpämnen: flytande maltitol 500 mg För fullständig
PRODUKTRESUMÉ 1. LÄKEMEDLETS NAMN Bisolvon 1,6 mg/ml oral lösning 2. KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 ml innehåller: bromhexinhydroklorid 1,6 mg Hjälpämnen: flytande maltitol 500 mg För fullständig
Ethambutol Orion 500 mg tabletter Datum: , Version 1.1 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN
 Ethambutol Orion 500 mg tabletter Datum: 21.10.2016, Version 1.1 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 VI.2.1 Delområden av en offentlig sammanfattning Information om sjukdomsförekomst
Ethambutol Orion 500 mg tabletter Datum: 21.10.2016, Version 1.1 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 VI.2.1 Delområden av en offentlig sammanfattning Information om sjukdomsförekomst
Bilaga III. Ändringar till berörda avsnitt i produktinformation
 Bilaga III Ändringar till berörda avsnitt i produktinformation Observera: Dessa ändringar till berörda avsnitt i produktresumé och bipacksedel är resultatet av hänskjutningsförfarandet. Produktinformationen
Bilaga III Ändringar till berörda avsnitt i produktinformation Observera: Dessa ändringar till berörda avsnitt i produktresumé och bipacksedel är resultatet av hänskjutningsförfarandet. Produktinformationen
4.1 Terapeutiska indikationer Typherix används för aktiv immunisering mot tyfoidfeber av vuxna och barn från 2 års ålder.
 PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Typherix, injektionsvätska, lösning, förfylld spruta Polysackaridvaccin mot tyfoidfeber. 2 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING Varje dos om 0,5 ml vaccin innehåller:
PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Typherix, injektionsvätska, lösning, förfylld spruta Polysackaridvaccin mot tyfoidfeber. 2 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING Varje dos om 0,5 ml vaccin innehåller:
Bipacksedel: Information till användaren. Imolopera 2 mg tabletter. loperamidhydroklorid
 Bipacksedel: Information till användaren Imolopera 2 mg tabletter loperamidhydroklorid Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för
Bipacksedel: Information till användaren Imolopera 2 mg tabletter loperamidhydroklorid Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för
XELJANZ. Den här broschyren är avsedd för dig som har ordinerats XELJANZ. Du hittar mer information i bipacksedeln som medföljer läkemedlet.
 XELJANZ Den här broschyren är avsedd för dig som har ordinerats XELJANZ. Du hittar mer information i bipacksedeln som medföljer läkemedlet. TILL DIG SOM BEHANDLAS MED XELJANZ, Din läkare har skrivit ut
XELJANZ Den här broschyren är avsedd för dig som har ordinerats XELJANZ. Du hittar mer information i bipacksedeln som medföljer läkemedlet. TILL DIG SOM BEHANDLAS MED XELJANZ, Din läkare har skrivit ut
XELJANZ. Den här broschyren är avsedd för dig som har ordinerats XELJANZ. Du hittar mer information i bipacksedeln som medföljer läkemedlet.
 XELJANZ Den här broschyren är avsedd för dig som har ordinerats XELJANZ. Du hittar mer information i bipacksedeln som medföljer läkemedlet. TILL DIG SOM BEHANDLAS MED XELJANZ, Din läkare har skrivit ut
XELJANZ Den här broschyren är avsedd för dig som har ordinerats XELJANZ. Du hittar mer information i bipacksedeln som medföljer läkemedlet. TILL DIG SOM BEHANDLAS MED XELJANZ, Din läkare har skrivit ut
Detta läkemedel är föremål för utökad övervakning. Viktiga saker att komma ihåg om din GILENYA (fingolimod) behandling
 Detta läkemedel är föremål för utökad övervakning. Viktiga saker att komma ihåg om din GILENYA (fingolimod) behandling Din läkare kommer att be dig att stanna kvar på mottagningen eller kliniken i minst
Detta läkemedel är föremål för utökad övervakning. Viktiga saker att komma ihåg om din GILENYA (fingolimod) behandling Din läkare kommer att be dig att stanna kvar på mottagningen eller kliniken i minst
XELJANZ. Den här broschyren är avsedd för dig som har ordinerats XELJANZ. Du hittar mer information i bipacksedeln som medföljer läkemedlet.
 XELJANZ Den här broschyren är avsedd för dig som har ordinerats XELJANZ. Du hittar mer information i bipacksedeln som medföljer läkemedlet. TILL DIG SOM BEHANDLAS MED XELJANZ, Din läkare har skrivit ut
XELJANZ Den här broschyren är avsedd för dig som har ordinerats XELJANZ. Du hittar mer information i bipacksedeln som medföljer läkemedlet. TILL DIG SOM BEHANDLAS MED XELJANZ, Din läkare har skrivit ut
Bipacksedel: information till användaren. Panodil 60 mg suppositorier Panodil 500 mg suppositorier. Panodil 1 g suppositorier.
 Bipacksedel: information till användaren Panodil 60 mg suppositorier Panodil 125 mg suppositorier Panodil 250 mg suppositorier Panodil 500 mg suppositorier Panodil 1 g suppositorier paracetamol Läs noga
Bipacksedel: information till användaren Panodil 60 mg suppositorier Panodil 125 mg suppositorier Panodil 250 mg suppositorier Panodil 500 mg suppositorier Panodil 1 g suppositorier paracetamol Läs noga
Bipacksedel: Information till användaren. Mucoangin Citron 20 mg sugtabletter ambroxolhydroklorid
 Bipacksedel: Information till användaren Mucoangin Citron 20 mg sugtabletter ambroxolhydroklorid Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som
Bipacksedel: Information till användaren Mucoangin Citron 20 mg sugtabletter ambroxolhydroklorid Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Doxyferm 100 mg tabletter doxycyklinmonohydrat Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Doxyferm 100 mg tabletter doxycyklinmonohydrat Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig
PRODUKTRESUMÉ. Vid besvär från andningsvägarna rekommenderas medicinsk rådgivning om symtomen inte förbättras.
 PRODUKTRESUMÉ 1. LÄKEMEDLETS NAMN Bisolvon 0,8 mg/ml oral lösning 2. KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 ml innehåller: bromhexinhydroklorid 0,8 mg Hjälpämne: flytande maltitol 500 mg För fullständig
PRODUKTRESUMÉ 1. LÄKEMEDLETS NAMN Bisolvon 0,8 mg/ml oral lösning 2. KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 ml innehåller: bromhexinhydroklorid 0,8 mg Hjälpämne: flytande maltitol 500 mg För fullständig
Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för dig.
 Flukloxacillin 500 mg, 750 mg filmdragerade tabletter flukloxacillin Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för dig. - Spara denna
Flukloxacillin 500 mg, 750 mg filmdragerade tabletter flukloxacillin Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för dig. - Spara denna
Bipacksedel: Information till patienten. Etrilect 0,5 mg/ml + 1 mg/ml oral lösning. Bromhexinhydroklorid och efedrinhydroklorid
 Bipacksedel: Information till patienten Etrilect 0,5 mg/ml + 1 mg/ml oral lösning Bromhexinhydroklorid och efedrinhydroklorid Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel.
Bipacksedel: Information till patienten Etrilect 0,5 mg/ml + 1 mg/ml oral lösning Bromhexinhydroklorid och efedrinhydroklorid Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel.
Sammanfattning av riskhanteringsplanen (RMP) för Portrazza (necitumumab)
 EMA/33513/2016 Sammanfattning av riskhanteringsplanen (RMP) för Portrazza (necitumumab) Detta är en sammanfattning av riskhanteringsplanen för Portrazza som beskriver åtgärder som ska vidtas för att säkerställa
EMA/33513/2016 Sammanfattning av riskhanteringsplanen (RMP) för Portrazza (necitumumab) Detta är en sammanfattning av riskhanteringsplanen för Portrazza som beskriver åtgärder som ska vidtas för att säkerställa
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Citodon 500 mg/30 mg brustabletter paracetamol och kodein Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
Bipacksedel: Information till användaren Citodon 500 mg/30 mg brustabletter paracetamol och kodein Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Citodon 500 mg/30 mg brustabletter paracetamol och kodein Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
Bipacksedel: Information till användaren Citodon 500 mg/30 mg brustabletter paracetamol och kodein Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
Diane huvudversion av patientkort och checklista för förskrivare 17/12/2014. Patientinformationskort:
 Patientinformationskort: Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de
Patientinformationskort: Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de
Metacam. meloxikam. Vad är Metacam och vad används det för? Sammanfattning av EPAR för allmänheten
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Sammanfattning av EPAR för allmänheten meloxikam Detta är en sammanfattning av det offentliga europeiska utredningsprotokollet (EPAR) för. Det förklarar hur EMA bedömt
EMA/CVMP/259397/2006 EMEA/V/C/000033 Sammanfattning av EPAR för allmänheten meloxikam Detta är en sammanfattning av det offentliga europeiska utredningsprotokollet (EPAR) för. Det förklarar hur EMA bedömt
Din guide till YERVOY Patientbroschyr
 Innehållet i denna broschyr är förenligt med villkor, enligt marknadsföringstillståndet, avseende en säker och effektiv användning av YERVOY TM Din guide till YERVOY Patientbroschyr Bristol-Myers Squibb
Innehållet i denna broschyr är förenligt med villkor, enligt marknadsföringstillståndet, avseende en säker och effektiv användning av YERVOY TM Din guide till YERVOY Patientbroschyr Bristol-Myers Squibb
Din guide till YERVOY (ipilimumab)
 Detta utbildningsmaterial är obligatoriskt enligt ett villkor i godkännandet för försäljning av YERVOY TM för att ytterligare minimera särskilda risker. Din guide till YERVOY (ipilimumab) Patientbroschyr
Detta utbildningsmaterial är obligatoriskt enligt ett villkor i godkännandet för försäljning av YERVOY TM för att ytterligare minimera särskilda risker. Din guide till YERVOY (ipilimumab) Patientbroschyr
PRODUKTRESUMÉ. 750 mg: Vit, avlång, bikonvex tablett märkt med F 750 på en sida och med brytskåra på den
 PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Flucloxacillin Sandoz 500 mg filmdragerade tabletter Flucloxacillin Sandoz 750 mg filmdragerade tabletter 2 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 tablett innehåller
PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Flucloxacillin Sandoz 500 mg filmdragerade tabletter Flucloxacillin Sandoz 750 mg filmdragerade tabletter 2 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING 1 tablett innehåller
Bilaga I. Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning
 Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning 1 Vetenskapliga slutsatser Med hänsyn till PRAC:s utredningsprotokoll om den periodiska säkerhetsrapporten
Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännande för försäljning 1 Vetenskapliga slutsatser Med hänsyn till PRAC:s utredningsprotokoll om den periodiska säkerhetsrapporten
Bipacksedel: Information till användaren. Citodon forte 1 g/60 mg suppositorier. paracetamol och kodein
 Bipacksedel: Information till användaren Citodon forte 1 g/60 mg suppositorier paracetamol och kodein Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
Bipacksedel: Information till användaren Citodon forte 1 g/60 mg suppositorier paracetamol och kodein Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
Bipacksedel: Information till användaren. Citodon 500 mg/30 mg tabletter. paracetamol och kodein
 Bipacksedel: Information till användaren Citodon 500 mg/30 mg tabletter paracetamol och kodein Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som
Bipacksedel: Information till användaren Citodon 500 mg/30 mg tabletter paracetamol och kodein Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som
Bipacksedel: Information till användaren. Alvedon forte 1 g filmdragerade tabletter. paracetamol
 Bipacksedel: Information till användaren Alvedon forte 1 g filmdragerade tabletter paracetamol Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som
Bipacksedel: Information till användaren Alvedon forte 1 g filmdragerade tabletter paracetamol Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som
Denna broschyr har du fått av din behandlande läkare. Guide för anhöriga. Svar på dina frågor. www.bms.se
 Denna broschyr har du fått av din behandlande läkare Guide för anhöriga Svar på dina frågor Att ta hand om någon med avancerat malignt melanom är inte en lätt uppgift. Det kan också kännas oroväckande
Denna broschyr har du fått av din behandlande läkare Guide för anhöriga Svar på dina frågor Att ta hand om någon med avancerat malignt melanom är inte en lätt uppgift. Det kan också kännas oroväckande
Skärpta rekommendationer avseende risken för allvarliga överkänslighetsreaktioner vid användning av Rienso (ferumoxytol)
 8 januari 2014 Skärpta rekommendationer avseende risken för allvarliga överkänslighetsreaktioner vid användning av Rienso (ferumoxytol) Bästa hälso- och sjukvårdspersonal, I oktober 2013 skickades ett
8 januari 2014 Skärpta rekommendationer avseende risken för allvarliga överkänslighetsreaktioner vid användning av Rienso (ferumoxytol) Bästa hälso- och sjukvårdspersonal, I oktober 2013 skickades ett
4.1 Terapeutiska indikationer Flukloxacillin Meda används när stafylokocketiologi misstänks eller verifierats:
 PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Flukloxacillin Meda 500 mg filmdragerade tabletter Flukloxacillin Meda 750 mg filmdragerade tabletter Flukloxacillin Meda 1 g filmdragerade tabletter 2 KVALITATIV OCH KVANTITATIV
PRODUKTRESUMÉ 1 LÄKEMEDLETS NAMN Flukloxacillin Meda 500 mg filmdragerade tabletter Flukloxacillin Meda 750 mg filmdragerade tabletter Flukloxacillin Meda 1 g filmdragerade tabletter 2 KVALITATIV OCH KVANTITATIV
TILL DIG SOM FÅTT LAMICTAL ORDINERAT PATIENTINFORMATION
 TILL DIG SOM FÅTT LAMICTAL ORDINERAT PATIENTINFORMATION TILL DIG SOM FÅTT LAMICTAL Du har fått en receptbelagd medicin som heter Lamictal utskrivet av din doktor. Lamictal är en förebyggande behandling
TILL DIG SOM FÅTT LAMICTAL ORDINERAT PATIENTINFORMATION TILL DIG SOM FÅTT LAMICTAL Du har fått en receptbelagd medicin som heter Lamictal utskrivet av din doktor. Lamictal är en förebyggande behandling
Information till hälso- och sjukvårdspersonal
 13 maj 2013 Information till hälso och sjukvårdspersonal Nya begränsningar för Protelos/Osseor (strontiumranelat) i behandling av osteoporos på grund av ökad risk för hjärtinfarkt Bästa förskrivare! Detta
13 maj 2013 Information till hälso och sjukvårdspersonal Nya begränsningar för Protelos/Osseor (strontiumranelat) i behandling av osteoporos på grund av ökad risk för hjärtinfarkt Bästa förskrivare! Detta
Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännandena för försäljning
 Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännandena för försäljning Vetenskapliga slutsatser Med hänsyn till PRAC:s utredningsprotokoll om de periodiska säkerhetsrapporterna
Bilaga I Vetenskapliga slutsatser och skäl till ändring av villkoren för godkännandena för försäljning Vetenskapliga slutsatser Med hänsyn till PRAC:s utredningsprotokoll om de periodiska säkerhetsrapporterna
Till dig som får behandling med Zyvoxid (linezolid) M-PRO-06-ZYV-023-SGn-ELIXIR
 Till dig som får behandling med Zyvoxid (linezolid) M-PRO-06-ZYV-023-SGn-ELIXIR Önskas mer info? Ring Pfizer Kunskapscentrum. Direktnummer för sjukvården: 08-550 522 00. Pfizer AB. Telefon 08-550 520 00.
Till dig som får behandling med Zyvoxid (linezolid) M-PRO-06-ZYV-023-SGn-ELIXIR Önskas mer info? Ring Pfizer Kunskapscentrum. Direktnummer för sjukvården: 08-550 522 00. Pfizer AB. Telefon 08-550 520 00.
Bipacksedel: Information till användaren. Tibinide 300 mg tabletter isoniazid
 Bipacksedel: Information till användaren Tibinide 300 mg tabletter isoniazid Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. - Spara denna information, du kan behöva läsa den igen.
Bipacksedel: Information till användaren Tibinide 300 mg tabletter isoniazid Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. - Spara denna information, du kan behöva läsa den igen.
OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN
 Hydroxyzinhydrochlorid EQL Pharma 25 mg filmdragerade tabletter datum 7.1.2014, version 1.1 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 Delområden av en offentlig sammanfattning VI.2.1 Information
Hydroxyzinhydrochlorid EQL Pharma 25 mg filmdragerade tabletter datum 7.1.2014, version 1.1 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 Delområden av en offentlig sammanfattning VI.2.1 Information
Handläggning av antibiotikaallergi
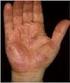 VO INFEKTIONSSJUKDOMAR Dokumenttyp: Medicinskt PM Titel: Antibiotikaallergi Dokumentansvarig: Simon Werner, Malmö Malin Inghammar, Lund Godkänt av: Peter Lanbeck Publicerat av: Irene Silfver Reviderad
VO INFEKTIONSSJUKDOMAR Dokumenttyp: Medicinskt PM Titel: Antibiotikaallergi Dokumentansvarig: Simon Werner, Malmö Malin Inghammar, Lund Godkänt av: Peter Lanbeck Publicerat av: Irene Silfver Reviderad
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Nitrofurantoin Alternova 50 mg tabletter nitrofurantoin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som
Bipacksedel: Information till användaren Nitrofurantoin Alternova 50 mg tabletter nitrofurantoin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som
Innehållet i denna broschyr är förenligt med villkor, enligt marknadsföringstillståndet, avseende en säker och effektiv användning av YERVOY
 Innehållet i denna broschyr är förenligt med villkor, enligt marknadsföringstillståndet, avseende en säker och effektiv användning av YERVOY Broschyr till hälso- och sjukvårdspersonal Vanliga frågor om
Innehållet i denna broschyr är förenligt med villkor, enligt marknadsföringstillståndet, avseende en säker och effektiv användning av YERVOY Broschyr till hälso- och sjukvårdspersonal Vanliga frågor om
OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN
 Telmisartan/Hydrochlorothiazide ratiopharm 4.12.2014, Version 2.0 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 Delområden av den offentliga sammanfattningen VI.2.1 Information om sjukdomsförekomst
Telmisartan/Hydrochlorothiazide ratiopharm 4.12.2014, Version 2.0 OFFENTLIG SAMMANFATTNING AV RISKHANTERINGSPLANEN VI.2 Delområden av den offentliga sammanfattningen VI.2.1 Information om sjukdomsförekomst
Bipacksedel: Information till användaren. Doxyferm 20 mg/ml koncentrat till infusionsvätska, lösning. doxycyklin
 Bipacksedel: Information till användaren Doxyferm 20 mg/ml koncentrat till infusionsvätska, lösning doxycyklin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller
Bipacksedel: Information till användaren Doxyferm 20 mg/ml koncentrat till infusionsvätska, lösning doxycyklin Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller
Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Dasselta 5 mg filmdragerade tabletter desloratadin Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig
Bipacksedel: Information till användaren Dasselta 5 mg filmdragerade tabletter desloratadin Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig
