EPP06 Patientinformation, Version
|
|
|
- Erik Hansson
- för 5 år sedan
- Visningar:
Transkript
1 Enrolleringsnummer: Initialer: Information till försökspersonerna (Enkel/Multipel stigande dos) Säkerhet och tolerabilitet av lokalt applicerad EP0003 kräm 0.45 % hos friska frivilliga försökspersoner och patienter med rosacea Du är tillfrågad om att delta i en studie där vi ska pröva ett nytt läkemedel, en kräm, som avser mildra besvären av rosacea, vilken är en relativt vanlig hudsjukdom. Krämen är tidigare ej prövad på människa och i denna studie är det första gången som krämen ska prövas på människa. Studien är granskad och godkänd av Etikprövningsnämnden i Göteborg Bakgrund Rosacea drabbar ca 2-10 % av vuxna personer över 30 år och huvudsakligen centralt i ansiktet såsom pannan, kinderna och hakan med ytliga blodkärl, röd hud, knottror, små varblåsor och ibland sveda. Det är oklart vad rosacea beror på, men sjukdomen är en inflammatorisk hudsjukdom som inte beror på bakterier och som inte är smittsam. Det finns flera olika förklaringar till uppkomsten av rosacea men ingen är allmänt accepterad. Ofta kan en försämring provoceras av sol, värme, kyla, blåst, starka kryddor, heta drycker, alkohol, stress eller olika irriterande kemikalier på huden (ibland även av vanliga hudkrämer). Dagens behandlingar innefattar krämer och geler som innehåller metronidazol, azelainsyra, ivermektin eller brimonidine. De har antibakteriella, antiinflammatoriska eller kärlsammandragande egenskaper. Det tar ofta flera veckor innan symptomen försvinner, effekten är kortvarig och efter avslutad behandling kommer symptomen oftast tillbaka. Tetracyklin i tablettform användas ibland när ovan preparat inte hjälper. Det finns ett medicinskt behov för en mer effektiv behandling, ett snabbare anslag och kortare behandlingsperioder. Syftet med studien är att pröva en ny substans (EP0003 kräm 0,45 %) som fungerar på ett annat vis än befintliga mediciner. EP0003 är ett blödningshämmande medel som hindrar effekten av det enzym som löser upp blodkoagel och tros kunna ha positiva effekter på rosacea. Hur går studien till? Både friska frivilliga personer och personer med rosacea ingår i studien som består av två delar, Enkel dos respektive Multipel dos, och omfattar totalt 5 besök på kliniken. Första besöket: Vi kommer att ställa frågor om ålder, tidigare och nuvarande sjukdomar, nikotinoch alkoholvanor samt vilka mediciner du tar. Hälsoundersökning genomförs och blodprover, EKG och blodtryck tas. På kvinnor i fertil ålder görs ett graviditetstest som upprepas på studiedag 1 och 2. Besöket tar ca 60 minuter. Om du uppfyller kriterierna för att kunna delta sätter vi upp tid till den första studiedagen. Studiedag 1, Enkel dos, ca 9 timmar: Sjuksköterskan applicerar studiekrämen på höger och vänster kind samt höger och vänster underarm. På ena ansiktshalvan och ena underarmen får du kräm med EP0003 och på andra sidan/underarmen får du kräm utan tillsats av EP0003 (placebo). Detta sker på ett dubbel-blint sätt vilket betyder att varken du eller vi vet vilken sida som får aktiv substans respektive placebo. Koden bryts efter studiens slut. 1
2 Under dagens lopp görs följande undersökningar: Puls och Blodtryck Blodprover tas under dagen ur en kanyl som sätts på morgonen när du kommer. Dessa prover kommer analyseras med avseende koncentrationen av EP0003 i blodet. Du samlar urin under hela dagen. På eftermiddagen får du med dig en plastflaska för att fortsätta samla urin i hemmet ända tills nästa morgon (=24 timmars-urin). Hudområdet på kinderna och underarmarna fotograferas vid totalt 4 tillfällen Huden bedöms av läkaren enligt en 5-gradig skala Vi registrerar biverkningar som eventuellt uppstår Studiedag 2, Enkel dos, ca 3 timmar Under förmiddagen görs följande undersökningar: Puls och Blodtryck Blodprov för koncentration av EP0003 i blodet och för fortsatt kontroll av dina blodvärden Fotografering av hudområdet på kinderna och underarmarna. Huden bedöms av läkare enligt en 5-gradig skala Vi registrerar eventuella biverkningar Studiedag 1, Multipel dos, ca 9 timmar: Efter några veckor kommer Du tillbaka till kliniken för en ny studiedag med samma upplägg som förra gången men med den skillnaden att krämen appliceras två gånger under dagen. Samma undersökningar som ovan förutom urinsamlingen. Du får med dig 2 olika slags tuber kräm hem som du själv skall applicera morgon och kväll under 7 dagar. Du får även med dig en dagbok för att fylla i tidpunkterna när du applicerar krämen och för att registrera hur huden ser ut och om du får några biverkningar. Studiedag 8, Multipel dos, ca 9 timmar: Efter 7 dagars behandling hemma morgon och kväll kommer du till kliniken en sista gång och undersökningarna upprepas återigen. Du kommer att få samla urin igen med start kvällen före besöket (du får med dig en plastflaska hem). Ytterligare blod tas för att se att dina värden fortfarande är normala. Telefonuppföljning. Cirka en vecka efter studiedag 1 Enkel dos och studiedag 8 Multipel dos ringer vi upp dig för att höra att allt är bra. Att tänka på Undvik följande under hela studieperiodens aktiva dagar: lotions, krämer, geler och parfym i ansiktet och på armarna alla typer av sminkprodukter i ansiktet t.ex. krämer, brunkrämer, puder, ögonskugga solexponering. Använd solhatt eller keps utomhus kryddad mat bastu alkohol och tobak från kl. 22:00 dagen före en studiedag på kliniken mediciner som innehåller: tretinoin, adapalene, antibiotika eller kortison du tar/tagit före och under studien. informera doktorn vilka mediciner 2
3 Vi ber dig vara noggrann med handhygien. Tvätta alltid händerna varje gång efter du har använt krämen. Gäller efter var och en av tuberna! Eventuella biverkningar, risker och obehag Liksom alla läkemedel kan detta läkemedel orsaka biverkningar. Biverkningar som man idag inte känner till kan uppkomma under studien. Denna studie tar hänsyn till detta och substansen kommer att prövas försiktigt i mycket små doser som långsamt ökas. På så vis kan man fånga upp eventuella biverkningar samt lokala hudreaktioner under kontrollerade former. De möjliga risker som kan kopplas till studieprodukten bedöms som små. Studien genomförs enligt protokoll med höga säkerhetsmarginaler. Gedigna tester på själva den aktiva substansen är gjorda. Det har också gjorts undersökningar med krämen på kaninöron utan att några uppenbara biverkningar har uppstått. Sticket när kanylen sätts på plats kan upplevas som obehagligt och ger ibland ett blåmärke och en ömhet som kan kvarstå ett par dagar. Maximalt 75 ml blod kommer att tas under hela studien, vilket kan jämföras med 450 ml som normalt tas vid en vanlig blodgivning. Finns det några fördelar med att delta? Det är inte säkert att det innebär några omedelbara fördelar för dig att medverka i denna studie förutom att du får genomgå en läkarundersökning och blodprovsanalys vid tre tillfällen. För patienterna kan lokalbehandlingen av hudsjukdom eventuellt ge positiva effekter. I förlängningen kan vidareutveckling av EP0003 leda till en godkänd och effektiv behandling av hudsjukdomar av typen rosacea. Kostnader, Ersättning och Försäkringsskydd Att vara med i studien medför inga kostnader för dig. Deltagare i studien ersätts med ett skattepliktigt belopp, kr. Om du avbryter studien i förtid ersätts du i förhållande till ditt deltagande. Beloppet är skattepliktigt. Liksom inom sjukvården i övrigt omfattas du av Läkemedelsförsäkringen och Patientförsäkringen. Hantering av personuppgifter och sekretess Under studien kommer vi att samla in data såsom födelsedatum, kön, hälsodata samt resultat av undersökningar i studien. Detta noteras i ett särskilt studieprotokoll. En person utsedd av kliniken eller en myndighetsperson kan komma att jämföra insamlad studiedata med din medicinska journal i kvalitetssyfte för att se om studien blivit rätt genomförd. Dessa personer måste underteckna en sekretessförbindelse innan de får tillgång till dina data. Personuppgifterna lagras i en databas och registreras i enlighet med personuppgiftslagen (SFS 1998:204). Information kopplad till undersökningarna och behandlingen lagras i din journal enligt patientjournallagen (SoSFS 1993:20). Utförarstyrelsen för Sahlgrenska Universitetssjukhuset är ansvarig för behandlingen av personuppgifterna. Du har rätt att få veta vilka uppgifter som har registrerats om dig och få utdrag av dessa. Vid ev. frågor kan du kontakta ansvarig läkare för studien. Du kan även vända dig till personuppgiftsombudet på sjukhuset: Susan Lindahl, Sahlgrenska universitetssjukhuset, Torggatan 1, Mölndal. Tel
4 Datahantering Studiedata (personuppgifter, provsvar och resultat från mätningar) kommer att förses med en kodsiffra som är specifik för dig. Insamlade uppgifter överlämnas till företaget som tillverkar substansen utan ditt namn eller personnummer. Ansvarig läkare ansvarar för den kodnyckel med vilken det går att koppla uppgifterna till just dig och som sparas i ett lösenordskyddat datordokument på sjukhuset. Signerade samtycken och data som genereras i studien lagras i minst 10 år och behandlas så att obehöriga inte har åtkomst. Endast läkare och sjuksköterskor involverade i studien har tillgång till studiedata. Resultaten kommer att presenteras och publiceras på vetenskapliga möten och i vetenskapliga tidskrifter. En sammanfattning av studien kommer att lämnas till läkemedelsverket. Resultaten redovisas endast på statistisk gruppnivå och kan inte kopplas till någon enskild individ Hantering av blod- och urinprover Rutinproverna analyseras på Sahlgrenska sjukhusets laboratorium. Blodet för att bestämma koncentrationen av läkemedlet i blodet analyseras av ett svenskt laboratorium som är förlagt till AstraZenecas lokaler i Mölndal. Prover kommer att tillhöra Sahlgrenska Biobank nr 890 under tiden tills dess att analyserna är genomförda och proverna förvaras och hanteras i kodad form liksom övriga studiedata. Samtliga prover kommer att förstöras i analysprocessen och kommer därmed inte att sparas för framtida bruk. Frivillighet Ditt deltagande i studien är helt frivilligt. Du har rätt att när som helst och utan närmare förklaring avbryta ditt deltagande. Ett sådant beslut påverkar inte omhändertagande eller behandling av din grundsjukdom. Om du väljer att avbryta ditt deltagande är det önskvärt att du kommer på ett avslutande besök. Hur får jag information om mina resultat? Resultaten kommer att publiceras i vetenskapliga tidskrifter och presenteras på vetenskapliga möten. Enbart statistik kommer att presenteras och ingen enskild person kommer att kunna identifieras. Kontaktpersoner Ansvarig läkare för studien är Dr. Dan Curiac på Gothia Forum, Sahlgrenska sjukhuset. Har Du några frågor angående studien, vänligen kontakta: Ingrid Hedenquist, studiesköterska på telefonnummer: Tel
5 Skriftligt samtycke Jag har muntligen informerats om ovanstående studie och läst bifogad skriftlig information. Jag har fått tillfälle att ställa frågor och fått eventuella frågor besvarade. Jag känner till att mitt deltagande är helt frivilligt. Jag är medveten om att jag när som helst och utan närmare förklaring kan avbryta mitt deltagande utan att det påverkar mitt framtida omhändertagande. Jag samtycker till: Att delta i studien Att studiedata (mina personuppgifter) får behandlas som beskrivits Att mina prover får användas som beskrivits Att en person utsedd av kliniken eller en myndighetsperson får jämföra insamlade Studiedata med information i min medicinska journal. Detta får ske under förbehåll av sekretess. Datum (ifylls av patienten) Patientens underskrift Behandlingsansvarig Namnförtydligande Jag har informerat patienten om studien och patienten har fått tillfälle att ställa frågor. Patienten har lämnat sitt samtycke till att delta. Läkarens namn Datum Underskrift En kopia av denna signerade patientinformation ges till patienten 5
Information till forskningsperson
 Information till forskningsperson En dosundersökande studie i två delar utförd på friska forskningspersoner med syfte att utvärdera säkerhet, tolerabilitet och effekter med LMW-DS infusionslösning efter
Information till forskningsperson En dosundersökande studie i två delar utförd på friska forskningspersoner med syfte att utvärdera säkerhet, tolerabilitet och effekter med LMW-DS infusionslösning efter
Syftet med det planerade försöket är att ta reda på hur kroppen påverkas vid belastning av en vikt, i det här fallet en viktväst.
 Forskningspersonsinformation och samtycke Du tillfrågas härmed att frivilligt delta i följande studie: Effekten av viktvästar på kroppsvikt hos överviktiga individer Syfte Syftet med det planerade försöket
Forskningspersonsinformation och samtycke Du tillfrågas härmed att frivilligt delta i följande studie: Effekten av viktvästar på kroppsvikt hos överviktiga individer Syfte Syftet med det planerade försöket
rosacea Information om ett vuxet problem
 rosacea Information om ett vuxet problem Rosacea. Rosacea drabbar omkring 2 10 procent av den vuxna befolkningen. Det är en kronisk hudsjukdom som ger rodnader, knottror och inflammerade utslag i ansiktet,
rosacea Information om ett vuxet problem Rosacea. Rosacea drabbar omkring 2 10 procent av den vuxna befolkningen. Det är en kronisk hudsjukdom som ger rodnader, knottror och inflammerade utslag i ansiktet,
Information om ett vuxet problem
 r o s a c e a Information om ett vuxet problem ROSACEA. Rosacea drabbar omkring 2 10 procent av den vuxna befolkningen. Det är en kronisk hudsjukdom som ger rodnader, knottror och inflammerade utslag i
r o s a c e a Information om ett vuxet problem ROSACEA. Rosacea drabbar omkring 2 10 procent av den vuxna befolkningen. Det är en kronisk hudsjukdom som ger rodnader, knottror och inflammerade utslag i
Försökspersonsinformation och Samtycke
 Försökspersonsinformation och Samtycke Titel BUP1502: En öppen studie som har för avsikt att bekräfta att farmakokinetiken av plåster innehållandes buprenorfin är liknande hos äldre och yngre personer.
Försökspersonsinformation och Samtycke Titel BUP1502: En öppen studie som har för avsikt att bekräfta att farmakokinetiken av plåster innehållandes buprenorfin är liknande hos äldre och yngre personer.
PATIENTINFORMATION. E-kod/Initialer:.
 PATIENTINFORMATION En placebo-kontrollerad, dubbel-blindad, randomiserad studie på patienter med typ 2-diabetes för att utvärdera om läkemedlen Epanova och dapagliflozin kan minska andelen fett i levern.
PATIENTINFORMATION En placebo-kontrollerad, dubbel-blindad, randomiserad studie på patienter med typ 2-diabetes för att utvärdera om läkemedlen Epanova och dapagliflozin kan minska andelen fett i levern.
Information till försökspersoner som deltar i en studie av ett nytt drickbart vaccin mot ETEC-diarré
 Information till försökspersoner som deltar i en studie av ett nytt drickbart vaccin mot ETEC-diarré Vill du vara med i en studie där vi prövar ett nytt drickbart vaccin mot diarré som orsakas av så kallade
Information till försökspersoner som deltar i en studie av ett nytt drickbart vaccin mot ETEC-diarré Vill du vara med i en studie där vi prövar ett nytt drickbart vaccin mot diarré som orsakas av så kallade
Vill du vara med i forskningsstudien ALASCCA?
 Vill du vara med i forskningsstudien ALASCCA? Du tillfrågas härmed om du vill delta i forskningsstudien ALASCCA. Läs igenom denna information noggrant och i lugn och ro innan du bestämmer dig för om du
Vill du vara med i forskningsstudien ALASCCA? Du tillfrågas härmed om du vill delta i forskningsstudien ALASCCA. Läs igenom denna information noggrant och i lugn och ro innan du bestämmer dig för om du
Patientinformation & Informerat samtycke PATIENTINFORMATION
 PATIENTINFORMATION Klinisk läkemedelsstudie ASA-CRCLM-2014 En multi-center, dubbel-blind, placebo-jämförande, randomiserad studie för att utvärdera säkerhet och effekt av acetylsalicylsyra eller placebo
PATIENTINFORMATION Klinisk läkemedelsstudie ASA-CRCLM-2014 En multi-center, dubbel-blind, placebo-jämförande, randomiserad studie för att utvärdera säkerhet och effekt av acetylsalicylsyra eller placebo
Rosacea I N F O R M AT I O N O M E T T V U X E T P R O B L E M
 Rosacea I N FO R M AT I O N O M E T T V UX E T P RO B L E M Rosacea. Rosacea drabbar omkring 10 procent av den vuxna befolkningen och är en kronisk hudsjukdom med utslag i de centrala delarna av ansiktet,
Rosacea I N FO R M AT I O N O M E T T V UX E T P RO B L E M Rosacea. Rosacea drabbar omkring 10 procent av den vuxna befolkningen och är en kronisk hudsjukdom med utslag i de centrala delarna av ansiktet,
rosacea Information om ett vuxet problem
 rosacea Information om ett vuxet problem 1 RosaceA är den medicinska termen för ett antal hudsymptom som oftast uppträder hos personer över 30 år. (ej att förväxla med akne) Hudproblem Finnar Hudproblem
rosacea Information om ett vuxet problem 1 RosaceA är den medicinska termen för ett antal hudsymptom som oftast uppträder hos personer över 30 år. (ej att förväxla med akne) Hudproblem Finnar Hudproblem
Vill du delta i en undersökning om matvanor?
 Till ungdomar i åk 2 på gymnasiet Vill du delta i en undersökning om matvanor? Bakgrund och syfte med Riksmaten ungdom Livsmedelsverket jobbar för säker mat och för bra matvanor. Livsmedelsverket behöver
Till ungdomar i åk 2 på gymnasiet Vill du delta i en undersökning om matvanor? Bakgrund och syfte med Riksmaten ungdom Livsmedelsverket jobbar för säker mat och för bra matvanor. Livsmedelsverket behöver
Patientinformation. Denna studie har godkänts av en oberoende etikprövningsnämnd för att garantera din säkerhet och dina rättigheter.
 Patientinformation En dubbel-blind, randomiserad, placebo-kontrollerad, multicenter, klinisk fas IV-studie för att utvärdera prestanda, säkerhet och användbarhet av myrsyra på patienter med vårtor på händer,
Patientinformation En dubbel-blind, randomiserad, placebo-kontrollerad, multicenter, klinisk fas IV-studie för att utvärdera prestanda, säkerhet och användbarhet av myrsyra på patienter med vårtor på händer,
rosacea Information om ett vuxet problem
 rosacea Information om ett vuxet problem 1 RosaceA är den medicinska termen för ett antal hudsymptom som oftast uppträder hos personer över 30 år. (ej att förväxla med akne) Cirka Symptomen på rosacea
rosacea Information om ett vuxet problem 1 RosaceA är den medicinska termen för ett antal hudsymptom som oftast uppträder hos personer över 30 år. (ej att förväxla med akne) Cirka Symptomen på rosacea
Patientinformationsblad för studien PPL07
 Prövningstitel: Studie för att utvärdera effekten av kontinuerlig infusion av tafoxiparin för behandling av långsamt eller avstannat värkarbete hos fullgångna förstföderskor. Du tillfrågas om att vara
Prövningstitel: Studie för att utvärdera effekten av kontinuerlig infusion av tafoxiparin för behandling av långsamt eller avstannat värkarbete hos fullgångna förstföderskor. Du tillfrågas om att vara
Patientinformation 1(5)
 1(5) Patientinformation Du tillfrågas härmed om att delta i en studie med läkemedlen Avastin (bevacizumab) Tarceva (erlotinib) och Xeloda (capecitabine) för patienter med spridd tjock- /ändtarmscancer.
1(5) Patientinformation Du tillfrågas härmed om att delta i en studie med läkemedlen Avastin (bevacizumab) Tarceva (erlotinib) och Xeloda (capecitabine) för patienter med spridd tjock- /ändtarmscancer.
Forskningspersonsinformation och Samtycke
 Titel: Disulfiram som tillägg till kemoterapibehandling vid recidiv av glioblastom; en randomiserad, kontrollerad studie. Vi tillfrågar dig som behandlas för en hjärntumör om du vill medverka i en forskningsstudie
Titel: Disulfiram som tillägg till kemoterapibehandling vid recidiv av glioblastom; en randomiserad, kontrollerad studie. Vi tillfrågar dig som behandlas för en hjärntumör om du vill medverka i en forskningsstudie
Patientinformation. Bakgrund och studiemål
 Patientinformation I PsAer-IgY studien kommer vi att undersöka om långtidsanvändning av en ny medicin mot Pseudomonas-bakterien har möjlighet att förlänga tiden till återfall av Pseudomonasinfektion hos
Patientinformation I PsAer-IgY studien kommer vi att undersöka om långtidsanvändning av en ny medicin mot Pseudomonas-bakterien har möjlighet att förlänga tiden till återfall av Pseudomonasinfektion hos
Patientinformation och informerat samtycke
 Patientinformation och informerat samtycke Patientinformation Du tillfrågas härmed om att delta i en studie vid ändtarmscancer. Studien testar om det finns fördel med att ge tilläggsbehandling med cytostatika
Patientinformation och informerat samtycke Patientinformation Du tillfrågas härmed om att delta i en studie vid ändtarmscancer. Studien testar om det finns fördel med att ge tilläggsbehandling med cytostatika
Apotekets råd om. Akne och rosacea
 Apotekets råd om Akne och rosacea Akne är ett samlingsnamn för förändringar i form av hudknottror, pormaskar och varblåsor och är mycket vanligt. Akne beror inte på dålig hygien eller speciell mat utan
Apotekets råd om Akne och rosacea Akne är ett samlingsnamn för förändringar i form av hudknottror, pormaskar och varblåsor och är mycket vanligt. Akne beror inte på dålig hygien eller speciell mat utan
Forskningsdeltagarinformation. Effekter av nyutvecklad madrass och kudde för nattlig bäckensmärta under graviditet
 Bilaga 1 Forskningsdeltagarinformation Effekter av nyutvecklad madrass och kudde för nattlig bäckensmärta under graviditet Bakgrund och syfte Bäckensmärta under graviditet är ett vanligt förekommande besvär.
Bilaga 1 Forskningsdeltagarinformation Effekter av nyutvecklad madrass och kudde för nattlig bäckensmärta under graviditet Bakgrund och syfte Bäckensmärta under graviditet är ett vanligt förekommande besvär.
Patientinformation. Denna studie har godkänts av en oberoende etikprövningsnämnd för att garantera din säkerhet och dina rättigheter.
 Patientinformation En dubbel-blind, randomiserad, placebo-kontrollerad, multicenter, klinisk fas IV-studie för att utvärdera prestanda, säkerhet och användbarhet av myrsyra på patienter med vårtor på händer,
Patientinformation En dubbel-blind, randomiserad, placebo-kontrollerad, multicenter, klinisk fas IV-studie för att utvärdera prestanda, säkerhet och användbarhet av myrsyra på patienter med vårtor på händer,
Information till deltagare i forskningsstudien:
 Information till deltagare i forskningsstudien: En single-center studie för utvärdering av ViscoGels säkerhet samt dess säkerhet och effekt som adjuvans i Act-HIB vaccinet administrerat intramuskulärt
Information till deltagare i forskningsstudien: En single-center studie för utvärdering av ViscoGels säkerhet samt dess säkerhet och effekt som adjuvans i Act-HIB vaccinet administrerat intramuskulärt
Om att delta i en klinisk prövning
 Om att delta i en klinisk prövning Innehåll Vad är en klinisk prövning och hur utförs den? 5 Varför görs kliniska prövningar? 7 Varför gör min läkare kliniska prövingar? 7 Hur utförs en klinisk prövning?
Om att delta i en klinisk prövning Innehåll Vad är en klinisk prövning och hur utförs den? 5 Varför görs kliniska prövningar? 7 Varför gör min läkare kliniska prövingar? 7 Hur utförs en klinisk prövning?
rosacea Information om ett vuxet problem
 rosacea Information om ett vuxet problem 1 RosaceA är den medicinska termen för ett antal hudsymptom som oftast uppträder hos personer över 30 år. (ej att förväxla med akne) Cirka Symptomen på rosacea
rosacea Information om ett vuxet problem 1 RosaceA är den medicinska termen för ett antal hudsymptom som oftast uppträder hos personer över 30 år. (ej att förväxla med akne) Cirka Symptomen på rosacea
En forskningsstudie om Kronisk Myeloisk Leukemi, KML
 En forskningsstudie om Kronisk Myeloisk Leukemi, KML FORSKNINGSPERSONINFORMATION Du tillfrågas härmed om du vill delta i studie angående Kronisk Myeloisk Leukemi, KML, och kan tänka dig att lämna extra
En forskningsstudie om Kronisk Myeloisk Leukemi, KML FORSKNINGSPERSONINFORMATION Du tillfrågas härmed om du vill delta i studie angående Kronisk Myeloisk Leukemi, KML, och kan tänka dig att lämna extra
Forskningspersonsinformation till frisk frivillig kontroll
 BILAGA 4 Version 4.0 2018-06-13 1(5) Forskningspersonsinformation till frisk frivillig kontroll Bakgrund och syfte Inflammation har tilldragit sig ett växande intresse som tänkbar mekanism bakom depression,
BILAGA 4 Version 4.0 2018-06-13 1(5) Forskningspersonsinformation till frisk frivillig kontroll Bakgrund och syfte Inflammation har tilldragit sig ett växande intresse som tänkbar mekanism bakom depression,
En studie av ett nytt kikhostevaccin
 En studie av ett nytt kikhostevaccin Sveriges expertmyndighet för smittskydd (Smittskyddsinstitutet, SMI) har tillsammans med INSERM, French Health and Medical Research National Institute (som är sponsor
En studie av ett nytt kikhostevaccin Sveriges expertmyndighet för smittskydd (Smittskyddsinstitutet, SMI) har tillsammans med INSERM, French Health and Medical Research National Institute (som är sponsor
PATIENTINFORMATION OCH SAMTYCKE TILL ATT DELTA I EN FORSKNINGSSTUDIE
 PATIENTINFORMATION OCH SAMTYCKE TILL ATT DELTA I EN FORSKNINGSSTUDIE Namn på forskningsstudien: Randomiserad, dubbelblind, placebokontrollerad, parallellgruppsstudie för att bedöma kardiovaskulära resultat
PATIENTINFORMATION OCH SAMTYCKE TILL ATT DELTA I EN FORSKNINGSSTUDIE Namn på forskningsstudien: Randomiserad, dubbelblind, placebokontrollerad, parallellgruppsstudie för att bedöma kardiovaskulära resultat
Rodnad och utslag? Läs mer om rosacea.
 Rodnad och utslag? Läs mer om rosacea. metronidazol Är du röd i ansiktet med akneliknande utslag, rodnad eller ytliga blodkärl? Det kan vara rosacea. Rosacea är en vanlig, kronisk hudsjukdom som kan uppträda
Rodnad och utslag? Läs mer om rosacea. metronidazol Är du röd i ansiktet med akneliknande utslag, rodnad eller ytliga blodkärl? Det kan vara rosacea. Rosacea är en vanlig, kronisk hudsjukdom som kan uppträda
Om att delta i en klinisk prövning
 Om att delta i en klinisk prövning 1 Innehållsförteckning Vad är en klinisk prövning och hur utförs den? 5 Varför görs kliniska prövningar? 7 Varför gör min läkare kliniska prövingar? 7 Hur utförs en klinisk
Om att delta i en klinisk prövning 1 Innehållsförteckning Vad är en klinisk prövning och hur utförs den? 5 Varför görs kliniska prövningar? 7 Varför gör min läkare kliniska prövingar? 7 Hur utförs en klinisk
Information om forskningsstudien Born into Life (5-6 årsuppföljning av Life Gene Gravidstudien och Födelsekohorten)
 Sid: 1 / 5 Information om forskningsstudien Born into Life (5-6 årsuppföljning av Life Gene Gravidstudien och Födelsekohorten) Vad är Born into Life? I studien har vi följt dig och ditt barn med frågeformulär
Sid: 1 / 5 Information om forskningsstudien Born into Life (5-6 årsuppföljning av Life Gene Gravidstudien och Födelsekohorten) Vad är Born into Life? I studien har vi följt dig och ditt barn med frågeformulär
SWEPI-STUDIEN: induktion (igångsättning) av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42
 SWEPI-STUDIEN: induktion (igångsättning) av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42 Information till dig som kommit till 40 fulla graviditetsveckor Du har nu kommit
SWEPI-STUDIEN: induktion (igångsättning) av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42 Information till dig som kommit till 40 fulla graviditetsveckor Du har nu kommit
Hur skriver man en bra patientinformation? Samtyckesprocessen
 Hur skriver man en bra patientinformation? Samtyckesprocessen Patientinformationen ska ge patienten all information den behöver för att ställning till om den vill delta i studien eller ej. Att delta i
Hur skriver man en bra patientinformation? Samtyckesprocessen Patientinformationen ska ge patienten all information den behöver för att ställning till om den vill delta i studien eller ej. Att delta i
Till dig som ska föda ditt första barn
 Till dig som ska föda ditt första barn Ett forskningsprojekt pågår om akupunktur som smärtlindring under förlossning. Vi vill undersöka vilken typ av akupunkturbehandling som ger bäst smärtlindring. Resultaten
Till dig som ska föda ditt första barn Ett forskningsprojekt pågår om akupunktur som smärtlindring under förlossning. Vi vill undersöka vilken typ av akupunkturbehandling som ger bäst smärtlindring. Resultaten
SWEPI-STUDIEN: induktion (igångsättning) av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42
 SWEPI-STUDIEN: induktion (igångsättning) av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42 Information till dig som kommit till 40 fulla graviditetsveckor Du har nu kommit
SWEPI-STUDIEN: induktion (igångsättning) av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42 Information till dig som kommit till 40 fulla graviditetsveckor Du har nu kommit
Information om undersökningen Riksmaten ungdom
 Till vårdnadshavare för ungdomar i åk 5 eller åk 8 Information om undersökningen Riksmaten ungdom Bakgrund och syfte med Riksmaten ungdom Livsmedelsverket jobbar för säker mat och för bra matvanor. Livsmedelsverket
Till vårdnadshavare för ungdomar i åk 5 eller åk 8 Information om undersökningen Riksmaten ungdom Bakgrund och syfte med Riksmaten ungdom Livsmedelsverket jobbar för säker mat och för bra matvanor. Livsmedelsverket
Vill du delta i en undersökning om matvanor?
 Till ungdomar i åk 5 eller åk 8 Vill du delta i en undersökning om matvanor? Bakgrund och syfte med Riksmaten ungdom Livsmedelsverket jobbar för säker mat och för bra matvanor. Livsmedelsverket behöver
Till ungdomar i åk 5 eller åk 8 Vill du delta i en undersökning om matvanor? Bakgrund och syfte med Riksmaten ungdom Livsmedelsverket jobbar för säker mat och för bra matvanor. Livsmedelsverket behöver
Men många tvekar att använda dessa produkter på grund av eventuella biverkningar.
 Appendix 1 INFORMATION TILL FÖRÄLDRAR Atopiskt eksem behandlas med kräm, salva eller lotion som innehåller kortison (kortisonprodukter, KP). Men många tvekar att använda dessa produkter på grund av eventuella
Appendix 1 INFORMATION TILL FÖRÄLDRAR Atopiskt eksem behandlas med kräm, salva eller lotion som innehåller kortison (kortisonprodukter, KP). Men många tvekar att använda dessa produkter på grund av eventuella
Förfrågan om att delta i forskningsprojekt STATICH: Blodproppsförebyggande läkemedelsbehandling efter hjärnblödning.
 Förfrågan om att delta i forskningsprojekt STATICH: Blodproppsförebyggande läkemedelsbehandling efter hjärnblödning. Bakgrund och syfte Efter hjärtinfarkt eller hjärninfarkt som beror på blodpropp i hjärtats
Förfrågan om att delta i forskningsprojekt STATICH: Blodproppsförebyggande läkemedelsbehandling efter hjärnblödning. Bakgrund och syfte Efter hjärtinfarkt eller hjärninfarkt som beror på blodpropp i hjärtats
Information till försökspersoner i studie med vaccin mot pandemi (H1N1) och säsongsinfluensa
 Deltagarnummer: Information till försökspersoner i studie med vaccin mot pandemi (H1N1) och säsongsinfluensa Du tillfrågas härmed om att delta i en vaccinstudie mot influensa orsakad av H1N1 (svininfluensa)
Deltagarnummer: Information till försökspersoner i studie med vaccin mot pandemi (H1N1) och säsongsinfluensa Du tillfrågas härmed om att delta i en vaccinstudie mot influensa orsakad av H1N1 (svininfluensa)
Nationellt kvalitetsregister samt stöd i den individuella vården för patienter med primär immunbrist och/eller ökad infektionskänslighet
 Nationellt kvalitetsregister samt stöd i den individuella vården för patienter med primär immunbrist och/eller ökad infektionskänslighet Kom med du också ditt bidrag hjälper till att göra vården bättre!
Nationellt kvalitetsregister samt stöd i den individuella vården för patienter med primär immunbrist och/eller ökad infektionskänslighet Kom med du också ditt bidrag hjälper till att göra vården bättre!
INFORMATION TILL STUDIEDELTAGARE
 INFORMATION TILL STUDIEDELTAGARE Information om studie gällande interaktioner mellan hjärna och tarm efter probiotiskt kosttillskott till friska personer Förfrågan om deltagande i forskningsstudie Du tillfrågas
INFORMATION TILL STUDIEDELTAGARE Information om studie gällande interaktioner mellan hjärna och tarm efter probiotiskt kosttillskott till friska personer Förfrågan om deltagande i forskningsstudie Du tillfrågas
Förfrågan om att delta i ett forskningsprojekt
 Förfrågan om att delta i ett forskningsprojekt Ändtarmscancer: operation med stomi där anus lämnas kvar eller tas bort. (Hartmann eller Abdominoperineal excision med intersfinkterisk dissektion vid rektalcancer:
Förfrågan om att delta i ett forskningsprojekt Ändtarmscancer: operation med stomi där anus lämnas kvar eller tas bort. (Hartmann eller Abdominoperineal excision med intersfinkterisk dissektion vid rektalcancer:
PATIENTINFORMATION. Studietitel: En dosutvärdering av ALK träd AIT (Allergi Immunterapi Tablett)
 PATIENTINFORMATION Studietitel: En dosutvärdering av ALK träd AIT (Allergi Immunterapi Tablett) Bakgrund och syfte Du tillfrågas om att delta i denna forskningsstudie eftersom du har hösnuva och är allergisk
PATIENTINFORMATION Studietitel: En dosutvärdering av ALK träd AIT (Allergi Immunterapi Tablett) Bakgrund och syfte Du tillfrågas om att delta i denna forskningsstudie eftersom du har hösnuva och är allergisk
Studie av internetförmedlad kognitiv beteendeterapi vid intermittent (paroxysmalt) förmaksflimmer
 Sidan 1 av 5 Studie av internetförmedlad kognitiv beteendeterapi vid intermittent (paroxysmalt) förmaksflimmer Bakgrund och syfte Förmaksflimmer är en vanlig hjärtsjukdom som beror på en störd elektrisk
Sidan 1 av 5 Studie av internetförmedlad kognitiv beteendeterapi vid intermittent (paroxysmalt) förmaksflimmer Bakgrund och syfte Förmaksflimmer är en vanlig hjärtsjukdom som beror på en störd elektrisk
Studie: 1237.19 DYNAGITO EudraCT nr: 2014-002275-28 Patient nr.:
 Titel: En randomiserad, dubbelblind studie, med syfte att utvärdera effekten av 52 veckors behandling med inhalation Olodaterol + Tiotropium i fast doskombination en gång per dag, jämfört med behandling
Titel: En randomiserad, dubbelblind studie, med syfte att utvärdera effekten av 52 veckors behandling med inhalation Olodaterol + Tiotropium i fast doskombination en gång per dag, jämfört med behandling
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Differin 1 mg/g gel adapalen Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. - Spara
Bipacksedel: Information till användaren Differin 1 mg/g gel adapalen Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. - Spara
En studie om barns hälsa i Västerbotten. Inbjudan till dig som blivande förälder
 En studie om barns hälsa i Västerbotten Inbjudan till dig som blivande förälder Fokus i studien Northpop är att undersöka risk- och friskfaktorer för vanligt förekommande sjukdomar hos barn. Alla blivande
En studie om barns hälsa i Västerbotten Inbjudan till dig som blivande förälder Fokus i studien Northpop är att undersöka risk- och friskfaktorer för vanligt förekommande sjukdomar hos barn. Alla blivande
Rodnad och utslag? Läs mer om rosacea.
 Rodnad och utslag? Läs mer om rosacea. metronidazol Är du röd i ansiktet med akneliknande utslag, rodnad eller ytliga blodkärl? Det kan vara rosacea. Rosacea är en vanlig, kronisk hudsjukdom som kan uppträda
Rodnad och utslag? Läs mer om rosacea. metronidazol Är du röd i ansiktet med akneliknande utslag, rodnad eller ytliga blodkärl? Det kan vara rosacea. Rosacea är en vanlig, kronisk hudsjukdom som kan uppträda
1. Förvaltning:... Verksamhetsområde: Kontaktperson: Personregistrets benämning. 4. Hur sker information till de registrerade?
 Register nr OBS! Ta ut en papperskopia som undertecknas. Anvisningar hur blanketten ska fyllas i finns i slutet av detta formulär. Anmälan om behandling av personuppgifter samt ändring av tidigare anmälan
Register nr OBS! Ta ut en papperskopia som undertecknas. Anvisningar hur blanketten ska fyllas i finns i slutet av detta formulär. Anmälan om behandling av personuppgifter samt ändring av tidigare anmälan
INFORMATION FÖR DIG SOM SKA BEHANDLAS MED QUTENZA
 INFORMATION FÖR DIG SOM SKA BEHANDLAS MED QUTENZA Den här broschyren är riktad till dig som ska behandlas med QUTENZA (kapsaicin). Här kan du läsa om vad QUTENZA är, hur det fungerar och hur behandlingen
INFORMATION FÖR DIG SOM SKA BEHANDLAS MED QUTENZA Den här broschyren är riktad till dig som ska behandlas med QUTENZA (kapsaicin). Här kan du läsa om vad QUTENZA är, hur det fungerar och hur behandlingen
INFORMATION TILL STUDIEDELTAGARE
 INFORMATION TILL STUDIEDELTAGARE Information om studie gällande interaktioner mellan hjärna och tarm efter probiotiskt kosttillskott till friska personer Förfrågan om deltagande i forskningsstudie Du tillfrågas
INFORMATION TILL STUDIEDELTAGARE Information om studie gällande interaktioner mellan hjärna och tarm efter probiotiskt kosttillskott till friska personer Förfrågan om deltagande i forskningsstudie Du tillfrågas
Tillsammans för bättre hälsa
 Tillsammans för bättre hälsa Vår vision är ett samhälle där alla får leva ett så friskt liv som möjligt.vi jobbar långsiktigt och brett för att kunna hjälpa forskare i deras strävan efter bättre hälsa
Tillsammans för bättre hälsa Vår vision är ett samhälle där alla får leva ett så friskt liv som möjligt.vi jobbar långsiktigt och brett för att kunna hjälpa forskare i deras strävan efter bättre hälsa
Donation av blodstamceller Informationsbroschyr till donator 18 år
 Donation av blodstamceller Informationsbroschyr till donator 18 år Giltigt i 2 år från 2015-04-24 Sida 1 av 6 Bakgrund De blodbildande stamcellerna finns framför allt i benmärgen. En liten mängd cirkulerar
Donation av blodstamceller Informationsbroschyr till donator 18 år Giltigt i 2 år från 2015-04-24 Sida 1 av 6 Bakgrund De blodbildande stamcellerna finns framför allt i benmärgen. En liten mängd cirkulerar
Om din behandling med Xiapex
 PATIENTINFORMATION PATIENTINFORMATION Om din behandling med Xiapex Dupuytrens kontraktur Dupuytrens kontraktur är en bindvävssjukdom som ibland även kallas vikingasjukan eftersom den är vanligare i Skandi
PATIENTINFORMATION PATIENTINFORMATION Om din behandling med Xiapex Dupuytrens kontraktur Dupuytrens kontraktur är en bindvävssjukdom som ibland även kallas vikingasjukan eftersom den är vanligare i Skandi
Patientinformation och samtycke
 Sida 1 av 7 Patientinformation och samtycke Dubbelblind, placebokontrollerad fas 2 studie för att undersöka effekt, säkerhet och tolerabilitet hos studieläkemedlet Lymfactin (adenovirusmedierad lymfkärlstillvätfaktor
Sida 1 av 7 Patientinformation och samtycke Dubbelblind, placebokontrollerad fas 2 studie för att undersöka effekt, säkerhet och tolerabilitet hos studieläkemedlet Lymfactin (adenovirusmedierad lymfkärlstillvätfaktor
En studie om barns hälsa i Västerbotten. Inbjudan till dig som blivande förälder
 En studie om barns hälsa i Västerbotten Inbjudan till dig som blivande förälder Fokus i studien Northpop är att undersöka risk- och friskfaktorer för vanligt förekommande sjukdomar hos barn. Alla blivande
En studie om barns hälsa i Västerbotten Inbjudan till dig som blivande förälder Fokus i studien Northpop är att undersöka risk- och friskfaktorer för vanligt förekommande sjukdomar hos barn. Alla blivande
Patientinformation för Hälso- och livsstilsverktyg
 Patientinformation för Hälso- och livsstilsverktyg Vi skriver till Dig som vill förbättra Din hälsa, Dina levnadsvanor och Ditt mående. Du inbjuds härmed att delta i en forskningsstudie om ett Hälso- och
Patientinformation för Hälso- och livsstilsverktyg Vi skriver till Dig som vill förbättra Din hälsa, Dina levnadsvanor och Ditt mående. Du inbjuds härmed att delta i en forskningsstudie om ett Hälso- och
En studie om barns hälsa i Västerbotten. Inbjudan till dig som blivande förälder
 En studie om barns hälsa i Västerbotten Inbjudan till dig som blivande förälder Fokus i studien Northpop är att undersöka risk- och friskfaktorer för vanligt förekommande sjukdomar hos barn. Alla blivande
En studie om barns hälsa i Västerbotten Inbjudan till dig som blivande förälder Fokus i studien Northpop är att undersöka risk- och friskfaktorer för vanligt förekommande sjukdomar hos barn. Alla blivande
Blankett för samtycke
 Blankett för samtycke ELEVENS NAMN PERSONNUMMER SKOLA ÅRSKURS Godkänner du att uppgifterna från frågeformuläret sparas i Norrbottens läns landstings databas? JA NEJ DATUM UNDERSKRIFT VÅRDNADSHAVARE 1 /ELEV*
Blankett för samtycke ELEVENS NAMN PERSONNUMMER SKOLA ÅRSKURS Godkänner du att uppgifterna från frågeformuläret sparas i Norrbottens läns landstings databas? JA NEJ DATUM UNDERSKRIFT VÅRDNADSHAVARE 1 /ELEV*
Kom med du också ditt bidrag hjälper till att göra vården bättre!
 Nationellt kvalitetsregister samt stöd i den individuella vården för patienter med primär immunbrist och/eller ökad infektionskänslighet Kom med du också ditt bidrag hjälper till att göra vården bättre!
Nationellt kvalitetsregister samt stöd i den individuella vården för patienter med primär immunbrist och/eller ökad infektionskänslighet Kom med du också ditt bidrag hjälper till att göra vården bättre!
Förfrågan om att delta i ett forskningsprojekt
 1 Förfrågan om att delta i ett forskningsprojekt Ändtarmscancer: operation med stomi där anus lämnas kvar eller tas bort. (Hartmann eller Abdominoperineal excision med intersfinkterisk dissektion vid rektalcancer:
1 Förfrågan om att delta i ett forskningsprojekt Ändtarmscancer: operation med stomi där anus lämnas kvar eller tas bort. (Hartmann eller Abdominoperineal excision med intersfinkterisk dissektion vid rektalcancer:
Information till deltagaren
 Information till deltagaren Bakgrund Är du i åldern 60 75 år? Har du funderingar om din hälsa och då specifikt kring övervikt, diabetes, högt blodtryck eller depression? Vill du veta mer om hur din livsstil
Information till deltagaren Bakgrund Är du i åldern 60 75 år? Har du funderingar om din hälsa och då specifikt kring övervikt, diabetes, högt blodtryck eller depression? Vill du veta mer om hur din livsstil
Patientinformation från Hudkliniken i Östergötland. Läs igenom denna produktinformation noggrant innan du börjar använda läkemedlet.
 Isotretinoin Patientinformation från Hudkliniken i Östergötland Läs igenom denna produktinformation noggrant innan du börjar använda läkemedlet. Spara denna produktinformation. Du kan komma att behöva
Isotretinoin Patientinformation från Hudkliniken i Östergötland Läs igenom denna produktinformation noggrant innan du börjar använda läkemedlet. Spara denna produktinformation. Du kan komma att behöva
Information till studiedeltagare
 Information till studiedeltagare Information om studie gällande effekten av ett kosttillskott innehållande probiotika, omega-3 fettsyror och vitamin D på låg-gradig inflammation och rörlighet hos äldre
Information till studiedeltagare Information om studie gällande effekten av ett kosttillskott innehållande probiotika, omega-3 fettsyror och vitamin D på låg-gradig inflammation och rörlighet hos äldre
- förebyggande uppföljning vid ryggmärgsbråck. Information för deltagare
 MMCUP - förebyggande uppföljning vid ryggmärgsbråck Information för deltagare Personer med ryggmärgsbråck behöver många olika sjukvårdskontakter under hela livet och det är lätt hänt att någon viktig insats
MMCUP - förebyggande uppföljning vid ryggmärgsbråck Information för deltagare Personer med ryggmärgsbråck behöver många olika sjukvårdskontakter under hela livet och det är lätt hänt att någon viktig insats
Forskningspersonsinformation
 Forskningspersonsinformation Jämförande studie mellan öppen kirurgi och robot-assisterad titthålskirurgi vid tidig livmoderhalscancer. Bakgrund och syfte Behandlingen av patienter med tidig livmoderhalscancer
Forskningspersonsinformation Jämförande studie mellan öppen kirurgi och robot-assisterad titthålskirurgi vid tidig livmoderhalscancer. Bakgrund och syfte Behandlingen av patienter med tidig livmoderhalscancer
Patientinformation (postoperativ)
 Patientinformation (postoperativ) Vi vill härmed fråga Dig om Du vill delta i en forskningsstudie rörande operation av lymfkörtlar i armhålan i samband med operation för bröstcancer enligt nedanstående
Patientinformation (postoperativ) Vi vill härmed fråga Dig om Du vill delta i en forskningsstudie rörande operation av lymfkörtlar i armhålan i samband med operation för bröstcancer enligt nedanstående
Ska du genomgå en IVF-behandling? Varför blir vissa kvinnor lättare gravida än andra? Varför får vissa missfall?
 UppStART Ska du genomgå en IVF-behandling? Varför blir vissa kvinnor lättare gravida än andra? Varför får vissa missfall? Det tar några minuter och kan ge forskningen enorma möjligheter till att förbättra
UppStART Ska du genomgå en IVF-behandling? Varför blir vissa kvinnor lättare gravida än andra? Varför får vissa missfall? Det tar några minuter och kan ge forskningen enorma möjligheter till att förbättra
Bipacksedel: Information till användaren. Locoid Lipid 0,1% kräm Locoid Crelo 0,1% kutan emulsion. hydrokortisonbutyrat
 Bipacksedel: Information till användaren Locoid Lipid 0,1% kräm Locoid Crelo 0,1% kutan emulsion hydrokortisonbutyrat Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller
Bipacksedel: Information till användaren Locoid Lipid 0,1% kräm Locoid Crelo 0,1% kutan emulsion hydrokortisonbutyrat Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller
Bipacksedel: Information till patienten. Mometasone Teva 1mg/g kräm Mometasone Teva 1mg/g salva. mometason
 Bipacksedel: Information till patienten Mometasone Teva 1mg/g kräm Mometasone Teva 1mg/g salva mometason Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
Bipacksedel: Information till patienten Mometasone Teva 1mg/g kräm Mometasone Teva 1mg/g salva mometason Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
BESLUT. Datum 2015-11-19. Namn Form Styrka Förp. Varunr AIP (SEK) AUP (SEK) Soolantra Kräm 10 mg/g Tub, 30 gram 119528 210,50 261,00
 BESLUT 1 (6) Datum 2015-11-19 Vår beteckning SÖKANDE Galderma Nordic AB Seminariegatan 21 752 28 Uppsala SAKEN Ansökan inom läkemedelsförmånerna BESLUT Tandvårds- och läkemedelsförmånsverket, TLV, beslutar
BESLUT 1 (6) Datum 2015-11-19 Vår beteckning SÖKANDE Galderma Nordic AB Seminariegatan 21 752 28 Uppsala SAKEN Ansökan inom läkemedelsförmånerna BESLUT Tandvårds- och läkemedelsförmånsverket, TLV, beslutar
SWEPI-STUDIEN: Induktion av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42
 SWEPI-STUDIEN: Induktion av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42 Information till dig som kommit till 40 fulla graviditetsveckor Du har nu kommit till 40 fulla
SWEPI-STUDIEN: Induktion av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42 Information till dig som kommit till 40 fulla graviditetsveckor Du har nu kommit till 40 fulla
Information om screeningstudie gällande prostatacancer GÖTEBORG 2- STUDIEN PROSTATACANCERSTUDIE
 PROSTATACANCERSTUDIE Information om screeningstudie gällande prostatacancer GÖTEBORG 2- STUDIEN Avdelningen för urologi Sahlgrenska akademin Göteborgs universitet Hemsida: www.g2screening.se E-post:g2@gu.se
PROSTATACANCERSTUDIE Information om screeningstudie gällande prostatacancer GÖTEBORG 2- STUDIEN Avdelningen för urologi Sahlgrenska akademin Göteborgs universitet Hemsida: www.g2screening.se E-post:g2@gu.se
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Differin 1 mg/g kräm adapalen Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. - Spara
Bipacksedel: Information till användaren Differin 1 mg/g kräm adapalen Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. - Spara
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN. Finacea, 15% gel Azelainsyra
 BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Finacea, 15% gel Azelainsyra Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. - Spara
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Finacea, 15% gel Azelainsyra Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. - Spara
Några minuter idag. Många liv i morgon.
 Några minuter idag. Många liv i morgon. Karma Kamera www.karmakamera.se Karolinska Institutet genomför under hösten 2013 forskningsstudien Karma Kamera i samarbete med Södersjukhuset. Vi ställer nu frågan
Några minuter idag. Många liv i morgon. Karma Kamera www.karmakamera.se Karolinska Institutet genomför under hösten 2013 forskningsstudien Karma Kamera i samarbete med Södersjukhuset. Vi ställer nu frågan
PATIENTINFORMATION Information om studie gällande interaktioner mellan hjärna och tarm efter
 PATIENTINFORMATION Information om studie gällande interaktioner mellan hjärna och tarm efter probiotiskt kosttillskott till personer med IBS, Irritable Bowel Syndrome. Förfrågan om deltagande i forskningsstudie
PATIENTINFORMATION Information om studie gällande interaktioner mellan hjärna och tarm efter probiotiskt kosttillskott till personer med IBS, Irritable Bowel Syndrome. Förfrågan om deltagande i forskningsstudie
Till dig som fått VELCADE. Information till patienter och anhöriga
 Till dig som fått VELCADE Information till patienter och anhöriga Information om Velcade till patienter och anhöriga Din läkare har rekommenderat behandling med VELCADE (bortezomib). VELCADE är det första
Till dig som fått VELCADE Information till patienter och anhöriga Information om Velcade till patienter och anhöriga Din läkare har rekommenderat behandling med VELCADE (bortezomib). VELCADE är det första
Ver. 2.0 ( )
 1/5 Information till deltagare i studien Effekten av fysisk och kognitiv träning på äldres kognitiva förmåga Studieansvarig: Martin Lövdén Tillfrågande om deltagande Du har anmält intresse för att delta
1/5 Information till deltagare i studien Effekten av fysisk och kognitiv träning på äldres kognitiva förmåga Studieansvarig: Martin Lövdén Tillfrågande om deltagande Du har anmält intresse för att delta
till dig som ska behandlas med idelvion
 PATIENTINFORMATION till dig som ska behandlas med idelvion (albutrepenonakog alfa) Coagulation Factor IX (Recombinant), Albumin Fusion Protein idelvion för dig som har hemofili b Hemofili B är en form
PATIENTINFORMATION till dig som ska behandlas med idelvion (albutrepenonakog alfa) Coagulation Factor IX (Recombinant), Albumin Fusion Protein idelvion för dig som har hemofili b Hemofili B är en form
Information till patient och närstående Hej och välkommen till avdelning 12-25
 Information till patient och närstående Hej och välkommen till avdelning 12-25 Lite bra att veta.. 1 Beskrivning av avdelningen Avdelning 12-25 har 33 vårdplatser och därtill tillkommer 3 vårdplatser på
Information till patient och närstående Hej och välkommen till avdelning 12-25 Lite bra att veta.. 1 Beskrivning av avdelningen Avdelning 12-25 har 33 vårdplatser och därtill tillkommer 3 vårdplatser på
Välkommen till Kärl-Thoraxkliniken
 Välkommen till Kärl-Thoraxkliniken Va lkommen till Ka rl-thoraxkliniken Våra patientgrupper är till största delen opererade i hjärta, lunga, kärl eller bröstkorg. Avdelningen har totalt 20 vårdplatser
Välkommen till Kärl-Thoraxkliniken Va lkommen till Ka rl-thoraxkliniken Våra patientgrupper är till största delen opererade i hjärta, lunga, kärl eller bröstkorg. Avdelningen har totalt 20 vårdplatser
- förebyggande uppföljning vid ryggmärgsbråck. Information för deltagare
 MMCUP - förebyggande uppföljning vid ryggmärgsbråck Information för deltagare Personer med ryggmärgsbråck behöver många olika sjukvårdskontakter under hela livet och det är lätt hänt att någon viktig insats
MMCUP - förebyggande uppföljning vid ryggmärgsbråck Information för deltagare Personer med ryggmärgsbråck behöver många olika sjukvårdskontakter under hela livet och det är lätt hänt att någon viktig insats
En informationsbroschyr om EpiHealth
 En informationsbroschyr om EpiHealth Information finns även på Vad är EpiHealth? EpiHealth (Epidemiologi för hälsa) är ett storskaligt forskningssamarbete mellan Uppsala universitet och Lunds universitet.
En informationsbroschyr om EpiHealth Information finns även på Vad är EpiHealth? EpiHealth (Epidemiologi för hälsa) är ett storskaligt forskningssamarbete mellan Uppsala universitet och Lunds universitet.
Om din behandling med Xiapex
 p a t i e n t i n f o r m a t i o n P a t i e n t i n f o r m a t i o n Om din behandling med Xiapex Dupuytrens kontraktur Dupuytrens kontraktur är en bindvävssjukdom som ibland även kallas vikingasjukan
p a t i e n t i n f o r m a t i o n P a t i e n t i n f o r m a t i o n Om din behandling med Xiapex Dupuytrens kontraktur Dupuytrens kontraktur är en bindvävssjukdom som ibland även kallas vikingasjukan
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
 Bipacksedel: Information till användaren Cortimyk 20 mg/g + 10 mg/g kräm Mikonazolnitrat och hydrokortison Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
Bipacksedel: Information till användaren Cortimyk 20 mg/g + 10 mg/g kräm Mikonazolnitrat och hydrokortison Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information
Bipacksedel: Information till användaren. Locoid 0,1% kräm Locoid 0,1% salva Locoid 0,1% kutan lösning. hydrokortisonbutyrat
 Bipacksedel: Information till användaren Locoid 0,1% kräm Locoid 0,1% salva Locoid 0,1% kutan lösning hydrokortisonbutyrat Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den
Bipacksedel: Information till användaren Locoid 0,1% kräm Locoid 0,1% salva Locoid 0,1% kutan lösning hydrokortisonbutyrat Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den
Information/Informerat samtycke -ebup-sömn implementering. Till vårdnadshavare: Behandling för ungdomar med sömnproblem
 Information/Informerat samtycke -ebup-sömn implementering Till vårdnadshavare: Behandling för ungdomar med sömnproblem Nu har ungdomar mellan 13-18 år möjlighet att delta i en forskningsstudie och få internetförmedlad
Information/Informerat samtycke -ebup-sömn implementering Till vårdnadshavare: Behandling för ungdomar med sömnproblem Nu har ungdomar mellan 13-18 år möjlighet att delta i en forskningsstudie och få internetförmedlad
PICC-line, perifert inlagd central venkateter
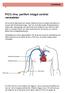 PICC-line, perifert inlagd central venkateter Om du ska få läkemedel som dropp i blodet kommer du troligen att behöva en central infart till ditt blodomlopp. I den kan du få läkemedel, blodtransfusioner,
PICC-line, perifert inlagd central venkateter Om du ska få läkemedel som dropp i blodet kommer du troligen att behöva en central infart till ditt blodomlopp. I den kan du få läkemedel, blodtransfusioner,
SWEPI-STUDIEN: Induktion av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42
 SWEPI-STUDIEN: Induktion av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42 Information till dig som kommit till 40 fulla graviditetsveckor Du har nu kommit till 40 fulla
SWEPI-STUDIEN: Induktion av förlossning i graviditetsvecka 41 jämfört med induktion i graviditetsvecka 42 Information till dig som kommit till 40 fulla graviditetsveckor Du har nu kommit till 40 fulla
BESLUT. Datum 2013-06-26
 BESLUT 1 (5) Datum 2013-06-26 Vår beteckning SÖKANDE Leo Pharma AB Box 404 201 24 Malmö SAKEN Ansökan inom läkemedelsförmånerna BESLUT Tandvårds- och läkemedelsförmånsverket, TLV beslutar att nedanstående
BESLUT 1 (5) Datum 2013-06-26 Vår beteckning SÖKANDE Leo Pharma AB Box 404 201 24 Malmö SAKEN Ansökan inom läkemedelsförmånerna BESLUT Tandvårds- och läkemedelsförmånsverket, TLV beslutar att nedanstående
Prislista hälsoundersökningar 2017
 Prislista hälsoundersökningar 2017 Hälsochecken Detta är en lite mindre hälsokoll men det viktigaste ingår: Längd Vikt Midjemått BMI (Body Mass Index) Blodtryck Puls Provtagning - blodsocker, kolesterol
Prislista hälsoundersökningar 2017 Hälsochecken Detta är en lite mindre hälsokoll men det viktigaste ingår: Längd Vikt Midjemått BMI (Body Mass Index) Blodtryck Puls Provtagning - blodsocker, kolesterol
PARTNER-studien. Det är en europeisk studie som kommer att omfatta cirka 950 manliga homosexuella par.
 Deltagarinformation och informerat samtycke för den HIV-negativa partnern PARTNER-studien PARTNER-studien är en studie som riktar sig till par där: (i) den ena partnern är HIV-positiv och den andra är
Deltagarinformation och informerat samtycke för den HIV-negativa partnern PARTNER-studien PARTNER-studien är en studie som riktar sig till par där: (i) den ena partnern är HIV-positiv och den andra är
1. VAD LAMISIL DERMGEL ÄR OCH VAD DET ANVÄNDS FÖR
 BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Lamisil Dermgel 1% gel Terbinafin Läs noga igenom denna bipacksedel. Den innehåller information som är viktig för dig. - Använd alltid detta läkemedel exakt enligt
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Lamisil Dermgel 1% gel Terbinafin Läs noga igenom denna bipacksedel. Den innehåller information som är viktig för dig. - Använd alltid detta läkemedel exakt enligt
Gilenya (fingolimod) Information för dig som ska starta behandling med GILENYA. För fullständig GILENYA information se bipacksedeln eller
 Novartis Neuroscience Gilenya (fingolimod) Information för dig som ska starta behandling med För fullständig information se bipacksedeln eller www.fass.se - ditt nya läkemedel En kapsel en gång om dagen
Novartis Neuroscience Gilenya (fingolimod) Information för dig som ska starta behandling med För fullständig information se bipacksedeln eller www.fass.se - ditt nya läkemedel En kapsel en gång om dagen
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN. Finacea, 15% gel azelainsyra
 BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Finacea, 15% gel azelainsyra Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. - Spara
BIPACKSEDEL: INFORMATION TILL ANVÄNDAREN Finacea, 15% gel azelainsyra Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig. - Spara
För bättre läkemedelsanvändning och bättre hälsa
 Handla klokt! För bättre läkemedelsanvändning och bättre hälsa Läkemedelskommittén ska verka för en rationell, säker och kostnadseffektiv hantering av läkemedel. Kommittén utses av landstingsstyrelsen
Handla klokt! För bättre läkemedelsanvändning och bättre hälsa Läkemedelskommittén ska verka för en rationell, säker och kostnadseffektiv hantering av läkemedel. Kommittén utses av landstingsstyrelsen
Mall för information om kliniska läkemedelsprövningar
 Information om forskning 1(5) Mall för information om kliniska läkemedelsprövningar Allmänt Eventuella försökspersoner nias vanligen. Tilltalsformen varierar dock beroende på målgrupp. Informationen får
Information om forskning 1(5) Mall för information om kliniska läkemedelsprövningar Allmänt Eventuella försökspersoner nias vanligen. Tilltalsformen varierar dock beroende på målgrupp. Informationen får
